Сохранение хвоста у ребенка. Гигантизм и карликовость эмбриона
Добавил пользователь Алексей Ф. Обновлено: 21.01.2026
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Для корректной оценки результатов ваших анализов в динамике предпочтительно делать исследования в одной и той же лаборатории, так как в разных лабораториях для выполнения одноименных анализов могут применяться разные методы исследования и единицы измерения.
Карликовый рост: причины появления, при каких заболеваниях возникает, диагностика и способы лечения.
Определение
Карликовым ростом (карликовостью, нанизмом, дварфизмом) считается состояние, когда высота взрослого мужчины не превышает 130 см, а женщины - 120 см. Дварфизм диагностируется, когда отставание в росте составляет более 40%. Если оно не превышает 20%, говорят о недостаточном росте.
Разновидности карликовости
В зависимости от причин замедления роста различают несколько вариантов карликовости. Значительная часть случаев карликовости приходится на замедление или остановку роста под влиянием токсических факторов или дефицита питательных веществ.
Большую роль играют эндокринные факторы, в первую очередь, низкий уровень гормона роста - соматотропина. При его недостатке или невосприимчивости к нему организма рост замедляется. Кроме того, нанизм может наблюдаться при дефиците гормона щитовидной железы (гипотиреозе) и половых гормонов (гипогонадизме).
Преждевременное прекращение роста возникает при избытке глюкокортикоидов - стероидных гормонов, которые вырабатываются в коре надпочечников.
Карликовость в результате генетических и хромосомных патологий относится к наследственным факторам задержки роста с нарушением внутриутробного развития.
В ряде случаев маленький рост может быть следствием системных заболеваний.
Нанизм можно классифицировать и по другому признаку - пропорциональное и непропорциональное телосложение.
Возможные причины карликовости
Влияние экзогенных факторов. Задержку роста в период внутриутробного развития могут вызывать различные химические соединения, в том числе лекарственные вещества, наркотики, а также рентгеновское облучение и длительная гипоксия.
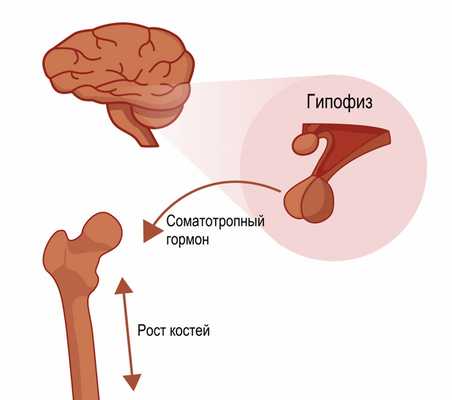
Гормональный дисбаланс. Преждевременное прекращение роста вследствие эндокринных нарушений относится к числу наиболее тяжелых пороков развития. Прямое воздействие на рост оказывает соматотропный гормон, или гормон роста, который вырабатывается в передней доле гипофиза.
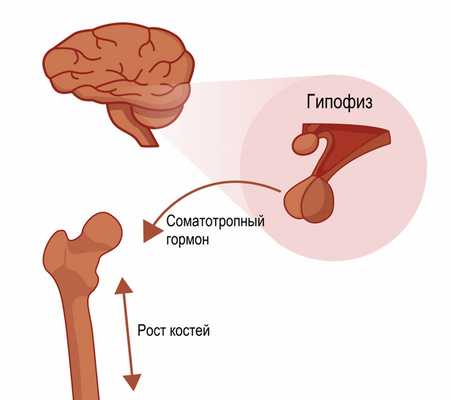
Карликовость может развиваться как по причине соматотропной недостаточности, так и вследствие невосприимчивости рецепторов различных тканей организма к соматотропину.
Очень часто дефицит гормона роста сочетается с недостаточной продукцией других гормонов аденогипофиза, что служит причиной развития пангипопитуитаризма.
Заболевание развивается очень долго, и первыми его симптомами являются задержка роста и изменение фигуры с развитием евнухоидных пропорций (укороченное туловище и длинные конечности). Задержка роста становится очевидной только на втором году жизни ребенка, а после 4 лет прибавка роста обычно не превышает 2-3 см в год. Характерным признаком заболевания служат мелкие, кукольные черты лица. Отмечается атрофия половых желез, задержка развития половых органов.
Недостаточность функции гипофиза приводит к нарушению роста и функций других желез внутренней секреции (щитовидной, поджелудочной, половых).
У взрослых пациентов с врожденной соматотропной недостаточностью, помимо задержки роста, имеют место ожирение с абдоминальным типом распределения жира, снижение мышечной массы тела, гипотония, остеопороз и ранний атеросклероз, снижение оволосения и атрофия наружных половых органов и молочных желез у женщин, низкий уровень физической и интеллектуальной активности.
При изолированном врожденном снижении выработки тиреотропных гормонов - гипотиреозе - также наблюдается задержка роста и диспропорция «костного» возраста. Но в отличие от пациентов с соматотропной недостаточностью, у детей с гипотиреозом нарушаются пропорции тела. Дети с врожденным гипотиреозом отличаются избыточным весом, отечностью лица и конечностей; хриплым голосом. У них отмечается плохая заживляемость пупочной ранки; длительная, больше недели, желтуха. При отсутствии своевременного лечения появляются другие типичные признаки: заторможенность, пониженный аппетит и ухудшение сосательного рефлекса, затруднения при глотании, метеоризм и запоры; сухая и шелушащаяся кожа; холодные кисти и стопы; ломкие, тусклые волосы. С возрастом проявляется задержка роста и отставание психомоторного развития.
Пороки «костного» роста заключаются в отставании развития лицевого скелета, позднем прорезывании и смене зубов.
При снижении продукции половых гормонов - гипогонадизме - помимо задержки роста отмечается недоразвитие половых органов, иногда ожирение. Врожденные формы гипогонадизма очень часто сочетаются с дефицитом других гипофизарных гормонов и синдромальными патологиями, в числе которых отмечают синдромы Прадера-Вилли, Барде-Бидля, Лоренса-Муна, Рода, а также синдром Мэдока.
Наследственные заболевания опорно-двигательного аппарата. Маленький рост может быть следствием ахондроплазии, или хондродисплазии, которая носит наследственный характер. Заболевание сопровождается замедлением роста костей и разрастанием клеток хрящевой ткани эпифизов. Кости конечностей становятся непропорционально короткими и утолщенными, кисти рук имеют форму трезубца. Отмечается макроцефалия с выступающим лбом и плоской переносицей. При рождении рост может находиться в пределах нижней границы нормы, но с возрастом происходит его задержка. Интеллект пациентов обычно сохранен, однако моторное развитие задерживается.
Остеопсатироз также относится к числу наследственных заболеваний костной системы. Нарушение синтеза коллагена приводит к раннему окостенению скелета и вследствие этого - к прекращению роста. В тяжелых случаях возможна смерть новорожденных. Могут наблюдаться значительные дефекты костной ткани в височной и затылочной области.
Один из ведущих симптомов заболевания - склонность к переломам костей, которые могут происходить как при внутриутробном развитии, так и во время родов и после них.
Пороки сердца. Карликовость может развиваться у детей, страдающих серьезными врожденными пороками сердца.
Хронические болезни почек. Хроническая почечная недостаточность почти всегда сопровождается задержкой роста. Особенно сильно заметна задержка роста в первые два года жизни и в пубертатном периоде. Кроме того, глюкокортикостероиды, которые в некоторых случаях вынужден принимать пациент, также вызывают нарушение роста.
Синдромальные виды нанизма. Карликовость присуща пациентам с врожденными генетически обусловленными синдромами. К их числу относят синдромы Шерешевского-Тернера (дисгенезия гонад), Нонне, Гетчинсона-Гилфорда, Рассела-Сильвера, Секкеля, Прадера-Вилли, Лоуренса-Муна-Барде-Бидля.
Все синдромальные заболевания характеризуются генетически обусловленными внутриутробными нарушениями развития, что приводит к многочисленным патологиям уже при рождении.
К каким врачам обращаться
Нарушение роста и диспропорции тела отмечаются уже в первые годы жизни ребенка, и первичный диагноз ставит педиатр. В дальнейшем может потребоваться помощь эндокринолога, ортопеда, уролога, нефролога или кардиолога.
Диагностика и обследования при карликовости
Диагностику начинают с опроса и оценки роста родителей пациента. Проводят антропометрические измерения (роста, веса и т.д.) и оценивают половое развитие. Определяют костный возраст ребенка, используя рентгенографию.
Исследуют гормональный фон: АКТГ, соматотропный гормон, инсулиноподобный фактор роста 1 (ИФР-1), гормоны щитовидной железы (Т3, Т4) и ТТГ, гонадотропины (лютеинизирующий гормон, фолликулостимулирующий гормон), тестостерон.
При обнаружении дефицита соматотропного гормона врач может порекомендовать магнитно-резонансную томографию головного мозга и молекулярно-генетическое исследование.
Что делать при карликовости
Первые признаки замедления роста отмечаются, как правило, с первого года жизни.
Необходимо проходить плановые врачебные осмотры детей до года (в 1, 3, 6, 9 и 12 месяцев), во время которых врач учитывает вес, рост, объем головы и груди ребенка.
Лечение карликовости
Лечение пациентов с нанизмом зависит от природы его возникновения. При карликовости, обусловленной недостаточной продукцией гормонов, при отсутствии опухолевого процесса проводят заместительную терапию. При тяжелых хронических заболеваниях сердца и почек необходимо лечение основных заболеваний.
- Федеральные клинические рекомендации (протоколы) по ведению детей с эндокринными заболеваниями / Под ред. И.И. Дедова и В.А. Петерковой. - М.: Практика, 2014. - 442 с.
- Большова-Зубковская Е.В., Тронько Н.Д. Патология роста и полового развития у детей и подростков. К.: Саммит.книга, 2003. - 94 с.
- Филина Н.Ю., Болотова Н.В., Назаренко К.А. Современная диагностика низкорослости у детей // Лечащий врач. - № 11, 2016. - С. 74.
Гипофизарный нанизм ( Карликовость , Микросомия , Наносомия )
Гипофизарный нанизм - эндокринное заболевание, в основе которого лежит нарушение синтеза гормона роста (соматотропина) в передней доле гипофиза, что приводит к задержке роста скелета, внутренних органов и физическому недоразвитию. Гипофизарный нанизм характеризуется аномальной низкорослостью: рост мужчин ниже 130 см, рост женщин ниже 120 см; отмечается отставание в развитии костно-мышечной системы, гипогонадизм, уменьшение размеров внутренних органов, гипотензия, брадикардия и др. Диагностика гипофизарного нанизма предполагает определение базальной концентрации СТГ в сыворотке крови, проведение фармакологических проб, рентгенографии черепа, кистей рук и лучезапястных суставов. Лечение гипофизарного нанизма включает заместительную терапию соматотропином, анаболическими стероидами, тиреоидными препаратами, половыми гормонами.
МКБ-10
Общие сведения
Гипофизарный нанизм - клинический синдром, обусловленный абсолютной или относительной соматотропной недостаточностью гипофиза (недостатком секреции соматотропного гормона или нарушением тканевой чувствительности к нему). Гипофизарный нанизм встречается в популяции с частотой 1:15 000 -1:20 000, несколько чаще среди мужчин. Понятием нанизм (микросомия, наносомия, карликовость) в широком смысле обозначают ряд патологических состояний, выражающихся в отставании роста и физического развития по сравнению со средней возрастной, половой, популяционной и расовой нормой. Нанизм может являться самостоятельным генетическим заболеванием или выступать симптомом ряда эндокринных и неэндокринных заболеваний.
Причины
Соматотропная недостаточность, лежащая в основе гипофизарного нанизма, может быть обусловлена тремя группами причин: врожденным дефицитом соматотропного гормона (СТГ), приобретенным гипосоматотропным состоянием и периферической резистентностью тканей к воздействию СТГ.
1. Врожденная недостаточность соматотропина может быть связана с генетическими дефектами (мутацией гена гормона роста, мутацией гена рецептора к соматолиберину и др.) либо аномалиями развития гипоталамо-гипофизарной системы (анэнцефалией, врожденной аплазией, гипоплазией или эктопией гипофиза).
2. Приобретенный гипофизарный нанизм развивается при:
- Опухолях гипоталамо-гипофизарной области (краниофарингиоме, гамартоме, нейрофиброме, герминоме, аденоме гипофиза) или других отделов головного мозга (например, глиоме зрительного перекреста).
- Травмах мозга. В некоторых случаях к гипофизарному нанизму могут приводить черепно-мозговые травмы, родовые травмы, повреждение ножки гипофиза при хирургических вмешательствах,
- Прочих церебральных заболеваниях:нейроинфекциях (вирусные, бактериальные энцефалиты и менингиты), аутоиммунном гипофизите, гидроцефалии, аневризмах сосудов гипофиза и т. д.
- Токсическом поражением гипофиза. Гипофизарный нанизм может быть связан с токсическими последствиями химиотерапии или облучения (при лейкемии, ретинобластоме, пересадке костного мозга и т. д.).
3. Гипофизарный нанизм вследствие нечувствительности тканей-мишеней к гормону роста может развиваться при дефиците СТГ-рецепторов, отсутствии биологической активности соматотропного гормона, резистентности к инсулиноподобному фактору роста 1.
Наряду с изолированной недостаточностью СТГ, при гипофизарном нанизме может отмечаться снижение синтеза других гормонов гипофиза: гонадотропинов, ТТГ, АКТГ, что сопровождается недостаточностью функции соответствующих периферических эндокринных желез (половых, щитовидной, надпочечников), что также влияет на рост и физическое развитие. В этом случае в эндокринологии говорят о пангипопитуитарной форме карликовости.
Классификация
Различают нанизм с пропорциональным и непропорциональным телосложением. К группе заболеваний с пропорциональным телосложением относят:
- гипофизарный нанизм
- микседематозный (тиреогенный) нанизм
- надпочечниковый нанизм при адреногенитальном синдроме (врожденной гиперплазии надпочечников)
- нанизм, связанный с поражением вилочковой железы
- инфантильный нанизм, развивающийся под влиянием экзогенных факторов (алиментарной недостаточности или интоксикации)
- нанизм, связанный с преждевременным половым созреванием и ранним закрытием зон роста.
Нанизм с непропорциональным телосложением представлен следующими формами:
- рахитической
- хондродистрофической
- карликовостью при несовершенном остеогенезе (врожденной ломкости костей).
От случаев нанизма следует отличать семейные (конституциональные) формы низкорослости, которые рассматриваются как вариант индивидуального физического развития и не являются патологией.
Симптомы гипофизарного нанизма
Дети рождаются с нормальными весо-ростовыми показателями. Задержка роста при врожденном гипофизарном нанизме обычно становится заметна к возрасту 2-3 лет и в дальнейшем нарастает. Скорость роста у детей с гипофизарным нанизмом составляет 1,5-2 см в год (при норме - 7-8 см). У взрослых мужчин рост не превышает 130 см, у женщин - 120 см. Телосложение пропорциональное, однако могут сохраняться пропорции, свойственные детскому возрасту.
Кожные покровы у пациентов с гипофизарным нанизмом бледные, сухие, морщинистые, с желтоватым или мраморным оттенком, что обусловлено тиреоидной недостаточностью. Волосы на голове часто тонкие, сухие, ломкие. Недоразвитие костей лицевого черепа обусловливает наличие мелких черт лица («кукольное лицо»), западение переносицы.
Распределение подкожно-жировой клетчатки может быть различным - от слабого развития до избыточного отложения жира по «кушингоидному» типу (на груди, животе, бедрах). Отмечается задержка окостенения скелета, слабое развитие мышечной системы, нарушение смены зубов. Из-за недоразвития гортани у взрослых с гипофизарным нанизмом сохраняется высокий детский тембр голоса. В соответствии с низким ростом и массой тела отмечается уменьшение размеров внутренних органов (спланхномикрия). Нередко при гипофизарном нанизме выявляется брадикардия и артериальная гипотензия.
Нарушение гонадотропной функции гипофиза приводит к задержке и неполноценности полового развития (гипогонадизму). У юношей с гипофизарным нанизмом наблюдается отсутствие оволосения по мужскому типу, гипоплазия яичек, крипторхизм, микропенис; у девушек - аменорея, микромастия, гипоплазия матки и яичников.
Интеллектуальное развитие при гипофизарном нанизме, как правило, сохранно. Могут отмечаться такие психологические особенности, как негативизм, замкнутость, снижение самооценки, инфантильное поведение. При наличии дополнительных жалоб на головную боль, рвоту, нарушение зрения следует заподозрить внутричерепную патологию. При пангипопитуитарном нанизме определяются признаки вторичного гипокортицизма и гипотиреоза.
Диагностика
Критериями диагностики гипофизарного нанизма служат данные анамнеза, объективного обследования, лабораторных и инструментальных исследований. У пациентов определяются абсолютные размеры тела, а также показатель дефицита роста - разница между фактическим ростом больного и средними нормативными половозрастными показателями в популяции. При гипофизарном нанизме дефицит роста составляет более чем 2-3 квадратичных отклонения.
Основная роль при диагностике гипофизарного нанизма принадлежит определению базального уровня СТГ в сыворотке крови, циркадного ритма секреции и резервов на фоне стимуляции. У пациентов с гипофизарным нанизмом исходный уровень СТГ значительно снижен, при проведении стимулирующих тестов с инсулином, тиреолиберином, аргинином и др. повышается незначительно.
Рентгенография турецкого седла выявляет его детскую форму («стоячий овал») и широкую (т. н. ювенильную) спинку. При увеличении размеров турецкого седла и наличии участков обызвествления, в первую очередь, следует думать об опухоли. Рентгенография лучезапястных суставов и кистей позволяет определить рентгенологический («костный») возраст. При гипофизарном нанизме отмечается значительное замедление процессов окостенения скелета.
Для выяснения формы нанизма необходимо исследование инсулиноподобного фактора роста (соматомедина-С), ТТГ, ЛГ, ФСГ, Т3, Т4, кортизола в плазме и моче, антител к тиреоглобулину, микросомальной фракции тироцитов и др. Для исключения опухолевого поражения проводится КТ (МРТ) головного мозга.
При гипофизарном нанизме пациент должен быть проконсультирован эндокринологом, гинекологом (женщины), андрологом (мужчины), неврологом или нейрохирургом, офтальмологом, генетиком.
Лечение гипофизарного нанизма
У детей младшего возраста для исключения диагностических ошибок на протяжении 6-12 мес. выдерживают период наблюдения, во время которого особое внимание уделяется полноценному питанию, общеукрепляющей терапии, приему витаминов (А и D) и минералов (фосфора, кальция). Отсутствие динамики роста и физического развития является основанием для перехода к гормонотерапии.
Основу патогенетического лечения гипофизарного нанизма составляет заместительная терапия препаратами гормона роста, которая проводится прерывистыми курсами (по 2-3 мес. с такими же интервалами). Соматотропин человека назначается пациентам с доказанной эндогенной недостаточностью гормона и дифференцировкой скелета, не превышающей возрастных показателей 13-14 лет. Лечение с помощью СТГ проводится до закрытия зон роста или до достижения приемлемых ростовых параметров.
В терапии гипофизарного нанизма применяются анаболические стероиды (метандиенон, нандролон), оказывающие стимулирующее действие на уровень эндогенного СТГ, синтез белков и рост. Лечение стероидными гормонами продолжается несколько лет с периодической заменой препаратов. Лечение анаболическими средствами целесообразно начинать с 5-7 лет. Для стимуляции функции половых желез в возрасте старше 16 лет юношам назначается хорионический гонадотропин и малые дозы андрогенов, девушкам - малые дозы эстрогенов.
В дальнейшем, после закрытия зон роста, пациентов с гипофизарным нанизмом переводят на постоянный прием половых гормонов в соответствии половой принадлежностью. При этом женщинам показан прием комбинированных эстрогенгестагенных препаратов, мужчинам - андрогенов пролонгированного действия.
При гипотиреозе назначается L-тироксин, тиреоидин; при недостаточности соматолиберина - его синтетические аналоги; при гипофункции коры надпочечников - глюкокортикостероиды. При органической патологии ЦНС может потребоваться противовоспалительная, рассасывающая, дегидратационная терапия. В случае выявления опухолей гипофиза показано их хирургическое удаление, иногда - проведение лучевой терапии.
Прогноз и профилактика
При гипофизарном нанизме, обусловленном генетическими причинами, прогноз хороший. Своевременная и рациональная ЗГТ позволяет пациентам быть в достаточной степени физически развитыми, социально активными и трудоспособными. При выборе профессии не рекомендуется работа, предусматривающая повышенные физические и нервно-психические нагрузки. При отсутствии необходимого лечения у пациентов остается малый рост и физическое недоразвитие. В случае органических поражений мозга прогноз определяется основным заболеванием и динамикой его развития.
Пациенты с гипофизарным нанизмом находятся на пожизненном диспансерном учете у эндокринолога и должны посещать его каждые 2-3 месяца. Профилактика гипофизарного нанизма заключается в предупреждении инфекций, физических и психических травм у беременных; недопущении родовых травм, нейроинфекций, ЧМТ, интоксикаций у детей.
Гигантизм
Гигантизм - патологическая высокорослость, обусловленная чрезмерной выработкой гормона роста (соматотропного гормона) передней долей гипофиза и проявляющаяся уже в детском возрасте. Наблюдается увеличение роста свыше 2 м, непропорциональность телосложения с преимущественным удлинением конечностей, при этом голова кажется очень маленькой. У больных наблюдается расстройство физического и психического состояния, половой функции. При гигантизме трудоспособность ограничена, высок риск бесплодия. Основным диагностическим критерием гигантизма, помимо яркой клинической картины, является выявление повышения СТГ в крови.
Гигантизм (или макросомия) развивается у детей с незавершенными процессами окостенения скелета, чаще встречается у подростков мужского пола, определяется уже в возрасте 9-13 лет и прогрессирует на протяжении всего периода физиологического роста. При гигантизме скорость роста ребенка и его показатели намного превышают анатомо-физиологическую норму и к концу пубертатного периода достигают более 1,9 м у женщин и 2 м у мужчин при сохранении относительно пропорционального телосложения. Частота встречаемости гигантизма составляет от 1 до 3 случаев на 1000 населения.
Родители пациентов, страдающих данной патологией, обычно нормального роста. Гигантизм следует дифференцировать с наследственной высокорослостью.
Классификация гигантизма
Современная эндокринология выделяет следующие варианты развития гигантизма:
- Акромегалический - гигантизм с признаками акромегалии;
- спланхномегалия или гигантизм внутренних органов - сопровождается увеличением размеров и массы внутренних органов;
- евнухоидный - гигантизм у пациентов с гипогонадизмом (гипофункцией или полным прекращением функций половых желез), проявляется непропорционально удлиненными конечностями, открытыми зонами роста в суставах, отсутствием вторичных половых признаков;
- истинный - характеризуется пропорциональным увеличением размеров тела и отсутствием отклонений со стороны физиологических и психических функций;
- парциальный или частичный - гигантизм с увеличением отдельных частей тела;
- половинный - гигантизм, сопровождающийся увеличением одной половины туловища;
- церебральный - гигантизм, вызванный органическим поражением головного мозга и сопровождающийся нарушением интеллекта.
Причины гигантизма
Гигантизм и акромегалия являются двумя возрастными вариациями одних и тех же патологических процессов: гиперплазии и гиперфункции клеток гипофиза, продуцирующего соматотропный гормон (гормон роста). Повышенная секреция гормона роста может наблюдаться при поражениях гипофиза в результате опухолей железы (аденомы гипофиза), интоксикации, нейроинфекций (энцефалита, менингита, менингоэнцефалита), черепно-мозговых травм.
Нередко причиной гигантизма служит понижение чувствительности эпифизарных хрящей, обеспечивающих рост костей в длину, к воздействию половых гормонов. В результате этого кости долго сохраняют способность увеличения в длину, даже в постпубертатном периоде. Гиперсекреция соматотропина после закрытия зон роста костей и завершения окостенения скелета приводит к акромегалии.
Симптомы гигантизма
Скачок увеличения длины тела при гигантизме происходит в 10-15 лет. Пациенты отличаются высоким ростом и темпами его увеличения, жалуются на быструю утомляемость и слабость, головокружения, головные боли, ухудшение зрения, боли в суставах и костях. Снижение памяти и работоспособности ведет к ухудшению успеваемости в школе. Гигантизм характеризуется гормональными нарушениями, расстройством психической и половой функции (инфантилизм). У женщин при гигантизме развивается первичная аменорея или раннее прекращение менструальной функции, бесплодие, у мужчин - гипогонадизм. Другими гормональными проявлениями гигантизма служат несахарный диабет, гипо- или гипертиреоз, сахарный диабет. Отмечается сначала увеличение мышечной силы, а затем мышечная слабость и астения.
При гигантизме возможно развитие артериальной гипертензии, миокардиодистрофии, сердечной недостаточности, эмфиземы легких, дистрофических изменений печени, бесплодия, сахарного диабета, нарушений функции щитовидной железы.
Диагностика гигантизма
Диагноз гигантизма устанавливается на основании внешнего осмотра пациента, результатов лабораторных, рентгенологических, неврологических и офтальмологических исследований. При гигантизме лабораторно определяется высокое содержание СТГ в крови.
Для выявления опухолей гипофиза проводится рентгенография черепа, КТ и МРТ головного мозга. При наличии аденомы гипофиза определяется увеличенное турецкое седло (ложе гипофиза). Рентгенограммы кистей рук показывают несоответствие между костным и паспортным возрастом. При офтальмологическом обследовании пациентов с гигантизмом выявляется ограничение зрительных полей, застойные явления в глазном дне.
Лечение гигантизма
Принципы лечения гигантизма аналогичны лечению акромегалии. Для нормализации уровня гормона роста при гигантизме применяются аналоги соматостатина, для более быстрого закрытия зон роста костей - половые гормоны. Этиологическое лечение гигантизма при аденомах гипофиза предусматривает применение лучевой терапии или их оперативное удаление в сочетании с медикаментозной поддержкой агонистами дофамина.
При евнухоидном типе гигантизма лечение направлено на устранение полового инфантилизма, ускорение окостенения скелета и прекращение его дальнейшего роста. Лечение частичного гигантизма включает ортопедическую коррекцию при помощи пластических операций. Применяемое эндокринологами комбинированное лечение гигантизма сочетает гормональную и лучевую терапию и позволяет добиться положительных результатов у значительного числа пациентов.
Прогноз и профилактика гигантизма
При адекватной терапии гигантизма прогноз для жизни относительно благоприятный. Однако, многие пациенты не доживают до старости и погибают от осложнений заболевания. Большинство пациентов, страдающих гигантизмом, бесплодны, их трудоспособность резко снижена.
Обеспокоенность родителей должно вызывать резкое, значительное увеличение роста ребенка в период полового созревания по сравнению с его сверстниками. Своевременное медицинское вмешательство позволит предотвратить осложнения.
Гипофизарный нанизм (карликовость) - симптомы и лечение
Что такое гипофизарный нанизм (карликовость)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Скворцовой Ольги Викторовны, детского эндокринолога со стажем в 9 лет.
Над статьей доктора Скворцовой Ольги Викторовны работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина
Определение болезни. Причины заболевания
Гипофизарный нанизм, или гипопитуитаризм — это заболевание, при котором частично или полностью прекращается выработка гормона роста — соматотропина (соматотропного гормона) [1] . Оно сопровождается нарушением роста скелета, из-за чего мужчины не вырастают выше 130 см, а женщины — выше 120 см. В связи с этим характерным проявлением болезнь также называют карликовостью.
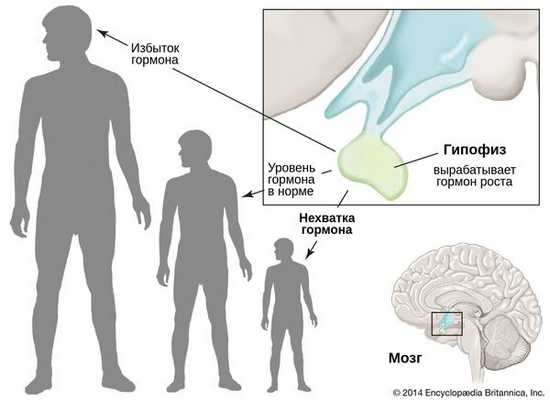
Наиболее частые причины гипофизарного нанизма:
- Наследственность — мутации в гене соматотропного гормона (GH1) или его рецепторах. Частота встречаемости врождённого гипопитуитаризма колеблется от 1:4000 до 1:10000 [5] .
- Дефекты развития гипоталамо-гипофизарной системы — области головного мозга, где вырабатывается соматотропный гормон:
- гипоплазия (недоразвитие) гипофиза;
- полное отсутствие гипофиза. При этом дефицит гормона роста сочетается с нехваткой других гормонов, которые вырабатываются в гипофизе. Такое состояние называется пангипопитуитаризмом. Оно проявляется надпочечниковой недостаточностью, ухудшением работы щитовидной железы (гипотиреозом), несахарным диабетом, гипогонадотропным гипогонадизмом (отсутствием полового развития и дефицитом гормона роста).
- Опухоли гипофиза:
- краниофарингиома — доброкачественная опухоль гипофизарной области, одна из самых распространённых в детском возрасте;
- гамартома — редкий вид доброкачественной опухоли;
- герминома — редкий вид опухоли, чаще всего бывает злокачественной — и др.
- Травмы головного мозга с повреждением гипофиза, возникшие до того, как человек достиг социально приемлемого роста — 155-170 см (например, родовая травма).
- Инфекционные заболевания — менингиты, энцефалиты и др.
- Облучение головы и шеи.
- Токсические последствия химиотерапии.
Теоретически, спровоцировать развитие гипофизарного нанизма может любое заболевание, которое будет затрагивать работу гипофиза.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Гипофизарный нанизм проявляется по-разному. Симптоматика зависит от причин дефицита гормона роста.
Основной симптом — отставание в темпах линейного роста [2] . Такие дети вырастают менее чем на 4 см в год. Нарушение динамики роста будет заметно уже в первые месяцы жизни ребёнка. Если повреждение гипоталамуса или гипофиза возникло в более позднем возрасте, то отставание в росте будет отмечаться позднее. Также для детей с гипофизарным нанизмом характерно отставание костного (биологического) возраста от паспортного (фактического) более чем на 2-3 года.
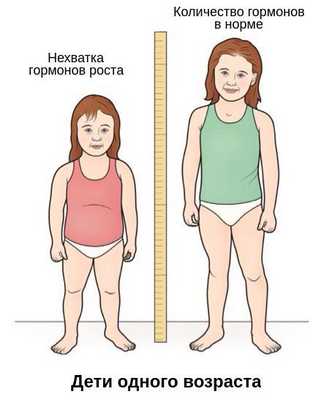
При нехватке гормонов роста телосложение остаётся пропорциональным. Это важный диагностический критерий: он позволяет исключить разные формы скелетных дисплазий [9] .
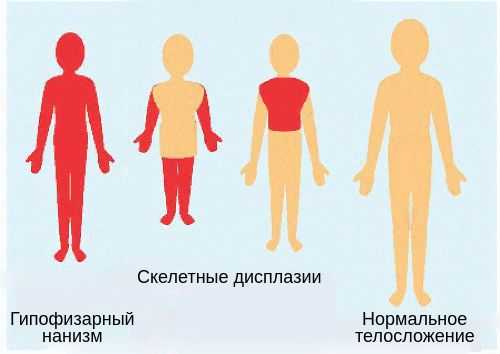
Симптомами врождённого гипофизарного нанизма у новорождённых являются:
- гипогликемия — низкий уровень глюкозы в крови натощак. Это физиологическое состояние может встречаться и у здоровых детей из-за незрелости поджелудочной железы. Дети с нанизмом сталкиваются с ним гораздо чаще, особенно на первом году жизни, поскольку гормон роста участвует в регуляции углеводного обмена;
- позднее закрытие большого родничка;
- задержка костного созревания;
- истончение кожи — может быть связано со снижением функции щитовидной железы;
- медленный рост ногтей и волос;
- высокий голос.
Часто у детей с гипопитуитаризмом встречается множественный кариес зубов. Это объясняется задержкой окостенения скелета и снижением обменных процессов в костной ткани.
Психоинтеллектуальное развитие у детей с гипофизарным нанизмом, как правило, не страдает, но возможны некоторые психологические проблемы: повышенная потребность в родительской опеке, снижение самооценки, трудности в общении со сверстниками.
Патогенез гипофизарного нанизма
В зависимости от причин дефицита соматотропного гормона есть несколько вариантов механизмов развития заболевания. При этом в основе патогенеза всегда будет лежать нарушение выработки гормона роста. В дальнейшем его нехватка станет причиной нарушения работы органов и систем, на которые он оказывает влияние: костной, мышечной и соединительной ткани, жирового углеводного обмена. В некоторых случаях первоначально будут развиваться гипоталамические нарушения, а недостаточность соматотропного гормона станет вторичным проявлением.
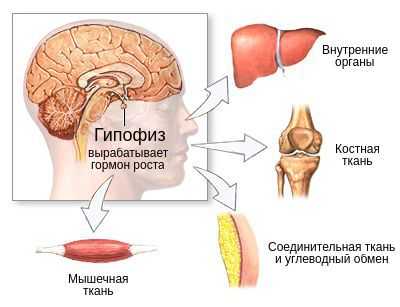
Молекулярной основой изолированного дефицита гормона роста является мутация определённого гена, которая не даёт организму синтезировать гормон. От видов генетических мутаций зависит, будет ли дефицит соматотропного гормона изолированным, или же он будет сочетаться с нехваткой других гормонов гипофиза, которые лежат в основе других патологий:
- дефицит тиреотропного гормона — вторичный гипотиреоз;
- дефицит пролактина — гипопролактинемия;
- дефицит гонадотропинов — аменорея и недоразвитие половых органов у женщин, снижение потенции и либидо у мужчин;
- дефицит АКТГ — вторичная недостаточность надпочечников;
- дефицит вазопрессина — несахарный диабет;
- дефицит кортизола — гипокортицизм.
У некоторых пациентов с мутацией конкретных генов выявляется гиперплазия передней доли гипофиза (аденогипофиза). В процессе жизни может произойти её атрофия вплоть до формирования синдрома "пустого турецкого седла" — недостаточности области головного мозга, где расположен гипофиз. Данный синдром приводит к внедрению мягкой мозговой оболочки в полость турецкого седла, сдавлению и уменьшению гипофиза, что нарушает или полностью прекращает его работу.
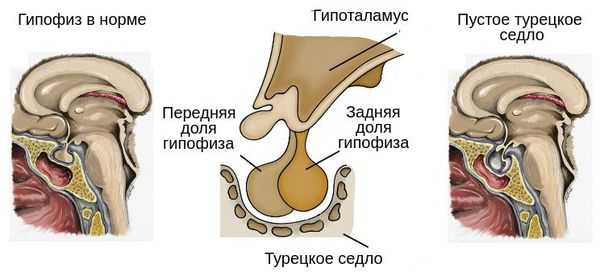
В подобных случаях дефицит гормона роста и других гормонов гипофиза будет возникать постепенно [3] .
Классификация и стадии развития гипофизарного нанизма
Единой, общепринятой классификации гипофизарного нанизма не существует. Наиболее удобной для практикующих врачей является классификация, основанная на причинах заболевания. Она выделяет две большие группы: врождённый и приобретённый гипопитуитаризм [4] .
Врождённый гипофизарный нанизм делится на три подгруппы:
- Наследственный:
- изолированный дефицит гормона роста: мутации гена самого гормона (GH1) или мутации гена рецептора к соматотропину (GHRHR);
- множественный дефицит гормонов передней доли гипофиза: мутации гена PIT-1 или гена PROP1.
- Идиопатический (незафисимый) дефицит СТГ-релизинг гормонов, которые стимулируют выработку гормонов передней доли гипофиза.
- Дефекты развития гипоталамо-гипофизарной системы:
- патология срединной трубки;
- нарушение развития гипофиза: врождённая аплазия (отсутствие гипофиза), гипоплазия (недоразвитие), эктопия (неправильное расположение).
Приобретённый гипофизарный нанизм включает в себя девять причин развития болезни:
- Опухоли гипоталамуса и гипофиза: краниофарингиома, гамартома, нейрофиброма, герминома, аденома гипофиза.
- Опухоли других отделов мозга: глиома зрительного перекреста.
- Травмы: черепно-мозговая, хирургическое повреждение ножки гипофиза.
- Инфекционные заболевания: вирусный, бактериальный энцефалит и менингит, неспецифический гипофизит (воспаление гипофиза).
- Супраселлярные арахноидальные кисты — полые опухоли, заполненные жидкостью (ликвором), которые распространяются в полость черепа.
- Сосудистые нарушения: аневризмы сосудов гипофиза, инфаркт гипофиза.
- Облучение головы и шеи по поводу лейкемии, медуллобластомы, ретинобластомы; общее облучение всего тела (при пересадке костного мозга).
- Токсические последствия химиотерапии.
- Инфильтративные болезни: саркоидоз, гистиоцитоз.
Осложнения гипофизарного нанизма
Осложнения заболевания связаны с утратой воздействия гормона роста на органы и системы. Они развиваются вследствие несвоевременной диагностики.
У новорождённого с дефицитом соматотропина относительную опасность может представлять гипогликемическое состояние, поскольку этот гормон играет важную роль в регуляции углеводного обмена. Клинически гипогликемия проявляется бледностью, потливостью, повышенным аппетитом, беспокойством ребёнка, иногда наблюдается судорожный синдром [5] .

Так как сомтатотропин усиливает синтез белка и тормозит его распад, у детей с дефицитом этого гормона может снизиться уровень общего белка в организме и его фракций. Это сказывается на общем физическом развитии: снижается иммунитет, повышается риск присоединения других гормональных сопутствующих нарушений.
Значительная часть эффектов гормона роста передаётся через ИПФР-I (инсулиноподобный фактор роста-I). Он вырабатывается в печени под действием соматотропина и стимулирует рост внутренних органов. Вследствие дефицита соматотропного гормона рост и своевременное развитие органов может частично нарушиться. Это приводит к нарушению работы печени, почек, сердечно-сосудистой системы. Такое осложнение встречается нечасто.
При дефиците гормона роста совместно с другими гормонами гипофиза (пангипопитуитаризме) будет развиваться недостаточность других эндокринных желёз — щитовидной железы, надпочечников, репродуктивной системы. Несвоевременная диагностика этих нарушений после рождения опасна для жизни, а также может стать причиной необратимым нарушений психического или интеллектуального развития.
Диагностика гипофизарного нанизма
Диагностика заболевания начинается с оценки линейного роста ребёнка и скорости прибавки в росте. Для этого врачи сравнивают фактические параметры ребёнка с предполагаемым ростом и среднестатистической скоростью роста. Подставив все данные в специальную формулу, они вычисляют коэффициент стандартного отклонения. Если у ребёнка отставание в росте больше двух сигмальных отклонений, плохая скорость прибавки роста, то проводится дальнейшее обследование.
Затем врачи определяют костный возраст. Сделать это можно с помощью рентгена или УЗИ запястья. В норме костный возраст может отставать или опережать паспортный на два года.
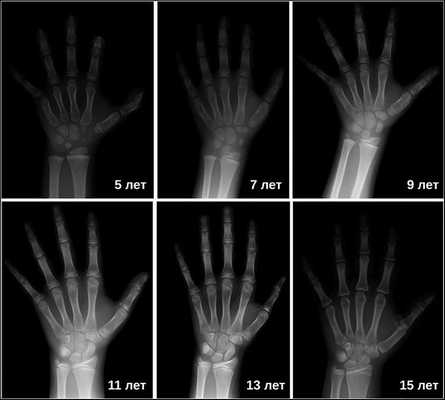
Также важно провести оценку гормонального профиля:
- уровень тиреотропного гормона (ТТГ) и свободного тироксина (Т4) — проверка работы щитовидной железы;
- уровень кортизола и АКТГ (кортикотропина) — исключение нарушений работы надпочечников [10] ;
- уровень лютеинизирующего гормона (ЛГ) и фоллитропина (ФСГ) — исключение гипогонадотропного гипогонадизма в возрасте, когда должно начаться половое созревание;
- инсулиноподобный фактор роста-I (ИПФР-I) — оценка уровня гормона роста.
Прямая оценка уровня соматотропина, как правило, не проводится. Гормон роста в течение суток выделяется в разном количестве, поэтому узнать его истинный уровень невозможно.
При необходимости проводится МРТ головного мозга и гипофиза с контрастированием [6] . Она позволяет исключить или подтвердить наличие объёмных образований области гипофиза и головного мозга.
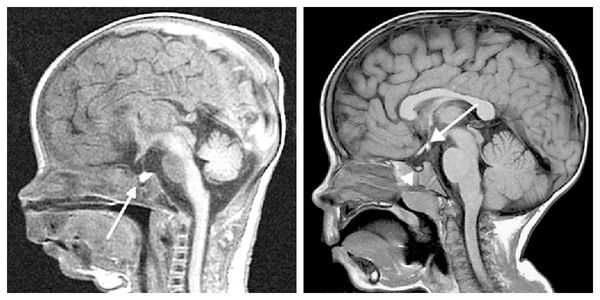
Для дифференциальной диагностики задержки роста, не связанной с гормоном роста, исключают дефицит железа, дефицит витамина D, общего белка и другие дефицитные состояния, т. к. их наличие может отрицательно влиять на скорость линейного роста. Рентгенография черепа в данном случае не информативна.
Для исключения определённых генетических синдромов может потребоваться консультация генетика.
При подозрении на истинный дефицит гормона роста проводятся пробы на стимуляцию соматотропина. Эти провокационные тесты стимулируют выброс гормона роста при введении определённых препаратов. Они проводятся только после исключения других возможных причин низкорослости. На основании этих проб, при отсутствии должного выброса гормона роста, будет установлен диагноз "гипопитуитаризм".
Лечение проводится рекомбинантным гормоном роста, который получают методом генной инженерии. Он назначается после исключения активных злокачественных новообразований и тяжёлых сопутствующих заболеваний (как физических, так и психических). Эти состояния являются противопоказанием к использованию данного препарата.
Если имеются другие дефициты гормонов гипофиза, то перед лечением их также нужно компенсировать. Иначе должного эффекта от применения гормона роста не будет.
Цели лечения:
- ускорить темп роста и нормализовать рост;
- стимулировать начало периода полового созревания с нормальным ростом;
- достичь генетически прогнозируемого роста ребёнка или опередить его;
- улучшить качество жизни;
- повысить минеральную плотность костей;
- снизить факторы риска сердечно-сосудистых заболеваний.
Противопоказания к назначению рекомбинантным гормоном роста:
- закрытые зоны роста, за счёт которых происходит линейный рост (при их закрытии человек перестаёт расти);
- активные злокачественные новообразования;
- прогрессирующий рост внутричерепных опухолей;
- аллергия на препарат.
Прекращают терапию гормоном роста при:
- закрытии зон роста;
- плохой скорости прибавки роста — менее 2 см в год;
- достижении социально приемлемого роста.
Крайне редко возможны побочные эффекты и осложнения при терапии гормоном роста:
- доброкачественная внутричерепная гипертензия — повышение внутричерепного давления;
- боли в суставах — обычно наблюдаются при значительном ускорении линейного роста;
- возможно усугубление заболеваний, связанных с недифференцированными дисплазиями соединительной ткани (сколиозов);
- отёки — связано с функцией гормона роста задерживать жидкости в организме;
- пубертатная гинекомастия — увеличение грудных желёз за счёт разрастания железистой ткани у мальчиков [7] .
Прогноз. Профилактика
Прогноз заболевания при своевременной диагностике и проведении должного лечения, как правило, благоприятный. Дети достигают своего генетически прогнозируемого роста и иногда даже опережают его.
Если дефицит гормона роста сочетается с дефицитом других гормонов гипофиза, то для достижения желаемого эффекта, профилактики ухудшения состояний и более лёгкой социальной адаптации ребёнка необходимо лечение других дефицитов.
Также очень важен чёткий и своевременный контроль во время лечения гормоном роста: оценка динамики линейного роста, гормонального статуса и костного возраста. Особое внимание необходимо уделять режиму лечения и своевременной коррекции дозы препарата с учётом прибавки в росте и весе. При применении соматотропного гормона доза препарата будет увеличиваться. При несвоевременной прибавке дозы динамика роста может ухудшится [8] .
Мониторинг детей, находящихся на лечении, проводится раз в полгода, при других сопутствующих дефицитах гормонов гипофиза — по показаниям.
Вопрос профилактики данного заболевания сложен, т. к. речь идёт о генетических нарушениях. В первую очередь важен ответственный подход будущих родителей к рождению ребёнка:
- своевременное обследование и лечение заболеваний;
- восполнение дефицитов при планировании беременности;
- отказ от вредных привычек.
Для профилактики дефицита гормона роста, который возникает вследствие другого заболевания (инфекции, опухоли, травмы), следует проводить профилактики первоисточника.
Карликовый, или маленький рост
Диагностику начинают с опроса и оценки роста родителей пациента. Проводят антропометрические измерения (роста, веса и т.д.) и оценивают половое развитие. Определяют костный возраст ребенка, используя рентгенографию.
Рентгенологическое исследование черепа для выявления нарушений структуры и целостности костей черепа различной природы.
Читайте также:
