Сроки развития узлов метахронного множественного рака. Течение метахронного рака ЖКТ
Добавил пользователь Владимир З. Обновлено: 22.01.2026
Скоропад В.Ю., Рагулин Ю.А., Рухадзе Г.О., Неборак Ю.Т.
ФГБУ Медицинский Радиологический научный центр Минздрава России, Обнинск, Россия
Первое описание первично-множественных опухолей было дано в 1793 г. английским хирургом Джоном Пирсоном, наблюдавшим больную раком обеих молочных желез и раком тела матки. Первично-множественными злокачественными новообразованиями принято считать опухоли двух и более локализаций, развившиеся в одном организме.
Критерии, сформулированные S. Warren, O. Gates еще в 1932 г., следующие: (1) злокачественный характер каждой опухоли должен быть подтвержден морфологически; (2) опухоли должны быть расположены раздельно; (3) возможность того, что вторая опухоль является метастазом первой, должна быть исключена. По времени возникновения опухоли делятся на синхронные (выявленные одновременно или в срок до 6 мес.) и метахронные.
В настоящее время первично-множественные опухоли не являются казуистической редкостью. Их частота постоянно возрастает, что связано с достижениями хирургии и развитием комбинированных методов лечения, внедрением новейших диагностических технологий, увеличением продолжительности жизни больных, а также влиянием неблагоприятных факторов окружающей среды.
По данным В.И. Чиссова и соавт. [1], число больных с первично-множественными опухолями среди больных с впервые в жизни установленным диагнозом злокачественного новообразования в России имеет неуклонную тенденцию к росту. Так, в 2011 г. были впервые выявлены 24774 первично-множественные опухоли (17,5 на 100000 населения), что составило 4,7% от всех впервые выявленных злокачественных новообразований (в 2010 г. - 2,8%, в 2000 г. - 1,9%).
В то же время, авторы отметили, что в хорошо сбалансированных отчетах данный показатель достигает 10% и подчеркнули, что этот раздел онкологии приобретает все большую актуальность и остроту. В структуре первично-множественных опухолей, новообразования желудочно-кишечного тракта занимают одно из ведущих мест [2, 3].
Б-ая В., 1953 г.р., жительница города Обнинска, по профессии экономист. Онкологические заболевания у ближайших родственников отрицает. Вредные привычки и вредные производственные факторы отсутствуют. Поступила в МРНЦ 22.11.2004 с жалобами на тупую боль в эпигастрии, тошноту, снижение аппетита.
Считает себя больной в течение последнего месяца. При эзофагогастродуоденоскопии в теле желудка выявлена блюдцеобразная опухоль, исходящая из передней стенки и малой кривизны. Проксимальный край опухоли расположен в 3 см от кардии. Взята биопсия, морфологическое заключение: аденокарцинома G1.
По данным СКТ: опухоль нижней трети тела и антрального отдела желудка с признаками изъязвления; данных за поражение регионарных лимфатических узлов не получено.
03.12.2004 выполнено оперативное вмешательство в объеме гастрэктомии D2. При ревизии выявлена опухоль тела желудка, прорастающая серозную оболочку, к ней подпаян большой сальник. Гистологическое исследование №29144-64: макроскопически на малой кривизне желудка изъязвленная блюдцеобразная опухоль 6 см в диаметре, прорастающая в малый сальник.
Микроскопически: аденокарцинома G2 (Рисунок 1), прорастающая все слои стенки желудка и жировую клетчатку. В краях резекции и исследованных 10 лимфатических узлах признаков опухоли не обнаружено. Заключительный диагноз: рак тела желудка T4аN0M0G2 - 2B стадия. Послеоперационный период без осложнений. Выписана в удовлетворительном состоянии на 13-е сутки после операции.
В последующем больная проходила регулярные обследования в МРНЦ амбулаторно и в стационарных условиях. Производились физикальный осмотр, ФГС, УЗИ брюшной полости и малого таза, рентгенологическое исследование легких, общий и биохимический анализы крови, анализ крови на опухолевые маркеры (CA19-9, CEA, CA125). Данных за рецидив заболевания получено не было.
19.02.2006 была госпитализирована в МРНЦ с жалобами на наличие образования внизу живота, которое больная отмечала у себя в течение последнего месяца с тенденцией к росту. При пальпации над лоном, преимущественно слева, определяется болезненное объемное опухолевидное образование.
Проведено обследование: при ФГС данных за рецидив рака желудка не получено; по данным рентгенологического исследования легких патологических изменений не выявлено. При УЗИ обнаружено образование левого яичника, преимущественно кистозной структуры, размерами 11х12х13 см, с инвазией в тело матки и аналогичное по структуре образование правого яичника 2,6х3,3 см.
В малом тазу умеренное количество свободной жидкости. Больная консультирована гинекологом. Случай расценен как метастатическое поражение яичников (метастазы Крукенберга).
28.02.2006 выполнена операция: надвлагалищная ампутация матки с придатками. При ревизии в брюшной полости до 500,0 мл серозной асцитической жидкости. Брюшина не изменена. Левый яичник кистозно изменен, увеличен в размерах до 12 см, правый яичник также кистозно изменен, увеличен до 5 см, инфильтрация распространяется на боковую поверхность матки.
Гистологическое исследование: в обоих яичниках на фоне пограничной муцинозной цистаденомы высокодифференцированная муцинозная аденокарцинома (Рисунок 2). В матке на серозной оболочке с инвазией в миометрий инфильтративный рост высокодифференцированной аденокарциномы.
Высказаться однозначно о гистогенезе рака не представляется возможным, вероятнее всего, это муцинозный рак яичников, однако возможно и метастатическое поражение.
Для уточнения характера поражения яичников проведено иммуногистохимическое исследование с антителами фирмы DAKO на парафиновых срезах операционных препаратов опухоли желудка (1) и яичников (2). Результаты: Выявлена диффузная яркая экспрессия СК7, СК20, СЕА; очаговая экспрессия muc5AC, слабая очаговая экспрессия CDX2, виллин; негативная экспрессия muc2.
Заключение: первичный иммунофенотип аденокарциномы желудка. Выявлена диффузная экспрессия СК7, СК20, СЕА, CDX2; виллин; незначительная очаговая экспрессия СА125, СА19-9. Выявлена негативная экспрессия рецепторов ER, PR, Wilms tumor, виментин. Заключение: иммунофенотип метастаза аденокарциномы желудка в яичнике.
В послеоперационном периоде проведено 4 курса химиотерапии по схеме FOLFOX 4. Перенесла тяжело, с токсическими явлениями 3 степени, от продолжения химиотерапии отказалась.
В конце января 2007 г. проведено очередное амбулаторное обследование в МРНЦ. При СКТ брюшной полости с контрастным усилением (Ультравист 300-50,0) в 4 сегменте печени выявлен округлый участок пониженной плотности с четкими контурами, не накапливающий РКВ, до 8 мм в диаметре.
Увеличенных лимфатических узлов в брюшной полости и забрюшинном пространстве не определяется. Заключение: КТ-картина солитарного очагового образования печени, рекомендован КТ-контроль в динамике.
В течение февраля 2007 г. обследована в различных специализированных онкологических учреждениях г. Москвы. По данным УЗИ: структура печени неоднородна. По нижнему краю 4-5 сегментов определяются метастатические узлы до 2,5 см, сливающиеся в конгломерат до 6,5х4,0х4,7 см. В поддиафрагмальных отделах правой доли узел до 2,0 см.
По данным МРТ: печень не увеличена. В паренхиме (в обеих долях) определяются метастазы 0,4-3,5 см в диаметре. В правой доле печени конгломерат узлов достигает 7,6х3,7 см. Метастатические узлы определяются также на брюшине. Асцита нет. Заключение: Метастатическое поражение печени, брюшины.
В течение марта 2007 г. больная за лечебной помощью не обращалась.
В начале апреля 2007 г. выполнены УЗИ и МРТ печени. УЗИ: печень умеренно увеличена, с неровными контурами. В обеих долях лоцируется несколько изоэхогенных узловых образований различного диаметра, с нечеткими границами, плохо выраженными анэхогенными венчиками, неправильной округлой формы. В 4 и 5 сегментах - большой опухолевый конгломерат аналогичной эхоструктуры, наибольший размер которого превышает 7,0 см.
В правой мезогастральной области - опухолевидное образование диаметром до 4,0 см, прорастающее прилежащий участок передней брюшной стенки. Заключение: множественные метастазы в печени, образования брюшной полости (вероятно, метастатического характера). Выполнена чрескожная пункционная биопсия образования брюшной полости. Гистологическое заключение: в биоптате на фоне выраженного фиброза фокусы клеток недифференцированного рака.
МРТ печени: печень увеличена в размерах. В правой доле печени на границе 5 и 6 сегментов определяется неправильной формы участок с нечеткими, неровными контурами, повышенной интенсивности сигнала на Т2-взвешенных изображениях и пониженной интенсивности сигнала на Т1-взвешенных изображениях, размерами 30х57х34 мм.
Справа от него определяется аналогичный участок размерами 27х23х23 мм. В 6 и 7 сегментах печени - аналогичные участки размерами 34х23х30 мм, 15х13х16 мм и 30х31х38 мм. Два аналогичных более мелких (1-15 мм) участка определяются в 7 сегменте печени. Заключение: МР картина множественных метастазов в печени.
С апреля по декабрь 2007 г. в различных специализированных медицинских учреждениях Москвы, Калуги и Обнинска проведено 9 курсов системной и регионарной внутриартериальной химиотерапии по схеме: кампто 400 мг, гемзар 1400 мг, карбоплатин 450 мг (в последних курсах заменен на элоксатин 100 мг); митомицин 10 мг - эмболизация печеночной артерии в 12 мг липойодола (первые два курса). Отмечалась лихорадка до 38,6о и лейкопения 3 ст., проводили стимуляцию нейпогеном.
В течение периода лечения отмечалась постоянная положительная динамика как по данным опухолевых маркеров (Рисунок 3), так и по данным УЗИ печени. В сентябре 2007 г. по данным УЗИ: в правой и левой долях печени с большим трудом лоцируется несколько очагов с нечеткими границами, без анэхогенных венчиков. В декабре 2007 г. по данным УЗИ очаговых образований в печени не выявлено.
В апреле 2009 г. получала лечение по поводу лекарственного гепатита препаратом гептрал (5,0 внутривенно №15).
С 2009 по 2011 г. больная регулярно наблюдалась в МРНЦ, проводили физикальное обследование, УЗИ брюшной полости и малого таза, анализы на опухолевые маркеры. Данных за рецидив получено не было.
В начале февраля 2012 г. больная обратилась в МРНЦ с жалобами на схваткообразные боли в эпигастрии, периодическую задержку стула и газов. При обследовании (УЗИ, СКТ брюшной полости, колоноскопия) выявлена стенозирующая опухоль восходящего отдела ободочной кишки. На СКТ органов грудной полости обнаружено очаговое образование в S3 правого легкого с неровными, нечеткими контурами, размером 15х13мм. Заключение: очаговое образование в S3 правого легкого.
Необходимо дифференцировать между метастатическим очагом и периферическим раком легкого. 14.02.2012 на фоне нарастающей клиники толстокишечной непроходимости выполнена операция: правосторонняя гемиколэктомия. При ревизии: в брюшной полости - выраженный спаечный процесс; данных за отдаленные метастазы не получено; после разделения спаек выявлена стенозирующая опухоль восходящего отдела ободочной кишки. Послеоперационный период без осложнений.
Гистологическое заключение: аденокарцинома G1, прорастающая в мышечный слой (Рисунок 4) и врастающая в прилежащую жировую клетчатку. В жировой клетчатке в проекции опухоли - одиночный раковый депозит. Лимфатические узлы и края отсечения без признаков опухоли. Заключительный диагноз: рак восходящего отдела ободочной кишки T3N0M0G1. Больная выписана в удовлетворительном состоянии 24 февраля 2012 г., рекомендована явка для дообследования и оперативного лечения опухоли легкого.
07.03.2012 была госпитализирована в торакальное отделение МРНЦ. При поступлении общее состояние удовлетворительное, жалобы на умеренную слабость. 20.03.2012 выполнена видеоторакоскопическая резекция опухоли верхней доли правого легкого. При ревизии - опухоль размером 2х1,5 см., прорастающая висцеральную плевру. Гистологическое заключение: сосочковая аденокарцинома G2 из эпителия сегментарного бронха с перибронхиальным ростом и множественными отсевами в ткань легкого - вероятно, первичный рак легкого (Рисунок 5).
Учитывая мультицентричность поражения, наличие опухолевых сателлитов в удаленной ткани легкого, вероятность опухолевой диссеминации в оставшейся части резецированной доли решено выполнить верхнюю лобэктомию справа. Проведение оперативного вмешательства данного объема позволяло уточнить распространенность процесса и обеспечить радикализм в случае выявления первичного рака легкого. 03.04.2012 выполнена операция: торакотомия, верхняя лобэктомия справа, медиастинальная лимфаденэктомия.
Гистологическое заключение: ткань легкого обычного строения, обнаружен единичный опухолевый эмбол в лимфатическом сосуде; 13 лимфатических узлов и край резекции долевого бронха без признаков опухолевого роста. Послеоперационный период без осложнений. Выписана на 10 сутки после операции в удовлетворительном состоянии.
Для уточнения характера поражения легкого проведено иммуногистохимическое исследование с антителами фирмы DAKO на парафиновых срезах операционных препаратов опухоли толстой кишки (1) и легкого (2). Результаты: (1) Выявлена диффузная яркая экспрессия СК20, CDX2; muc5AC; диффузная менее выраженная экспрессия СЕА, СК7; слабо выраженная экспрессия виллин. Выявлена негативная экспрессия muc2. Заключение: первичный иммунофенотип аденокарциномы толстой кишки.
(2) Выявлена диффузная экспрессия СЕА, CKLMW, CKHMW, CD2, CK7, CK20, виллин, muc5AC. Выявлена негативная экспрессия рецепторов ER, PR; TTF1, VEGF, muc2. Заключение: иммунофенотип метастаза аденокарциномы толстой кишки в легком.
Данное наблюдение представляет интерес в связи с успешным лечением больной первично-множественным раком желудка и ободочной кишки, имевшим метахронные (в первом случае) и синхронные (во втором случае) метастазы. Безусловно, дифференциальная диагностика между полинеоплазиями и метастазами представляет значительные трудности. Особенно она сложна, если новообразования имеют характерные для метастазов локализации - яичники, печень, легкие. В этих случаях даже наличие операционного/биопсийного материала и стандартного морфологического исследования является недостаточным для постановки истинного диагноза.
В таких случаях необходимо проведение иммуногистохимического исследования, поскольку характер опухоли - первичный либо метастатический - определяет дальнейшую тактику лечения. К сожалению, очень высок процент выявления вторых опухолей на поздних стадиях заболевания, что говорит о необходимости применения активного диагностического алгоритма, для чего, в свою очередь, необходимы соответствующие исследования с целью более полного понимания закономерностей развития полинеоплазий.
Представленное наблюдение обосновывает необходимость придерживаться активной тактики лечения больных первично-множественными злокачественными опухолями даже при наличии отдаленных метастазов.
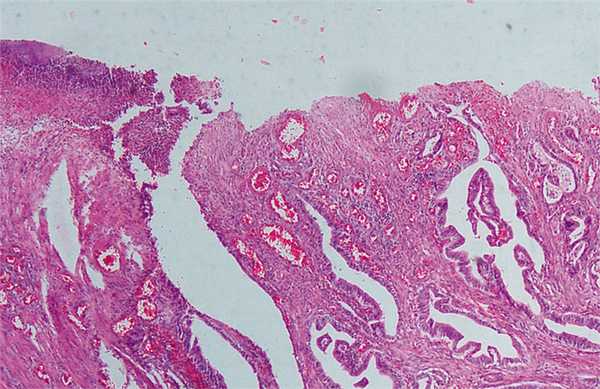
Рисунок 1. Изъязвленная умереннодифференцированная аденокарцинома желудка.
Окраска гематоксилином и эозином, х40.
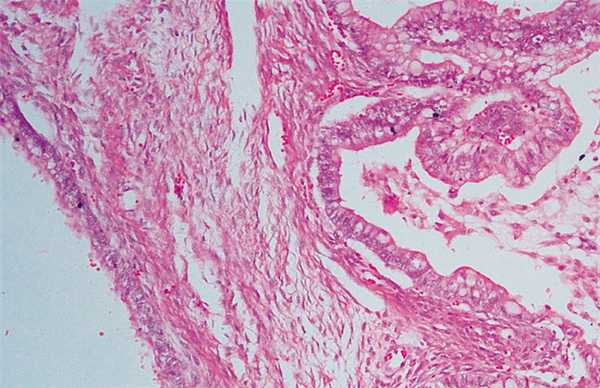
Рисунок 2. Метастаз рака желудка в яичнике. Окраска гематоксилином и эозином, х100.
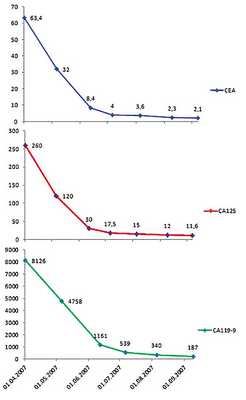
Рисунок 3. Динамика опухолевых маркеров в процессе проведения химиотерапии.
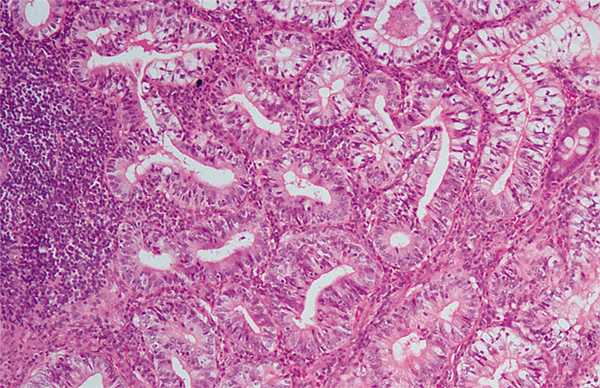
Рисунок 4. Высокодифференцированная ааденокарцинома восходящего отдела ободочной кишки.
Окраска гематоксилином и эозином, Х100.
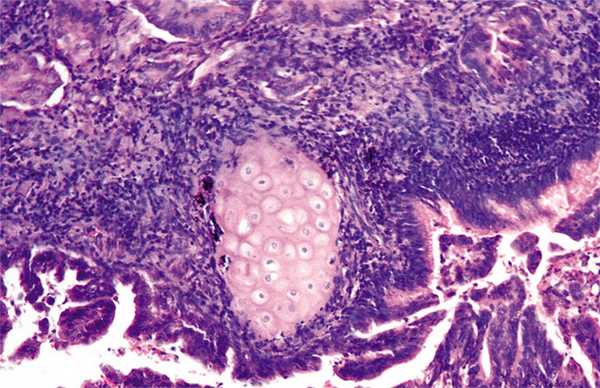
Рисунок 5. Метастаз рака толстой кишки в легкое. Окраска гематоксилином и эозином, Х100.
Ключевые слова: первично-множественный рак; рак желудка; рак ободочной кишки; хирургическое лечение; комбинированное лечение.
- Состояние онкологической помощи населению России в 2011 году. Под ред. В.И. Чиссова, В.В. Старинского, Г.В. Петровой. М.: 2012.
- Первично-множественные злокачественные опухоли. Под ред. В.И. Чиссова, А.Х. Трахтенберга. М.: 2000; 233-41.
- Полинеоплазии у больных ранним раком желудка. Скоропад В.Ю., Бердов Б.А. Российский онкологический журнал. 2008; 1: 10-3.
Согласен Данный веб-сайт содержит информацию для специалистов в области медицины. В соответствии с действующим законодательством доступ к такой информации может быть предоставлен только медицинским и фармацевтическим работникам. Нажимая «Согласен», вы подтверждаете, что являетесь медицинским или фармацевтическим работником и берете на себя ответственность за последствия, вызванные возможным нарушением указанного ограничения. Информация на данном сайте не должна использоваться пациентами для самостоятельной диагностики и лечения и не может быть заменой очной консультации врача.
Сроки развития узлов метахронного множественного рака. Течение метахронного рака ЖКТ
Ростовский научно-исследовательский онкологический институт Минздрава РФ
Ростовский научно-исследовательский онкологический институт, Ростов-на-Дону, Россия
ФГБУ «Ростовский научно-исследовательский онкологический институт» Минздрава России, Ростов-на-Дону, Россия
Первично-множественный колоректальный рак: клинические аспекты
Резюме Цель исследования. Определить некоторые клинические особенности синхронного и метахронного колоректального рака (КРР). Материалы и методы. Объектом исследования послужили данные о 150 больных первично-множественным КРР T1-4N0-2M0-1. Проведен анализ клинических, биологических, морфологических особенностей синхронных и метахронных опухолей. Результаты. Первично-множественные опухоли составили 6,01% от всех форм КРР. Преобладал синхронный КРР (63,75%) с локализацией опухоли в сигмовидной и прямой кишке. Синхронные колоректальные опухоли у женщин чаще сочетались с раком молочной железы, метахронные выявлялись после лечения опухолей половых органов. У мужчин синхронные колоректальные опухоли чаще сочетались с раком почки, метахронные выявлялись после лечения рака желудка. Заключение. Выявленные особенности первично-множественных колоректальных опухолей возможно учитывать в программах как первичной диагностики, так и диспансерного наблюдения после лечения больных со злокачественными опухолями, что позволит улучшить раннее выявление и результаты лечения онкологических больных.
КРР - колоректальный рак
МКО - метахронная колоректальная опухоль
Проблема колоректального рака (КРР) на протяжении нескольких десятилетий продолжает оставаться актуальной, что обусловлено как ростом заболеваемости, так и прогрессивными достижениями в лечении [1]. Наряду с увеличением общей онкологической заболеваемости наблюдается увеличение заболеваемости первично-множественными опухолями толстой и прямой кишки [2], которые в настоящее время составляют 17% от всех первично-множественных злокачественных новообразований и являются одной из наиболее частых локализаций первично-множественных злокачественных опухолей после первично-множественного рака кожи [3, 4].
В настоящее время проводится изучение как клинических, так и онкобиологических аспектов первичной множественности опухолей толстой и прямой кишки 6, тем не менее многие аспекты в этой проблеме остаются открытыми, что и побудило нас коснуться некоторых вопросов первично-множественного КРР.
Цель исследования: определить некоторые клинические особенности синхронного и метахронного КРР.
Материалы и методы
Из 2497 больных КРР T1-4N0-M0-1, подвергшихся хирургическому лечению в клинике ФГБУ «РНИОИ» МЗ РФ за последние 5 лет, первично-множественный рак выявлен у 150 (6,01%), данные о которых мы и использовали для анализа. Статистическую обработку результатов выполняли с применением пакетов программ Microsoft Excel 2010 и Statistica 8.0. Оценку различий проводили с использованием критерия χ 2 , статистически значимыми считали различия при р
Результаты
Анализ клинических проявлений первично-множественного КРР показал, что отдельные симптомы многообразны и соответствуют таковым при одиночной опухоли толстой или прямой кишки. Известно, что при локализации опухоли в правой половине ободочной кишки это чаще всего хроническая анемия, нарушение общего состояния (слабость, похудание), кишечный дискомфорт (снижение аппетита, чувство тяжести в верхней половине живота, иногда рвота через несколько часов после еды), боли в животе и наличие пальпируемой опухоли. При локализации опухоли в левой половине ободочной кишки преобладают: кишечные расстройства (запоры, поносы и их чередование), патологические выделения (кровь, слизь) при дефекации. При локализации опухоли в прямой кишке основными симптомами являются тенезмы, выделение крови и слизи при дефекации, боли в прямой кишке.
При синхронных колоректальных опухолях наблюдаются симптомы, соответствующие локализации опухоли в кишке. Так, анемия в течение нескольких лет, пальпируемая опухоль в правой подвздошной области и тенезмы свидетельствуют о синхронной опухоли слепой и прямой кишки. Оценка клинической картины заболевания с обязательным обследованием всех отделов толстой и прямой кишки позволят выявить синхронный КРР и избежать диагностических ошибок. В большинстве случаев нераспознанной синхронная колоректальная опухоль остается в случае, если в связи со стенозирующим характером дистальной опухоли эндоскоп не проходит в проксимальные отделы кишки и не позволяет произвести их осмотр. Об этом следует помнить, и в таких случаях производить дополнительное обследование вышележащих отделов толстой кишки (это может быть исследование пассажа бария по кишке, спиральная рентгеновская компьютерная томография органов брюшной полости и малого таза с пероральным контрастированием).
Следует отметить возможность развития одновременно опухоли колоректальной локализации и других органов. В этом плане важным является наличие в клинической картине симптомов, не характерных для КРР, даже если диагноз уже установлен. При этом следует продолжить обследование больного для исключения опухоли другой локализации. Анализ преимущественного поражения других органов синхронным раком будет произведен далее.
В случае метахронного развития опухолей как толстой и прямой кишки, так и других органов после излечения КРР диагностика не вызывает особых трудностей. Это связано с регулярной диспансеризацией и обследованием излеченных больных, приводящей к своевременной постановке диагноза.
Оценка частоты проявления симптомов заболевания показала, что при одиночном КРР преобладали боли (60%), кровь в кале (56,7%) и запоры (46,7%). При синхронных колоректальных опухолях наиболее частыми симптомами были боль (56,7%), слабость (53,3%) и похудание (40%). При метахронном КРР в клинической картине преобладали слабость (63,6%) и боль (56,7%) (табл. 1).
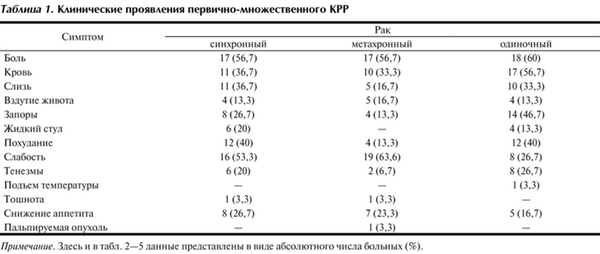
Таблица 1. Клинические проявления первично-множественного КРР Примечание. Здесь и в табл. 2-5 данные представлены в виде абсолютного числа больных (%).
В нашем исследовании время от появления первых клинических симптомов до момента обращения в специализированный онкологический стационар у больных одиночным раком составило преимущественно 6-12 мес (40% больных), а первично-множественным раком - 2-3 мес (48,3% больных).
Среди больных первично-множественным КРР синхронные и метахронные опухоли, локализующиеся только в толстой и прямой кишке, выявлены у 80 (53,3%). В этой группе больных преобладал синхронный КРР - 51 (63,75%) больной. Средний возраст пациентов составил 62,9 года. Преобладали мужчины - 32 (62,75%), средний возраст 63,2 года, женщин 19 (37,25%), средний возраст 62,5 года. Локализация синхронных опухолей в толстой и прямой кишке представлена в табл. 2. Согласно представленным данным синхронные опухоли преимущественно локализовались в сигмовидной (у 32 больных, 62,75%) и прямой кишке (у 29 больных, 56,86%). При этом сочетание опухолей в прямой и сигмовидной кишке выявлено у (35,29%). Половые различия по локализации синхронных опухолей в толстой и прямой кишке отсутствовали.

Таблица 2. Локализация синхронных опухолей в толстой и прямой кишке Примечание. Здесь и в табл. 3-5 * - различия между подгруппами достоверны (р<0,05).
У 34 (66,67%) мужчин и женщин распространение синхронных колоректальных опухолей ограничено только кишкой, без регионарных и отдаленных метастазов. Опухоли с регионарными метастазами имелись у 11 (21,57%) больных, с отдаленными - у 6 (11,76%). Распределение синхронных колоректальных опухолей по гистологической структуре свидетельствует о преобладании синхронных умереннодифференцированных аденокарцином (у 25, 49,02%), в основном у мужчин (у 17, 53,13%). У женщин часто встречались и слизеобразующие аденокарциномы (у 6, 31,58%).
Таким образом, синхронные опухоли составили 34% от всего первично-множественного КРР. Средний возраст больных достигал 62,9 года. Среди заболевших преобладали мужчины (62,75%). Синхронные опухоли преимущественно локализовались в сигмовидной (62,75%) и прямой кишке (56,86%), представлены в основном умереннодифференцированными аденокарциномами (49,02%), без регионарных и отдаленных метастазов (66,67%).
Метахронный КРР среди первично-множественного рака с локализацией опухолей только в толстой и прямой кишке выявлен у 29 (36,25%) больных (средний возраст 64,7 года). В этой группе было 16 (55,17%) женщин (средний возраст 66,9 года). Метахронная колоректальная опухоль (МКО) выявлена у них в среднем через 8,3 года после выявления первой опухоли. Среди больных метахронным первично-множественным КРР было 13 (44,83%) мужчин (средний возраст 62,5 года), метахронная опухоль выявлена у них в среднем через 4,5 года после первой опухоли.
Данные по локализации метахронных опухолей в толстой и прямой кишке отражены в табл. 3, представляющей распределение по локализации опухоли в следующем порядке: прямая кишка (51,72%, 15 больных), сигмовидная и правая половина ободочной кишки (по 48,28%, 14 больных), левая половина ободочной кишки (37,93%, 11 больных). В группе больных метахронным первично-множественным КРР наблюдались половые различия по локализации опухоли. Так, у женщин метахронные опухоли чаще локализовались в правой половине ободочной кишки - у 9 (56,25%) и прямой кишке - у 8 (50%). У мужчин МКО преимущественно локализовались в прямой и сигмовидной кишке - по 7 (53,85%) больных.

Таблица 3. Локализация метахронных опухолей в толстой и прямой кишке
У 14 (48,28%) больных распространение МКО ограничено только кишкой, без регионарных и отдаленных метастазов. Статистически значимых половых различий МКО по стадии TNM мы не наблюдали. Распределение МКО по гистологической структуре свидетельствует о значительном преобладании метахронных умереннодифференцированных аденокарцином - у 22 (75,86%) больных, как у мужчин, так и у женщин.
Итак, метахронный КРР составил 19,33% от всего первично-множественного рака толстой и прямой кишки. Средний возраст больных достигал 69,9 года, женщины были на 4 года старше мужчин. Среди заболевших было одинаковое число мужчин и женщин. Интервал между первой и последующей колоректальной опухолью у женщин в 2 раза больше (8,31 года), чем у мужчин (4,5 года). Метахронные опухоли у женщин преимущественно локализовались в правой половине ободочной кишки (56,25%) и прямой кишке (50%), у мужчин - в прямой и сигмовидной кишке (по 53,85%). МКО представлены в основном умереннодифференцированными аденокарциномами (75,86%), без регионарных и отдаленных метастазов (48,28%).
Среди больных первично-множественным КРР синхронные и метахронные опухоли, локализующиеся помимо толстой или прямой кишки, также в других органах, выявлены у 70 (46,7%). В этой группе синхронный первично-множественный рак наблюдался у 26 (37,14%) больных. Средний возраст пациентов составил 67,1 года. Женщин и мужчин было поровну - по 13 больных. Женщины на 7 лет моложе мужчин (63,6 и 70,5 года соответственно).
Локализация синхронных первично-множественных опухолей представлена в табл. 4, из которой видно, что синхронные колоректальные опухоли у женщин чаще сочетались с опухолями гениталий - у 8 (61,5%), причем у 5 - с раком молочной железы. У половины 7 (53,8%) мужчин синхронный КРР сочетался с опухолями мочевыделительной системы, причем у 6 из них - с раком почки.
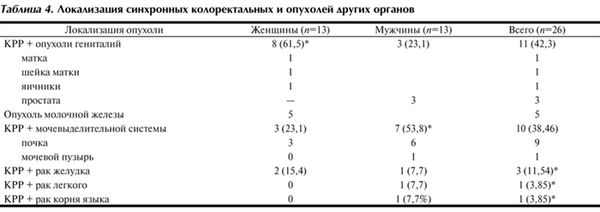
Таблица 4. Локализация синхронных колоректальных и опухолей других органов
У 65,4% больных опухоль была местно-распространенной, с наличием регионарных метастазов у одной из опухолей. Статистически значимых половых различий по стадии TNM синхронных колоректальных опухолей и других локализаций рака мы не наблюдали.
Распределение синхронных колоректальных опухолей при наличии и другой локализации рака по гистологической структуре свидетельствует о значительном преобладании синхронных умереннодифференцированных аденокарцином (80,8%) у мужчин и женщин.
Итак, синхронный КРР с другими локализациями опухолей составил лишь 17,33% от всего первично-множественного рака толстой и прямой кишки. Средний возраст больных достигал 67,1 года, женщины были на 7 лет моложе мужчин. Среди заболевших было одинаковое число женщин и мужчин. Синхронные колоректальные опухоли у женщин чаще сочетались с раком молочной железы. У мужчин синхронный КРР чаще сочетался с раком почки. Синхронные колоректальные опухоли представлены в основном умереннодифференцированными аденокарциномами (80,8%), местно-распространенными, с наличием регионарных метастазов (65,4%).
Метахронный КРР после лечения первой опухоли, локализующейся в других органах, составил 44 (29,33%) случая среди первично-множественных КРР и 62,86% среди первично-множественного КРР, сочетающегося с опухолями других органов. Средний возраст больных достигал 65,1 года. В этой группе больных было 24 (54,55%) женщины (средний возраст 61,3 года) и 20 (45,45%) мужчин (средний возраст 69 лет) на 8 лет старше женщин. Среднее время выявления МКО после лечения опухоли другой локализации у женщин составило 5,7 года, у мужчин - 4,4 года.
Локализация метахронных первично-множественных опухолей показана в табл. 5. Согласно представленным данным МКО у женщин чаще сочетались с опухолями половых органов - у 19 (79,23%), преимущественно матки и молочной железы. У мужчин метахронный КРР чаще сочетался с раком желудка - у 11 (55%).
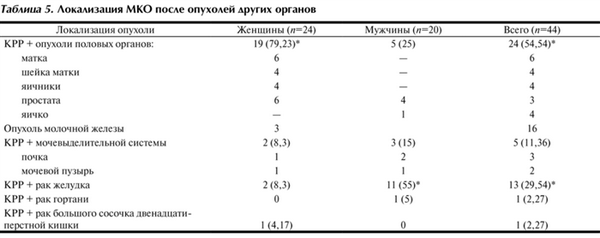
Таблица 5. Локализация МКО после опухолей других органов
28 (63,6%) больных имели местно-распространенную форму МКО и других локализаций рака, без отдаленных метастазов. Половые различия при этом отсутствовали.
Распределение МКО при наличии и другой локализации рака свидетельствует о значительном преобладании метахронных умеренно дифференцированных аденокарцином у мужчин и женщин - 33 (75%) больных.
Итак, метахронный КРР с другими локализациями опухолей составил 29,33% от всего первично-множественного рака толстой и прямой кишки. Средний возраст больных достигал 65,1 года, женщины на 8 лет моложе мужчин. Среди заболевших одинаковое число женщин и мужчин. Среднее время выявления МКО после лечения опухоли другой локализации у женщин составило 5,7 года, у мужчин - 4,4 года. МКО у женщин преимущественно выявлялись после лечения опухолей половых органов (79,23%). У мужчин метахронный КРР чаще наблюдался после лечения рака желудка (55%). МКО представлены в основном умереннодифференцированными аденокарциномами (75%), местно-распространенными, без отдаленных метастазов (63,64%).
Заключение
Клиническая картина первично-множественного КРР характеризуется наличием симптомов, не свойственных только одной локализации рака. Это обусловливает необходимость расширения диагностического поиска для исключения синхронной опухоли. При этом более выраженное клиническое проявление симптомов первично-множественного заболевания приводит к уменьшению до 3 мес сроков от появления клинической картины недуга до обращения за специализированной помощью у большинства больных (50% больных синхронным и 70% больных метахронным раком). В этот срок при одиночном КРР обращаются лишь 30% больных.
Диагностика метахронных опухолей облегчается наличием диспансеризации и регулярного обследования больных после излечения первой опухоли.
Первично-множественный КРР с локализацией опухолей только в толстой и прямой кишке составил 53,33% от всех форм первично-множественного КРР. В этой группе больных преобладал синхронный КРР (63,75%), которым заболевают чаще в 62,9 года, несколько чаще мужчины (62,75%). Синхронные опухоли преимущественно локализовались в сигмовидной (62,75%) и прямой кишке (56,86%). Средний возраст больных при выявлении МКО был старше, чем синхронных - 69,9 года. Интервал между выявлением первой и последующей колоректальной опухоли у женщин был в 2 раза больше, чем у мужчин (8,3 и 4,5 года соответственно). Метахронные опухоли у женщин преимущественно локализовались в правой половине ободочной кишки (56,25%) и прямой кишке (50%), у мужчин - в прямой и сигмовидной кишке (по 53,85%).
Если КРР выявлялся одновременно с опухолями других органов, то средний возраст больных (67,1 года) был на 4,2 года больше, чем при выявлении синхронного КРР, а женщины при выявлении опухолей на 7 лет моложе мужчин. Синхронные колоректальные опухоли у женщин чаще сочетались с раком молочной железы, у мужчин - с раком почки. Выявление колоректальной опухоли после лечения опухоли другой локализации наблюдается примерно в том же возрасте, что и синхронное (65,1 года), но несколько чаще, чем их одновременное выявление (62,86%). МКО у мужчин выявлялась в среднем через 4,4 г, чаще после лечения рака желудка (55%). У женщин колоректальная опухоль выявлялась в среднем через 5,7 года, преимущественно после лечения опухолей половых органов (79,17%).
Все первично-множественные колоректальные опухоли представлены в основном умереннодифференцированными аденокарциномами (как наиболее распространенного гистологического типа колоректальной опухоли), местно-распространенными, без отдаленных метастазов (возможно, в связи с тем что больные отобраны для хирургического лечения). Преобладание при первично-множественном КРР, сочетающемся с опухолями других органов, регионарных метастазов, возможно, свидетельствует о его более агрессивном течении по сравнению с другими видами первично-множественных колоректальных опухолей.
Выявленные особенности первично-множественных колоректальных опухолей можно учитывать в программах как первичной диагностики, так и диспансерного наблюдения после лечения больных со злокачественными опухолями, что позволит улучшить раннее выявление и результаты лечения больных с первично-множественными опухолями.
Рак толстой кишки и желудка — наиболее распространенные злокачественные новообразования в мире наряду с раком легких, молочной железы и простаты [1].
Синхронным считается рак, который возникает в течение 6 мес после впервые выявленного рака, тогда как метахронный рак — это рак, который диагностируют по крайней мере через 6 мес после впервые выявленного рака [2].
Вторичные очаги при синхронном раке встречаются наиболее часто, в то время как рецидивные опухоли и их метастазы относительно редки [3].
По данным литературы, частота множественных синхронных новообразований варьирует от 2 до 17% [4].
Материал и методы
Представлены 2 наблюдения пациентов с местнораспространенным осложненным раком желудка, поступивших в клинику последовательно и без предварительного отбора. Помимо стандартного сбора анамнеза, анализов крови и клинического обследования, включавшего ЭГДС, МСКТ и рентгенографию, пациентам проведена фиброколоноскопия.
Клинический случай 1
Больной А., 80 лет, поступил в клинику с жалобами на тошноту, рвоту съеденной пищей, снижение массы тела на 10 кг за последние 2 мес, головокружение, слабость. По данным комплексного обследования у больного диагностирован первично-множественный синхронный рак: рак тела и антрального отдела желудка (гистологически — умеренно-дифференцированная аденокарцинома), осложненный субкомпенсированным опухолевым стенозом выходного отдела желудка и рецидивирующим кровотечением из опухоли (Hb 63 г/л); рак слепой кишки (гистологически — умеренно-дифференцированная аденокарцинома) (рис. 1). Из сопутствующих заболеваний у больного гипертоническая болезнь III стадии, III степень, риск сердечно-сосудистых осложнений 4, постоянная форма фибрилляции предсердий, имплантация электрокардиостимулятора Zephyr DR в 2010 г., радиочастотная абляция АВ-соединения, неустойчивый пароксизм желудочковой тахикардии. Хроническая сердечная недостаточность IIA стадии, III функуциональный класс.
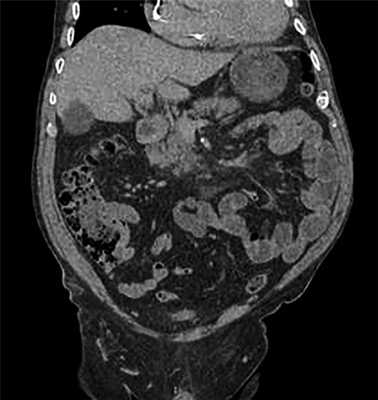
Рис. 1. МСК-томограмма органов брюшной полости больного А.

Рис. 2. Фотография удаленного органокомплекса больного А., состоящего из дистального отдела желудка с опухолью, большого и малого сальников, правой половины толстой кишки с регионарными лимфатическими узлами.
Клинический случай 2
Больная Д., 61 год, поступила в клинику с жалобами на затруднение прохождения твердой и жидкой пищи по пищеводу, снижение массы тела на 18 кг за 6 мес, слабость, утомляемость. По данным комплексного обследования диагностирован первично-множественный синхронный рак: рак пищеводно-желудочного перехода (рис. 3), осложненный дисфагией и рецидивирующим кровотечением из опухоли (Hb 87 г/л); гистологически — умеренно-дифференцированная аденокарцинома; аденокарцинома толстой кишки in situ. Сопутствующие заболевания: гипертоническая болезнь I стадии, II степень. Хроническая сердечная недостаточность II стадии, II ФК по NYHA. Синусовая тахикардия. Хроническая болезнь почек — С3а. Гиперлипидемия. Облитерирующий атеросклероз сосудов нижних конечностей. Хроническая венозная недостаточность нижних конечностей.
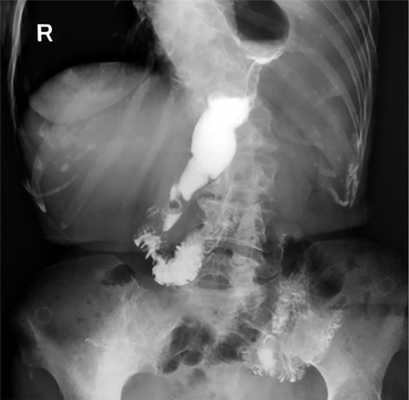
Рис. 3. Рентгенограмма пищевода и желудка больной Д. с кардио-эзофагеальным раком.
Рис. 4. Послеоперационная рентгенограмма пищевода и культи желудка больной Д., перенесшей проксимальную резекцию желудка с абдоминальным отделом пищевода.
Рис. 5. Фотография макропрепарата после проксимальной резекции желудка с абдоминальным отделом пищевода.
Патоморфологическое заключение: аденокарцинома кардиального отдела желудка G2, pT4aN1M0 стадия IIIA, опухоль в толстой кишке соответствует карциноме in situ на фоне тубулярно-ворсинчатой аденомы, pTisN0M0.
У пациентов с раком желудка повышен риск развития синхронной опухоли. Кроме того, 80% всех больных раком желудка с вторичным очагом синхронного рака — мужчины [2]. В настоящее время не существует однозначных рекомендаций по лечению первично-множественных синхронных форм злокачественной опухоли. Наиболее распространенным подходом является операция, ассоциированная с адъювантным лечением. При резектабельных первично-множественных синхронных новообразованиях предпочтительным является радикальное хирургическое вмешательство с химиотерапией или без нее [5].
Доказана целесообразность проведения фиброколоноскопии в плане предоперационного обследования у пациентов с раком желудка [6].
Тщательное предоперационное обследование пациентов с раком желудка с целью выявления возможно имеющегося синхронного колоректального рака, особенно пожилых, дает возможность лечить оба рака одновременно, улучшая прогноз и качество жизни этих больных [7—10].
В представленных клинических случаях адекватное предоперационное обследование пациентов с местно-распространенным осложненным раком желудка позволило выявить синхронный рак толстой кишки и провести эндовидеохирургические симультанные оперативные вмешательства у больных старшей возрастной группы с наличием сопутствующих заболеванияй, а также способствовало быстрой послеоперационной реабилитации и более раннему началу курса адъювантной химиотерапии.
Проведение фиброколоноскопии в предоперационном периоде способствует своевременному выявлению синхронного колоректального рака, улучшая, таким образом, результаты лечения и качество жизни пациентов.
ЧОУ ВО «Санкт-Петербургский медико-социальный институт»;
ГБУЗ «Санкт-Петербургский клинический научно-практический центр специализированных видов медицинской помощи (онкологический)»
ГБУЗ «Санкт-Петербургский клинический научно-практический центр специализированных видов медицинской помощи (онкологический)»
ЧОУ ВО «Санкт-Петербургский медико-социальный институт»;
ГБУЗ «Санкт-Петербургский клинический научно-практический центр специализированных видов медицинской помощи (онкологический)»;
ФГБВОУ ВО «Военно-медицинская академия им. С.М. Кирова» Министерства обороны России
Оценка метастатического потенциала локализованных форм колоректального рака
Журнал: Архив патологии. 2021;83(5): 5‑12
ЦЕЛЬ ИССЛЕДОВАНИЯ
Оценка риска рецидива после хирургического лечения является неотъемлемой частью ведения пациентов с колоректальным раком. Обычно используется категориальная система стадирования TNM AJCC/UICC, в которой риск определяется путем группирования пациентов на основе анатомических признаков. Несмотря на простоту реализации, внутри каждой стадийной группы остается значительная неоднородность. В эпоху мультимодального лечения необходим более совершенный инструмент для прогнозирования рецидива.
МАТЕРИАЛ И МЕТОДЫ
Выполнен ретроспективный анализ 1350 архивных случаев колоректального рака за период с 2012 по 2015 г., из числа которых были отобраны три группы пациентов: 1-я (n=53) с неметастатическим раком толстой кишки в течение как минимум 5-летнего периода, во 2-ю группу (n=45) вошли случаи с метахронными метастазами, выявленными в течение того же периода, и в 3-ю (n=53) — с синхронными метастазами. С помощью многомерного анализа из оцениваемого 31 параметра были выбраны 6 наиболее значимых прогностических факторов, вошедших в итоговую модель, построенную на основе логистического регрессионного анализа. Полученная модель была использована для оценки риска метастазирования после циторедуктивной операции. Модель прошла внутреннюю и внешнюю валидацию с помощью экзаменационной группы (n=25).
РЕЗУЛЬТАТЫ
Модель имеет чувствительность 97,78% и специфичность 96,23%, улучшая стратификацию риска метастазирования аденокарцином толстой кишки. Факторы в модели включают: экстрамуральную венозную инвазию, выраженность почкования, экспрессию E-кадгерина и β-катенина, долю цитотоксических CD8+ лимфоцитов из общего числа T-лимфоцитов в микроокружении, соотношение новообразованных сосудов к плотности микрососудов в опухолевой строме.
ЗАКЛЮЧЕНИЕ
Используя патоморфологические факторы, при помощи полученной модели можно лучше учесть особенности опухоли у конкретного пациента и тем самым обеспечить более индивидуальный прогноз исхода, чем тот, который предоставляется категориальной системой TNM AJCC/UICC. За счет идентификации пациентов как с высоким, так и с низким риском метастазирования модель может быть полезной в планировании лечения и выборе клинической тактики ведения пациентов с колоректальным раком.
Дата принятия в печать:
По данным мировой статистики, колоректальный рак является 3-м по распространенности онкологическим заболеванием у мужчин и 2-м — у женщин. В России он занимает 2-е место по частоте после опухолей желудка, при этом прирост составляет более 40 тыс. новых случаев ежегодно [1]. Хирургическая резекция — основа лечения пациентов с локализованным неметастатическим заболеванием, адъювантная химиотерапия может снизить риск рецидива на 40—50% у пациентов из группы высокого риска [2, 3]. Однако существующие схемы химиотерапии имеют значительные неблагоприятные эффекты. У подавляющего большинства пациентов появляются признаки периферической нейропатии, а у 40% пациентов наблюдается 3-я или 4-я степень нейтропении [2, 3]. Следовательно, признаки, позволяющие предсказывать рецидив, могли бы оказать значительную помощь онкологам с определением тактики ведения пациентов и целесообразности назначения адъювантной химиотерапии. В настоящее время золотым стандартом оценки риска неблагоприятных исходов при новообразованиях толстой кишки является система стадирования опухолей TNM, принятая по оригинальной схеме, разработанной еще более 75 лет назад C. Dukes [4]. Общепринятая система TNM, предложенная Американским объединенным комитетом по исследованию рака (AJCC) и Международным союзом по борьбе с раком (UICC), базируется на ключевых и доступных характеристиках опухоли, которые, в свою очередь, лежат в основе стадирования [5]. Система TNM получила широкое распространение за свою простоту реализации и малые экономические затраты при использовании. Для пациентов без отдаленных метастазов существенными для прогноза считаются следующие два признака: уровень проникновения опухоли в кишечную стенку и количество регионарных лимфатических узлов, содержащих метастазы. Пациенты группируются в широкие когорты (стадия с I по III) с отличающимся исходом, однако точность индивидуального прогноза для каждого отдельного пациента ограничена. Предполагается, что пациенты в каждой группе имеют схожие исходы, хотя на самом деле результаты довольно неоднородны вследствие вариабельности клинико-патологических особенностей и биологии опухоли [6]. Кроме того, система TNM вынуждает преобразовывать непрерывные переменные опухолевого процесса в категориальные, что еще больше ограничивает точность прогнозов. Таким образом, хотя схема стадирования обеспечивает оценку исходов заболевания, клиницисты и пациенты часто задаются вопросом, где в клиническом спектре находится их конкретный результат. Попытки уточнить прогностические оценки с помощью подкатегорий оказались менее чем удовлетворительными и подчеркивают ограничения любой промежуточной системы, которая создает отдельные группы [7—9].
Цель исследования — разработка методики для индивидуализации прогноза метастазирования локализованных форм колоректального рака после потенциально курабельной операции, для идентификации и стратификации рисков отдаленных рецидивов у пациентов, помогающей в определении дальнейшей клинической тактики.
Когорты пациентов
Проведен анализ 1350 опухолей толстой кишки архивного оперативно удаленного материала, полученного из патолого-анатомической лаборатории ГБУЗ «Санкт-Петербургский клинический научно-практический центр специализированных видов медицинской помощи (онкологический)» с 2012 по 2015 г. включительно. Из них выбраны случаи локализованных форм колоректального рака (n=98) с известным как минимум 5-летним катамнезом. Для включения в группу исследования использовали следующие критерии: 1) инвазивные опухоли категории T1-4, 2) отсутствие метастазов в регионарных лимфатических узлах; 3) отсутствие неоадъювантного химиотерапевтического и/или лучевого лечения; 4) отсутствие клинически выявленных синхронных отдаленных метастазов на момент операции; 5) отсутствие синхронных и метахронных опухолей других локализаций.
После установления катамнеза по материалам медицинской документации и посредством сбора данных у пациента и/или его представителя исследуемая группа была разделена на две категории в зависимости от отсутствия (n=53) или выявления отдаленных метахронных метастазов (n=45) по данным как минимум 5-летнего клинического наблюдения. Группу контроля (n=53) составили инвазивные опухоли без метастазов в регионарных лимфатических узлах, но имеющие морфологически верифицированные отдаленные синхронные метастазы.
Исследуемые характеристики
Каждый случай оценивался по 31 параметру, которые включали: 1) пол; 2) возраст на момент операции; 3) локализацию опухоли; 4) глубину инвазии; 5) количество исследованных регионарных лимфатических узлов; 6) степень дифференцировки в соответствии с утвержденными рекомендациями 5-го издания Классификации опухолей желудочно-кишечного тракта Всемирной организации здравоохранения [10]; 6) степень ядерного плеоморфизма опухолевых клеток; 7) пролиферативную активность опухоли, оцениваемую в процентном соотношении положительных и отрицательных ядер при иммуногистохимическом окрашивании с Ki-67 (MIB-1, 1:300, Dako); 8) апоптотическую активность в эпителиальных клетках опухоли, вычисляемую посредством подсчета среднего числа иммуногистохимически окрашенных клеток к маркеру CytoDEATH (M30, 1:150, Roche) в одном поле зрения большого увеличения (´40); 9) наличие экстрацеллюлярного муцина; 10) присутствие и распространенность «грязных некрозов»; 11) функциональную сохранность системы репарации ошибочно спаренных нуклеотидов с использованием ядерных маркеров четырех белков репарации ДНК: MLH1 (ES05, 1:70, Dako), MSH2 (G219-1129, 1:100, CellMarque), MSH6 (EP49, 1:120, Epitomics) и PMS2 (EP51, 1:70, CellMarque); 12) мутацию в экзоне V600E гена BRAF по иммуногистохимическому выявлению аномального белкового продукта в опухолевых клетках (VE1, 1:800, Abcam); 13) экстрамуральную венозную инвазию, которая определялась по двум ключевым признакам: «одинокая» артерия — очерченный узел опухоли, прилежащий к артерии в месте предполагаемой вены, и признак «клина» — вдающийся в клетчатку за границы мышечной оболочки клин опухоли по ходу вены. В сомнительных случаях для подтверждения наличия венозной инвазии использовалась гистохимическая окраска, выявляющая остаточные эластические волокна, сохраняющиеся в сосудистой стенке; 14) периневральную инвазию, определяемую по охвату опухолевыми комплексами как минимум 1 /3 окружности нерва; 15) оценку почкования (англ. budding), которая проводилась согласно рекомендациям международного консенсуса 2016 г. [11]; 16) определение коллективного или индивидуального типа миграции клеток в инвазивном фронте опухоли, которое выполнялось с помощью оценки экспрессии E-кадгерина (NCH-38, 1:120, Dako) и β-катенина (14, 1:150, CellMarque) в отпочковывающихся клетках. Сохранение мембранной экспрессии обоих маркеров в клетках инвазивного фронта свидетельствовало о сохранении межклеточных контактов и, следовательно, коллективном типе миграции. Полное отсутствие мембранной экспрессии E-кадгерина даже при сохранении цитоплазматической окраски при сочетании с ядерным окрашиванием на β-катенин позволяло выявлять индивидуальный тип миграции; 17) характер десмопластической реакции стромы, который гистологически классифицировался как зрелый, промежуточный или незрелый по системе, предложенной H. Ueno и соавт. [12]; 18) определение соотношения стромы и паренхимы в опухоли, устанавливаемое по критериям J. Park и соавт. [13]; 19) выявление преобладания I или III типа коллагена в строме опухоли, определяемого на срезах, гистохимически окрашенных пикросириусом красным F3BA, с дальнейшей оценкой в поляризованном свете; 20) полуколичественную оценку плотности воспалительного инфильтрата по модифицированной схеме Klintrup—Mäkinen, предложенной в 2005 г. [14]; 21) процентное содержание иммунного воспалительного инфильтрата в строме опухоли (sTIL от англ. stromal tumor-infiltrating lymphocytes) согласно методике, разработанной международной рабочей группой по биомаркерам в иммуноонкологии под руководством R. Salgado [15, 16]; 22) определение числа T-лимфоцитов на 1 мм 2 в строме инвазивного фронта опухоли с использованием иммуногистохимической окраски на CD3 (MRQ39, 1:150, CellMarque); 23) оценку качественного состава популяции T-лимфоцитов, а именно количества цитотоксических лимфоцитов на 1 мм 2 в тех же участках стромы с использованием иммуногистохимической окраски на CD8 (C8/144B, 1:120, CellMarque); 24) определение соотношения CD8/CD3 для выявления доли цитотоксических лимфоцитов из всей популяции T-лимфоцитов по упрощенной системе Immunoscore [17, 18]. Полученное соотношение обозначалось как Index-T; 25) оценку среднего числа интраэпителиальных лимфоцитов (iTIL от англ. intraepithelial tumor-infiltrating lymphocytes) при большом увеличении (´40) на препаратах, окрашенных гематоксилином и эозином; 26) подсчет количества тучных клеток в опухолевом микроокружении на 1 мм 2 , для визуализации которых использовалось гистохимическое окрашивание толуидиновым синим; 27) подсчет числа NK-клеток в опухолевом микроокружении инвазивного фронта на 1 мм 2 с использованием иммуногистохимической окраски на CD57 (NK-1, 1:300, CellMarque); 28) подсчет числа альтернативно-активированных опухолеассоциированных макрофагов в опухолевом микроокружении на 1 мм 2 , для верификации которых использовалось иммуногистохимическое окрашивание с антителом к маннозному рецептору aka CD206 (D-1, 1:1500, SantaCruz); 29) плотность кровеносных микрососудов на 1 мм 2 с помощью тройной иммуногистохимической окраски с антителами к ERG (EP111, 1:150, Epitomics) — антигену ядер эндотелиальных клеток как кровеносных, так и лимфатических сосудов, α-SMA (1A4, 1:200, Dako), — выявляющему гладкомышечный актин в цитоплазме перицитов, и Podoplanin (D2-40, 1:50, CellMarque), специфичному к эндотелию лимфатических сосудов; 30) подсчет количества новообразованных сосудов на 1 мм 2 , отличающихся неполноценной стенкой, лишенной перицитарного окружения; 31) определение соотношения сосудов без перицитов к общему числу кровеносных микрососудов, обозначаемого как Index-V.
Все микроскопически оцениваемые характеристики анализировались в инвазивном фронте опухоли, определявшемся как участок шириной в 1 мм, отделяюший окружающие ткани от наиболее инфильтрирующих опухолевых комплексов.
Статистическая обработка данных проводилась с использованием пакета программы Statistica для Windows (версия 9). Сопоставление частотных характеристик проводилось с помощью комплекса непараметрических методов χ 2 , χ 2 с поправкой Йетса, критерия Фишера. Для сравнения полученных данных также использовались непараметрические методы: U-критерий Манна—Уитни и критерий согласия Пирсона. Критерием статистической достоверности считали p
В процессе построения модели были выделены 6 значимых показателей, достоверно связанных с появлением отдаленных метастазов: 1) экстрамуральная венозная инвазия (ЭМВИ); 2) почкование; 3) утрата E-кадгерина; 4) ядерная экспрессия β-катенина; 5) Index-T; 6) Index-V.
Показатели Index-T и Index-V количественные, их распределение не соответствует нормальному, поэтому в табл. 1 показаны их характеристики, описывающие данные показатели с учетом этого факта. На рис. 1 наглядно представлены различия в группах с метастазами и без таковых.
Таблица 1. Показатели Index-T и Index-V в группах без метастазов и с отдаленными метастазами
Читайте также:
- Признаки повреждения сухожилия общего разгибателя на уровне локтевого сустава
- Актин в составе цитоскелета клетки
- Гормоны поджелудочной железы. Островки Лангерганса. Соматостатин. Амилин. Регуляторные функции гормонов поджелудочной железы.
- Аденовирусная инфекция. Причины и клиника аденовирусных болезней
- Причины синдрома токсичной органической пыли (СТОП) и его диагностика
