Техника изъятия поджелудочно-дуоденального комплекса. Принципы
Добавил пользователь Алексей Ф. Обновлено: 01.02.2026
Дуоденальное зондирование, цель: получение дуоденального содержимого для лабораторного исследования.
Показания к дуоденальному зондированию: заболевания печени, желчного пузыря, желчевыводящих путей.
Противопоказания. Острый холецистит; обострение хронического холецистита; варикозное расширение вен пищевода; коронарная недостаточность.
Оснащение. Стерильный дуоденальный зонд с оливой на конце; стерильный шприц емкостью 20 мл; мягкий валик; теплая грелка; полотенце; лоток; 50 мл 25 % раствора магния сульфата подогретого до +40. +42 °С; штатив с лабораторными пробирками (не менее трех пробирок, на каждой пробирке указывают порцию желчи А, В, С); направление в лабораторию; чистая сухая баночка; жесткий топчан без подушки; скамеечка; комплект белья; стакан с кипяченой водой (раствором калия перманганата розового цвета, 2 % раствором натрия гидрокарбоната или слабосолевым раствором).
1. Объясняют пациенту необходимость процедуры и ее последовательность.
2. Накануне вечером предупреждают, что предстоящее исследование проводится натощак, а ужин перед исследованием должен быть не позднее 18.00.
3. Приглашают пациента в зондажный кабинет, удобно усаживают на стул со спинкой, слегка наклоняют его голову вперед.
4. На шею и грудь пациента кладут полотенце, просят его снять зубные протезы, если они есть. Дают в руки лоток для слюны.
5. Достают из бикса стерильный зонд, увлажняют кипяченой водой конец зонда с оливой. Берут его правой рукой на расстоянии 10 - 15 см от оливы, а левой рукой поддерживают свободный конец.
6. Встав справа от пациента, предлагают ему открыть рот. Кладут оливу на корень языка и просят сделать глотательное движение. Во время проглатывания продвигают зонд в пищевод.
7. Просят пациента глубоко подышать носом. Свободное глубокое дыхание подтверждает нахождение зонда в пищеводе и снимает рвотный рефлекс от раздражения задней стенки глотки зондом.
8. При каждом глотании пациента зонд вводят глубже до четвертой отметки, а затем еще на 10 - 15 см для продвижения зонда внутри желудка.
9. Присоединяют к зонду шприц и тянут поршень на себя. Если в шприц поступает мутноватая жидкость, значит зонд находится в желудке.
10. Предлагают пациенту проглотить зонд до седьмой отметки. Если позволяет его состояние, лучше это сделать во время медленной ходьбы.
11. Пациента укладывают на топчан на правый бок. Под таз подкладывают мягкий валик, а под правое подреберье - теплую грелку. В таком положении облегчается продвижение оливы к привратнику.
12. В положении лежа на правом боку пациенту предлагают проглотить зонд до девятой отметки. Зонд продвигается в двенадцатиперстную кишку.
13. Свободный конец зонда опускают в баночку. Баночку и штатив с пробирками ставят на низкую скамеечку у изголовья пациента.
14. Как только из зонда в баночку начинает поступать желтая прозрачная жидкость, свободный конец зонда опускают в пробирку А (дуоденальная желчь порции А имеет светло-желтую окраску). За 20 - 30 мин поступает 15 - 40 мл желчи - количество, достаточное для исследования.
15. Используя шприц как воронку, вводят в двенадцатиперстную кишку 30 - 50 мл 25 % раствора магния сульфата, подогретого до +40. +42°С. На зонд накладывают зажим на 5-10 мин или свободный конец завязывают легким узлом.
16. Через 5-10 мин снимают зажим. Опускают свободный конец зонда в баночку. Когда начинает поступать густая желчь темно-оливкового цвета, опускают конец зонда в пробирку В (порция В из желчного пузыря). За 20 - 30 мин выделяется 50 - 60 мл желчи.
17. Как только из зонда вместе с пузырной желчью будет поступать желчь ярко-желтого цвета, опускают его свободный конец в баночку до выделения чистой ярко-желтой печеночной желчи.
18. Опускают зонд в пробирку С и набирают 10 - 20 мл печеночной желчи (порция С).
19. Осторожно и медленно усаживают пациента. Извлекают зонд. Пациенту дают прополоскать рот приготовленной жидкостью (водой или антисептиком).
20. Поинтересовавшись самочувствием пациента, доставляют его в палату, укладывают в постель, обеспечивают покой. Ему рекомендуют полежать, так как магния сульфат может снизить АД.
21. Пробирки с направлениями доставляют в лабораторию.
22. Зонд после исследования замачивают в 3 % растворе хлорамина на 1 ч, потом обрабатывают по ОСТ 42-21-2-85.
23. Результат исследования подклеивают в историю болезни.
Дуоденальное зондирование, техника выполнения.
Примечания. В отделении пациенту должен быть оставлен завтрак (постовой медицинской сестре следует заранее сообщить на раздаток номер диеты и количество порций). Контролируют самочувствие пациента, показания АД. Предупреждают его о том, что магния сульфат обладает слабительным действием и у него может быть жидкий стул. Для исследования на лямблии желчь порции В следует доставить в лабораторию в теплом виде.
Фракционное дуоденальное зондирование.
Цель. Получение дуоденального содержимого для лабораторного исследования; изучение динамики желчевыделения.
Показания. Заболевания печени, желчного пузыря, желчевыводящих путей.
Противопоказания. Острый холецистит; обострение хронического холецистита; варикозное расширение вен пищевода; коронарная недостаточность.
Оснащение. Стерильный дуоденальный зонд с оливой на конце; стерильный шприц емкостью 20 мл; мягкий валик; теплая грелка; полотенце; лоток; 50 мл 25 % раствора магния сульфата, подогретого до +40. +42 °С; штатив с лабораторными пробирками (не менее трех пробирок, на каждой пробирке указана порция желчи: А, В, С); направление в лабораторию; чистая сухая баночка; жесткий топчан без подушки; скамеечка; комплект белья; стакан с кипяченой водой (раствором калия перманганата розового цвета, 2 % раствором натрия гидрокарбоната или слабосолевым раствором).
Техника выполнения фракционного дуоденального зондирования.
Техника проведения исследования аналогична технике выполнения дуоденального зондирования.
Фракционное дуоденальное зондирование состоит из пяти фаз или этапов.
На первой фазе получают первую порцию желчи из общего желчного протока - прозрачную светло-желтую желчь. Длится фаза 20 мин. Обычно за это время выделяется 15 - 40 мл желчи. Получение более 45 мл свидетельствует о гиперсекреции или расширении общего желчного протока. Меньшее количество желчи означает гипосекрецию желчи или уменьшение емкости общего желчного протока. Через 20 мин от начала получения желчи вводят раздражитель - 25 % раствор магния сульфата, подогретый до +40. +42 °С. В конце первой фазы на зонд накладывают зажим.
В начале второй фазы фракционного дуоденального зондирования снимают зажим, опускают свободный конец зонда в баночку и ждут начала поступления желчи. В норме фаза длится 2 - 6 мин. Удлинение фазы свидетельствует о гипертонусе общего желчного протока или наличии препятствия в нем.
Третья фаза - это время до появления пузырной желчи. В норме она длится 2 - 4 мин. За это время выделяется 3 - 5 мл желчи светло-желтого цвета - остаток желчи из общего желчного протока. Удлинение фазы свидетельствует о повышении тонуса сфинктера. Желчь, получаемая в течение первой и третьей фаз, составляет порцию А классического дуоденального зондирования.
Четвертая фаза - это регистрация продолжительности опорожнения желчного пузыря и объема пузырной желчи. В норме за 30 мин выделяется 30 - 70 мл желчи темно-оливкового цвета - это классическая порция В. Скорость выделения пузырной желчи составляет 2 - 4 мл/мин. Скорость выделения пузырной желчи в течение 10 мин менее этого показателя характерна для гипомоторной функции желчного пузыря, а более - для гипермоторной функции.
Пятая фаза дуоденального зондирования- получение печеночной желчи (порции С). В норме за 20 мин выделяется 15 - 30 мл желчи золотистого цвета (печеночной желчи).
Примечания. В отделении пациенту должен быть оставлен завтрак (постовой медицинской сестре следует заранее сообщить на раздаток номер диеты и количество порций).
Желудочное и дуоденальное зондирование проводит персонал, получивший подготовку для работы в зондажном кабинете.
Особенности оперативной техники при резекционных вмешательствах по поводу гастродуоденальных язв, осложненных кровотечением или перфорацией (часть II)
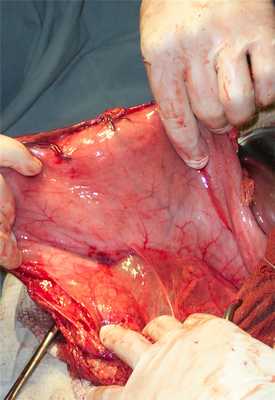
Следующим после ревизии брюшной полости этапом резекции желудка является мобилизация гастродуоденального комплекса. В большинстве классических руководств по оперативной хирургии мобилизация стандартно начинается с пересечения желудочно-ободочной связки. Мы же придерживаемся мнения авторов, рекомендующих вне зависимости от локализации язв начинать манипуляции с широкой мобилизации ДПК по Кохеру. Помимо увеличения подвижности гастро-дуоденального комплекса, что необходимо для последующего наложения гастро-дуоденоанастомоза в случае выбора резекции по Бильрот-I, широкая мобилизация ДПК по Кохеру позволяет точно контролировать взаимоотношение анатомических структур (прежде всего - гепато-дуоденальной связки) и относительно легко верифицировать для последующего лигирования и пересечения правые желудочную и желудочно-сальниковую артерии. Критерием адекватности мобилизации ДПК по Кохеру мы считаем визуализацию оператором аорто-кавального промежутка.
В дальнейшем при мобилизации гастро-дуоденального комплекса следует руководствоваться правилом «от простого к сложному», то есть начинать разъединение тканей, максимально удаленных от язвы с постепенным приближением к патологическому очагу. Так, при дуоденальной локализации язвы вначале проводят мобилизацию желудка по большой и малой кривизне, а затем приступают к выделению стенки ДПК в пилоро-бульбарной зоне. При предполагаемых сложностях с выделением пилоро-бульбарного сегмента и обработкой культи ДПК (III и IV степень сложности по Guarneri) следует мобилизовать желудок до уровня резекции дистальных 2/3 или ¾, пересечь его и сформировать малую кривизну культи. Последующее смещение отсеченной дистальной части желудка вправо и вниз позволяет получить практически циркулярный доступ к пилоро-бульбарному сегменту, что весьма облегчает выделение его стенки. При достаточной подвижности желудка его пересечение можно отложить до момента собственно резекции .
И, напротив, локализация язвы в субкардиальном отделе или верхней трети тела желудка по малой кривизне делает необходимым начало мобилизации с выделения пилоро-бульбарного сегмента и мобилизации правой половины желудка по большой кривизне. Затем производится пересечение ДПК на 1,5 см дистальнее привратника и подготовка культи ДПК к анастомозированию или ее ушивание. Возможность свободных тракций и ротации отсеченного от ДПК желудка значительно облегчает его мобилизацию по малой кривизне, выделение язвы, а также, что очень важно, выделение, лигирование и пересечение левой желудочной артерии.
Для максимально быстрого и асептичного пересечения желудка и ДПК следует использовать линейные сшивающие аппараты: Proximate® TLC55-10 (с возможностью одновременного рассечения тканей между рядами скрепочных швов) или Proximate® TL60-90, TX60 (производство Ethicon®), либо GIA Premium®50, ILA75 (с возможностью одновременного рассечения тканей между рядами скрепочных швов) или TA Premium®55-90, PA Premium®55-90 (производство Сovidien).
Особо ответственным и требующим высокой техники препарирования этапом мобилизации является выделение стенки пилоро-бульбарного сегмента. Выделение стенки ДПК из рубцов следует производить с использованием прецизионной техники оперирования и соответствующего инструментария: остроконечных диссекторов, зажимов типа «москит» Холстеда, длинных препаровочных ножниц типа Нельсон-Метценбаума и Мэйо-Харрингтона, атравматичных пинцетов типа Де Бейки. Учитывая, что работать приходиться в глубине раны, следует использовать инструменты длиной не менее 190 мм. Непременными условиями для применения прецизионной техники препарирования являются достаточная освещенность операционного поля, хорошая экспозиция и контролируемый гемостаз с постоянно «сухой» зоной оперирования. Для лигирования мелких сосудистых ветвей применяется нерассасывающийся шовный материал 00 - 000, подаваемый оператору только на зажиме. Рассечение рубцов должно проводится в непосредственной близости от стенки ДПК малыми (2 - 3 мм) порциями, после предварительного выделения участка ткани диссектором. Желательно пересечение ткани проводить между двумя зажимами или после предварительной биполярной электрокоагуляции, поскольку визуально отличить рубцовую ткань от ветвей гастродуоденальной или панкреатодуоденальных артерий достаточно сложно, а остановка кровотечения из этих ветвей нарушает темп операции .
Как указывалось выше, сложность выделения стенки пилоро-бульбарного сегмента при осложненных язвах определяется наличием как правило выраженного периульцерозного рубцово-спаечного процесса. При этом рассечению подвергаются как нежные плоские спайки и наложения фибрина на серозе кишки, так и плотные
плоскостные сращения между измененной стенкой кишки в зоне язвы и соседними анатомическими структурами. Плотные плоскостные наложения, обозначаемые как рубцовая мантия, непосредственно сращены со стенкой ДПК только в зоне язвенного процесса, откуда они и исходят. Отступив от периульцерозной зоны на 1 - 1,5 см, при осторожной препаровке можно «попасть в слой» между собственно стенкой ДПК и рубцовой мантией. В дальнейшем, продвигаясь центрипетально, рассекая маленькими порциями и отслаивая рубцовую мантию, доходят но границ язвенного кратера по оральному, верхнему и нижнему его краям. Особенно сложным этапом мобилизации является выделение задней стенки пилоро-бульбарного сегмента при кровоточащих язвах ДПК. При выделении задней стенки дистальной части луковицы ДПК особое внимание следует уделить определению проекции гастродуоденальной артерии по ее пульсации или проследив ее путь от общей печеночной артерии. Повреждение гастродуоденальной артерии чревато не только массивным кровотечением, но и возможностью острого ишемического повреждения правой доли печени при нередко встречающейся аномалии ее кровоснабжения. Для идентификации гастродуоденальной артерии следует вначале выделить переднюю стенку общей печеночной артерии, рассекая листок париетальной брюшины чуть выше и параллельно верхнему краю головки поджелудочной железы. Продвигаясь по общей печеночной артерии вправо, в сторону ворот печени, определяют первую крупную (сопоставимую по диаметру с самой общей печеночной артерией) ее ветвь, отходящую вниз, в сторону головки поджелудочной железы. Данная ветвь и будет являться гастро-дуоденальной артерией.
Незапланированное вскрытие просвета ДПК происходит, как правило, в области задней стенки, по краю пенетрирующего язвенного кратера. Данная ситуация служит сигналом к поперечному рассечению передней стенки ДПК в проекции проксимального края язвы и последующей открытой обработке культи ДПК.
Мобилизация желудка по большой кривизне проводится рассечением желудочно-ободочной связки порциями на зажимах или отсечением большого сальника от поперечно-ободочной кишки в бессосудистой зоне при невозможности исключения злокачественного характера желудочной язвы. В проксимальном направлении мобилизация при планируемой резекции дистальных 2/3 желудка завершается в зоне границы кровоснабжения правой и левой желудочно-сальниковой артерий (на 1-2 см правее последней ветки левой желудочной артерии). При планируемой резекции дистальных ¾ желудка мобилизация по большой кривизне проводится до уровня нижнего полюса селезенки. В данном случае при мобилизации производится лигирование и пересечение 2-3 коротких артерий желудка.
В дистальном направлении мобилизация по большой кривизне проводится до уровня на 1,5-2 см дистальнее пилорического жома, при этом лигируется и пересекается правая желудочно-ободочная артерия. В условиях выраженного рубцового перидуоденита, когда большой сальник, мезоколон и луковица ДПК оказываются плотно спаянными между собой, создается реальная угроза повреждения средних ободочных сосудов, проходящих как раз в этой зоне. Во избежание этого осложнения следует произвести тракцию антрального отдела вверх и вперед, визуализировать поджелудочную через сальниковую сумку поджелудочную железу, передний листок мезоколон и место его перехода на ДПК. Место прохождения средней ободочной артерии определяется пальпаторно через мезоколон по характерной пульсации или трансиллюминацией. Для предупреждения ранения или лигирования средней ободочной артерии следует рассечь передний листок мезоколон в проекции артерии и тупым путем отслоить ткань мезоколон вместе со средними ободочными сосудами вниз и каудально. Затем из жировой ткани по нижней стенке пилоробульбарного сегмента выделяется, лигируется и пересекается правая желудочно-сальниковая артерия. Правая желудочная артерия, правая желудочная и пилорическая вены выделяются инструментом чуть выше гепато-дуоденальной связки в прекции ее дистального отдела, лигируется и пересекается.
При мобилизации малой кривизны до уровня дистальной резекции 2/3 проксимальная граница мобилизации находится на 2-3 см дистальнее пищеводно-желудочного перехода, в проекции деления левой желудочной артерии на восходящую и нисходящую ветви. В этом случае последняя выделяется в толще малого сальника, лигируется и пересекается.
При мобилизации малой кривизны до уровня дистальной резекции 3/4 проксимальная граница мобилизации находится на 1 см дистальнее пищеводно-желудочного перехода. При дистальной резекции ¾ желудка лигируется и пересекается левая желудочная артерия. Критерием достаточной мобилизации желудка по малой кривизне при таком объеме резекции является обязательная визуализация перехода правой полуокружности пищевода на малую кривизну желудка. Для облегчения манипуляций в ходе высокой мобилизации желудка, например при субкардиальной язве, целесообразно начать процедуру мобилизации с пересечения на зажимах левой треугольной связки печени и рассечения брюшинного листка, покрывающего переднюю стенку абдоминального отдела пищевода. После идентификации пищевода по находящемуся в его просвете назо-гастральному зонду указательным пальцем производится его циркулярное выделение. Взятие пищевода на держалку (силиконовая трубка или пластиковая лента) дает возможность тракций кардии и субкардиального отдела во всех плоскостях, что значительно облегчает мобилизацию и последующую резекцию желудка. Подозрение на злокачественный характер язвы является показанием к удалению клетчатки всего малого сальника, включая клетчатку гепато-дуоденальной связки, лигированию и пересечению левой желудочной артерии непосредственно у чревного ствола со смещением клетчатки, ее окружающей, к резецируемому препарату. В данной ситуации выделение левой желудочной артерии начинают с идентификации и диссекции общей печеночной артерии над головкой поджелудочной железы в проксимальном направлении с выделением чревного ствола. После мобилизации на освобожденную от клетчатки стенку желудка по малой и большой кривизне на границе резекции накладывают по одному шву-держалке.
Очевидно, что совершенно иначе производится мобилизация при операциях по поводу кровоточащей язвы гастро-энтероанастомоза. В данном случае рассечением более или менее выраженных спаек и плоскостных сращений следует идентифицировать переднюю стенку культи желудка, затем - его малую кривизну. После визуализации культи желудка необходимо определить ее взаимоотношения с мезоколон. При ранее наложенном позадиободочном гастро-энтероанастомозе культя желудка или несущая анастомоз петля тонкой кишки со всех сторон фиксирована в мезоколон. Пальпаторно или путем трансиллюминции определив месторасположение средней ободочной артерии, следует вначале острым путем, а затем, попав «в слой», малыми порциями разъединить мезоколон и стенку культи желудка. При ранее наложенном впередиободочном анастомозе необходимость в данных манипуляциях отпадает.
Освобождая малую кривизну в дистальном направлении, визуализируют зону анастомоза, непосредственно участвующую в его формировании петлю тонкой кишки. С полной уверенностью судить о том, какая петля тонкой кишки приводящая, а какая - отводящая становится возможным только после полного освобождения участвующего в формировании анастомоза отрезка тонкой кишки от спаек, то есть проведения интестинолиза. При выделении петли тонкой кишки становится ясным, по какому методу производилась реконструкция на предыдущей операции. Как правило, это реконструкция по Гофмейстеру-Финстереру на короткой петле с формированием шпоры у малой кривизны или по Бальфуру с межкишечным соустьем, расположенным дистальнее гастро-энтероанастомоза на 15 - 20 см. Поскольку после ререзекции реконструктивный этап будет проводиться по методу Ру, принципиальное значение имеет идентификация приводящей к гастро-энтероанастомозу (отходящей от дуодено-еюнального перехода) петли. Расположение участков тонкой кишки в зоне гастро-энтероанастомоза (у малой кривизны - приводящий, у большой кривизны - отводящий), тем более после реконструкции по Бальфуру - крайне ненадежный критерий. Для достоверного определения отводящей и приводящей петель необходимо выделение из спаек обоих прилежащих к гастро-энтеро- или энтеро-энтероанастомозу участков тонкой кишки до обнаружения дуодено-еюнального перехода. Идущий от дуодено-еюнального перехода участок тонкой кишки и будет являться приводящей к анастомозу петлей.
Само возникновение пептической язвы гастро-энтероанастомоза свидетельствует о недостаточном объеме ранее произведенной резекции. Нам не доводилось наблюдать пациентов с пептическими язвами анастомоза после дистальной резекции 2/3 и, тем более, ¾ желудка. Как правило, на повторной операции определяется состояние после гемигастрэктомии или антрумэктомии, что определяет необходимость дополнительной резекции желудка, прежде всего - малой кривизны. Освобождая желудок от спаек по передней и задней стенки, дополнительно мобилизуют большую и малую кривизну до уровня резекции дистальных ¾. При этом мобилизация малой кривизны предполагает снятие «шпоры» и, как указывалось выше, сопровождается лигированием и пересечением левой желудочной артерии.
Гастропанкреатодуоденальная резекция (Kausch-Wipple procedure)
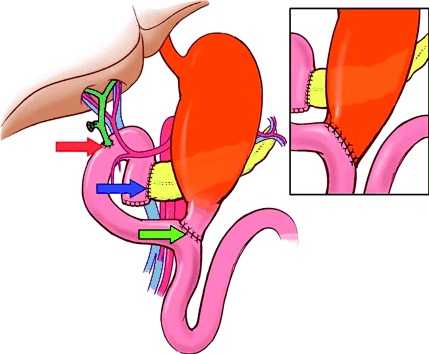
Гастропанкреатодуоденальная резекция (ГПДР), синоним - операция Уиппла (Whipple’s procedure) включает одномоментное удаление головки поджелудочной железы, дистальной части желудка, двенадцатиперстной кишки, начального отдела тощей кишки, части желчных протоков, желчного пузыря и регионарных лимфатических узлов.
Показанием к проведению ГПДР являются: верифицированное опухолевое поражение головки поджелудочной железы, терминального отдела холедоха, большого дуоденального сосочка и двенадцатиперстной кишки, а также невозможность исключения злокачественного процесса указанной локализации. Кроме этого ГПДР в ряде случаев показана пациентам, страдающим хроническим панкреатитом.
Операция ГПДР, являясь единственным средством избавления пациента от опухоли панкреатодуоденальной зоны, является, тем не менее, весьма травматичным вмешательством. Необходимость формирования нескольких анастомозов обусловливает вероятность развития в послеоперационном периоде их несостоятельности с формированием свищей и развитием других достаточно тяжелых осложнений. Впервые ГПДР была проведена в Европе немецким хирургом Walter Kausch в 1909 году, в США - хирургом Allen Whipple в 1932 году. Результаты гастропанкреатодуоденальной резекции на протяжении десятилетий были весьма неутешительны: ГПДР сопровождалась большим количеством осложнений и достаточно высокой летальностью. Однако в настоящее время, благодоря отработанной технике этой операции, современной оснащенности операционной, профессиональной подготовке врачей анестезиологов-реаниматологов, ГПДР сопровождается минимальным количеством осложнений и послеоперационной летальности, хорошими отдаленными результатами выживаемости и качества жизни.

M.Evseev, A.Vladykin, I.Klyshin. Multivisceral resection for locally advanced colorectal cancer. Case report. Одним из направлений научных исследований.

В историческом обзоре приводятся в хронологической последовательности этапы рождения и эволюции панкреатодуоденальной резекции. Описаны первые опыты проведения.
Пациентам: Эндосонография ЭндоУЗИ - что это? Подготовка?
Эндосонография (ЭндоУЗИ, эндоскопическая ультрасонография)
Эндосонография — диагностическая методика , высокотехнологическое исследование, одновременно сочетающее в себе возможности эндоскопической и ультразвуковой диагностики.
Для исследования используют гибкий эндоскоп с видеокамерой и ультразвуковым датчиком. Его можно ввести в пищевод, желудок, двенадцатиперстную, прямую, толстую кишку, а также в дыхательные пути. Во время обычного ультразвукового исследования через кожу, когда нужно осмотреть орган, который находится глубоко, страдает четкость изображения. Эндосонография решает эту проблему. При помощи эндоскопа УЗ-датчик подводят максимально близко к исследуемому образованию. Во время исследования врач может провести тонкоигольную биопсию подозрительного образования. Использование в приборе очень высоких частот ультразвука (5,0; 7,5; 12 и 20 МГц) обеспечивает высокое качество изображения с разрешающей способностью менее 1 мм, недоступное другим методам исследования, таким как обычное ультразвуковое исследование, компьютерная и магнитно-резонансная томография, эндоскопическая холангиопанкреатикография. При этом эндосонография не сопряжена с риском рентгенологического облучения персонала и пациента, отсутствует опасность возникновения осложнений, свойственных ЭРХПГ.
Как подготовиться к эндосонографии?
Перед исследованием врач выясняет, есть ли у пациента аллергия на лекарства, страдает ли он хроническими заболеваниями сердечно-сосудистой, дыхательной системы, сахарным диабетом, принимает ли какие-нибудь препараты. Если планируется тонкоигольная биопсия, потребуется сдать анализы на свертываемость крови. За несколько часов до исследования нельзя есть и пить. Могут быть назначены очищающие клизмы, слабительные препараты, пеногасители. Более подробные рекомендации даст врач.
Как проводится эндосонография?
Эндосонография верхних отделов желудочно-кишечного тракта напоминает гастроскопию, нижних отделов - сигмоскопию, колоноскопию. Процедура продолжается от 20 до 60 минут. Она занимает больше времени, когда ее дополняют тонкоигольной биопсией. Обычно эндосонографию проводят в состоянии медикаментозного сна - разновидность легкого наркоза. В этом состоянии пациент во время процедуры практически ничего не чувствует, может ощущать лишь небольшой дискомфорт. В ходе эндосонографии врач следит за артериальным давлением пациента, пульсом, уровнем кислорода в крови. Примерно через час врач разрешает встать, и, если состояние пациента в порядке, отпускает домой. В этот день нельзя садиться за руль и заниматься работой, требующей концентрации внимания.
Основные показания для проведения эндосонографии:
- Диагностика рака поджелудочной железы. Метод обладает высокой чувствительностью и позволяет установить диагноз в 90-95% случаев.
- Диагностика рака пищевода, желудка, двенадцатиперстной кишки. Выявление доброкачественных образований верхних отделов желудочно-кишечного тракта.
- Выявление, осмотр и биопсия очаговых поражений верхнего отдела ЖКТ.
- Выявление причины болей в животе, когда при помощи других исследований не удается установить диагноз.
- Обнаружение патологических образований в желчном пузыре и желчевыводящих протоках, протоке поджелудочной железы.
- Биопсия подозрительных образований в пищеводе, желудке, двенадцатиперстной кишке, соседних органах, лимфатических узлах.
- Уточнение степени расширения вен пищевода.
- Диагностика рака толстой и прямой кишки.
- Биопсия подозрительных образований в кишечнике, лимфатических узлах. Оценка целостности анального сфинктера.
- Диагностика рака легких и бронхов.
- Оценка состояния внутригрудных лимфатических узлов.
Какое оборудование используется?
- радиального - перпендикулярны оси эндоскопа - сканируют 360 градусов - диагностический
- конвексного - параллельно оси эндоскопа - сканируют примерно 100 градусов - имеет специальный "инструментальный" канал
Эхоэндоскопы конвексного типа сканирования введены в клиническую практику с 1990-х годов и позволяют получать 100° секторное ультразвуковое изображение, параллельное оси эндоскопа. Использование аппаратов данного типа, оснащенных инструментальным каналом, позволяет проводить пункционную биопсию под ЭСГ-контролем (ЭСГ-ПБ). Комплектация эхосканеров допплеровским и соно-эластографическими блоками значительно расширяет диагностические и лечебные возможности исследования.
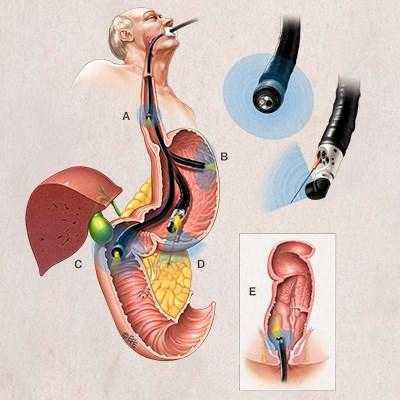
Панкреатодуоденальная резекция
Панкреатодуоденальная резекция (ПДР, операция Уиппла) - операция, которое проводится для лечения рака поджелудочной железы. Опухоли в этом месте - редкое явление, но крайне тяжелое, и хирургическое вмешательство сегодня - единственный эффективный метод лечения. Методика применяется для удаления опухоли в головке поджелудочной железы, большом сосочке или верхней части двенадцатиперстной кишки.
Акции
Полное обследование на онкологические заболевания для мужчин и женщин.
Онкоконсилиум может потребоваться как при лечении в «СМ-Клиника», так и пациентам других медицинских учреждений с целью получения альтернативного мнения.
«СМ-Клиника» предоставляет своим пациентам предоперационное обследование со скидкой до 72%!
Консультация врача-хирурга по поводу операции бесплатно!
Основные преимущества операции Уиппла
- удаляется вся опухоль целиком;
- восстанавливаются протоки поджелудочной железы и желчных путей;
- практически единственный эффективный метод лечения рака поджелудочной железы.
Показания
- рак и опухоли головки поджелудочной железы;
- рак и опухоли большого дуоденального сосочка;
- новообразования билиарнопанкреатической области;
- рак и опухоли 12-перстной кишки.
Противопоказания
- тяжелые общетерапевтические болезни в стадии декомпенсации;
- кахексия - раковая или другая;
- выраженное метастазирование рака.
Возможность проведения такой операции в «СМ-Клиника» определяется после полного обследования пациента и онкологического и терапевтического консилиума.
Подготовка и предоперационные исследования
Перед операцией ПДР пациент проходит расширенное предоперационное исследование. Оно включает ряд стандартных процедур:
- клинический и биохимический анализы крови;
- общий анализ мочи;
- анализы крови на ВИЧ, гепатиты В и С, сифилис;
- флюорографию;
- ЭКГ.
Кроме этого, нужно сделать:
- КТ органов брюшной и грудной полости с контрастированием;
- онкоскрининг - МРТ, КТ, кровь на онкомаркеры, УЗИ.
С результатами нужно пойти к терапевту и хирургу, посетить анестезиолога, потому что вмешательство проходит под общим наркозом.
Как проходит панкреатодуоденальная резекция?
Операция Уиппла проходит под общим наркозом и может выполняться двумя способами:
- традиционная (открытая) операция через разрез в брюшной полости;
- лапароскопическое вмешательство через небольшие проколы в животе.
Иногда перед резекцией выполняется диагностическая лапароскопия, которая позволяет визуально оценить распространение рака за пределы поджелудочной железы. Если опухоль дала метастазы, хирург может решить не продолжать операцию.
Техники проведения классической и лапароскопической панкреатодуоденэктомии практически одинаковы - в ходе операции удаляется полностью опухоль и часть поджелудочной железы, 12-перстной кишки, при необходимости - часть желудка, желчный пузырь. Между удаленными частями ЖКТ накладываются анастомозы (соединяющие их элементы), чтобы восстановить проходимость и целостность соединений желудка, 12-перстной кишки, желчных протоков и протоков поджелудочной железы.
Операция выполняется только в стационаре в условиях командной работы хирургов и онкологов. Одновременно в операционной бригаде работают 3-4 хирурга. Время выполнения операции зависит от сложности - от 3 часов.
Восстановление после панкреатодуоденэктомии
После вмешательства пациент от 3 суток проводит в отделении интенсивной терапии, а потом - от 14 суток в стационаре. Ему ставят капельницы, обеспечивают уход за дренажными трубками и швами.
В первый день после операции разрешено пить прозрачные жидкости небольшими глотками. Во второй день необходимо соблюдать нулевую лечебную диету. Начиная с третьего дня после операции можно вводить в рацион твердую пищу.
После операции рекомендована химиотерапия и облучение. Это повышает выживаемость на 10%.
Возможные осложнения
- Внутрибрюшной абсцесс, лихорадка, вздутие живота, лейкоцитоз, непроходимость.
- Свищ поджелудочной железы.
- Паралич желудка от 4 до 6 недель, появляется у 25% пациентов, потому что орган адаптируется к новым условиям функционирования.
- Диарея при употреблении жирной пищи, которая уходит после курса лечения ферментами.
- Потеря веса от 5% до 10%.
- Рецидив онкологии, метастазирование в легкие, печень и брюшину.
Наши специалисты
Читайте также:
- Диагностика причины болей в спине. Лазерная вапоризация.
- Синдром Уотерхауса Фридериксена (аддисонический криз): причины, симптомы и лечение
- Диагностика стадии рака молочной железы и их критерии
- Техника, этапы операций по поводу несостоятельности тотального эндопротеза голеностопного сустава (операций спасения)
- Переломы (травмы) голеностопного сустава. Классификация, диагностика и лечение
