Техника медиального доступа к плечевой кости
Добавил пользователь Алексей Ф. Обновлено: 08.01.2026
В зависимости от локализации различают переломы плечевой кости в области проксимального метаэпифиза, диафизарные переломы и в области дистального метаэпифиза.
Патогенез (что происходит?) во время Переломов плечевой кости:
Характерными видами повреждения проксимального конца плечевой кости у детей являются переломы в области хирургической шейки, остеоэпифизеолизы и эпифизеолизы, причем типично смещение дистального фрагмента кнаружи с углом, открытым кнутри. При переломах со смещением костных отломков клиническая картина типична: рука свисает вдоль туловища и резко ограничено отведение конечности; боль в области плечевого сустава, припухлость, напряжение дельтовидной мышцы; при значительном смещении (абдукционный перелом) в подмышечной ямке пальпируется периферический отломок. Рентгенография производится в двух (!) проекциях.
Симптомы Переломов плечевой кости:
При показаниях репозиция выполняется, как правило, в условиях стационара под общим обезболиванием и периодическим контролем рентгеновского экрана. После репозиции при абдукционных переломах руку фиксируют в среднефизиологическом положении. При аддукционном переломе со смещением отломков не всегда удается обычной репозицией сопоставить костные отломки, в связи с чем целесообразно применять метод, разработанный Уитменом и М. В. Громовым. В процессе репозиции один из помощников фиксирует надплечье, а другой осуществляет постоянную тягу по длине конечности, максимально отводя руку кверху. Хирург в это время устанавливает отломки в правильном положении, надавливая на их концы (осторожно - сосудисто-нервный пучок!). Руку фиксируют гипсовой лонгетой, переходящей на туловище, в том положении, в котором было достигнуто правильное положение отломков. Срок фиксации в гипсовой лонгете - 2 нед (время, необходимое для образования первичной костной мозоли). На 14- 15-й день снимают торакобрахиальную повязку, руку переводят в среднефизиологическое положение и вновь накладывают гипсовую лонгету на 2 нед (в общей сложности срок иммобилизации 28 дней). На фоне лечебной физкультуры и физиопроцедур движения в плечевом суставе восстанавливаются в ближайшие 2-3 нед.
При эпифизеолизах и остеоэпифизеолизах со значительным повреждением ростковой зоны в отдаленные сроки может быть вызвано нарушение роста кости в длину. Диспансерное наблюдение осуществляют в течение 1,5-2 лет.
Переломы диафиза плечевой кости у детей встречаются нечасто. Клиническая картина типична. Переломы в средней трети плечевой кости опасны вследствие возможного повреждения лучевого нерва, который на этом уровне огибает плечевую кость. Смещение отломков может вызвать травматический парез или, в тяжелых случаях, нарушение целости нерва. В связи с этим все манипуляции при переломе в средней трети диафиза плечевой кости необходимо производить с особой осторожностью. Применяют метод одномоментной закрытой репозиции с последующей фиксацией в гипсовой лонгете или метод скелетного вытяжения за проксимальный метафиз локтевой кости, что дает лучший результат. Если при последующем рентгенологическом контроле обнаруживают вторичное смещение отломков, то его устраняют наложением корригирующих тяг. Обращают внимание на правильность оси плечевой кости, ибо смещение костных отломков по длине до 2 см хорошо компенсируется, в то время как угловые деформации в процессе роста не устраняются.
Переломы дистального конца плечевой кости у детей встречаются часто. Они составляют 64 % от всех переломов плечевой кости. Для диагностики повреждений в области дистального метаэпифиза плечевой кости наиболее удобной является классификация, предложенная Г. А. Баировым в 1960 г..
Чрез- и надмыщелковые переломы плечевой кости у детей - не редкость. Плоскость перелома при чрезмыщелковых повреждениях проходит через сустав и сопровождается разрывом суставной сумки и капсульно-связочного аппарата (95 % от всех повреждений). При надмыщелковых переломах плоскость перелома проходит через дистальный метафиз плечевой кости и не проникает в полость сустава (5 %). Механизм повреждения типичен - падение на вытянутую или согнутую в локтевом суставе руку. Смещение дистального отломка плечевой кости может быть в трех плоскостях: кпереди (при сгибательном чрез- или надмыщелковом переломе), кзади (при разгибательном переломе), кнаружи - в радиальную сторону или кнутри - в ульнарную; отмечается также ротация отломка вокруг оси. При значительном смещении может наблюдаться нарушение иннервации в результате травмы локтевого, лучевого или срединного нерва. Важно своевременно выявить нарушение периферического кровообращения. Пульс на лучевой и локтевой артериях может отсутствовать по 4 причинам: вследствие посттравматического спазма артериальных сосудов, сдавления артериального сосуда костным отломком или нарастающим отеком и гематомой и разрыва сосудисто-нервного пучка (самое серьезное осложнение).
При чрез- и надмыщелковых переломах плечевой кости со смещением в подавляющем большинстве случаев применяют консервативное лечение. Закрытую репозицию производят под общим обезболиванием и периодическим рентгенологическим контролем. Введение новокаина в область перелома не обеспечивает достаточной анестезии и релаксации мышц, что затрудняет манипуляции по сопоставлению отломков и удержанию их во вправленном положении. После хорошего сопоставления костных отломков обязателен контроль за пульсом, так как возможно сдавление плечевой артерии отечными мягкими тканями. После репозиции накладывают глубокую заднюю гипсовую лонгету в том положении руки, в котором удалось зафиксировать костные отломки.
При значительных отеках, неудаче одномоментной закрытой репозиции целесообразно применить метод скелетного вытяжения за проксимальный метафиз локтевой кости с грузом от 2 до 3 кг. Если перелом нестабильный (чаще наблюдается при косой плоскости), можно воспользоваться чрескожной фиксацией костных отломков по К. Паппу (диафиксация) или чрескожным остеосинтезом перекрещенными спицами Киршнера по методике Джуде. При неудаче консервативного лечения и недопустимом смещении отломков может возникнуть необходимость в открытой репозиции. Операцию производят в крайних случаях: при повторных безуспешных попытках закрытой репозиции, при интерпозиции сосудисто-нервного пучка между отломками с угрозой образования ишемической контрактуры Фолькманна, при открытых и неправильно срастающихся переломах.
Среди осложнений, которые возможны при этом виде перелома, следует отметить оссифицирующий миозит и оссификацию суставной сумки. Они наблюдаются у детей, которым производят неоднократные закрытые репозиции, сопровождающиеся разрушением грануляций и первичной костной мозоли. По мнению Н. Г. Дамье, осси-фикация суставной сумки чаще всего развивается у детей со склонностью к образованию келоидных рубцов.
Неустраненные в процессе лечения внутренняя ротация и смещение дистального фрагмента плечевой кости кнутри приводят к варусной деформации локтевого сустава. При отклонении оси предплечья на 15° у девочек и на 20° у мальчиков показана корригирующая чрезмыщелковая клиновидная остеотомия плечевой кости.
Ее выполняют не ранее чем через 1 - 2 года после травмы по методу Баирова-Ульриха. Важное значение имеет предварительный расчет объема предполагаемой резекции кости. Производят рентгенографию двух локтевых суставов в строго симметричных проекциях. Проводят ось плечевой кости и ось костей предплечья. Определяют величину полученного угла а. Измеряют степень физиологического отклонения оси предплечья на здоровой руке - угол /3, прибавляют его значение к величине угла а и таким образом определяют угол предполагаемой резекции кости. Построение угла на контурограмме производят в области дистального метафиза плечевой кости на уровне или несколько ниже вершины ямки локтевого отростка. Стороны клина по величине должны максимально приближаться друг к другу.
Переломы надмыщелков плечевой кости являются характерными повреждениями для детского возраста (наиболее часто встречается у детей от 8 до 14 лет). Они относятся к апофизеолизам, так как в большинстве случаев плоскость перелома проходит по апофизарной хрящевой зоне. Наиболее часто встречается отрыв медиального над-мыщелка плечевой кости. Его смещение связано с натяжением внутренней боковой связки и сокращением большой группы мышц, прикрепляющихся к надмыщелку. Нередко отрыв этого надмыщелка у детей сочетается с вывихом костей предплечья в локтевом суставе. При разрыве капсульно-связочного аппарата смещенный костный отломок может внедриться в полость локтевого сустава. В подобном случае происходит ущемление апофиза в плечелоктевом сочленении; возможен парез локтевого нерва. Последствия несвоевременной диагностики внедренного в полость сустава оторванного медиального надмыщелка могут быть тяжелыми: нарушение артикуляции в суставе, тугоподвижность, гипотрофия мышц предплечья и плеча вследствие частичного выпадения функции руки.
Лечение Переломов плечевой кости:
Извлечь костно-хрящевой фрагмент из полости сустава можно четырьмя способами:
- при помощи однозубого крючка (по Н. Г. Дамье);
- воспроизведением вывиха костей предплечья с последующим повторным вправлением (во время манипуляции отломок может быть извлечен из сустава и репонирован);
- в процессе оперативного вмешательства;
- по методу В. А. Андрианова.
Способ закрытого извлечения ущемленного медиального надмыщелка плечевой кости из полости локтевого сустава по Андрианову состоит в следующем. Под общим обезболиванием поврежденную руку удерживают в разогнутом положении и вальгируют в локтевом суставе, что приводит к расширению суставной щели с медиальной стороны. Кисть руки отводят в радиальную сторону для натяжения разгибателей предплечья. Легкими качательными движениями предплечья и толчкообразным давлением по продольной оси конечности медиальный надмыщелок выталкивают из сустава, после чего производят репозицию. Если консервативное вправление не удается, показана открытая репозиция с фиксацией медиального надмыщелка.
Перелом головчатого возвышения плечевой кости (эпифизеолиз, остеоэпифизеолиз, перелом эпифиза) является внутрисуставным переломом и наиболее часто встречается у детей в возрасте от 4 до 10 лет. Повреждение сопровождается разрывом капсульно-связочного аппарата, а смещение костного отломка происходит кнаружи и книзу; нередко наблюдается ротация головчатого возвышения до 90° и даже до 180°. В последнем случае костный отломок своей хрящевой поверхностью бывает обращен к плоскости излома плечевой кости. Столь значительное вращение костного отломка зависит, во-первых, от направления силы удара и, во-вторых, от тяги прикрепляющихся к латеральному надмыщелку большой группы мышц-разгибателей.
При лечении детей с переломом головчатого возвышения плечевой кости надо стремиться к идеальной адаптации костных отломков. Неустраненное смещение костного фрагмента нарушает артикуляцию в плечелучевом сочленении, приводит к развитию псевдоартроза и контрактуре локтевого сустава. При эпифизеолизах и остеоэпифизеолизах головчатого возвышения с небольшим смещением и ротацией костного отломка до 45-60° производят попытку консервативного вправления. Во время репозиции (для раскрытия суставной щели) локтевому суставу придают варусное положение, после чего давлением на костный отломок снизу вверх и снаружи кнутри производят вправление. Если репозиция не удается, а оставшееся смещение грозит возникновением стойкой деформации и контрактуры, возникает необходимость оперативного вмешательства. Открытая репозиция также показана при смещении и ротации костного фрагмента более чем на 60°, так как попытка вправления в подобных случаях почти всегда безуспешна. Кроме того, во время ненужных манипуляций усугубляются уже имеющиеся повреждения капсульно-связочного аппарата и прилежащих мышц, излишне травмируются эпифиз и суставные поверхности костей, образующих локтевой сустав. Удобен оперативный доступ к локтевому суставу по Кохеру. После репозиции костные отломки фиксируют двумя перекрещенными спицами Киршнера. Хороший результат достигается с помощью компрессирующего устройства, предложенного В. П. Киселевым и Э. Ф. Самойловичем.
Дети, перенесшие указанную травму, подлежат диспансерному наблюдению в течение 2 лет, так как не исключено повреждение ростковой зоны с образованием в поздние сроки деформации.
К каким докторам следует обращаться если у Вас Переломы плечевой кости:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Переломов плечевой кости, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Техника медиального доступа к плечевой кости
Переломы мыщелков плечевой кости в структуре ежегодной заболеваемости составляют, по разным оценкам, от 5,7 до 34 на 100 000 населения в год [5, 7]. Распределение имеет бимодальный характер с первым пиком заболеваемости у молодых мужчин в возрасте до 19 лет, как правило, в результате высокоэнергетических травм и вторым пиком у женщин пожилого возраста с сопутствующим остеопорозом и нарушениями процесса ремоделирования костной ткани [6].
Цель настоящего исследования - улучшить результаты хирургического лечения внутрисуставных оскольчатых переломов мыщелков плечевой кости с помощью чрескостного остеосинтеза аппаратом внешней фиксации.
Материал и методы
С 1998 по 2013 г. в клиниках травматологии и ортопедии Управления делами Президента РФ оперированы 55 пациентов с внутрисуставными оскольчатыми переломами мыщелков плечевой кости, которым был выполнен чрескостный остеосинтез аппаратом внешней фиксации конструкции А.И. Городниченко.
Хирургическое лечение переломов мыщелков плечевой кости осуществляли методом чрескостного остеосинтеза с применением спице-стержневого аппарата, основными преимуществами которого являлись стабильность достигаемого остеосинтеза на весь период лечения, элементы аппарата, изготовленные из высокопрочного рентгенопрозрачного углепластика, что позволяло контролировать точность закрытой репозиции во всех проекциях, одностороннее расположение, компактные размеры и незначительная масса всей конструкции, а также «плавающие» держатели стержней, не препятствующие устранению всех видов смещения костных отломков [2]. Наш опыт наглядно показал простоту и безопасность остеосинтеза данным аппаратом, минимальную травматичность операции и высокую стабильность фиксации костных отломков даже у больных с остеопорозом.
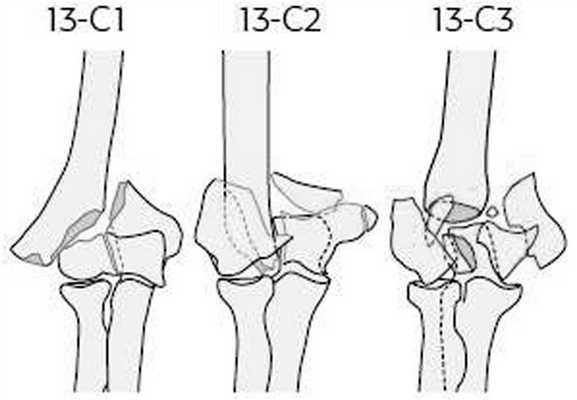
Показаниями к чрескостному остеосинтезу аппаратом внешней фиксации являлись открытые и закрытые оскольчатые внутрисуставные переломы мыщелков плечевой кости типов 13-С1,2,3 по классификации АО [4] (рис. 1). Рисунок 1. Классификация АО внутрисуставных оскольчатых переломов мыщелков плечевой кости (тип 13-С1,2,3). Среди повреждений преобладали открытые и закрытые переломы типов 13-C1,2 по классификации AO. В случае открытых повреждений подобного типа больные были оперированы в течение первых 6 ч с момента поступления. Переломы 13-С1 встречались в 26 (47,2%) наших наблюдениях, переломы 13-С2 - в 20 (36,4%) и переломы 13-С3 - в 9 (16,4%) наблюдениях.
Все оперативные вмешательства проводили на ортопедическом столе под контролем электронно-оптического преобразователя. Методом анестезии являлась либо проводниковая анестезия - блок плечевого сплетения, либо внутривенный наркоз. Репозицию перелома, как правило, проводили закрыто, и только при многооскольчатых внутрисуставных переломах типа 13-С3 выполняли открытую репозицию с целью наиболее точного восстановления конгруэнтности суставных поверхностей. Количество вводимых стержней зависело от характера перелома и наличия сопутствующего остеопороза. В область дистального метаэпифиза плечевой кости вводили 1 или 2 стержня и 1 или 2 спицы с упорными площадками, которые крепили с наружной стороны в аппарате внешней фиксации. В диафиз плечевой кости вводили 1 или 2 кортикальных стержня. Все стержни вводили через разрезы кожи длиной до 5 мм, что позволяло сократить интраоперационную кровопотерю до 10-30 мл, а продолжительность операции до 30-45 мин. Окончательной репозиции достигали на операционном столе с помощью средств ручной репозиции, чему в значительной мере способствовало то обстоятельство, что основные элементы аппарата были выполнены из рентгенопрозрачного углепластика.
Результаты и обсуждение
Консолидация перелома наступила во всех наблюдениях. Вторичного смещения отломков в аппарате нами не отмечено. Средний срок фиксации составил 78 дней (от 65 до 98 дней). Ближайшие результаты оценивали через 2,5-3 мес после операции при демонтаже аппарата, отдаленные - через 10-12 мес после остеосинтеза на основании клинико-рентгенологических данных.
Отличным считали результат, при котором наступала консолидация перелома, объем движений восстанавливался более чем на 80% исходного (110° и более), субъективная оценка больным функции очень хорошая, пациент вернулся к предыдущей работе.
Результат расценивали как хороший, если наступала консолидация перелома, объем движений восстанавливался более чем на 65% исходного (от 90° до 109°), субъективная оценка больным функции хорошая, пациент вернулся к некоторым видам работы.
Удовлетворительным считали результат, при котором наступала консолидация перелома, объем движений восстанавливался более чем на 50% исходного (от 70° до 89°), субъективная оценка больным функции удовлетворительная, пациент полностью пригоден к облегченному труду.
Как неудовлетворительный оценивали результат при восстановлении объема движений менее чем на 50% исходного (менее 70°), субъективной оценке больным функции как неудовлетворительной, пациент нетрудоспособен.
Демонтаж аппаратов производили в амбулаторных условиях либо пациентов госпитализировали в стационар на один день. Через 1 год после остеосинтеза из 51 (92,7%) обследованного у 9 (17,6%) отмечены отличные результаты, у 24 (47,1%) - хорошие и у 18 (35,3%) - удовлетворительные. Неудовлетворительных результатов не было. Из осложнений у 4 (7,3%) пациентов отмечалось воспаление мягких тканей вокруг стержней, которое было купировано в стационаре и не потребовало демонтажа аппарата.
С целью иллюстрации полученных результатов приводим клинический пример.
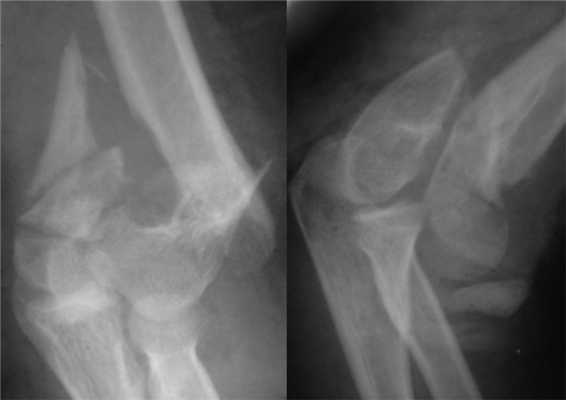
Больная П., 25 лет, поступила в стационар с жалобами на боли в левом локтевом суставе через 2 ч после травмы в результате падения на улице. При осмотре отмечены отек левого локтевого сустава, болезненность при пальпации, невозможность движений в суставе из-за боли. После клинико-рентгенологического обследования установлен диагноз: закрытый внутрисуставной оскольчатый чрезмежмыщелковый перелом левой плечевой кости со смещением отломков тип 13-С2 (рис. 2). Рисунок 2. Рентгенограммы больной П. с внутрисуставным оскольчатым чрезмежмыщелковым переломом левой плечевой кости со смещением отломков тип 13-С2.
Сосудистых и неврологических расстройств в дистальных отделах левой верхней конечности выявлено не было. При поступлении произведена анестезия места перелома, внешняя иммобилизация гипсовой лонгетной повязкой.
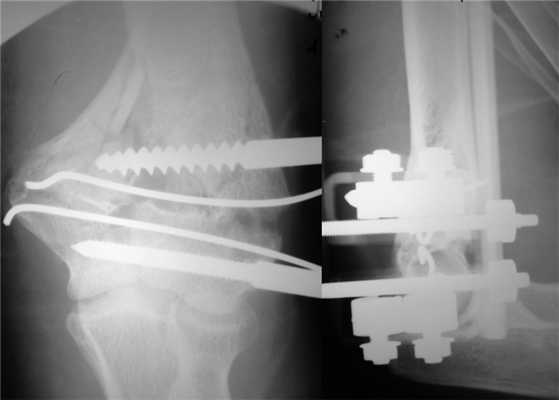
На следующий день под новокаиновым блоком плечевого сплетения произведена операция: закрытая репозиция и чрескостный остеосинтез левой плечевой кости спице-стержневым аппаратом внешней фиксации конструкции А.И. Городниченко. Через разрезы кожи и мягких тканей по наружной поверхности левого плеча длиной до 5 мм введено 2 кортикальных стержня в диафиз плечевой кости, один кортикальный и один спонгиозный стержень и 2 спицы с упорной площадкой в мыщелки и надмыщелки плечевой кости. После фиксации проксимальных стержней в аппарате под контролем электронно-оптического преобразователя произведена закрытая репозиция с помощью съемных рукояток с последующей стабилизацией дистальных стержней и спиц (рис. 3). Рисунок 3. Рентгенограммы больной П. после остеосинтеза левой плечевой кости спице-стержневым аппаратом. Кожа вокруг стержней ушита одиночными швами. Кровопотеря в ходе операции 20 мл. Продолжительность операции 40 мин.

Послеоперационное течение без осложнений, проводили регулярные перевязки с обработкой кожи вокруг стержней и спиц растворами антисептиков и сменой асептических повязок. Швы вокруг стержней сняты через 8 дней после операции, пациентка выписана на амбулаторное лечение с рекомендациями по дальнейшему восстановительному лечению. Движения в левом локтевом суставе перед выпиской из стационара показаны на рис. 4. Рисунок 4. Рентгенограммы больной П. после остеосинтеза левой плечевой кости спице-стержневым аппаратом.
После консолидации перелома через 71 день произведен демонтаж аппарата (рис. 5). Рисунок 5. Рентгенограммы больной П. после остеосинтеза левой плечевой кости спице-стержневым аппаратом. Движения в левом локтевом суставе после демонтажа аппарата от 0 до 128° (рис. 6). Рисунок 6. Внешний вид больной П. после демонтажа аппарата (объем движений в левом локтевом суставе от 0 до 128°).
Таким образом, полученные нами результаты лечения оскольчатых внутрисуставных переломов мыщелков плечевой кости (тип С по классификации АО) с применением чрескостного остеосинтеза аппаратом внешней фиксации конструкции А.И. Городниченко свидетельствуют о его высокой эффективности по созданию стабильного остеосинтеза, позволяющего сохранить функцию поврежденного сустава на протяжении всего периода лечения, что при регулярных занятиях лечебной физкультурой обеспечивает восстановление объема движений в поврежденном суставе и создает условия для восстановления трудоспособности пациентов. Применение малотравматичного чрескостного остеосинтеза дает возможность избежать значительной кровопотери в ходе оперативного вмешательства, а конструктивные особенности аппарата - сократить продолжительность операции.
Многократность использования в сочетании с меньшей стоимостью фиксатора по сравнению с пластинами с угловой стабильностью гарантируют достижение значительного экономического эффекта. Одностороннее расположение и компактные размеры создают условия для улучшения качества жизни пациентов в послеоперационном периоде. Применение аппарата внешней фиксации конструкции А.И. Городниченко позволяет улучшить функциональные результаты хирургического лечения оскольчатых внутрисуставных переломов мыщелков плечевой кости и избежать неудовлетворительных результатов. Применение аппарата обеспечивает сокращение сроков стационарного лечения, реабилитации и временной нетрудоспособности пациентов. Предложенный метод лечения переломов дистального отдела плечевой кости можно рекомендовать для широкого практического применения.
Центральный научно-исследовательский институт травматологии и ортопедии им. Н.Н. Приорова Министерства здравоохранения и социального развития РФ, Москва
ФГАОУ ВО «Российский Университет Дружбы Народов», Москва, Россия
ФГБУ «НМИЦ ТО им. Н.Н. Приорова» Минздрава России, Москва, Россия
Тактика хирургического лечения посттравматических ложных суставов и дефектов диафиза плечевой кости
Журнал: Вестник травматологии и ортопедии им Н.Н. Приорова. 2019;(1): 35‑41
Актуальность. Переломы плечевой кости составляют от 5 до 8% от всех переломов костей скелета. Несращения их встречаются нечасто, однако в случае наличия инфекции, нарушенного кровоснабжения, при открытых, многооскольчатых переломах вторичное костное сращение может быть затруднено. В случае нарушенного местного репаративного потенциала выбор в пользу становится практически неизбежным. Цель исследования: определение показаний к кровоснабжаемой костной пластике при ложных суставах и дефектах плечевой кости и анализ ее эффективности. Пациенты и методы. В отделении микрохирургии и травмы кисти ФГБУ «НМИЦ ТО им. Н.Н. Приорова» в период с 2010 по 2017 г. было проведено оперативное лечение с использованием васкуляризованных костных трансплантатов 41 пациента с ложными суставами и дефектами плечевой кости. У 38 пациентов использовался васкуляризованный трансплантат из малоберцовой кости, у 3 — из медиального мыщелка бедренной кости. Во всех случаях применялся накостный остеосинтез пластиной. Оценка результатов проводилась на основании рентгенологического исследования и компьютерной томографии. Результаты. Консолидация перелома при кровоснабжаемой костной пластике была достигнута в 36 (88%) случаях в течение 4-6 мес: в группе с применением малоберцового трансплантата — в 33 случаях, в группе с применением трансплантата из мыщелка бедренной кости — у 3 пациентов. Заключение. Каждый ложный сустав плечевой кости имеет уникальный комплекс причин возникновения и требует индивидуализированного подхода. При длительно существующих посттравматических ложных суставах и дефектах плечевой кости кровоснабжаемая костная пластика является эффективным способом лечения. Конфликт интересов: не заявлен Источник финансирования: исследование проведено без спонсорской поддержки
Введение. Переломы плечевой кости составляют от 5 до 8% от всех переломов костей скелета [1]. Несращения их встречаются нечасто: накостный остеосинтез — в 5,5-8,7% случаев, блокируемый интрамедуллярный остеосинтез — в 3-5,6% [15]. Однако, несмотря на редкую встречаемость, они могут представлять значительные трудности для травматолога-ортопеда.
Существуют различные факторы, которые могут предрасполагать к несращению плечевой кости у пациента. Ожирение, остеопороз, алкоголизм, курение, сопутствующие заболевания могут увеличить частоту несращения, однако их невозможно скорректировать перед выполнением ревизионной хирургии [1]. Тем более что обычно у пациента имеется более одного фактора, приводящего к слабости репаративного потенциала при переломе плечевой кости [14].
Плохое качество кости, связанное с наличием у пациента остеоартрита или остеопороза может в дальнейшем компрометировать среду, необходимую для заживления перелома. В дополнение — рубцовые ткани, оставшиеся от предыдущих хирургических вмешательств, и близость сосудисто-нервных образований к медиальной стенке плечевой кости могут осложнить хирургический доступ к зоне несращения даже для опытного травматолога-ортопеда 8.
Описано много способов лечения ложных суставов плечевой кости, дающих различную вероятность успеха. Применяются открытая репозиция и внутренняя фиксация, интрамедуллярный остеосинтез, аппараты наружной фиксации, однако выбор оптимальной методики до настоящего времени остается предметом научных дебатов.
Частота сращения ложных суставов плечевой кости при использовании традиционных методик остеосинтеза в комбинации с использованием костных трансплантатов варьирует от 70 до 92% 4, однако в случае наличия инфекции, нарушенного кровоснабжения, при открытых, сегментарных или многооскольчатых переломах вторичное костное сращение может быть затруднено [7].
Распространенность костной консолидации при открытой репозиции и внутренней фиксации неинфицированного ложного сустава плечевой кости варьирует от 64 до 100% [11]. Присутствие инфекции часто ассоциировано со значительно более низкой вероятностью достижения костного сращения, ограничивает возможности хирургического лечения и приводит к ухудшению функциональных результатов [1, 4]. Лечение инфицированных ложных суставов, ложных суставов у пациентов с множеством предшествующих неудавшихся попыток оперативного лечения в анамнезе должно быть комплексным [15]. В таких ситуациях использование васкуляризованного костного трансплантата становится практически неизбежным, так как оно обусловливает большую вероятность успеха и ускорения репаративного процесса 16.
Дополнительным преимуществом васкуляризованного костного трансплантата является возможность его применения в сочетании с кожно-мышечным лоскутом для реконструкции сопутствующего мягкотканного дефекта.
Цель настоящего исследования — определение показаний к кровоснабжаемой костной пластике при ложных суставах и дефектах плечевой кости и анализ ее эффективности.
Материал и методы
В отделении микрохирургии и травмы кисти ФГБУ «НМИЦ ТО им. Н.Н. Приорова» в период с 2010 по 2017 г. было проведено оперативное лечение 41 пациента (19 мужчин, 22 женщины) с ложными суставами и дефектами плечевой кости с использованием васкуляризованных костных трансплантатов. Средний возраст пациентов составил 41 год (18-65 лет), средний период времени с момента травмы — 2 года и 4 мес (1-8 лет).
До поступления в НМИЦ ТО им. Н.Н. Приорова некоторые пациенты уже были оперированы с применением различных методик наружного и погружного остеосинтеза: среднее количество операций — 2,2 (2-7).
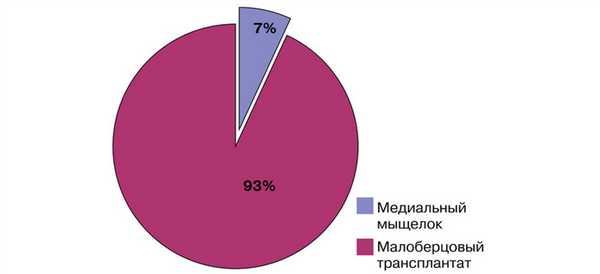
Кровоснабжаемый трансплантат из малоберцовой кости использовался у 38 (93%) пациентов, васкуляризованный трансплантат из медиального мыщелка бедренной кости — у 3 (7%) пациентов (рис. 1). Рис. 1. Распределение пациентов по типу васкуляризованного трансплантата.
Во всех случаях применялся накостный остеосинтез пластиной без контакта пластины с трансплантатом (мостовидная костная пластика).
Перед использованием лоскута из малоберцовой кости проводился тщательный костный и мягкотканный дебридмент.
При наличии показаний в раннем послеоперационном периоде проводилась ранняя хирургическая ревизия трансплантата, чтобы избежать нарушения в нем микроциркуляции.
Оценка результатов проводилась на основании данных рентгенологического исследования и компьютерной томографии.
Результаты
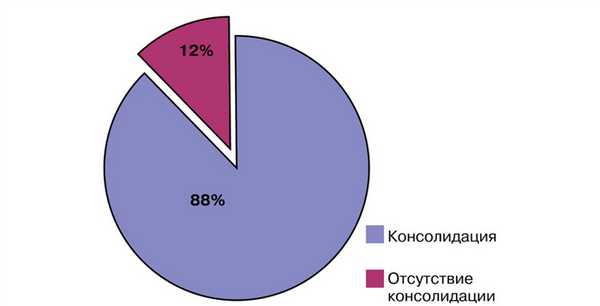
Консолидация перелома при кровоснабжаемой костной пластике была достигнута в 36 (88%) случаях в течение 4-6 мес (рис. 2): Рис. 2. Результаты оперативного лечения с использованием кровоснабжаемой костной пластикой. в группе применения малоберцового трансплантата консолидация была достигнута в 33 случаях, в группе трансплантата из мыщелка бедренной кости — в 3 случаях.
Клинический пример 1
Пациентка И., 34 лет.
Диагноз: последствия минно-взрывного ранения левого плеча с дефектом плечевой кости, мягких тканей, лучевого нерва. Остеомиелит.
На рис. 3-9 Рис. 3. Пациентка И., 34 лет. Внешний вид до операции. Рис. 9. Внешний вид и функция через год после операции. представлены все этапы обследования и лечения пациентки И.
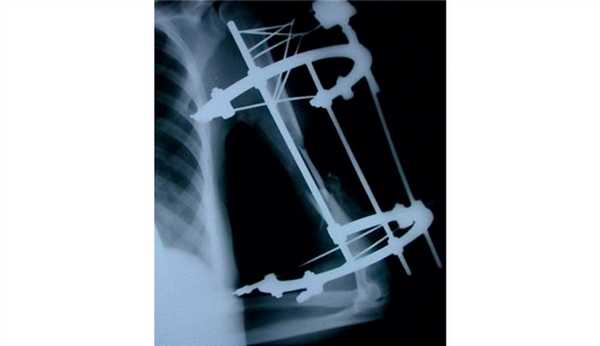
Рис. 4. Рентгенограмма пациентки И. до операции.
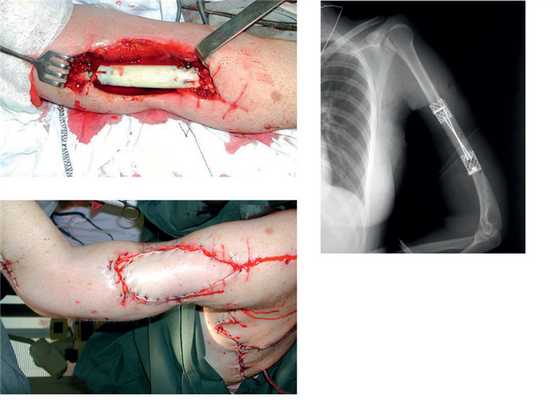
Рис. 5. Пациентка И. Этапное оперативное вмешательство. а — замещение дефекта плечевой кости цементным спейсером; б — транспозиция торакодорсального лоскута в область мягкотканного дефекта плеча; в — послеоперационная рентгенограмма.
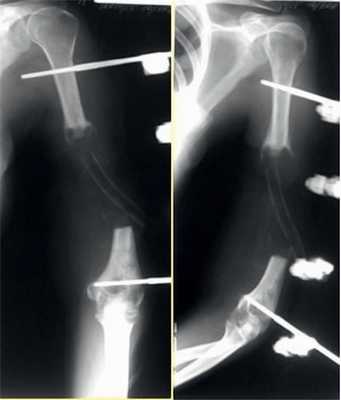
Рис. 6. Рентгенограммы пациентки И. после удаления цементного спейсера.
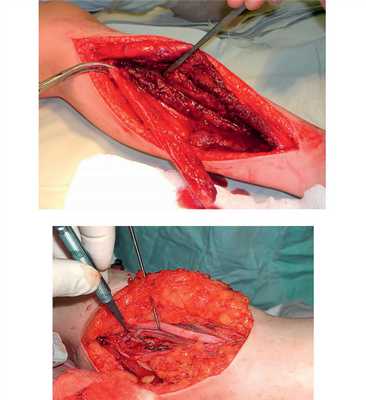
Рис. 7. Оперативное лечение пациентки И.: пластика левой плечевой кости свободным кровоснабжаемым трансплантатом из малоберцовой кости.
Клинический пример 2
Пациентка Н., 41 года.
Диагноз: ложный сустав левой плечевой кости.
На рис. 10-14 Рис. 10. Рентгенограмма пациентки Н. до операции. Рис. 14. Внешний вид и функция пациентки Н. через 8 мес после операции. представлены этапы обследования и лечения пациентки Н.
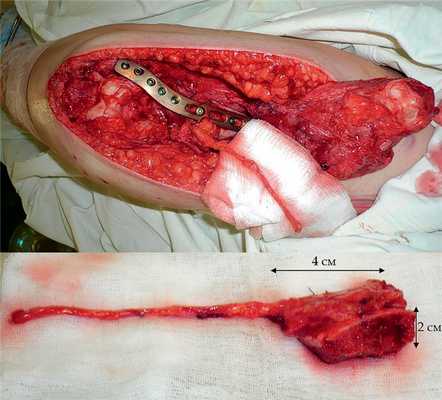
Рис. 11. Пациентка Н. Оперативное лечение: резекция зоны ложного сустава левой плечевой кости, остеосинтез пластиной и винтами. Пластика свободным кровоснабжаемым трансплантатом из внутреннего мыщелка бедренной кости.
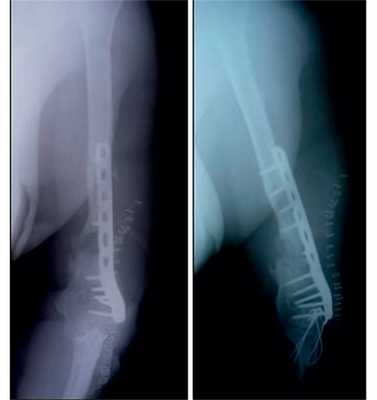
Рис. 12. Рентгенограммы пациентки Н. после операции.
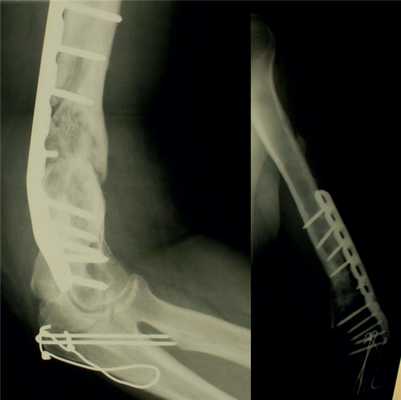
Рис. 13. Рентгенограммы пациентки Н. через 8 мес после операции.
Васкуляризованные костные трансплантаты могут быть использованы при лечении посттравматических ложных суставов, аваскулярных некрозов, некрозов кости после лучевого поражения, остеомиелита, для реконструкции костного дефекта. Выбор вида костного трансплантата остается до настоящего времени неопределенным.
В последнее время трансплантат из мыщелков бедра используется для лечения тяжелых ложных суставов конечностей, не поддающихся другому лечению [15].
В противоположность васкуляризованному трансплантату из малоберцовой кости, трансплантат из медиального мыщелка бедренной кости меньше в размерах, более гибкий и может быть с легкостью встроен в дефект неправильной формы. Эластичность трансплантата допускает его более тугую укладку вокруг трубчатой кости. Это особенно удобно при малом размере дефекта, когда использование аутокости из крыла подвздошной кости или малоберцового трансплантата может быть проблематичным [13].
A. King и соавт. [13] достигли успехов в лечении 5 пациентов с ложными суставами плечевой кости с помощью васкуляризованного кортикопериостального трансплантата из медиального мыщелка бедренной кости. Средний срок достижения костной консолидации составил 7,5 мес, ревизионное вмешательство не потребовалось ни в одном случае. Все пациенты имели отличную функцию локтевого и плечевого суставов. Эти данные совпадают с нашими наблюдениями, однако показания к выбору методики требуют уточнения в дальнейших исследованиях.
Атрофические ложные суставы без значительного костного дефекта могут быть эффективно скорректированы при помощи васкуляризованного кортикопериостального трансплантата из медиального мыщелка бедренной кости [15].
Васкуляризованный трансплантат из малоберцовой кости имеет преимущества в случае больших костных дефектов, при нестабильности и инфицированности ложного сустава, особенно при наличии множественных неудавшихся попыток получить сращение другими способами, при атрофии костной ткани и повреждении окружающих мягких тканей. Использование васкуляризованного трансплантата из малоберцовой кости, как правило, приводит к заживлению перелома с хорошим восстановлением мягких тканей и разрешением хронической инфекции [15].
Заключение. Таким образом, при длительно существующих посттравматических ложных суставах и дефектах плечевой кости, при наличии двух и более оперативных вмешательств с неудовлетворительным результатом в анамнезе кровоснабжаемая костная пластика является эффективным способом лечения.
Каждый ложный сустав плечевой кости имеет уникальный комплекс причин возникновения и требует индивидуализированного подхода.
Открытая репозиция и фиксация спицей Киршнера переломов медиального надмыщелка плечевой кости с внутрисуставным ущемлением костного фрагмента в локтевом суставе у детей

Обоснование. Перелом медиального надмыщелка часто встречается при всех переломах в локтевом суставе у детей и подростков и ассоциирован с вывихом предплечья. Вместо традиционной иммобилизации гипсовой повязкой в настоящее время все чаще применяют раннюю открытую репозицию с фиксацией спицей Киршнера или винтами. Согласно данным медицинской литературы единого мнения в отношении правильного метода лечения перелома медиального надмыщелка не существует.
Цель этого исследования заключалась в описании клинического и рентгенологических результатов и осложнений у пациентов с переломом медиального надмыщелка с внутрисуставным ущемлением костного фрагмента, которым была выполнена открытая репозиция с фиксацией спицей Киршнера.
Материалы и методы. Проведен ретроспективный анализ данных 13 детей (8-13 лет) с переломом медиального надмыщелка с внутрисуставным ущемлением костного фрагмента. Всем включенным в исследование пациентам выполнена открытая репозиция с фиксацией спицей Киршнера без ревизии локтевого нерва. Клинические исходы оценены с помощью показателей положения верхней конечности во фронтальной плоскости, объема движений в локтевом суставе, шкалы функциональной оценки локтевого сустава Mayo elbow performance score и визуально-аналоговой шкалы. Были также учтены рентгенологические данные и осложнения.
Заключение. Согласно результатам исследования открытая репозиция с фиксацией без ревизии локтевого нерва при переломе медиального надмыщелка с внутрисуставным ущемлением костного фрагмента является безопасным и эффективным методом лечения.
Ключевые слова
Полный текст
Перелом медиального надмыщелка (ПМН) составляет 11-20 % всех переломов в локтевом суставе у детей и подростков. Пик заболеваемости приходится на возраст 11-12 лет [1]. В медиальном надмыщелке (МН) располагается вторая точка окостенения, которая появляется в 5-7 лет. Слияние с диафизом плечевой кости происходит в последнюю очередь — в возрасте между 18 и 20 годами [2]. Поскольку МН не участвует в росте плечевой кости в длину, он является не истинным эпифизом, а апофизом [1]. Анатомически МН представляет собой место, откуда берет свое начало группа мышц сгибателей-пронаторов, и место прикрепления локтевой коллатеральной связки. По данным литературы, передний пучок локтевой коллатеральной связки служит одной из наиболее важных структур, стабилизирующих локтевой сустав, особенно важную роль он играет в вальгусной стабильности. Другая анатомическая роль МН заключается в осуществлении связи с локтевым нервом: МН образует медиальную стенку локтевого канала [1]. При ПМН различают три типа механизма повреждения. Первый тип — прямое повреждение. Второй тип — непрямое повреждение при падении на вытянутую руку с вальгусным направлением силового воздействия на локтевой сустав при полном разгибании. При этом мышцы — сгибатели-пронаторы оказывают отрывное воздействие на МН. Третий тип механизма повреждения ассоциирован с вывихом предплечья. В этом случае отрывное воздействие оказывает локтевая коллатеральная связка. В 15-25 % случаев МН может ущемляться внутри сустава [1].
В литературе описано несколько систем классификации, большинство из которых основано на степени смещения МН. В широко используемой классификации выделяют острые, хронические ПМН и острые переломы при сопутствующей хронической патологии [3]. В настоящее время, согласно данным медицинской литературы, единого мнения в отношении правильного метода лечения ПМН не существует, нет также четких показаний относительно величины смещения. Некоторые авторы полагают, что открытая репозиция с внутренней фиксацией показана при смещении надмыщелка более чем на 2-5 мм [1, 4, 5], в то время как другие — сообщают о хороших результатах при консервативном лечении даже таких случаев [6]. Абсолютными показаниями к хирургическому лечению считают ущемление фрагмента надмыщелка в локтевом суставе, подозрение на сдавление и дисфункцию локтевого нерва, выраженную нестабильность и открытый перелом [1, 7]. Описаны различные виды хирургических методов лечения ПМН. Хирургические методы включают открытую репозицию и фиксацию спицами Киршнера или винтами [1]. Фиксация металлическими винтами является жесткой и позволяет осуществлять ранние движения, но ассоциирована с плохой переносимостью имплантатов. С другой стороны, преимущество фиксации спицами Киршнера состоит в простоте удаления металлоконструкции без повторной операции, при этом стабильность фиксации меньше, и поэтому необходима более длительная иммобилизация [8].
Цель заключалась в описании клинического и рентгенологических результатов и осложнений у пациентов с ПМН и внутрисуставным ущемлением костного фрагмента, которым выполнена открытая репозиция с фиксацией спицей Киршнера.
Материалы и методы
Пациенты
После утверждения протокола исследования местным этическим комитетом из базы данных детской больницы Salesi были отобраны записи всех пациентов, которые в период с 1 января 2014 г. по 31 декабря 2017 г. обращались в отделение неотложной помощи по поводу ПМН. Хирург-ортопед проводил классификацию ПМН по Watson-Jones (WJ) [9] и Papavasiliou [10]. Критериями включения в данное исследование были ПМН с внутрисуставным ущемлением в локтевом суставе, изолированные ПМН (III тип по WJ) или ПМН с вывихом предплечья (IV тип по WJ). В исследование включено 13 детей (5 мальчиков и 8 девочек), средний возраст которых составил 10,9 года (8-13 лет). Согласно записям в исследование было включено 6 пациентов с изолированным ПМН с внутрисуставным ущемлением в локтевом суставе (III тип по WJ) и 7 пациентов с ПМН с внутрисуставным ущемлением в локтевом суставе после закрытой репозиции по поводу сопутствующего заднелатерального вывиха предплечья (IV тип по WJ) (рис. 1). У 6 пациентов до операции наблюдалась парестезия в зоне иннервации локтевого нерва. В отделении неотложной помощи была выполнена рентгенография локтевого сустава в стандартных переднезадней и боковой проекциях. Для подтверждения внутрисуставного ущемления до операции одному пациенту была проведена трехмерная компьютерная томография (рис. 2). Перед исследованием было получено информированное согласие родителей/опекунов пациентов на использование медицинских карт их детей. Среднее время наблюдения составило 24,1 мес. (11-44 мес.).
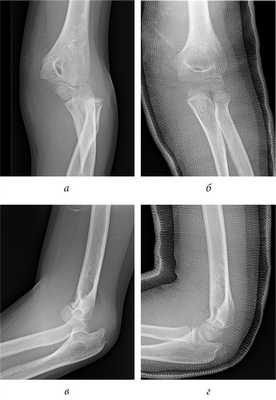
Рис. 1. Пациент С. Вывих предплечья с внутрисуставным ущемлением медиального надмыщелка: а, б — рентгенограмма вывиха предплечья; в, г — рентгенограмма после устранения вывиха предплечья с внутрисуставным ущемлением медиального надмыщелка
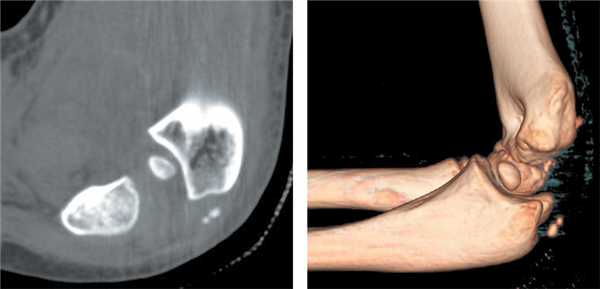
Рис. 2. Пациент С. Компьютерная томограмма с 3D-реконструкцией после устранения вывиха: внутрисуставное ущемление медиального надмыщелка
После операции оценивали объем пассивных и активных движений, анализировали функциональные результаты по шкале функциональной оценки локтевого сустава Mayo elbow performance score (MEPS) [11, 12], определяли интенсивность боли по визуально-аналоговой шкале (ВАШ) (VAS) [13]. Рентгенологическую оценку заживления перелома осуществляли с помощью стандартной рентгенографии локтевого сустава после удаления имплантатов. Все операции были выполнены главным автором. При заключительном осмотре у всех пациентов деформацию в результате ПМН после внутренней фиксации оценивали с использованием классификации, описанной Skak et al. [14]. Были также учтены развившиеся осложнения (табл. 1).
Данные пациентов, сроки наблюдения и неврологический статус при поступлении
Тип по Watson-Jones
Примечание. М — мужчины, Ж — женщины.
Хирургическая техника
Среднее время от травмы до операции составило 1,5 сут (0-4 сут). Во время операции пациенты находились в положении на спине, поврежденная верхняя конечность была расположена на рентгенопрозрачном операционном столе с ручным управлением. Операцию выполняли под внутривенной анестезией в условиях самостоятельного дыхания и с блокадой плечевого сплетения 0,5 % раствором ропивакаина под ультразвуковой навигацией. Для седации применяли мидазолам, фентанил вместе с кетамином и пропофолом. Местную анестезию осуществляли 0,5 % раствором ропивакаина. На пораженную руку накладывали нестерильный кровоостанавливающий пневматический жгут. Затем стерильное операционное поле обрабатывали от проксимальной части верхней конечности до кисти, кисть оставляли непокрытой. Руку обескровливали с помощью стерильного жгута Эсмарха, после чего пневматический жгут отпускали. Разрез начинали на 2-3 см выше локтевого сустава и на 1 см кзади от медиального надмыщелкового гребня и МН. Локтевой нерв был визуализирован и защищен с помощью ретрактора Хоманна, но ревизии нерва не выполняли. Место перелома осматривали, выявляли фрагмент медиального надмыщелка и удаляли его из полости локтевого сустава. С помощью ложки Фолькмана место перелома со стороны плечевой кости было освежено до губчатого вещества с сохранением ростковой зоны. Для расслабления мышц — сгибателей-пронаторов предплечью придавали положение пронации под углом 90° с согнутыми кистью и пальцами. Фрагмент медиального надмыщелка фиксировали скобкой Кодивиллы или Вебера так, чтобы не сломать сам фрагмент (рис. 3). После рентгенологического контроля правильности положения МН фиксировали через обе кортикальные пластины двумя скрещивающимися спицами Киршнера диаметром 1,5 мм (рис. 4).
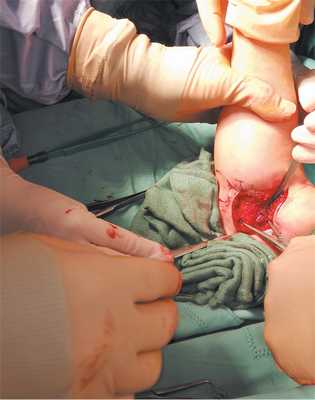
Рис. 3. Пациент С. Заднемедиальный доступ к медиальному надмыщелку. Ретрактор Хоманна установлен под медиальным гребнем для защиты локтевого нерва, а фрагмент медиального надмыщелка временно фиксирован скобкой Кодивиллы
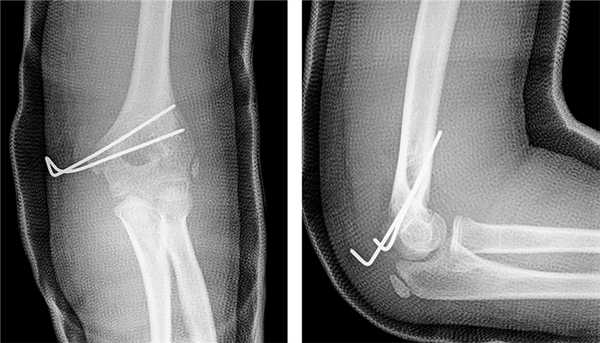
Рис. 4. Пациент С. Послеоперационная рентгенограмма: наложение изображений медиального надмыщелка и двух скрещивающихся спиц Киршнера диаметром 1,5 мм, проведенных через две кортикальные пластинки
Послеоперационное ведение
После операции с помощью гипсовой повязки локтевой сустав иммобилизировали под углом 90° с предплечьем в нейтральном положении на 4 нед. Для контроля положения спиц первую рентгенографию выполняли через 7 сут после операции. Через 4 нед. после операции гипсовую повязку снимали, до удаления спиц Киршнера выполняли вторую рентгенографию. После этого пациентам разрешали вернуться к повседневной деятельности с исключением спортивной активности минимум на 4 нед.
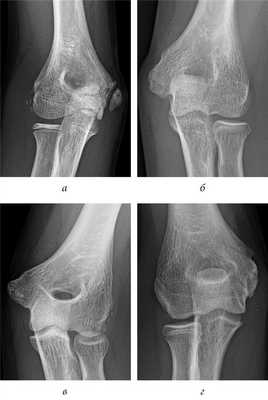
Рис. 5. Заключительные контрольные рентгенограммы: a — несращение; б — двойной контур; в — гиперплазия; г — гипоплазия
Примечание. Δ — разница в объеме движений между стороной поражения и нормальной стороной. ΔF — разница в сгибании; ΔE — разница в разгибании; ΔS — разница в супинации; ΔP — разница в пронации. ВСА — возвращение к занятиям спортом; MEPS — шкала функциональной оценки локтевого сустава Mayo; ВАШ — визуально-аналоговая шкала; ИП — исчезновение парестезии; ГО — гетеротопическая оссификация.
Во время операции мы всегда выявляем локтевой нерв и всегда защищаем его с помощью ретракторов Хоманна, но никогда не проводим его ревизию. В послеоперационном периоде не появилось каких-либо новых неврологических симптомов или усиления предшествующей парестезии. Все чувствительные нарушения со стороны локтевого нерва, установленные при поступлении, исчезли в среднем через 4,3 мес. Наши результаты совпадают с данными литературы. В нескольких исследованиях у детей показано, что 86-100 % повреждений нервов относились к нейропраксии, которая проходила самостоятельно в течение 6 мес., среднее время восстановления составляло 2 или 3 мес. [22]. Некоторые авторы во время операции рутинно выделяли и осуществляли ревизию локтевого нерва, особенно при наличии парестезии до операции, но ревизия поврежденного нерва необязательна при повреждении нерва, обусловленном закрытым переломом. Хирургическая ревизия может быть обоснована в случае персистирующего неврологического нарушения при отсутствии восстановления по клиническим или электрофизиологическим данным в течение 3 мес. [23]. Частота осложнений в нашем исследовании составила 23 % (15 % несращений и 8 % раневой инфекции), что несколько ниже, чем у других авторов [20, 21], выполнявших фиксацию винтами.
В действительности, несмотря на то, что золотым стандартом хирургического лечения ПМН является открытая репозиция с фиксацией канюлированными винтами [1], частота осложнений при этом методе достигает 31-41 % [19, 24], что вызвано, главным образом, непереносимостью винтов. Кроме того, некоторые авторы сообщают о необходимости повторного хирургического вмешательства для извлечения винтов в 70 % случаев вследствие осложнений, связанных с фиксирующими аппаратами [24]. Так, согласно данным литературы, наиболее часто при использовании винтов встречаются клинически значимое выступление головки винта, сдавление и раздражение сухожилия трехглавой мышцы плеча при сгибании/разгибании предплечья вплоть до частичного поражения дистального мышечно-сухожильного соединения трехглавой мышцы плеча [19]. У всех наших пациентов спицы Киршнера были удалены через 4 нед. без седации или анестезии и без необходимости повторной операции. Исследование ограничено небольшим размером выборки и отсутствием контрольной группы.
Заключение
Можно сделать вывод, что лечение ПМН с внутрисуставным ущемлением костного фрагмента с использованием спиц Киршнера дает отличные функциональные результаты, характеризуется частотой осложнений, сопоставимой с золотым стандартом лечения при помощи канюлированных винтов, без необходимости проведения повторной операции. Открытая репозиция с фиксацией спицами Киршнера при ПМН с внутрисуставным ущемлением костного фрагмента у детей является высокоэффективным методом лечения, который может составить альтернативу применению канюлированных винтов. Считаем, что рутинная ревизия локтевого нерва во время операции необязательна, поскольку при наличии парестезии существует тенденция к самостоятельному исчезновению симптомов в течение 6 мес., достаточно выявить и защитить локтевой нерв с помощью ретракторов. Четкой корреляции между методом лечения и видом патологических изменений МН не существует. Необходимо проведение дальнейших исследований.
Дополнительная информация
Источник финансирования. Авторы заявляют об отсутствии денежного вознаграждения.
Конфликт интересов. Авторы сообщают об отсутствии явных или потенциальных конфликтов интересов, связанных с публикацией статьи.
Этическая экспертиза. Все процедуры, выполненные с участием включенных в исследование людей, соответствовали этическим нормам научного комитета учреждения и/или национального научного комитета и Хельсинкской декларации 1964 г. и ее поздним версиям или аналогичным этическим нормам. Протокол, локальные формы информированного согласия (версия на местном и английском языке), материалы для обучения участников и для набора пациентов в исследование и другие необходимые документы, любые последующие изменения были рассмотрены и утверждены комитетом отдела клинической молекулярной науки (Department of Clinical and Molecular Science — DISCLIMO) в соответствии с принципами клинической ортопедии согласно уставу регионального этического комитета № 160/DG Политехнического университета Марке, Анкона, Италия (27.02.2019).
Вклад авторов
Д. Массетти, М. Маринелли, В. Коппа — концепция и дизайн исследования.
Д. Фальчиони — анализ полученных результатов.
Н. Спеккиа, А.П. Гиганте — обработка материала, редактирование текста.
Н. Джампаолини — написание текста.
Все авторы внесли существенный вклад в проведение исследования и подготовку статьи, прочли и одобрили финальную версию перед публикацией.
Читайте также:
- Симптомы заболевания вестибулярного аппарата. Признаки поражения слуха при паротите
- Причины травматического шока. Механизмы развития травматического шока
- Показания для артродеза первого плюснефалангового сустава
- Редкие опухоли головного мозга: пинеальные опухоли, лимфомы, хордомы
- Оценка ремоделирования левого желудочка. Оценка ишемической митральной регургитации и инфаркта правого желудочка
