Введение в лучевую диагностику лимфатических узлов шеи: лучевая анатомия, методы исследования
Добавил пользователь Алексей Ф. Обновлено: 28.01.2026
Легкие - один из самых частых объектов лучевого исследования. О важной роли рентгенолога в изучении морфологии органов дыхания и распознавании патологических процессов свидетельствует тот факт, что принятые классификации многих заболеваний, например пневмоний, туберкулеза, саркоидоза, пневмокониозов, злокачественных опухолей, в большой мере основаны на рентгенологических данных. Известно также, что скрыто протекающие поражения легких выявляют при проверочных флюорографических обследованиях населения.
С развитием компьютерной томографии значение рентгенологического метода в диагностике болезней легких еще более возросло. С ее помощью удается выявить самые ранние изменения в органах грудной полости. Важное место в оценке функциональной патологии легких, в частности нарушений капиллярного кровотока в них, занял радионуклидный метод.
Показания к рентгенологическому исследованию легких весьма широки: повышение температуры тела, кашель, выделение мокроты, одышка, боли в груди, кровохарканье и многие другие патологические состояния.
Лучевая анатомия легких
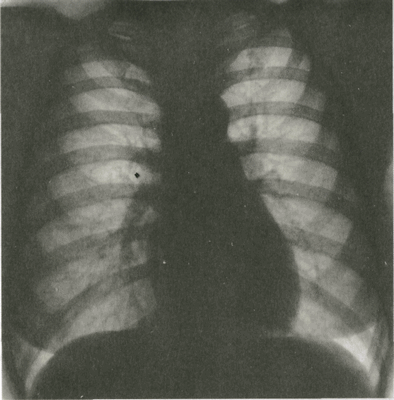
На обзорной рентгенограмме в прямой проекции (рис 1) почти на всем протяжении вырисовываются верхние 5-6 пар ребер. У каждого из них можно выделитьтело, передний и задний концы. Нижние ребра частично или полностью скрыты за тенью средостения и органов, расположенных в поддиафрагмальном пространстве. Изображение передних концов ребер обрывается на расстоянии 2-5 см от грудины, так как реберные хрящи не дают различимой тени на снимках. У лиц старше 17-20 лет в этих хрящах появляются отложения извести в виде узких полосок по краю ребра и островков в центре хряща. Их, разумеется, не следует принимать за уплотнения легочной ткани. На рентгенограммах легких имеется также изображение костей плечевого пояса (ключиц и лопаток), мягких тканей грудной стенки, молочных желез и органов, расположенных в грудной полости (легкие, органы средостения).
Рис.1 Передняя обзорная рентгенограмма органов грудной полости и схема к ней.
1 — передний конец ребра; 2 — трахея и главные бронхи; 3 — тело ребра; 4 -правая нижнедолевая артерия; 5 — диафрагма; 6 — задний конец ребра; 7 -корень левого легкого; 8 — контур левой молочной железы.
Оба легких на обзорной прямой рентгенограмме видны раздельно; они образуют так называемые легочные поля, которые пересекаются тенями ребер. Между легочными полями находится интенсивная тень средостения. Легкие здорового человека заполнены воздухом, поэтому на рентгенограмме представляются очень светлыми. Легочные поля имеют определенную структуру, которую называют легочным рисунком. Он образован тенями артерий и вен легких и в меньшей степени окружающей их соединительной тканью. В медиальных отделах легочных полей, между передними концами II и IV ребер, вырисовывается тень корней легких. Главным признаком нормального корня является неоднородность его изображения: в нем можно различить тени отдельных крупных артерий и бронхов. Корень левого легкого расположен немного выше корня правого, его нижняя (хвостовая) часть скрывается за тенью сердца.
Легочные поля и их структура видны только потому, что в альвеолах и бронхах содержится воздух. У плода и мертворожденного ребенка ни легочные поля, ни их рисунок на снимке не отражаются. Только при первом
вдохе после рождения воздух проникает в легкие, после чего появляется изображение легочных полей и рисунка в них.
Легочные поля делят на верхушки - участки, расположенные выше ключиц, верхние отделы - от верхушки до уровня переднего конца II ребра, средние - между II и IV ребрами, нижние - от IV ребра до диафрагмы. Снизу легочные поля ограничены тенью диафрагмы. Каждая половина ее при исследовании в прямой проекции образует плоскую дугу, идущую от бокового отдела грудной стенки до средостения. Наружный отдел этой дуги составляет с изображением ребер острый реберно-диафрагмальный угол, соответствующий наружному отделу реберно-диафрагмального синуса плевры. Наиболее высокая точка правой половины диафрагмы проецируется на уровне передних концов V-VI ребер (слева - на 1-2 см ниже).
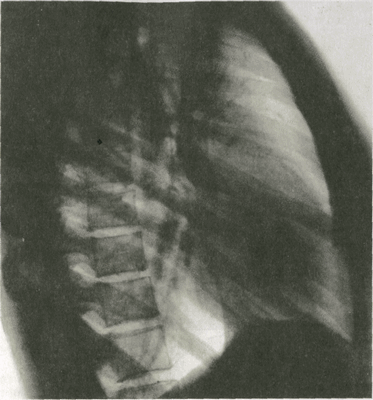
На боковом снимке изображения обеих половин грудной клетки и обоих легких накладываются друг на друга, но структура ближайшего к пленке легкого выражена резче, чем противоположного. Четко выделяются изображение верхушки легкого, тень грудины, контуры обеих лопаток и тени грудных позвонков с их дугами и отростками (рис.2). От позвоночника к грудине в косом направлении вниз и вперед идут ребра.
Рис 2. Обзорная рентгенограм органов грудной полости в боков проекции и схема к ней. 1 -- край лопатки (спереди -- право сзади — левой); 2 — нисходящая час аорты; 3 -- тела ребер левой сторон 4 — задняя поверхность правого легк го; 5 — задняя поверхность левого ле кого; 6 — тела позвонков; 7 — бифурк ция трахеи; 8 — сосуды в корне легк го; 9 — грудина в профиль.
В легочном поле на боковом снимке выделяются два светлых участка: позадигрудинное (ретростернальное) пространство — область между грудиной и тенью сердца и восходящей аорты, а также позадисердечное (ретрокардиальное) пространство — между сердцем и позвоночником. На фоне легочного поля можно различить рисунок, образованный артериями и венами, которые направляются в соответствующие доли легких. Обе половины диафрагмы на боковом снимке имеют вид дугообразных линий, идущих от передней грудной стенки до задней. Высшая точка каждой дуги находится примерно на границе ее передней и средней третей. Вентральнее этой точки расположен короткий передний скат диафрагмы, а дорсальнее — длинный задний скат. Оба ската со стенками грудной полости составляют острые углы, соответствующие реберно-диафрагмальному синусу.
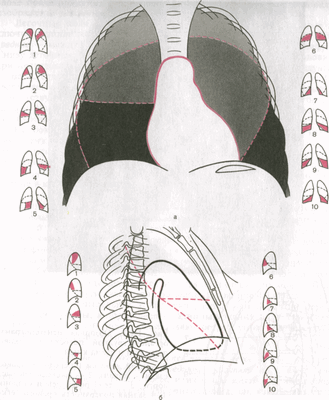
Междолевыми щелями легкие делятся на доли: левое на две— верхнюю и нижнюю, правое на три — верхнюю, среднюю и нижнюю. Верхняя доля отделяется от другой части легкого косой междолевой щелью. Знание проекции междолевых щелей очень важно для рентгенолога, так как позволяет устанавливать топографию внутрилегочных очагов, но непосредственно на снимках границы долей не видны. Косые щели направляются от уровня остистого отростка Thnr к месту соединения костной и хрящевой частей IV ребра. Проекция горизонтальной щели идет от точки пересечения правой косой щели и средней подмышечной линии к месту прикрепления к грудине IV ребра.
Рис. 3. Проекция долей и сегментов легких на рентгенограмме.
Более мелкой структурной единицей легкого является бронхолегочный сегмент. Это участок легкого, вентилируемый отдельным (сегментарным) бронхом и получающий питание от отдельной ветви легочной артерии. Согласно принятой номенклатуре, в легком выделяют 10 сегментов (в левом легком медиальный базальный сегмент часто отсутствует).
Элементарной морфологической единицей легкого является ацинус - совокупность разветвлений одной концевой бронхиолы с альвеолярными ходами альвеолами. Несколько ацинусов составляют легочную дольку. Границ нормальных долек на снимках не дифференцируются, но их изображение появляется на рентгенограммах и особенно на компьютерных томограмм; при венозном полнокровии легких и уплотнении интерстициальной ткан легкого.
На обзорных рентгенограммах получается суммационное изображение толщи тканей и органов грудной клетки — тень одних деталей частично или полностью наслаивается на тень других. Для более углубленного изучения структуры легких применяют рентгеновскую томографию
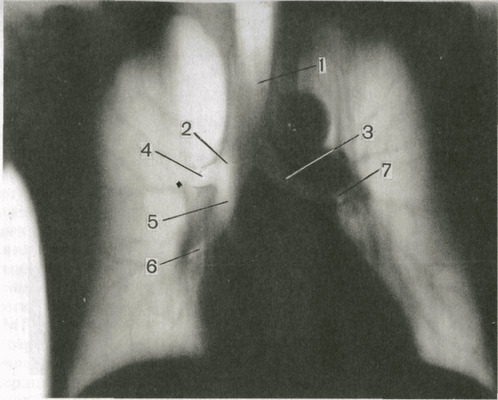
Как уже указывалось, различают два типа рентгеновской томографии-линейную и компьютерную (КТ). Линейная томография может быть выполнена во многих рентгеновских кабинетах. Благодаря доступности и дешевизне она пока еще широко распространена.
Рис.4. Томограмма на уровне срединной фронтальной плоскости грудной клетки.
1 — трахея; 2 — правый главный бронх; 3 — левый главный бронх; 4 — правый верхнедолевой бронх; 5 — промежуточный бронх; 6 — среднедолевой бронх; 7 -левый верхнедолевой бронх.
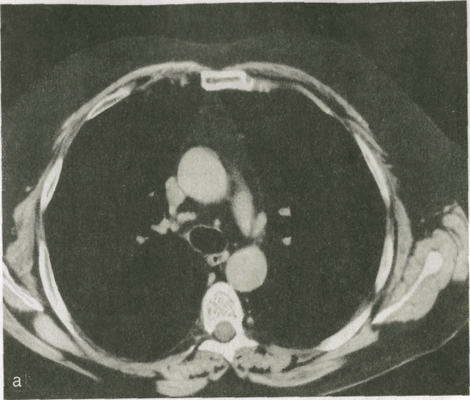
На линейных томограммахполучается резкое изображение тех образований, которые находятся в исследуемом слое. Тени структур, лежащих на иной глубине, на снимке нерезкие («размазанные») (рис. III.4). Основные показания к линейной томографии следующие: изучение состояния крупных бронхов, выявление участков распада или отложений извести в легочных инфильтратах и опухолевых образованиях, анализ структуры корня легкого, в частности определение состояния лимфатических узлов корня и средостения.
Более ценные сведения о морфологии органов грудной полости позволяет получить компьютерная томография. В зависимости от цели исследования врач выбирает «ширину окна» при анализе изображения. Тем самым он делает упор на изучение структуры либо легких, либо органов средостения.
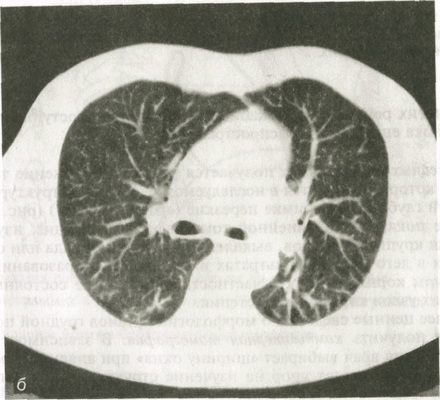
В нормальных условиях плотность легочной ткани, по данным денсито-метрии, колеблется от —650 до -850 Н. Такая низкая плотность объясняется тем, что 92 % легочной паренхимы составляет воздух и лишь 8 % — мягкие ткани и кровь в капиллярах. На компьютерных томограммах определяются тени легочных артерий и вен, четко дифференцируются главные, долевые и сегментарные бронхи, а также межсегментарные и междолевые перегородки.
Рис. 5. Компьютерные томограммы легких одного и того же пациента, выполненные при разных технических условиях.
а - для исследования органов средостения; б - для исследования легочной ткани.
Фоном для медиастинальных органов является жировая клетчатка средостения. Ее плотность колеблется от -70 до —120 HU. В ней могут быть заметны лимфатические узлы. В норме они круглой, овальной или треугольной формы. Если величина узла превышает 1 см, то его считают патологически измененным. С помощью срезов на разной глубине получают отображение пре- и паратрахеальных лимфатических узлов, узлов в аортопульмональном «окне», в корнях легких и под бифуркацией трахеи. КТ играет важную роль в оценке состояния органов средостения: она позволяет изучить тонкие детали морфологии легочной ткани (оценка состояния долек и перидольковой ткани, выявление бронхоэктазий, участков бронхиолярной эмфиземы, мелких очагов воспаления и опухолевых узелков). КТ часто необходима для установления отношения обнаруженного в легком образования к пристеночной плевре, перикарду, ребрам, крупным кровеносным сосудам.
Магнитно-резонансную томографию пока реже используют при исследовании легких из-за низкого сигнала, который дает легочная ткань. Достоинство МРТ — возможность выделения слоев в разных плоскостях (аксиальной, сагиттальной, фронтальной и др.).
Ультразвуковое исследование приобрело большое значение при исследовании сердца и крупных сосудов грудной полости, но оно позволяет получить немаловажные сведения также о состоянии плевры и поверхностного слоя легкого. С ее помощью небольшое количество экссудата плевральной полости выявляют раньше, чем при рентгенографии.
В связи с развитием КТ и бронхоскопии значительно сузились показания к специальному рентгенологическому исследованию бронхов — бронхографии. Бронхография заключается в искусственном контрастировании бронхиального дерева рентгеноконтрастными веществами (рис.6). В клинической практике показанием к ее выполнению является подозрение на наличие аномалии развития бронхов, а также внутреннего бронхиального или бронхоплеврального свища. В качестве контрастного вещества применяют пропилйодон в виде масляной взвеси или водорастворимый йодистый препарат. Исследование проводят преимущественно под местной анестезией дыхательных путей с помощью 1 % раствора дикаина или лидо-каина, но в отдельных случаях, главным образом при выполнении бронхографии у маленьких детей, прибегают к внутривенному или ингаляционному наркозу. Контрастное вещество вводят через рентгеноконтрастные катетеры, которые хорошо видны при рентгеноскопии. Некоторые типы катетеров имеют систему управления концевой частью, что позволяет вводить катетер в любые участки бронхиального дерева.
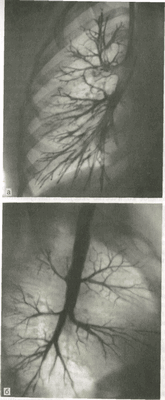
При анализе бронхограмм идентифицируют каждый контрастированный бронх, определяют положение, форму, калибр и очертания всех бронхов (рис. 6). Нормальный бронх имеет конусовидную форму, отходит от более крупного ствола под острым углом и под такими же углами отдает ряд последующих ветвей. В начальной части бронховII и III порядков нередко отмечаются неглубокие циркулярные перетяжки, соответствующие местам расположения физиологических сфинктеров. Контуры тени бронха ровные или слегка волнистые.
Рис.6. Бронхограммы правого легкого и схемы к ним.
а - прямая проекция; б - боковая проекция; 1 - верхушечный бронх 2 - задний - передний, 4 - наружный, 5 - внутренний, 6 - верхний нижней доли 7 - ниж-невнутреннии, 8 - нижнепередний, 9 - нижнёнаружный, 10 - нижнезадний.
Кровоснабжение легких осуществляется легочными и бронхиальными артериями. Первые составляют малый круг кровообращения; они выполняют функцию газообмена между воздухом и кровью. Система бронхиальных артерий относится к большому кругу кровообращения и обеспечивает питание легких. Бронхиальные артерии на рентгенограммах и томограммах не дают изображения, но ветви легочной артерии и легочные вены вырисовываются довольно хорошо. В корне легкого выделяется тень ветви легочной артерии (соответственно правой* или левой), а от нее радиально отходят в легочные поля их долевые и далее сегментарные разветвления. Легочные вены не исходят из корня, а пересекают его изображение, направляясь к левому предсердию.
Лучевые методы позволяют исследовать морфологию и функцию кровеносных сосудов легких. С помощью спиральной рентгеновской томографии и магнитно-резонансной томографии можно получить изображение начальной и проксимальных частей легочного ствола, его правой и левой ветвей и установить их взаимоотношения с восходящей аортой, верхней полой веной и главными бронхами, проследить ветвление легочной артерии в легочной ткани вплоть до самых мелких подразделений, а также обнаружить дефекты наполнения сосудов при тромбоэмболии ветвей легочной артерии.
По специальным показаниям проводят рентгенологические исследования, связанные с введением контрастного вещества в сосудистое русло,— ангиопульмонографию, бронхиальную артериографию, венокавографию.
Под ангиопульмонографией понимают исследование системы легочной артерии. После катетеризации вены локтевого сгиба или бедренной вены конец катетера проводят через правое предсердие и правый желудочек в легочный ствол. Дальнейший ход процедуры зависит от конкретных задач: если необходимо контрастировать крупные ветви легочной артерии, то контрастное вещество вливают непосредственно в легочный ствол или его главные ветви, если же изучению подлежат мелкие сосуды, то катетер продвигают в дистальном направлении до желаемого уровня.
Бронхиальная артериография — это контрастирование бронхиальных артерий. Для этого тонкий рентгеноконтрастный катетер через бедренную артерию вводят в аорту, а из нее — в одну из бронхиальных артерий (их, как известно, несколько с каждой стороны).
Показания к ангиопульмонографии и бронхиальной артериографии б клинической практике не очень широки. Ангиопульмонографию производят при подозрении на аномалию развития артерии (аневризма, стеноз, ар-териовенозный свищ) или тромбоэмболию легочной артерии. Бронхиальная артериография оказывается необходимой при легочном кровотеченвд (кровохарканье), природу которого не удалось установить посредством других исследований, в том числе при фибробронхоскопии.
Лимфатические узлы шеи
Современная классификация Американского объединенного комитета по изучению злокачественных опухолей и Американской академии оториноларингологии и хирургии головы и шеи изменена K. Robbins с соавт. в 2000 г. и утверждена AJCC-AAOHNS в 2001 г. В ней предложено разделить 3 уровня на подуровни. Классификация лимфатических узлов по уровням известна во всем мире, удобна в использовании, легка для запоминания и, что самое главное, позволяет специалистам говорить на одном языке. Она уже стала основой для классификации шейных диссекций.
Использование классификации лимфатических узлов шеи по уровням позволит решить целый ряд проблем, возникающих, в частности: 1) при определении объема хирургического вмешательства и планировании лучевой терапии; 2) при обращении больного, лечившегося в одном лечебном учреждении, в другое с выпиской, в которой указано, что больному проведено фасциально-футлярное иссечение клетчатки шеи и не указан точный объем вмешательства. В первой ситуации, где по заключению УЗИ имеется поражение шейно-надключичной зоны без указания уровней, нам трудно оценить объем поражения. Во второй ситуации без протокола хирургического вмешательства невозможно узнать точный объем ранее выполненной операции.
Классификация
I (IA и IB) - ниже тела нижней челюсти (позади ветви нижней челюсти - это уже IIA);
IA — группа подбородочных узлов
IB — группа подчелюстных лимфатических узлов (находятся спереди и сзади от подчелюстной слюнной железы). При поражении лимфатических узлов этого уровня или самой железы, то она удаляется.
II, III, IV - яремные - вдоль сосудисто-нервного пучка (внутренней яремной вены) прикрыты m.sternoclaidomastoideus
II - верхние яремные - от уровня основания черепа до уровня нижнего края подъязычной кости
IIA — верхние яремные передние — кпереди от заднего края внутренней яремной вены;
IIB — верхние яремные задние — кзади от заднего края внутренней яремной вены.
III — средние яремные - от уровня нижнего края подъязычной кости до уровня нижнего края перстневидного хряща гортани;
IV - нижние яремные — от уровня нижнего края перстневидного хряща гортани до ключиц (в т.ч. Вирховские);
V - заднего (латерального) треугольника шеи соответствует анатомическим границам
VA - акцессорные - выше уровня нижнего края перстневидного хряща, по передней поверхности трапецевидной мышцы,
VB - надключичные — ниже уровня нижнего края перстневидного хряща (исключая Вирховские);
VI - переднего пространства шеи — пре- и паратрахеальные ЛУ, предгортанные (Delphian (Дельфийские) и околощитовидные ЛУ, включающие ЛУ вдоль возвратного гортанного нерва)

Группы лимфатических узлов не входящих в классификацию.
При описании всех перечисленных ниже групп лимфатических узлов необходимо использовать традиционные названия.
1. Лимфатические узлы заушной области.
2. Подзатылочные лимфатические узлы.
3. Околоушные лимфатические узлы (внутри и внеоколоушной слюнной железы).
4. Латеральные и медиальные ретрофарингеальные лимфатические узлы (их поражение имеет значение при раке носоглотки и ротоглотки).
5. Лицевые лимфатические узлы.
6. Верхние медиастинальные лимфатические узлы (не относятся к лимфатическим узлам шеи).
Примеры лимфаденопатии разных групп лимфатических узлов шеи.
На ниже представленном КТ снимке визуализируется некроз лимфатических узлов группы IA.

На ниже представленном КТ снимке визуализируется лимфаденопатия группы IB справа.

На ниже представленном постконтрастном КТ снимке представлен пациент с карциномой языка и лимфаденопатией II группы лимфатических узлов.

На ниже представленном постконтрастном КТ изображении визуализируется увеличение и контрастное усиление лимфатических узлов III группы.

На постконтрастном изображении белой стрелкой указан увеличенный лимфатический узел IV группы. У пациента удалена правая доля щитовидной железы и правая яремная вена, что указано чёрной стрелкой, всвязи с папиллярной карциномой.

На постконтрастном изображении белой стрелкой указан увеличенный лимфатический узел V группы.

На постконтрастном изображении белой стрелкой указан увеличенный лимфатический узел VI группы.
Метастатическое поражение шейных лимфатических узлов
Шейные лимфатические узлы являются частым местом метастазирования злокачественных опухолей, первичный очаг которых располагается в области головы и шеи. К ним, например, относятся плоскоклеточный рак верхних отделов дыхательных путей, а также метастазы рака слюнных желез и щитовидной железы.
Наиболее распространенным клиническим признаком является увеличивающееся образование шеи, которое обычно обнаруживается пациентом или его врачом. При подозрении на метастатическое поражения лимфатических узлов шеи для диагностики и определения наилучшей тактики лечения потребуется осмотр врачом-онкологом, инструментальные методы и биопсия.
Иногда новообразования вне области головы и шеи могут неожиданно метастазировать в шейные лимфатические узлы, что требует особенно тщательной диагностики для выявления первичного очага.
Лечение будет зависеть от типа и локализации первичной опухоли, которая распространилась в лимфатические узлы шеи, и, скорее всего, будет включать в себя комбинацию хирургического вмешательства, лучевой терапии и/или химиотерапии.
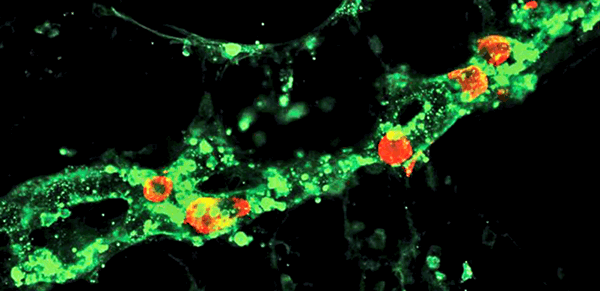
Иммунофлюоресцентная визуализация метастатических клеток меланомы (красные) внутри лимфатических сосудов (зеленые). Масштабная линейка: 100 мкм
(Science Advances/Michael Detmar Group ©)
Из чего состоит лимфатическая система шеи
Лимфатическая система шеи включает в себя сосуды и узлы.
Лимфатические капилляры — это тонкостенные структуры, состоящие из одного слоя эндотелиальных клеток. Они находятся во всех тканях организма и, объединяясь друг с другом, способствуют оттоку лимфатической жидкости в более крупные лимфатические сосуды.
Стенка лимфатических сосудов состоит из трех слоев: внутреннего слоя эндотелиальных клеток, среднего мышечного слоя и внешнего слоя соединительной ткани. В лимфатических сосудах гораздо больше клапанов, чем в венозных, при этом циркуляция лимфы полностью зависит от сжатия сосудов окружающими мышцами. Лимфатические сосуды дренируют лимфу в лимфатические узлы.
В среднем на каждой стороне шеи расположено до 75 лимфатических узлов. Снаружи узел покрывает капсула, под которой располагается субкапсулярные синусы - место куда попадает лимфатическая жидкость из приносящих лимфатических сосудов. Жидкость проходит сквозь ткань лимфатического узла, которая состоит из коркового и мозгового вещества, а затем выходит через ворота лимфатического узла и попадает в отводящие лимфатические сосуды. В итоге лимфа попадает в венозную систему в месте соустья внутренней яремной и подключичной вены.
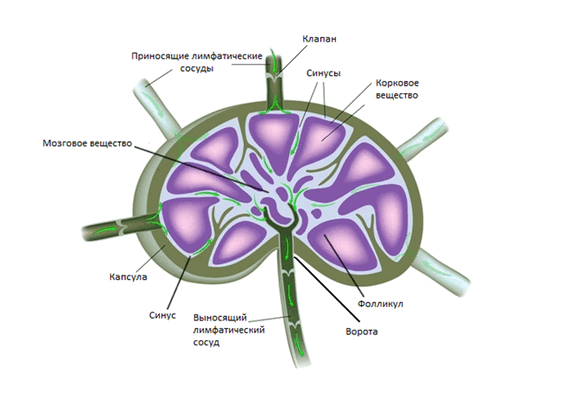
Анатомическая структура лимфатического узла (Alila Medical Media/ Shutterstock ©)
Классификация лимфатических узлов шеи
На данный момент во всем мире рекомендована к использованию классификация Американского объединенного комитета по раку (American Joint Committee on Cancer (AJCC)) 8 издания от 2018 года:
- Уровень I (IA и IB): подбородочные и поднижнечелюстные лимфатические узлы;
- Уровень II (IIA и IIB): верхняя яремная группа (делится на 2 подуровня, границей между которыми является добавочный нерв);
- Уровень III: средняя яремная группа;
- Уровень IV: нижняя яремная группа;
- Уровень V (VА и VB): лимфатические узлы заднего треугольника шеи;
- Уровень VI: передние шейные лимфатические узлы;
- Уровень VII: верхние медиастинальные лимфатические узлы.
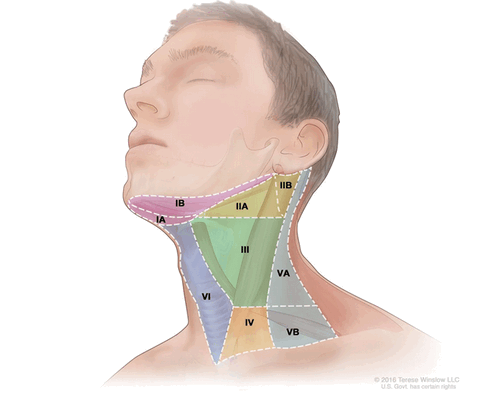
Уровни лимфатических узлов шеи (Tenese Winslow LLC ©)
Диагностика
Осмотр
При пальпации шеи врач обращает внимание на расположение, размер, плотность и подвижность каждого узла. Особое внимание уделяется узлам, которые кажутся фиксированными к подлежащим сосудисто-нервным структурам и внутренним органам. Описание каждого узла становится важной частью медицинской документации, которая в дальнейшем может использоваться для оценки эффекта лечения.
Лучевые методы
Преимуществами УЗИ перед другими методами визуализации являются цена, скорость исследования и низкая лучевая нагрузка на пациента.
Ультразвуковыми признаками метастатического поражения лимфатических узлов может быть образование сферической формы, нарушение структуры, нечеткие границы, наличие центрального некроза и др.
Поскольку не всегда по УЗИ можно с уверенностью сказать является лимфатический узел пораженным или нет, иногда одновременно выполняют тонкоигольную аспирационную биопсию под ультразвуковым контролем с последующим цитологическим исследованием материала из этого узла. Результат цитологического исследования зависит от навыков врача УЗИ и качества образца (т.е. наличия достаточного количества репрезентативных клеток).
С появлением систем высокого разрешения и специальных контрастных веществ КТ позволяет обнаруживать лимфатические узлы, которые могли быть пропущены при иных методах диагностики.
Ценность МРТ - превосходная детализация мягких тканей. МРТ превосходит КТ в качестве предпочтительного исследования при оценке ряда новообразований головы и шеи, таких как основание языка и слюнные железы. Размер, наличие нескольких увеличенных узлов и центральный некроз - критерии, общие для протоколов исследования КТ и МРТ.
Этот новый метод визуализации все чаще используется для определения стадии опухолей головы и шеи. Метод основан на поглощении 2-фтор-2-дезокси-D-глюкозы (ФДГ) метаболически активными тканями. Исследование также может быть объединено с КТ, чтобы улучшить разрешение получаемого изображения и более точно определить расположение образования.
Биопсия
Биопсия — это удаление небольшого кусочка ткани для исследования под микроскопом или для тестирования в лаборатории на предмет наличия признаков злокачественности. В подавляющем большинстве случаев проводится тонкоигольная аспирационная биопсия. Врач, выполняющий биопсию, может использовать УЗИ или КТ для выполнения процедуры. Иногда тонкоигольная аспирационная биопсия не позволяет поставить окончательный диагноз, и требуются другие виды биопсии, такие как трепан-биопсия или эксцизионная биопсия.
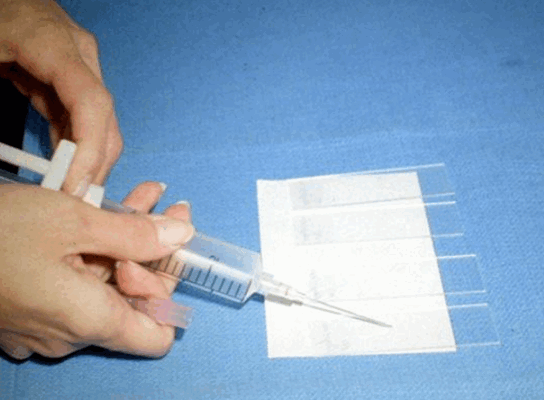 | 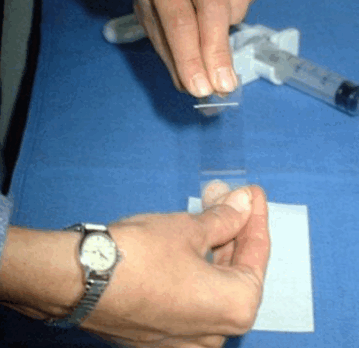 |
| Процесс приготовления предметных стекол для цитологического исследования. Материалом служит содержимое шприца после выполнения тонкоигольной аспирационной биопсии | |
План лечения
После определения диагноза и проведения всех диагностических исследований врач порекомендует оптимальный для пациента курс лечения. В конечном итоге лечение метастатического поражения лимфатических узлов зависит от типа и локализации первичной опухоли.
Существует три различных варианта лечения, которые могут быть использованы отдельно или в комбинации:
- хирургическое вмешательство,
- лучевая терапия,
- химиотерапия.
Хирургическое лечение
Хирургическое лечение обычно включает удаление лимфатических узлов шеи (лимфодиссекция) и последующее гистологическое исследование для точного определения стадии, так как это может существенно повлиять на дальнейшую тактику лечения. Хоть и не всегда, но чаще всего лимфодиссекция выполняется одновременно с удалением первичной опухоли.
Существуют различные виды лимфодиссекций:
- радикальная лимфодиссекция: удаление всех лимфоузлов, удаление внутренней яремной вены, удаление мышц и нервов;
- модифицированная радикальная лимфодиссекция: удаление всех лимфоузлов с сохранением мышц. Нервы и/или внутренняя яремная вена могут быть удалены;
- селективная лимфодиссекция: удаление только определенных групп лимфоузлов.
Лучевая терапия
Лучевая терапия может быть назначена в качестве самостоятельного метода лечения в послеоперационном периоде, чтобы снизить вероятность рецидива либо в комбинации с химиотерапией в качестве самостоятельного или адъювантного лечения. Обычно адъювантная лучевая терапия необходима, если по результатам гистологического исследования обнаруживается несколько пораженных лимфатических узлов.
Химиотерапия
Химиотерапия обычно добавляется к лучевой терапии в качестве самостоятельного или адъювантного (послеоперационного) лечения. В некоторых случаях может использоваться индукционная химиотерапия с целью уменьшения объема образования и последующего хирургического вмешательства.
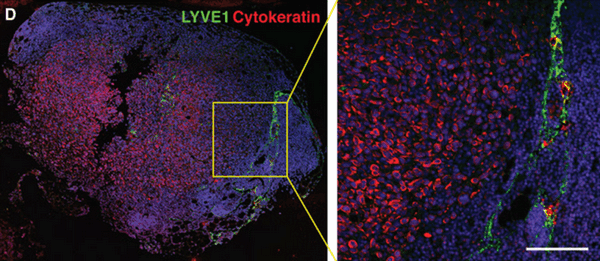
Иммунофлюоресцентная визуализация метастатически пораженного лимфатического узла с окраской на Цитокератин (красный) - маркер характерный для опухолевых клеток эпителиального происхождения. Масштабная линейка: 50 мкм
(Science Advances/Michael Detmar Group ©)
Прогноз
Метастазы в лимфатические узлы шеи могут возникать при онкологических заболеваниях различных локализаций, поэтому давать прогностические оценки для этой группы пациентов следует только после выявления первичной опухоли.
Факторы, влияющие на прогноз:
- стадия заболевания,
- локализация первичной опухоли,
- гистологический подтип и степень дифференцировки,
- количество и размер пораженных лимфатических узлов,
- характеристика края резекции опухоли.
Наблюдение после лечения
Пациенты должны регулярно посещать своего специалиста по опухолям головы и шеи для оценки состояния на предмет любых признаков рецидива заболевания.
Стандартный график наблюдения
В первые 1-2 года осмотр и сбор жалоб рекомендуется проводить каждые 3-6 месяца, на сроке 3-5 лет - один раз в 6-12 месяцев. После 5 лет с момента операции посещать врача необходимо один раз в год или при появлении жалоб. У пациентов с высоким риском рецидива перерыв между обследованиями может быть сокращен.
Список литературы:
- RUSSCO Практические рекомендации по лечению злокачественных опухолей головы и шеи. 2020г
- NCCN Clinical Practice Guidelines in Oncology Head and Neck Cancers Version 1.2021 — November 9, 2020
- DeVita, Hellman, and Rosenberg’s Cancer: Principles & Practice of Oncology (Cancer Principles and Practice of Oncology) 11th Edition 2019
- AJCC (American Joint Committee on Cancer). Cancer Staging Manual - 8th Edition. New York, NY: Springer; 2018
- Pisani, Paolo et al. “Metastatic disease in head & neck oncology.” Acta otorhinolaryngologica Italica 2020
- Van den Brekel MW. Lymph node metastases: CT and MRI. Eur J Radiol. 2000
- Chen ZW, Zhu LJ, Hou QY, Wang QP, Jiang S, Feng H. Clinical application of positron-emission tomography for the identification of cervical nodal metastases of head and neck cancer compared with CT or MRI and clinical palpation. Chinese journal of stomatology. 2008
- Qiaoli Ma et al. Unexpected contribution of lymphatic vessels to promotion of distant metastatic tumor spread. ScienceAdvances 08 Aug 2018
- Sun, J et al. Computed tomography versus magnetic resonance imaging for diagnosing cervical lymph node metastasis of head and neck cancer: a systematic review and meta-analysis. OncoTargets and therapy. 2015
- Robbins KT, Shaha AR, Medina JE, et al. Consensus statement on the classification and terminology of neck dissection. Arch Otolaryngol Head Neck Surg. 2008
- López, Fernando et al. Cervical lymph node metastases from remote primary tumor sites. Head&neck 2016

Авторская публикация:
Амиров Николай Сергеевич
Клинический ординатор НМИЦ онкологии им. Н.Н. Петрова

Под научной редакцией:
Раджабова З.А.
Заведующий отделением опухолей головы и шеи
НМИЦ онкологии им. Н.Н. Петрова,
врач-онколог, научный сотрудник, кандидат медицинских наук, доцент
Что вам необходимо сделать
Если вы хотите узнать побольше о бесплатных возможностях ФБГУ НМИЦ онкологии им. Н.Н. Петрова Минздрава России, получить очную или заочную консультацию по диагностике и лечению, записаться на приём, ознакомьтесь с информацией на официальном сайте.
Если вы хотите общаться с нами через социальные сети, обратите внимание на аккаунты в ВКонтакте и Одноклассники.
Сто оттенков лучевой диагностики: у каждого вида рака — свой «золотой стандарт» исследования
8 ноября — День рентгенолога. В этот день, в 1895 году, немецкий физик Вильгельм Конрад Рентген, проводя очередной эксперимент, открыл рентгеновское излучение. Сегодня это самый доступный и распространенный метод диагностики в мире.
Ни один метод лучевой диагностики не является универсальным, каждый имеет свои преимущества и недостатки, поэтому в реальной клинической практике врачи применяют все возможности медицинской визуализации, обсуждая в рамках мультидисциплинарной команды оптимальный алгоритм обследования пациента. С помощью Сергея Сергеевича Багненко, доктора медицинских наук, профессора, заведующего научным отделением диагностической и интервенционной радиологии НМИЦ онкологии им. Н.Н. Петрова, разбираемся, какие лучевые исследования нужно делать при конкретных онкопатологиях.

Методы лучевого исследования
Принято считать, что всего существует пять методов лучевой диагностики. В целом, деление базируется на видах лучевого воздействия, которое применяется в том или ином случае.
Рентгеновский метод — рентгеновское излучение, ультразвуковое (УЗИ) - ультразвуковые волны, МРТ - электромагнитные колебания, радионуклидный метод (позитронно-эмиссионная томография — ПЭТ, одно-фотонная эмиссионная томография - ОФЭКТ) — гамма и другие виды ионизирующего воздействия. Исключение - компьютерная томография (КТ). Данный вариант лучевой визуализации в своей основе предполагает рентгеновское излучение, и должен был бы относиться к рентгеновскому, однако его появление настолько расширило возможности классической рентгенодиагностики, что в свое время было принято решение вынести КТ в самостоятельный метод.
По большому счету, задачи, которые они выполняют, следующие:
Рентгенодиагностика — оценка состояния костей и органов грудной клетки, как правило, в рамках первичной диагностики, а также желудочно-кишечного тракта, желчных протоков и сосудов, если речь идет о рентген-контрастных методиках.
УЗИ — первичная диагностика практически любой онкопатологии, а также экспертная оценка при злокачественных поражениях щитовидной и паращитовидных желез, наружных половых органах, опухолях мягких тканей, имеющих поверхностное расположение, в том числе патологии молочных желез.
КТ — анализ состояния грудной клетки, скелета и органов живота в рамках предоперационного планирования (инвазия сосудов, поражение лимфатических узлов и пр.)
МРТ — головной, спинной мозг, молочные железы, связки и мышцы, органы малого таза и другие мягкотканные структуры.
Радионуклидный метод — решение отдельных вопросов дифференциальной диагностики (доброкачественный/злокачественный процесс и др.), оценка функционального состояния органов, а также стадирование онкологического заболевания (визуализация отдаленных метастазов и пр.).
Независимо от конкретного варианта лучевой диагностики, нативное исследование (без применения контрастных веществ) изредка может быть оправдано, однако в подавляющем большинстве случаев, особенно, если речь идет об онкопатологии, применение контрастных препаратов является обязательным.
Виды рака и методы лучевой диагностики
Рассмотрим лучевую диагностику по отдельным анатомическим локализациям.
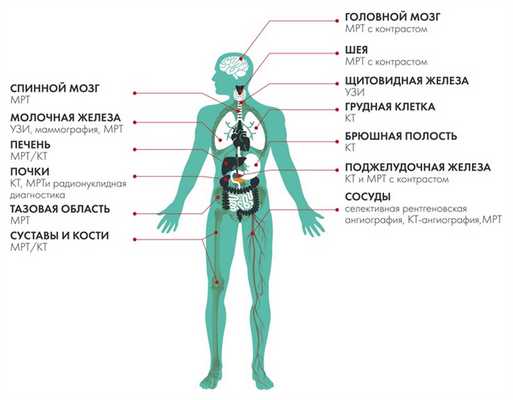
Головной мозг
Основной метод оценки непосредственно вещества головного мозга (в том числе первичных опухолей и метастазов) — МРТ с применением контрастного усиления.
Вопросы стадирования (поиск отдаленных метастазов) лучше всего решаются с помощью ПЭТ, в том числе с метионином.
Компьютерная томография используется как дополнительный метод в случае, если требуется оценка состояния костных структур, а также при наличии абсолютных противопоказаний к МРТ исследованию (наличие металла в теле — например, кардиостимулятора, ферромагнитных инородных металлических соединений: пластины, протезы, импланты и т.п.)
Первичный метод диагностики опухолей шеи — УЗИ.
Экспертная оценка - МРТ с контрастом.
КТ используется, когда необходимо оценить процесс разрушения (деструкции) костной ткани, требуется детальный анализ состояния гортани, а также есть показания к выполнению исследования сосудов (КТ-ангиография).
Радионуклидная диагностика - определение наличия онкологического процесса как такового, а также стадирование заболевания (применяются различные фармпрепараты: 18F-дезоксиглюкоза, метионин и пр.).
Щитовидная железа
Основной метод диагностики опухолевого процесса в щитовидной и паращитовидных железах — УЗИ. Отсутствие лучевой нагрузки, высокая разрешающая способность, а также доступность оборудования являются очевидными достоинствами эхографии. Особенно справедлив данный тезис, если речь идет об УЗИ с контрастным усилением и применением эластографии. Так называемое, мультипараметрическое УЗИ, то есть вариант исследования с включением в процедуру максимально количества различных методик, является наиболее перспективным вариантом реализации сонографической диагностики, особенно при злокачественной патологии.
Радионуклидная диагностика (к примеру, ПЭТ с 18F-DOPA) информативна в рамках подтверждения злокачественного характера имеющегося процесса, а также для выявления отдаленных метастазов.
Грудная клетка
С момента своего открытия (ровно 101 год назад) и по сей день рентгенодиагностика сохраняет свою актуальность (прежде всего, как метод первичной визуализации) в рамках оценки состояния легких и костной ткани. Однако «золотым стандартом» в данных областях заслужено стала КТ, базирующаяся на рентгеновском излучении, но существенно расширившая возможности классической рентгенографии. Компьютерная томография позволяет детально проанализировать состояние органов грудной клетки, оценить стадию и распространенность патологического процесса, вовлечение сосудов и других тканей, ответ на проводимую терапию.
У пациентов с острой патологией (например, реанимационных больных) может быть оправдано применение УЗИ (плевриты и др.).
МРТ эффективно для диагностики нейрогенных образований, которые располагаются в заднем средостении, а также как дополнительный метод диагностики при стадировании других опухолей средостения, например, рака пищевода.
Молочная железа
В настоящее время основными методами исследования молочных желез являются: маммография, УЗИ и МРТ. Все они обладают очевидными достоинствами и активно конкурируют между собой. Классическим вариантом визуализации (широкодоступным и понятным подавляющему большинству специалистов) является рентгеновская маммография.
УЗИ - неинвазивный метод, не предполагающий лучевую нагрузку, обладающий чрезвычайно высокими характеристиками в плане разрешающей способности изображений. Многие учреждения именно сонографический вариант диагностики рассматривают как «золотой стандарт», однако «операторозависимость» (когда два разных специалиста могут по-разному трактовать увиденное), а также невозможность оценить результаты другим специалистом (альтернативное мнение), ограничивают «зону ответственности» ультразвуковой диагностики.
МРТ решает большинство рассматриваемых вопросов, также не предполагает лучевой нагрузки, но имеет определенные ограничения в плане доступности и стоимости процедуры.
Печень
Первичная диагностика - УЗИ.
Экспертная оценка — КТ/МРТ с динамическим контрастированием.
КТ - доступнее, необременительна для пациента (само сканирование происходит за считанные секунды/минуты), позволяет в ходе одного визита исследовать в том числе легкие (что часто требуется в рамках онкоскриннинга).Это более простой, а потому более стандартизированный метод, который позволяет детально оценить состояние сосудов, что крайне важно при предоперационном планировании. Независимо от того, в каком центре проводится исследование, качество собранных данных будет, как правило, на достаточном уровне.
МРТ дает максимум информации в плане выявления и дифференциальной диагностики очаговой патологии печени, особенно если сканирование проводится с гепатотропными контрастными препаратами. Не предполагает лучевой нагрузки (то есть безвредно), а потому может выполняться многократно, в том числе беременным и детям. Однако многое зависит от того, в каком конкретно центре выполнено исследование (аппарато- и операторозависимость), занимает больше времени (сложности при обследовании пожилых, ослабленных пациентов), имеет ограничения в плане исследования легких (МРТ легких обычно не проводится и для их анализа приходится совершить визит в КТ отделение), имеет абсолютные противопоказания (например, металл в теле), уступает КТ в отношении предоперационной оценки.
Поджелудочная железа
По большому счету ситуация аналогична применяемым методам лучевой диагностики печени, однако есть некоторые нюансы. Так, из-за центрального расположения органа в теле визуализация при УЗИ может быть затруднена (тучные пациенты, при метеоризме — вздутие кишечника). Локальные обызвествления значительно лучше выявляются при КТ.
МРТ эффективнее для дифференциальной диагностики выявленных изменений.
Почки
Основные методы диагностики опухоли почки — КТ, МРТ и радионуклидный. Только в совокупности эти три составляющие могут дать врачам-онкологам полную информацию о состоянии органов. Традиционное УЗИ активно применяется для первичной оценки зоны интереса. Большие перспективы связывают с внедрением в клиническую практику УЗИ с контрастным усилением, однако по ряду технических моментов доступность данной методики сейчас ограничена.
Малый таз
«Золотым стандартом» оценки состояния органов малого таза, независимо от пола пациента, считают МРТ. И женские и мужские внутренние половые органы лучше всего оценивать с помощью МРТ с динамическим контрастированием. Впрочем, существуют ситуации, когда КТ может дать ценную дополнительную информацию.
Суставы и кости
В онкологической практике основными методами диагностики опухолей костно-мышечной системы являются МРТ и КТ.
Определенный приоритет имеет МРТ, однако, если требуется детальная оценка структуры кости или речь идет о параметрах деструкции, без КТ не обойтись.
Также в НИМЦ онкологии им. Петрова используется SLOT-рентгенография костей, когда с помощью специальной методики вся конечность, позвоночник или весь скелет целиком визуализируются на одном рентгеновском изображении. Этот метод позволяет точно определить параметры опухоли и соотнести ее с размером кости, что чрезвычайно важно хирургам при планировании вмешательства, подбора протеза или изготовления импланта.
Сосуды
Определенную информацию о состоянии некоторых сосудов можно получить при допплерографическом УЗИ, однако в онкологической практике чаще требуется более детальная информация и приходится прибегать к ангиографическим методикам.
Наиболее информативны - артериография на фоне плоскодетекторной компьютерной томографии (ПДКТ-артериография) и селективная цифровая субтракционная ангиография (ЦСА).
В 2021 году в НМИЦ онкологии им. Н.Н. Петрова в рентгеноперационной отделения рентгенохирургических методов диагностики и лечения был установлен современный ангиографический комплекс Artis Zee Flor (Siemens), позволяющий выполнять весь спектр диагностических и лечебных вмешательств, применяемых в интервенционной онкологии (в том числе с использованием ПДКТ-артериографии, ЦСА, внутрисосудистой и чрескожной 3D навигации). Однако основным недостатком данных методов визуализации является их инвазивность, требующая госпитализации пациентов для проведения вмешательства с соблюдением строгих правил асептики и антисептики.
Поэтому в рутинной практике чаще прибегают к менее инвазивным КТ-ангиографии и неинвазивной МР-ангиографии. Эти варианты визуализации позволяют проследить ход сосудов, выявить наличие тромбов, оценить наличие и степень опухолевой инвазии. КТ быстрее и обеспечивает более высокое пространственное разрешение изображений. Если применение йодсодержащих контрастов противопоказано (аллергические реакции, почечная недостаточность), выполняют магнитно-резонансное исследование. Современные технологии позволяют проводить сканирование с ЭКГ синхронизацией (требуется при изучении сосудов сердца), а также выполнять бесконтрастную МР-ангиографию (без введения контрастных препаратов в сосудистое русло).
Спинной мозг
Основной метод диагностики опухолей в спинном мозге — МРТ с контрастом. Он позволяет определить локализацию патологического процесса (интрамедуллярный или экстрамедуллярный, то есть находящийся в структуре спинного мозга или вне его), оценить его распространённость, вовлечение соседних структур. Если есть противопоказания к МРТ, а также, когда нужно детально разобраться с состоянием расположенных рядом позвонков, проводят КТ.
Пациенту важно помнить, что любые обследования, их последовательность и объем должен назначить врач-онколог. В подавляющем большинстве случаев диагностика нужна не сама по себе, а для планирования лечения, которое будет проводить соответствующий врач. Поэтому «назначенные» самостоятельно процедуры без предварительной консультации со специалистом могут быть абсолютно не информативны, то есть бесполезны, а с учетом возможной лучевой нагрузки даже вредны.


Автор:
Ирина Фигурина
специалист по связям с общественностью НМИЦ онкологии им. Н. Н. Петрова
Оренбургский государственный университет, факультет филологии
Лимфоузлы шеи. +
Но не стоит отчаиваться. Вполне себе разобраться в топике лимфоузлов можно даже с помощью более привычных анатомических ориентиров, типа грудинно-ключично-сосцевидной или трапецевидной мышц.
Для начала, современная классификациия лимфоузлов шеи (утвержденная AJCC-AAOHNS в 2001 г. на основе изменений K.Robbins с соавт. в 2000 г.) , выделяет 6 уровней (групп) лимфатических узлов. Из ни 3 (I, II и V) делятся на подгруппу (подуровни) А и В:
IA - подбородочные ЛУ;
IB - подчелюстные (в которых, по отношению к подчелюстной слюнной железе, различают пре- и постгландулярные);
II - верхние яремные (IIA - верхние яремные передние, IIB - верхние яремные задние);
III - средние яремные;
IV - нижние яремные (в т.ч. Вирховские);
V - заднего (латерального) треугольника шеи (VA - акцессорные, VB - надключичные (исключая Вирховские);
VI - переднего пространства шеи.
В современную классификацию не включены ретрофарингеальные, паротидные, щечные, около (пре- и за-) ушные и затылочные ЛУ (включаемые в предыдущую (Rouviere) классификацию 1992 г.), должны упоминаться отдельно
Желательно вспомнить анатомию лимфоузлов головы и шеи (цифры не соответствуют группам по классификации)
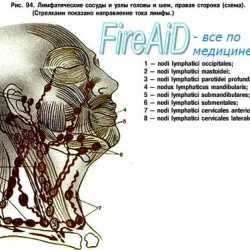
Вот еще схема, на которой также можно ознакомиться с положением лимфоузлов шеи (обозначены зеленым)
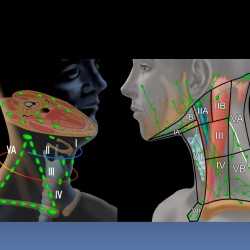
Вот еще хирургическая схема
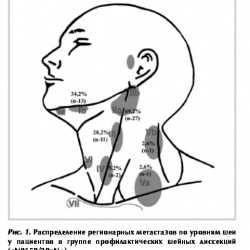
Схема разделения шеи на 3 горизонтальных уровня 2 плоскостями: по нижней границе тела подъязычной кости, по нижней границе перстневидного хряща (последний хрящ гортани, ниже него только хрящи трахеи)
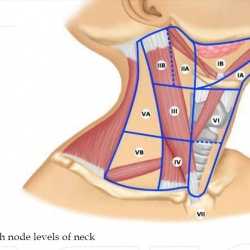
Среди не вполне привычных анатомических ориентиров упоминаются, например «(спинальная часть) добавочного нерва» или «поперечная артерия шеи».
N. accessorius, вместе с IX, X парами черепных нервов, выходит из полости черепа через яремное отверстие (foramen jugularis). После выхода из яремного отверстия он делится на две ветви - внутреннюю и наружную. Наружная ветвь (ramus externus) идет назад и вниз позади внутренней яремной вены к m. sternoclaidomastoideus и m. trapezius.
Ход его (сначала по задне-наружной поверхности внутренней яремной вены, а затем по верхнему контуру трапецевидной мышцы) хорошо виден на рисунке из атласа топографической анатомии (Ю.Л. Золотко).
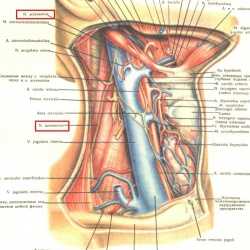
Поперечная артерия шеи - ветвь подключичной артерии, идущая назад и кнаружи к мышцам лопатки.
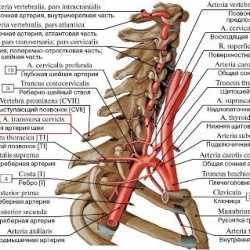
Схема вариантов отхождения ветвей поперечной артерии шеи [7] от подключичной артерии из атласа Золотко
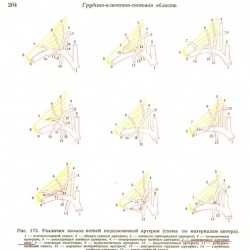
Таким образом, еще раз, глядя на схему (см.):
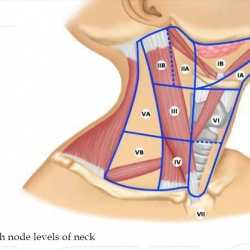
II - верхние яремные - от уровня основания черепа до уровня нижнего края подъязычной кости
IIA - верхние яремные передние - кпереди от заднего края внутренней яремной вены;
IIB - верхние яремные задние - кзади от заднего края внутренней яремной вены.
III - средние яремные - от уровня нижнего края подъязычной кости до уровня нижнего края перстневидного хряща гортани;
IV - нижние яремные - от уровня нижнего края перстневидного хряща гортани до ключиц (в т.ч. Вирховские);
VA - акцессорные - выше уровня нижнего края перстневидного хряща, по передней поверхности трапецевидной мышцы,
VB - надключичные - ниже уровня нижнего края перстневидного хряща (исключая Вирховские);
VI - переднего пространства шеи - пре- и паратрахеальные ЛУ, предгортанные (Delphian (Дельфийские) и околощитовидные ЛУ, включающие ЛУ вдоль возвратного гортанного нерва)
Читайте также:
- Синдром Меллера-Гунтера (Moeller-Hunter)
- Системная терапия диффузного атопического дерматита. Антигистаминные средства
- Страшные попутчики случайных связей. Как защитить себя от нежелательных инфекций?
- Формирование черепных ямок черепа. Развитие верхней челюсти
- Тепловой удар. Признаки ( клиника ) теплового удара. Причины ( этиология ) теплового удара. Патогенез теплового удара.
