Микоплазмы и микобактерии туберкулеза
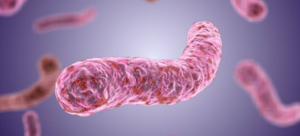
Одним из самых опасных и распространённых во всём мире инфекционных заболеваний не только человека, но и животных является туберкулёз. Возбудителем туберкулёза более чем в 90% случаев выступает mycobacterium tuberculosis (микобактерия туберкулёза).
Что такое микобактерия туберкулёза
На протяжении долгих столетий человечество страдало и умирало от туберкулёза, называемого ранее чахоткой. Медикам из многих стран мира никак не удавалось обнаружить и выделить коварного возбудителя туберкулёза, даже с появлением микроскопа. И только в 1882 году доктор Генрих Герман Роберт Кох из Германии сумел в результате многочисленных лабораторных опытов, проводимых на протяжении 17 лет, обнаружить продолговатую бактерию и позднее идентифицировать её. Эта бактерия также получила в медицине название по имени своего первооткрывателя: микобактерию туберкулёза называют палочкой Коха. В 1905 году Роберт Кох получил за своё открытие Нобелевскую премию.
Именно Роберт Кох предложил алгоритм для идентификации вызывающих туберкулёз бацилл, получивший также его имя (триада Коха) и применяемый до сих пор. Суть алгоритма состоит в следующем:
- Из тканей больного пациента извлекаются бактерии.
- Из них выращивается чистая культура – колонии бактерий.
- Далее, для получения клинической картины болезни, происходит заражение здорового организма (лабораторные мыши).
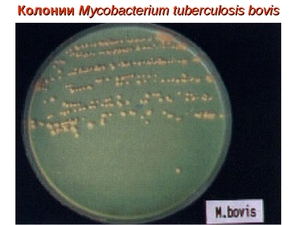
По своей форме микобактерия туберкулёза представляет собой продолговатую прямую или изогнутую палочку со слегка закруглёнными концами, размер бактерии обычно составляет 1 – 10 мкм в длину и 0,2 – 0,6 мкм в ширину.
Клетка МБТ состоит из:
- микрокапсулы, защищающей микобактерию от внешних воздействий и связанной с клеточной стенкой;
- клеточной стенки, которая обеспечивает клетке стабильность её формы и размера;
- гомогенной цитоплазмы и цитоплазматической мембраны;
- ядерной субстанции (собственно набор хромосом и плазмиды).
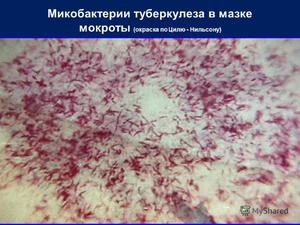
Размножение микобактерий происходит путём простого деления на две клетки. Цикл деления клетки составляет от 14 до 24 часов. Реже встречаются случаи размножения МБТ почкованием или ветвлением. На скорость размножения влияют многие факторы окружающей среды.
За свою тысячелетнюю историю бактерии приобрели различные механизмы защиты и приспособления к неблагоприятным для них внешним условиям.
Оптимальная для роста МБТ температура – 37 – 38°С. Размножаются они при температурном режиме от 29°С до 42°С. Однако, туберкулёзные палочки в состоянии сохранить свою жизнеспособность в условиях как очень низких, так и довольно высоких температур (н.п., при температуре в 80°С палочка является жизнеспособной ещё на протяжении 5 минут, при кипячении гибнет через 15 минут).
Наиболее комфортно бактерии чувствуют себя в сырых и тёмных условиях, на ярком солнце и при высокой температуре окружающей среды они прекращают интенсивное размножение и гибнут через полтора-два часа. Ультрафиолетовые лучи в состоянии уничтожить микобактерии за 2 – 3 минуты.
На протяжении многих месяцев МТБ в состоянии выжить, находясь вне живого организма. В водной среде они сохраняются около 150 дней, в пыли на улицах – до 10 дней, на книжных страницах до 3 месяцев. В высушенной форме микобактерии могут выживать в периоде до 3-х лет, а в замороженном состоянии их жизнеспособность может достигать и 30 лет.
В неблагоприятных для бактерии условиях, при лечении туберкулёза с помощью химиотерапии или при мощном иммунитете, палочка Коха быстро вырабатывает устойчивость к препаратам, может принять L -форму, способна сохраняться в таком состоянии целые десятилетия и вызывать противотуберкулёзный иммунитет. У пациентов, длительное время принимавших противотуберкулёзные препараты, бактерии могут принимать мелкие фильтрующиеся формы.
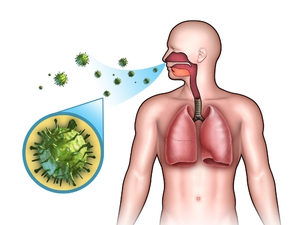
Основной путь передачи mycobacterium tuberculosis – воздушно-капельный. Этим путём передаётся до 95% из всех случаев заболевания туберкулёзом. Заражение происходит при кашле, чихании и даже во время разговора с инфицированным активной формой туберкулёза больным. Достаточно редко (в пределах 3 – 5 % от общего числа заболеваний) встречается передача МТБ через инфицированные продукты питания или от заражённых животных. Наиболее часто подвержен этому заболеванию крупный рогатый скот и свиньи. Гораздо реже им страдают собаки и кошки.
Практически любой орган или ткань человеческого организма, включая костные ткани, может быть подвержен заболеванию туберкулёзом. Более 90% всех случаев заболевания поражает органы дыхания. Наиболее часто из других внелегочных форм происходит поражение микобактериями мочеполовой системы, суставов, печени и почек.
Лабораторная диагностика и методы исследования материала на содержание микобактерий

При подозрении на туберкулёз органов дыхания материалом для лабораторного исследования является мокрота. При этом лучшие результаты даёт анализ мокроты, собранной на протяжении от 12 часов до суток. При локализации заболевания в других органах в качестве материала для анализа могут выступать разнообразные виды жидкостной среды человеческого организма: жидкость из брюшной полости или из полости суставов, спинномозговая жидкость, промывные воды бронхов кровь и гнойные выделения из ран.
При подозрении на туберкулёз внелегочных форм в качестве материала для лабораторного анализа также используют кусочки тканей органов, взятые при биопсии, пункциях и соскобах.
Если речь идёт о возможном заражении половой или мочевыделительной системы, на анализ берут мочу, собранную после ночного сна утром, как правило, это средняя порция мочи. У женщин для обследования на туберкулёз женских половых органов используют менструальную кровь, которую собирают с помощью колпачка Кафки.
В исследовании материала современная медицина применяет следующие методы:
- бактериологические;
- микроскопические;
- аллергологические;
- биологические;
- молекулярно – генетические и серологические методы (применяются достаточно редко).
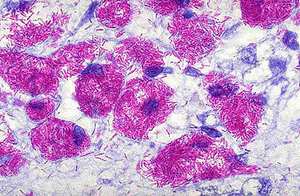
Этот метод является наиболее распространённым и заключается в исследовании мазков, выделенных из собранного материала (мокроты, мочи, спинномозговой жидкости и др.). Суть заключается в окрашивании материала по методу Циля-Нильсена или флуорохромом (как правило, аурамин-родомином или другим), и в дальнейшей обработке спиртом и промывании водой. После чего материал исследуется под люминесцентным микроскопом. Mycobacterium tuberculosis , обработанные флуорохромами, излучают золотистый цвет на тёмно-зелёном фоне. Обработанные по методу Циля - Нильсена туберкулёзные палочки имеют рубиново-красный цвет.
Для обнаружения L -форм используется в большинстве случаев фазово-контрастная микроскопия.
Необходимо просмотреть не менее 100 полей зрения для вынесения положительного ответа при обнаружении mycobacterium tuberculosis , при этом следует указать число бактерий в каждом поле. Однако следует отметить, что наличие отрицательного результата при микроскопии не даёт гарантии полностью исключить диагноз туберкулёза.
Микроскопический метод анализа имеет определённые недостатки, к которым в первую очередь относится низкая чувствительность: mycobacterium tuberculosis обнаруживается только при присутствии не менее 50 – 100 тысяч микробов на 1 мл исследуемого материала. Этот метод не позволяет отличить mycobacterium tuberculosis от других видов mycobacterium , он также не в состоянии определить чувствительность микобактерий к определённым химиотерапевтическим препаратам.
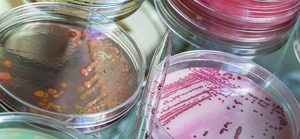
Этот метод представляет собой посев штаммов бактерий на специальные питательные среды и в состоянии определить наличие туберкулёзных палочек при концентрации 200 – 300 микробов на 1 мл. Посев помещается в термостат и на протяжении трёх месяцев при температуре 37 °С еженедельно наблюдается рост микобактерий.
Главный недостаток этого метода состоит в том, что получение конечных результатов требует определённых затрат времени (от 3 до 12 недель). На искусственных средах рост микобактерий наступает через 3 – 6 недель. У пациентов, проходящих курс химиотерапии, выделенные штаммы вырастают на ещё более поздних сроках (от 50 до 80 дней). На сегодня современной медициной испытаны и ускоренные методы выращивания культур mycobacterium tuberculosis по методу Прайса (на препаратах – мазках) и по методу посева на кровяной среде.
С помощью бактериологического метода можно определить не только вирулентность культуры, но и её чувствительность к различным медицинским препаратам.
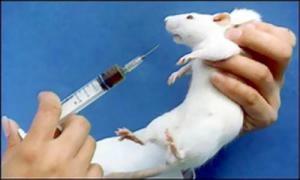
Этот метод относится, пожалуй, к самым рациональным методам исследования. Он позволяет определять микобактерии туберкулёза при малых количествах их содержания в материале (до 10 бактерий на 1 мл).
При этом методе материал вводиться морским свинкам подкожно или в брюшную полость. Если в материале присутствуют вирулентные mycobacterium tuberculosis , то обычно через 10 – 12 дней на месте инъекции образуется уплотнение, которое переходит в незаживающую язву. На протяжении 2 – 4 месяцев развивается генерализованный туберкулёз и свинки погибают.
Ускоренный биологический метод заключается во введении материала в региональный лимфоузел морской свинки. Увеличенный узел вырезается на 8 – 10 день и исследуется на присутствие микобактерий туберкулёза в препаратах-отпечатках.
В связи, с распространением в последние годы изменённых и устойчивых микобактерий чувствительность этого метода заметно снизилась. На сегодняшний день метод применяется в крупных специализированных лабораториях и требует строгого соблюдения режима проведения.
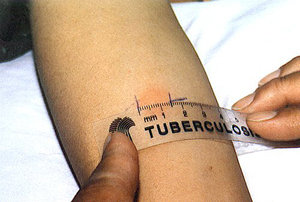
К этому методу относятся широко применяемые кожные туберкулиновые пробы. Проба Манту предусматривает введение туберкулина в предплечье, даёт положительные, отрицательные и резко положительные реакции. У детей и взрослых вводится различная концентрация вещества.
При помощи пробы Манту определяется круг лиц для проведения ревакцинации. Положительная проба Манту не является обязательным признаком наличия заболевания.
Профилактика

Основной профилактикой распространения микобактерий и предотвращение заболевания туберкулёзом является вакцина БЦЖ (Бацилла Кальметта-Герена). Вакцину изготовляют из штамма ослабленной живой mycobacterium bovis (бычий вид туберкулёзной палочки). При отсутствии противопоказаний вакцинацию проводят новорождённым в роддоме на 5 – 7 день жизни. Ревакцинация проводится в возрасте 7, 12, 17 и 22 лет при отрицательном результате пробы Манту и при отсутствии противопоказаний.
Взрослым с целью выявления туберкулёза на ранних стадиях не реже 1 раза в год необходимо проходить флюорографию лёгких в поликлинике. При резких изменениях реакции Манту за год или в случаях контакта с инфицированным больным фтизиатр может предложить проведение курса профилактической химиотерапии.
Аннотация научной статьи по фундаментальной медицине, автор научной работы — Катола Виктор Моисеевич
Дана общая характеристика класса Mollicutes семейства Mycoplasmataceae, распространение и источники микоплазменной инфекции, ее клинические особенности и методы диагностики. При сканирующей электронной микроскопии плазмы крови больных с тяжелым течением фиброзно-кавернозного туберкулеза легких в фазе инфильтрации и обсеменения выявлены элементарные тельца не идентифицированных L-форм бактерий и нитевидные ветвящиеся формы с различными структурами на поверхности, предположительно, клетки микоплазм . Все эти образования совместно с микобактериями туберкулеза формируют суперинфекцию, которая является причиной прогрессирования и исхода туберкулезного процесса.
Похожие темы научных работ по фундаментальной медицине , автор научной работы — Катола Виктор Моисеевич
MYCOPLASMAS: BIOLOGY, DISTRIBUTION AND ROLE IN PATHOLOGY
The general characteristics of the Mollicutes class of the family Mycoplasmataceae, the distribution and sources of mycoplasma infection, its clinical features and diagnostic methods are given. In scanning electron microscopy of blood plasma in patients with severe fibrous cavernous pulmonary tuberculosis in the phase of infiltration and seeding, elementary bodies of unidentified L-forms of bacteria and filamentous branching forms with various structures on the surface, presumably cells of mycoplasmas , were identified. All these formations together with mycobacterium tuberculosis form superinfection, which is the cause of the progression and outcome of the tuberculosis process.
УДК 579.887.11(616-076:611-018.54)]616.24-002.5 DOI: 10Л2737/а111с1е_5Ь975аЬЙ13аЬ8.91657125 МИКОПЛАЗМЫ: БИОЛОГИЯ, РАСПРОСТРАНЕНИЕ И РОЛЬ В ПАТОЛОГИИ
Федеральное государственное бюджетное учреждение науки Институт геологии и природопользования Дальневосточного отделения Российской академии наук, 675000, г. Благовещенск, пер. Релочный, 1
Дана общая характеристика класса Mollicutes семейства Mycoplasmataceae, распространение и источники микоплазменной инфекции, ее клинические особенности и методы диагностики. При сканирующей электронной микроскопии плазмы крови больных с тяжелым течением фиб-розно-кавернозного туберкулеза легких в фазе инфильтрации и обсеменения выявлены элементарные тельца не идентифицированных L-форм бактерий и нитевидные ветвящиеся формы с различными структурами на поверхности, предположительно, клетки микоплазм. Все эти образования совместно с микобактериями туберкулеза формируют суперинфекцию, которая является причиной прогрессирования и исхода туберкулезного процесса.
Ключевые слова: микоплазмы, электронная микроскопия, плазма крови, элементарные тельца, нитевидные структуры, туберкулез легких.
MYCOPLASMAS: BIOLOGY, DISTRIBUTION AND ROLE IN PATHOLOGY
Institute of Geology and Nature Management of Far Eastern Branch RAS, 1 Relochniy Lane, Blagoveshchensk, 675000, Russian Federation
The general characteristics of the Mollicutes class of the family Mycoplasmataceae, the distribution and sources of mycoplasma infection, its clinical features and diagnostic methods are given. In scanning electron microscopy of blood plasma in patients with severe fibrous cavernous pulmonary tuberculosis in the phase of infiltration and seeding, elementary bodies of unidentified L-forms of bacteria and filamentous branching forms with various structures on the surface, presumably cells of mycoplasmas, were identified. All these formations together with mycobacterium tuberculosis form superinfection, which is the cause of the progression and outcome of the tuberculosis process.
Key words: mycoplasmas, electron microscopy, blood plasma, elementary bodies, filamentary structures, pulmonary tuberculosis.
Микоплазмы, выделенные в 1898 году Е.Нокар и Е.Ру в лаборатории Луи Пастера как неизвестные возбудители смертельной плевропневмонии крупного рогатого скота, заселяют все живые существа на Земле. Несмотря на то, что они являются промежуточной формой между вирусами и бактериями, их отнесли к
Все микоплазмы представляют собою округлые, овальные, кольцевидные, разветвленные нитевидные и коккобациллярные клетки размером от 150 до 700 нм (рис. 1, 2). Они не имеют клеточной стенки, жгутиков и спор, делятся бинарно, почкованием и фрагментацией с высвобождением в нитях множества репродуктивных телец. Микоплазмы - мембранные и внутриклеточные паразиты со сложной молекулярной структурой, быстро передвигающиеся от клетки к клетке, используя для питания клеточный холестерин или другие стерины [2, 17]. В отличие от вирусов и хла-мидий микоплазмы могут размножаться в неклеточной среде. Они обладают высокой чувствительностью к ультразвуку, замораживанию и оттаиванию, антибиотикам тетрациклинового ряда, макролидам и фторхи-нолонам и резистентностью к пенициллину, стрептомицину и сульфаниламидам. Их генетический аппарат в четыре раза меньше, чем у Escherichia coli. Например, M. genitalium состоит из 482 генов, содержащих 582 970 пар оснований на кольцевой хромосоме [16]. В ходе эволюции микоплазмы адаптировались к паразитическому образу жизни и приобрели способность стимулировать либо супрессировать иммунные реакции хозяина [7, 11, 17]. Класс Mollicutes широко распространен в природе, организме человека, животных и растений. Многие его виды выделены из горячих источников, каменного угля, бактерий и грибов (рис. 3, 4). Наряду с бактериями, грибами и вирусами M. ho-minis, М. orale, M. arginini и Acholeplasma laidlawii активно загрязняют культуры клеток [13, 14, 15].
В здоровом организме человека обитает 11-16 видов микоплазм, которые передаются воздушно-капельным, половым и вертикальным (от матери) путями. Контактно-бытовое заражение через предметы быта, медицинский инструментарий и нательное белье пока не доказано. Существуя и размножаясь в орга-
низме, эти бактерии вызывают заболевания лишь при отсутствии другого патогена и только на фоне угнетенной иммунной системы. Заодно могут поражать сердечно-сосудистую и скелетно-мышечную системы, печень, формировать конкременты в почках и мочевом пузыре, быть причиной бронхиальной астмы, полиартритов и др. С учетом локализации возбудителя и развития патологии выделяют: 1) респираторный ми-коплазмоз - острый инфекционно-воспалительный процесс дыхательных путей, вызываемый M. pneumoniae; 2) урогенитальный микоплазмоз - инфекционно-воспалительное заболевание, провоцируемое M. hominis и M. genitalium и часто возникающее при гонорее, трихомониазе и гинекологических болезнях; 3) генерализованный микоплазмоз вследствие гематогенного распространения возбудителя. Однако выделить его из крови культуральным методом не удается, хотя в опытах in vitro в сыворотке крови человека при 37°С клетки M. hominis, их ДНК и антигены сохраняют жизнеспособность в течение 12 суток, внутриклеточная ДНК - на протяжении всего срока наблюдения (40 суток) [9]. Особенностью микоплаз-менных инфекций является бессимптомное течение, рецидивы (возбудитель сохраняется в организме при антибиотикотерапии), его участие в составе mixt-ин-фекций и в качестве синергиста других патогенных бактерий.
Диагностика микоплазмозов затруднена, поскольку световой микроскопией их агенты не выявляются, микробиологическое выделение из природных источников и биоматериала (мокроты, плевральной жидкости, ткани легких и пр.) почти не применяется, так как для этого требуются питательные среды, содержащие сыворотку крови человека, крупного рогатого скота, лошадей либо кроликов, дрожжевой экстракт, асцитическую жидкость, смесь холестерина с сывороточным альбумином и др. Преимущественно используются методы серотипирования (иммуноферментный анализ, реакция связывания комплемента и реакция непрямой иммунофлюоресценции), полимеразная цепная реакция и тест ELISA - преобладание в парных сыворотках крови титров IgA и IgG в острую стадию заболевания и в период реконвалесценции.
Учитывая, что микоплазмы способны вызывать глубокие патологические процессы в организме человека и с трудом диагностируются, решено с помощью сканирующей электронной микроскопии исследовать плазму крови пациентов с прогрессирующим фиб-розно-кавернозным туберкулезом легких.
Материалы и методы исследования
Плазма крови от двух пациентов, госпитализированных в Амурский областной противотуберкулезный диспансер по поводу фиброзно-кавернозной формы туберкулеза легких в фазе инфильтрации и обсеменения с двусторонней деструкцией легочной ткани, интоксикацией и выделением микобактерий туберкулеза, была доставлена в лабораторию биогеохимии Института геологии и природопользования ДВО РАН для элек-тронномикроскопического исследования. Одну каплю
плазмы (0,1 мл) наносили на липкую поверхность ленты, прикрепленной к торцу предметного столика электронного микроскопа. Полученные препараты просушивали в стерильной чашке Петри, напыляли углеродом в вакуумной установке ВУП-4 и просматривали в сканирующем электронном микроскопе JEOL ^М 35С (Япония).
Результаты исследования и их обсуждение
По клиническим, рентгенологическим и патомор-фологическим изменениям туберкулез легких и респираторный микоплазмоз мало чем различаются. Между тем, известно, что при неблагоприятных условиях присутствующие в организме микоплазмы способны усугублять иммуносупрессию, активизировать вспышку туберкулезного процесса, деструкцию и осложнения. В наших случаях выявленные в плазме крови предполагаемые микоплазмы в ассоциации с элементарными тельцами L-форм неизвестных бактерий и первоначальным этиологическим агентом (микобактериями) у пациентов с фиброзно-кавернозным туберкулезом легких сформировали эндогенную смешанную суперинфекцию, которая спровоцировала прогрессирование туберкулезного процесса с неутешительным исходом. Именно похожее скоротечное течение туберкулеза легких со склонностью к летальному исходу наблюдается у ВИЧ-инфицированных лиц.
196.Экологический профиль большинства микобактерий:
1. Симбионты-комменсалы животных. 2. Симбионты-паразиты животных. 3. Симбионты-паразиты человека. 4. Сапрофиты.5. Облигатно-патогенные виды.
197.Возбудители микобактериальных антропонозов:
1. Mycobacterium bovis. 2. Mycobacterium leprae. 3. Mycobacterium avis/intarcellulare. 4. Mycobacterium tuberculosis. 5. Mycobacterium bovis, ssp. BCG.
198.Возбудитель микобактериального зооноза:
1. Mycobacterium bovis. 2. Mycobacterium leprae. 3. Mycobacterium kansasii. 4. Mycobacterium tuberculosis. 5. Mycobacterium bovis, ssp. BCG.
199.Возбудители туберкулеза человека:
1. Mycoplasma pneumoniae. 2. Mycobacterium avis/intracellulare.3. Mycobacterium tuberculosis. 4. Mycobacterium leprae.5. Mycobacterium bovis.
200.Признаки микобактерий туберкулеза,связанные с
особенностями их клеточной стенки:
1. Кислотоустойчивость. 2. Медленная скорость размножения.3. Резистентность к фагоцитам. 4. Устойчивость во внешней среде. 5. Высокая чувствительность к антибиотикам.
201.Факторы и механизмы,определяющие тинкториальные,эколого-физиологические и патогенетические особенности микобактерий туберкулеза:
1. Капсулоподобный экзополисахарид. 2. Эндоспоры.
3. Склонность к трансформации в L-формы. 4. Липиды клеточной стенки. 5. Отсутствие пептидогликана.
202.Липиды/гликолипиды клеточной стенки микобактерий
туберкулеза:
1. Миколовые кислоты. 2. Корд-фактор. 3. Туберкулин.
4. Микозиды. 5. Сульфатиды. 6. Пептидогликан.
203.Последовательность событий при развитии туберкулезного (M. tuberculosis)процесса:
1. Проникновение возбудителя в альвеолы. 2. Т-зависимая
активация макрофагов. 3. Размножение возбудителя в
альвеолярных макрофагах. 4. Формирование неспецифической (доиммунной) гранулемы. 5. Индукция Т-клеточного иммунитета. 6. Проникновение возбудителя в регионарные лимфатические узлы. 7. Формирование специфической (постиммунной гранулемы).
204.В инициации инфекционного процесса участвуют следующие факторы и механизмы микобактерий туберкулеза:
1. Внутриэпителиальная инвазия. 2. Пиогенная инвазия
субэпителиальных тканей. 3. Внутримакрофагальная инвазия.4. Внутрисосудистая инвазия (бактериемия). 5. Деструктивные ферменты и токсины.
205.Туберкулин:
1. Комплекс липидов клеточной стенки туберкулезной палочки. 2. Комплекс туберкулопротеинов (белковых дериватов). 3. Обладает прямой болезнетворностью. 4. Обладает иммунологически опосредованной болезнетворностью. 5. Используется для вакцинопрофилактики туберкулеза.6. Используется в аллергодиагностике туберкулезной инфекции.
206.Положения,справедливые для белковых антигенов
туберкулезной палочки (туберкулопротеинов):
1. Обладают прямой болезнетворнстью. 2. Определяют
культуральные и тинкториальные особенности микобактерий.3. Проявляют имунологически зависимую болезнетворность.4. Участвуют в реализации протективного иммунитета.5. Используются в аллергодиагностике. 6. Обладают иммуноадъювантным эффектом.
207.Положения,справедливые для липидов/гликолипидов
клеточной стенки микобактерий туберкулеза:
1. Обладают антимакрофагальной активностью. 2. Участвуют в индукции Т-клеточного иммунитета (иммуноадъювантный эффект). 3. Действующее начало туберкулина. 4. Проявляют иммунологически зависимую болезнетворность. 5. Определяют культуральные и тинкториальные особенности микобактерий.
208.Главная функция,реализуемая макрофагами в зоне
неспецифической (доиммуной)гранулемы при уберкулезной
инфекции:
1. Уничтожение микобактерий. 2. Возбуждение реакций
клеточного (Т- зависимого) иммунитета. 3. Индукция реакций гуморального иммунитета. 4. Функциональная кооперация с Т- эффекторами. 5. Предупреждение микробной инвазии.
209.Положения,справедливые для специфической
(постиммунной)туберкулезной гранулемы:
1. Возникает на фоне аллергии замедленного типа к
туберкулопротеинам. 2. Зона для функциональной кооперации между макрофагами и Т-эффекторами. 3. Основа для деструктивных реакций. 4. Основа для саногенеза. 5. Обычно завершается бессимптомной персистенцией возбудителя.
210.Решаюшую роль в интоксикации при туберкулезе играют следующие факторы и механизмы:
1. Микобактериальные токсины. 2. Туберкулопротеины.
3. Антигенная стимуляция Т-лимфоцитов. 4. Т-зависимая
активация макрофагов. 5. Цитокины иммунокомпетентных
211.Деструктивные процессы при туберкулезе определяются следующими механизмами:
1. Прямое действие микобактериальных токсинов.
2. Иммунологически опосредованные эффекты
микобактериальных антигенов. 3. Цитокин-зависимая активация макрофагов.4. Аллергия к туберкулопротеинам.
5. Аллергия к липидам клеточной стенки микобактерий.
212.Наиболее вероятные исходы специфической (постиммунной)гранулемы:
1. Заживление (фиброз, кальцификация). 2. Полное уничтожение возбудителя. 3. Формирование латентной (персистентной) инфекции. 4. Генерализация процесса. 5. Формирование иммунитета к экзогенному реинфицированию.
213.Положения,справедливые для противотуберкулезного
иммунитета:
1. Нестерильный иммунитет. 2. Антитоксический иммунитет.2. Антибактериальный иммунитет. 4. Гуморальный иммунитет.5. Клеточный иммунитет.
214.Положения,справедливые для первичного туберкулеза:
1.Результат экзогенного инфицирования. 2. Следствие
215.Положения,справедливые для вторичного туберкулеза:
1. Реактивационный туберкулез. 2. Может быть следствием
экзогенного реинфицирования. 3. Хроническая патология легких (типичное течение). 4. Развивается на фоне аллергии к туберкулопротеинам. 5. Результат прямого действия
216.В аллергодиагностике туберкулезной инфекции используют препарат на основе следующих продуктов микобактерий:
1. Липиды/гликолипиды. 2. Пептидогликан. 3. Протеины.
4. Нуклеиновые кислоты. 5. Полисахариды.
217.Диагностическая значимость бактериоскопии (мокроты)при туберкулезе основана на следующем признаке возбудителя:
1. Морфологические особенности. 2. Образование эндоспор.
3. Подвижность. 4. Тинкториальное своеобразие.
5. Образование внутриклеточных включений.
218.Метод,на котором основана классическая экспресс-
диагностика туберкулеза:
1. Бактериоскопия. 2. Выявление микобактериальных антигенов.3. Ускоренные культуральные методы 4. Выявление специфических метаболитов. 5. Обнаружение специфических фрагментов ДНК (ПЦР).
219.Наиболее очевидные метаболические процессы,которые могут служить мишенью для специфических
противотуберкулезных антибиотиков:
1. Синтез пептидогликана. 2. Синтез белка. 3. Синтез
нуклеиновых кислот. 4. Синтез миколовых кислот.
5. Организация межмолекулярных контактов в клеточной стенке
.220.Положения,справедливые для туберкулезной вакцины (BCG):
1. Живая аттенуированная вакцина. 2. Анатоксин. 3. Убитая вакцина.4. ДНК-вакцина. 5. Конъюгированная вакцина.
2.10.РИККЕТСИИ
221.Признаки,отражающие атипичность риккетсий:
1. Отсутствие рибосом. 2."Энергетические паразиты".
3. Факультативные внутриклеточные паразиты. 4. Отсутствие пептидогликана. 5. "Мембранные паразиты".
222.Позиции,справедливые для риккетсий:
1. Зависимость от энергетического метаболизма клеток.
2. Размножение путем деления. 3. Дизъюнктивный способ
репродукции. 4. Размножение внутри фагосом. 5. Размножение в цитоплазме и/или ядре.
223.Признаки,характерные для экологии риккетсий:
1.Симбионты кровососущих членистоногих. 2. Возможность
трансовариальной передачи у кровососущих насекомых.
3. Персистенция в организме животных.
4. Почвенный резервуар (сапрофитическая фаза).
5. Циркуляция в системе "животные--членистоногие".
224.Возможная позиция членистоногих в экологии риккетсий:
1.Естественный резервуар инфекции. 2. Вектор (переносчики) инфекции. 3. Поддержка циркуляции риккетсий среди животных.4. Стабилизация природных очагов риккетсиозной инфекции.5. Участие в эпидемическом процессе.
225.Механизмы,определяющие болезнетворность риккетсий:
1. Размножение в макрофагах региональных лимфатических узлов. 2. Риккетсемия. 3. Паразитирование внутри эпителиальных клеток. 4. Паразитирование внутри
эндотелиальных клеток. 5. Прямое поражение клеток нервной ткани. 6. Иммунологически зависимое поражение тканей.
226.Наиболее приемлемый для практики метод лабораторной диагностики риккетсиозов:
1. Выделение и идентификация чистой культуры. 2. Выявление риккетсиозных антигенов в пораженных тканях. 3. Выявление специфических антител (серодиагностика). 4. Выявление генетических маркеров (полимеразная цепная реакция). 5. Биопробы на животных.
227.Риккетсии,для которых человек является природным
(естественным)резервуаром:
1. Rickettsia typhi. 2. Rickettsia prowazekii. 3. Rickettsia rickettsii. 4. Orientia tsutsugamushi. 5. Rickettsia sibirica.
228.Эпидемиологическая характерстика большинства
риккетсиозов,исходящая из экологии риккетсий:
1. Зооноз. 2. Антропоноз. 3. Трансмиссивный механизм передачи. 4. Природная очаговость. 5. Сапроноз.
229.Риккетсиозный антропоноз:
1. Лихорадка цуцугамуши. 2. Пятнистые лихорадки.
3. Эпидемический сыпной тиф. 4. Эндемичный сыпной тиф. 5. Лихорадка Ку.
230.Позиция человека в экологии риккетсий (за исключением R.prowazekii):
3. Обязательный участник жизненного цикла риккетсий.
4. Случайный хозяин. 5. Вектор инфекции.
231.Позиция вшей в экологии риккетсий эпидемического сыпного
тифа:
1.Обязательный участник жизненного цикла риккетсий.2. Природный резервуар инфекции. 3. Биологический вектор инфекции. 4. Механический вектор инфекции. 5. Естественный хозяин.
232.Существование риккетсий эпидемического сыпного тифа в природе поддерживается следующими факторами:
1. Социальное неблагополучие. 2. Персистенция возбудителя в организме переболевших людей. 3. Реактивация эдогенной инфекции. 4. Возможность внечеловеческого резервуара инфекции. 5. Трансовариальная передача возбудителя у вшей-переносчиков.
233.Экологическая система,поддерживающая существование R.prowazekiiв природе:
1. Грызуны -- клещи. 2. Крысы -- блохи. 3. Человек -- вши.
4. Человек -- вши -- животные. 5. Животные -- клещи -- человек.
234.Основная категория клеток,поражаемых при риккетсиозах:
1. Эпителиоциты. 2. Эритроциты. 3. Нейтрофилы.
4. Эндотелиоциты. 5. В-лимфоциты. 6. Т-лимфоциты.
235.Клиническое проявление реактивации персистентной R.prowazekii-инфекции:
1. Ку-лихорадка. 2. Болезнь Цинссера-Брилля. 3. Йерсинеоз.
4. Пситтакоз. 5. Трахома.
236.Экологическая система,поддерживающая существование
большинства риккетсий в природе:
1. Грызуны (мелкие млекопитающиеся) -- клещи. 2. Крысы --блохи. 3. Человек -- вши. 4. Человек -- вши -- животные.
5. Животные -- клещи -- человек.
237.Возбудитель эпидемического сыпного тифа:
1. Rickettsia prowazekii. 2. Rickettsia rickettsii. 3. R. sibirica.
4. Rickettsia (Orientia) tsutsugamushi. 5. Rickettsia typhi. 6. Coxiella burnetii.
238.Возбудитель эндемичного сыпного тифа:
1. Rickettsia prowazekii. 2. Rickettsia rickettsii. 3. R. sibirica.
4. Rickettsia Orientia) tsutsugamushi. 5. Rickettsia typhi. 6. Coxiella burnetii.
239.Риккетсии группы пятнистых лихорадок:
1. Rickettsia prowazekii. 2. Rickettsia rickettsii. 3. R. sibirica.
4. Rickettsia (Orientia) tsutsugamushi. 5. Rickettsia typhi.
240.Риккетсии группы сыпных тифов:
1. Rickettsia prowazekii. 2. Rickettsia rickettsii. 3. R. sibirica.
4. Rickettsia (Orientia) tsutsugamushi. 5. Rickettsia typhi.
241.Болезнь Цинссера-Брилля:
1.Эндогенная инфекция. 2. Реактивация персистентной инфекции (Rickettsia prowazekii). 3. Повторная экзогенная инфекция (Rickettsia prowazekii). 4. Эпидемиологически опасная инфекция. 5. Вариант эпидемического тифа.
2.10.ХЛАМИДИИ
242.Признаки,отражающие "атипичность"хламидий:
1. Неспособность к росту на искусственных питательных средах.2. Холестеролзависимость (мембранный паразитизм).
3. Дизъюнктивный способ репродукции. 4. Фильтруемость.
5. Отсутствие пептидогликана.
243.Положения,отражающие своеобразие репродукции хламидий:
1.Дизъюнктивный способ размножения. 2. Чередование фаз
элементарных и ретикулярных тел. 3. Синтез белка на рибосомах клетки-хозяина. 4. Размножение внутри эндосом (фагосом).5. Зависимость от энергетического метаболизма клетки-хозяина.
244.Для элементарных тел хламидий справедливы следующие положения:
1. Метаболическая инертность. 2. Фильтруемость.
3. Устойчивость во внешней среде. 4. Деление.
5. Трансформация в ретикулярные тела. 6. Инфекционность
(инфекционное начало хламидий).
245.Положения,справедливые для ретикулярных тел хламидий:
1. Репродуктивная (вегетативная) форма хламидий
2. Метаболическая инертность. 3. Способность к делению.
4. Трансформация в элементарные тела. 5. Устойчивость во
246.Причины относительной резистентности хламидий к
антибиотикам:
1. Отсутствие пептидогликана. 2. Внутриклеточный паразитизм.3.Метаболическая инертность элементарных тел.4. Метаболическая инертность ретикулярных тел. 5. Отсутствие молекулярных мишеней для ингибиторов белкового синтеза.
247.Хламидии --возбудители зоонозной инфекции:
1.Chlamydia trachomatis, серотипы A-C. 2. Chlamydia trachomatis, серотипы D-K. 3. Chlamydia trachomatis, серотипы L1-L3. 4. Chlamydia psittaci. 5. Chlamydia pneumoniae.
248.Хламидийный зооноз:
1. Трахома. 2. Генитальный хламидиоз. 3. Венерическая
лимфогранулема. 4. Пситтакоз/орнитоз. 5. Респираторный
хламидиоз (Ch. pneumoniae).
249.Хламидии,для которых человек служит естественным
хозяином (природным резервуаром):
1.Chlamydia trachomatis, серотипы A-C. 2. Chlamydia trachomatis, серотипы D-K. 3. Chlamydia trachomatis, серотипы L1-L3.4. Chlamydia psittaci. 5. Chlamydia pneumoniae.
.250.Высокая инвазивность характерна для следующих хламидий:
1. Chlamydia trachomatis, серотипы A-C. 2. Chlamydia trachomatis, серотипы D-K. 3. Chlamydia trachomatis, серотипы L1-L3.4. Chlamydia psittaci. 5. Chlamydia pneumoniae.
251.Патогенетические варианты Chlamdia trachomatis:
1. "Глазные" хламидии. 2. "Генитальные" хламидии.
3. "Респираторные" хламидии. 4. "Зоонозные" хламидии
5. Возбудители венерической лимфогранулемы.
252.Наиболее реальные методы лабораторной диагностики
генитального хламидиоза и носительства генитальных хламидий:
1. Выделение и идентификация чистой культуры.
2. Выявление антихламидийных антител. 3. Выявление
эпителиальных клеток с включениями (микроколониями
хламидий). 4. Выявление хламидийных антигенов
(иммуноферментный анализ). 5. Выявление фрагментов
хламидийной ДНК (полимеразная цепная реакция).
2.11.МИКОПЛАЗМЫ
253. "Атипичность"микоплазм подразумевает:
1. Облигатность внутриклеточного паразитизма.
2. Образование уникальных токсинов. 3. Облигатную
анаэробность. 4. Особенности строения бактериальных мембран.5. Отсутствие пептидогликана.
254.Позиции,справедливые для микоплазм:
1. Дизъюнктивный способ репликации. 2. Плеоморфизм.
3. Отсутствие пептидогликана. 4. Энергетические паразиты.5. Мембранные паразиты.
255.Позиции,справедливые для микоплазм:
1. Наличие многослойной липидной мембраны.
1. Фильтруемость. 3. Облигатность внутриклеточного
паразитизма. 4. Наличие ригидной клеточной стенки.
256.Термин "молликуты" (класс Mollicutes)отражает:
1. Структурное своеобразие клеточной оболочки.
2. Облигатность внутриклеточного паразитизма.
3. Ауксотрофность. 4. Особенности энергетического метаболизма.5. Патогенетическую значимость микоплазм.
257.Название микоплазм на уровне класса:
1. Риккетсии. 2. Хламидии. 3. Молликуты. 4. Прокариоты.
258.Родовые таксоны "медицинских"молликут:
1. Mycoplasma. 2. Chlamydia. 3. Haemophilus. 4. Ureaplasma.
5. Mycobacteria. 6. Helicobacter. 7. Neisseria. 8. Bordetella.
259.Антибиотики,не действующие на микоплазмы:
1. Ингибиторы цитоплазматической мембраны. 2. Бета-
лактамные антибиотики. 3. Ингибиторы синтеза пептидогликана.4. Ингибиторы синтеза белка. 5. Ингибиторы синтеза нуклеиновых кислот.
260.Признаки,по которым микоплазмы принципиально
отличаются от L-форм бактерий:
1. Отсутствие генов, детерминирующих синтез пептидогликана.2. Дефицит генов, детерминирующих синтез рибосомальных РНК.3. Нарушение синтеза пептидогликана. 4. Дефекты энергетического метаболизма. 5. Морфологическая нестабильность (дисбаланс клеточного роста).
261.Микоплазмы --первичные патогены человека:
1. Mycoplasma hominis. 2. Ureaplasma urealyticum. 3. Mycoplasma oralis. 4. Mycoplasma pneumoniae. 5. Chlamydia trachomatis.
262.Условно-патогенные микоплазмы --возбудители
урогенитальных микоплазмозов:
1. Mycoplasma hominis. 2. Ureaplasma urealyticum. 3. Mycoplasma oralis. 4. Mycoplasma pneumoniae. 5. Chlamydia trachomatis.
263.Микоплазмы,принимающие участие в образовании камней внутри мочевыводящей системы:
1. Mycoplasma hominis. 2. Ureaplasma urealyticum. 3. Mycoplasma oralis. 4. Mycoplasma pneumoniae. 5. Chlamydia trachomatis.
264.В реализации патогенетического потенциала микоплазм задействованы следующие факторы и механизмы:
1. Мембранный паразитизм. 2. Оксиданты. 3. Высокая
инвазивность. 4. Иммунологически опосредованная
агрессивность. 5. Прямое повреждение клеточных мембран.
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Читайте также:


