Интенсивная терапия системной красной волчанки
За последние два десятилетия благодаря рациональному использованию кортикостероидных гормонов (КГ) и цитотоксических иммунодепрессантов (ЦИ) удалось значительно улучшить жизненный прогноз больных системной красной волчанкой (СКВ). Проведение пульс-терапи
За последние два десятилетия благодаря рациональному использованию кортикостероидных гормонов (КГ) и цитотоксических иммунодепрессантов (ЦИ) удалось значительно улучшить жизненный прогноз больных системной красной волчанкой (СКВ). Проведение пульс-терапии метилпреднизолоном (МП) и циклофосфаном (ЦФ) у больных с волчаночным нефритом, поражением центральной нервной системы (ЦНС) и цитопеническим кризом способствует ускорению сроков достижения клинического улучшения. Патофизиологическим обоснованием для применения ударных доз метилпреднизолона является его способность активно влиять на систему иммунитета и подавлять воспалительные реакции. Один из важнейших эффектов ударных доз КГ — подавление активности нейтрофилов и моноцитов и способность вызывать транзиторную перераспределительную лимфопению. Угнетающее воздействие мегадоз кортикостероидов на функцию В-лимфоцитов приводит к стойкому снижению продукции иммуноглобулинов, а следовательно, и аутоантител, а также к уменьшению образования патологических иммунных комплексов. Из других важных компонентов механизма действия ударных доз КГ заслуживают внимания воздействие на систему цитокинов-интерлейкинов-1,6, фактора некроза опухоли, металлопротеиназ и липокортина, ингибиция экспрессии и функциональной активности Fc и СЗ рецепторов мононуклеарных фагоцитов.
Консервативная терапия с использованием подавляющих доз преднизолона и цитостатиков, назначаемых внутрь, у некоторых больных улучшает клиническую картину, но почти не влияет на жизненный прогноз, особенно в случаях прогрессирующего волчаночного нефрита, церебрального криза и геморрагического пневмонита. Однократное трехдневное применение ПТ МП может за сравнительно короткое время уменьшить клиническую и лабораторную активность при нефротическом синдроме. Однако 5-летняя выживаемость пациентов, как правило, не превышает 60%. Другими словами, ударные дозы МП прекрасно зарекомендовали себя в качестве фактически ургентной терапии, с успехом применяющейся в ситуациях, непосредственно угрожающих жизни пациента, при нарастании симптоматики и в случаях неэффективности или невозможности использования консервативной схемы лечения.
Практически при всех прогрессирующих хронических заболеваниях, в том числе и аутоиммунных, жизненный и социальный прогноз в огромной степени зависит от системного, программного подхода к терапии.
Различные схемы и программы интенсивной терапии у больных СКВ стали появляться уже с середины 80-х годов и сводились к назначению ПТ в ежемесячном режиме в течение полугода. Несколько позже появилась схема программного назначения ПТ в комбинации с циклофосфаном: 1 г циклофосфана может быть добавлен к стандартной пульс-терапии обычно на 2-3-й день лечения или дополнительно к метипреду при ежемесячном режиме. Показанием для комбинированного использования циклофосфана и метипреда является манифестная высокоактивная СКВ с выраженными иммунологическими нарушениями. Программное применение пульс-терапии ЦФ у больных быстро прогрессирующим люпус-нефритом впервые в стране предложила группа исследователей во главе с профессором И. Е. Тареевой. Согласно этой методике, ЦФ вводится внутривенно из расчета 1 г на 1 м 2 поверхности тела 1-2 раза в месяц в течение года. По сравнению с пероральным назначением ЦФ эта программа позволяет добиться хороших и стабильных результатов более чем у 70% больных с прогрессирующим нефритом. Особенно важным представляется то, что внутривенное введение мегадоз ЦФ оказывает значительно меньшее токсическое воздействие на эпителий мочевого пузыря и костный мозг, практически не вызывая геморрагических циститов и агранулоцитоза.
Другое направление интенсивной терапии ревматических заболеваний — экстракорпоральные методы лечения: плазмаферез (ПФ) и практически все сорбционные технологии, гемо- и плазмосорбция. В современном исполнении ПФ осуществляется с помощью центрифужной или мебранной технологии с удалением 40-60 мл плазмы на 1 кг веса больного. Для замещения потери белка используется альбумин или свежезамороженная плазма. Стандартные курсы ПФ состоят из 3-6 процедур, проводимых последовательно или с короткими интервалами, с суммарной эксфузией плазмы до 15 л.
Интерес к ПФ у ревматологов возник на рубеже 60-80-х годов после фундаментальных исследований, посвященных иммунокомплексной природе СКВ, изучению механизмов иммунокомплексного поражения органов и тканей и патогенетической роли антител к нативной ДНК. Представлялось вполне рациональным уменьшить степень тканевых повреждений за счет удаления из циркуляции иммунных комплексов (ЦИК), антител к ДНК (а-ДНК), криоглобулинов и цитокинов.
Первые попытки применения терапевтического ПФ у больных СКВ продемонстрировали возможности этого метода в первую очередь в ситуациях, когда кортикостероидная и иммуносупрессивная терапия оказывается неэффективной, при наличии высокого уровня ЦИК, а-ДНК, криоглобулинемии, цитопениях. Выявлена прямая зависимость между адекватным удалением из циркуляции патологических белковых структур и клиническим эффектом, изучены механизмы деблокирования РЭС и повышения естественного клиренса.
Эффективность плазмафереза (от нескольких процедур до многократно повторяемых серий при неблагоприятном течении СКВ) хорошо известна и доказана в ходе многочисленных, в основном зарубежных, исследований 80-90-х годов. Пока не получено убедительных данных об эффективности ПФ у больных люпус-нефритом. Результаты проведенных в США и Канаде открытых и контролируемых испытаний весьма противоречивы.
Идея синхронной ИТ материализовалась уже в 80-х годах и является практически неотъемлемой частью лечения некоторых системных васкулитов, синдрома Гудпасчера, Вегенера, Хаммана-Ричи, криоглобулинемической пурпуры и поражения центральной и периферической нервной системы при болезни Шегрена. Первые успешные попытки применения синхронной ИТ у больных СКВ были предприняты в 1984 году в Японии, России и Германии: за рубежом — плазмаферез в комбинации с ЦФ, в России — ПФ в комбинации с пульс-терапией МП и ЦФ.
В Институте ревматологии начиная с середины 80-х изучалась эффективность синхронного применения ПФ и пульс-терапии МП и ЦФ у 56 больных СКВ с неблагоприятным жизненным прогнозом. Методика проведения синхронной интенсивной терапии (СИТ) заключалась в следующем: в течение первого месяца больным проводились три процедуры ПФ с удалением не менее 1500 мл плазмы за сеанс, интервалы между процедурами составляли 5-6 дней. После каждой процедуры назначался внутривенно 1 г метипреда, а после второй процедуры к МП добавлялся 1 г ЦФ. Далее в течение года через каждые 3 месяца проводилась одна процедура ПФ с последующим введением 1 г МП и 1 г ЦФ. Основу группы составляли молодые женщины, в подавляющем большинстве с небольшим сроком заболевания, с развернутой клиникой СКВ. Почти у каждого пациента наблюдался прогрессирующий волчаночный нефрит, более чем у половины — нефротический синдром, церебропатия, у трети больных на фоне криоглобулинемии наблюдался распространенный генерализованный васкулит кожи и слизистых оболочек. Высокая клиническая активность сопровождалась значительным повышением уровня антител к ДНК, ЦИК и гипокомплементемией.
Особо следует подчеркнуть, что у половины больных этой группы стандартная терапия, включавшая в себя массивные дозы кортикостероидов и иммунодепрессантов, была неэффективной, а почти трети пациентов адекватная терапия вообще не проводилась.
Многолетнее наблюдение за этой группой больных по окончании 12-месячной СИТ позволило сделать заключение о ее высокой эффективности. Среди этих пациентов 5-летняя выживаемость составила 81%. Наиболее показательными оказались результаты применения СИТ в группе из 12 подростков, у которых течение волчанки, как правило, приобретает фатальный характер. За весь период наблюдения состояние, близкое к клинико-лабораторной ремиссии, было отмечено у 8 из 12 больных, у 2 пациентов эпизодически наблюдались кратковременные обострения СКВ. Ежедневная доза преднизолона составляла от 2,5 до 15 мг, у одной пациентки кортикостероиды были полностью отменены. Большинству больных удалось вернуться к нормальной жизни, учебе, посильной работе, некоторые пациентки вышли замуж и имеют здоровых детей.
Таким образом, программа синхронной интенсивной многомесячной терапии оказывает значительное влияние на клинико-лабораторные проявления и существенно улучшает жизненный и социальный прогноз у больных СКВ с прогностически неблагоприятным вариантом течения. Синхронное назначение ПФ и внутривенное введение ударных доз МП и ЦФ могут использоваться по жизненным показаниям в случаях так называемого волчаночного криза — при тромбоцитопенической пурпуре, церебральной коме, развитии тромбозов, инфарктов и инсультов у больных с антифосфолипидным синдромом и геморрагическим пневмонитом. В этих ситуациях проведение СИТ обычно ограничивается 3-4 последовательными процедурами — вплоть до купирования ургентной ситуации. В случаях с заведомо неблагоприятным долгосрочным жизненным прогнозом — прогрессирующий гломерулонефрит или поражение ЦНС, язвенно-некротический васкулит, острое начало болезни у подростка — требуется проведение длительных программ СИТ.
Нам представляется, что возможности программной СИТ далеко не исчерпаны. Перспективным может оказаться добавление в схему внутривенного иммуноглобулина, моноклональных антител и интерферонов, применение которых способно блокировать образование аутоантител и патологических ЦИК. Весьма актуальным остается индивидуальный подбор программы с более частым (ежемесячным, еженедельным) назначением плазмафереза и ПТ. Особенно важным аспектом, обеспечивающим возможность проведения более длительных и полноценных курсов экстракорпоральных процедур, является внедрение новых технологий обработки плазмы, таких, как каскадная фильтрация и иммуносорбция, применение которых позволяет сводить к минимуму потерю альбумина и селективно удалять из циркуляции патологические аутоантитела и иммунные комплексы.
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
Даны подробные сведения об интенсивной терапии системной красной волчанки, ее современном содержании и перспективе.
С.К. Соловьев, В.А. Насонова — Институт ревматологии РАМН, Москва
S.K.Solovyev, V.A.Nasonova, Institute of Rheumatology, Russian Academy of Medical Sciences, Moscow
С истемная красная волчанка (СКВ) является классическим примером аутоиммунного заболевания. Прогрессирующее поражение жизненно важных органов и систем определяет жизненный и социальный прогноз больных СКВ [1]. За последние два десятилетия принципы терапии СКВ претерпели существенные, практически революционные изменения. На смену прерывистому назначению малых и средних доз глюкокортикостероидных гормонов (ГКС) пришли схемы длительного, многомесячного приема “подавляющих” доз – от 1 до 1,5 мгкгдень и цитотоксические иммунодепрессанты. Комбинированная терапия преднизолоном, циклофосфамидом или азатиоприном позволила увеличить до 40 – 60% 5-летнюю выживаемость в различных группах больных СКВ. Начиная с середины 70-х годов, в практическую ревматологию активно внедряется внутривенное введение сверхвысоких доз метилпреднизолона (МП) и циклофосфана (ЦФ), обозначаемое впоследствии термином “пульс-терапия” (ПТ). С начала 80-х годов для купирования острой моно- или полиорганной недостаточности у больных СКВ все чаще с успехом применяется экстракорпоральная терапия – гемосорбция (ГС) и плазмаферез (ПФ), внутривенное введение мегадоз иммуноглобулина G(ВИГ). Вскоре различные схемы и комбинации экстракорпоральных методов лечения и внутривенного введения ударных доз ГКС, ЦФ и иммуноглобулина послужили основой для определения принципов интенсивной терапии (ИТ) СКВ.
Пульс-терапия метилпреднизолоном
Наиболее известным и распространенным методом ИТ, безусловно, является ПТ. Традиционным, классическим вариантом ПТ считается внутривенное введение 1г МП за 30 – 40 мин в течение 3 последующих дней [2]. Патофизиологическим обоснованием для применения ударных доз ГКС является их способность активно взаимодействовать с системой иммунитета и подавлять воспалительные реакции. Один из важнейших эффектов ПТ – подавление активности нейтрофилов и моноцитов и способность вызывать транзиторную лимфопению. Тормозящее воздействие ПТ на b-лимфоциты приводит к достаточно стойкому (2 – 4 нед) снижению уровня иммуноглобулинов и иммунных комплексов в плазме крови, что важно в случаях гиперпродукции аутоантител и повышенным уровнем циркулирующих иммунных комплексов (ЦИК). Иммуномодулирующее действие ПТ определяется и ингибированием экспрессии и функциональной активности Fc и C3 рецепторов мононуклеаров, что, видимо, и обусловливает клинический эффект у больных с цитопениями.
Противовоспалительный и иммунорегуляторный эффект ПТ в значительной степени обусловлен ее воздействием на систему цитокинов (в особенности на противовоспалительные цитокины – интерлейкины -1,-6 и -8), фактор некроза опухоли и подавлением транскрипции генов металлопротеиназ и липокортина.
Впервые ПТ 6-МП была с успехом применена у больных с активным волчаночным нефритом Kimberly в 1976 г. В дальнейшем 3-дневная ПТ оказалась высокоэффективным способом лечения при многих внепочечных проявлениях СКВ – лихорадке, полисерозите, полиартрите, в некоторых случаях волчаночной церебропатии и цитопении [1, 2]. Лихорадочный синдром, полиартрит и полисерозит обычно бывают полностью купированы на 2 – 3 день от начала ПТ. Эффективность ПТ при церебропатии подтверждается в случаях органического поражения мозга. При появлении первых симптомов (головные боли, зрительные расстройства) 1 г МП вводится в течение 3 – 7 последующих дней. В случаях поперечного миелита эффективность ПТ невысока, около 50%, и зависит от сроков начала лечения. ПТ высокоэффективна у больных СКВ с лейкопениями, в том числе и лекарственными, в некоторых случаях аутоиммунной анемии и тромбоцитопении (синдром Верльгофа). При лечении наиболее прогностически неблагоприятного и сложного для курации волчаночного нефрита ПТ, безусловно, занимает одно из центральных мест. Эффективность лечения во многом зависит от длительности нефрита, морфологической стадии и выраженности почечной недостаточности. Наиболее эффективно назначение 3-дневной ПТ МП на самых ранних стадиях нефрита, без признаков серьезного изменения почечной ткани и почечной недостаточности. В этих случаях длительность “почечной” ремиссии может достигать многих месяцев и даже лет. У больных с активным быстропрогрессирующим люпус-нефритом стандартная ПТ приводит к быстрому уменьшению протеинурии, мочевого осадка и отеков, улучшению функции почек и стабилизации АД. Для повышения клинической эффективности ПТ при прогрессирующем нефрите используется ежемесячное, повторное внутривенное введение 1 г МП в течение 6 – 12 мес [3, 4]. Программное проведение ПТ у больных люпус-нефритом способствует стойкому улучшению азотовыделительной функции почек, уменьшению протеинурии и уровня антиядерных антител в сыворотке крови. Нестабильный клинический эффект ПТ наблюдается у больных с длительным, многолетним течением люпус-нефрита, преобладанием склероза клубочкового аппарата (Y класс по классификации ВОЗ), стойкой артериальной гипертензией и прогрессирующей азотемией.
Побочные явления ПТ МП обычно ограничены тахикардией, гиперемией лица и небольшим эмоциональным возбуждением. Значительно более редко можно наблюдать брадикардию, артериальную гипер- или гипотензию, кратковременный артрит крупных суставов, икоту. Известны единичные случаи внезапной смерти, желудочковые аритмии, вероятно, обусловленные острыми метаболическими нарушениями в миокарде. Для уменьшения риска кардиальных осложнений запрещено сочетание ПТ и фуросемида.
Ударные дозы циклофосфана
Алкилирующий цитотоксик ЦФ по частоте применения у больных с острым и неблагоприятным течением СКВ прочно занимает второе место после ГКС. Наиболее эффективным в настоящее время считается внутривенное введение ударных доз ЦФ [1, 5]. При активном волчаночном нефрите ЦФ назначают из расчета 1000 мг/м2 поверхности тела или 15 – 20 мг на 1 кг массы тела. Наилучшие результаты достигаются при ежемесячном назначении 1 г препарата в течение 6 мес, и далее по 1 г каждые 3 мес до 1,5 лет. Существует и более интенсивная схема внутривенного применения ЦФ – по 500 мг еженедельно, длительностью до 10 нед. У больных СКВ с одновременным поражением почек, кожи, ЦНС и высокой иммунологической активностью целесообразно комбинированное назначение ударных доз МП и ЦФ. Добавление 1 г ЦФ во 2-й или 3-й день стандартной ПТ МП существенно повышает эффективность лечения, приводит к быстрому улучшению клинической картины, нормализации иммунологических и воспалительных показателей активности [6]. Одновременно назначение ударных доз МП и ЦФ может быть высокоэффективным в лечении аутоиммунной волчаночной тромбоцитопении, анемии, распространенном поражении кожи и слизистых оболочек. Особенно актуальна комбинированная ПТ у больных с геморрагическим пневмонитом и такими поражениями ЦНС, как поперечный миелит и поражение зрительного нерва. Внутривенное введение МП в дозах от 250 до 1000 мг одновременно с ЦФ не только значительно усиливает противовоспалительный эффект терапии, но и обладает определенным протективным действием, нивелируя цитотоксические проявления ЦФ. Интенсивная терапия ЦФ, значительно расширяя возможности курации СКВ с полиорганнной недостаточностью, имеет свои особенности и ограничения. Так, у больных с люпус-нефритом, успешно пролеченных ЦФ, может развиться обострение вскоре после отмены препарата. Значительно снижается эффективность ПТ ЦФ при преобладании фиброзных и склеротических изменений в гломерулах (IY класс классификации ВОЗ), нарушении азотовыделительной функции почек с развитием креатининемии. Среди побочных реакций и осложнений наиболее часто можно наблюдать лейко- и нейтропению, учащение вторичной инфекции и аменорею. Ударные дозы ЦФ, вводимые внутривенно, практически никогда не приводят к развитию геморрагического цистита, а угроза развития опухолей реально рассматривается только при суммарной дозе более 60 г.
Внутривенный иммуноглобулин G
ВИГ является препаратом нормального полиспецифического иммуноглобулина, полученного из пула сывороток не менее чем 5000 доноров. Коммерческий ВИГ должен содержать не менее 97% очищенной фракции IgG с сохранной функцией фрагментов F(ab) и Fc, без спонтанной агрегации, быть безопасным по ВИЧ и гепатиту и с периодом полужизни – 21 день. Стандартными препаратами ВИГ, отвечающими этим требованиям, являются сандоглобулин, октагам и некоторые другие препараты IY поколения. Основные механизмы действия ВИГ сводятся к блокаде Fc-рецепторов клеток, ингибированию синтеза антител, модуляции Т-лимфоцитов и влиянию на синтез цитокинов. Большое значение в реализации лечебного эффекта имеет наличие в препарате антиидиотипических антител. При СКВ наибольшую эффективность препарата наблюдают у больных с аутоиммунными цитопениями и при развитии тяжелой церебропатии, сопровождающейся комой, судорогами и психозом [2]. ВИГ в этих случаях назначают как “последнее средство” по 0,5 г на 1 кг массы тела в течение 5 последующих дней. Описаны единичные наблюдения успешного применения ВИГ у больных с генерализованным кожным васкулитом, рецидивирующим полисерозитом и в случаях привычного невынашивания беременности при антифосфолипидном синдроме (АФС).
У больных с волчаночным нефритом назначение ВИГ требует большой осторожности из-за опасности резкого прогрессирования почечной недостаточности. Встречаются аллергические реакции в виде озноба, сыпи, лихорадочной реакции, головокружения и тошноты. Абсолютным противопоказанием для применения ВИГ является дефицит IgA.
Плазмаферез. Сорбционные методы лечения
В современном исполнении ПФ осуществляют с помощью центрифужной или мембранной технологии, с удалением за одну процедуру 40 – 60 мл/кг плазмы. Рекомендуемые курсы ПФ состоят из 3 – 6 процедур, проводимых последовательно или с короткими интервалами. ПФ у больных СКВ показан как “острое вмешательство” при осложненной криоглобулинемии, гипервязком синдроме и тромбоцитопенической пурпуре [2]. ПФ может быть использован как дополнительное высокоэффективное средство при состояниях, непосредственно угрожающих жизни: молниеносный васкулит, полимиелорадикулоневрит, церебральная кома, геморрагический пневмонит. Оправдано подключение ПФ в случаях волчаночного нефрита, рефрактерного к ГКС и цитотоксикам, у больных с АФС с привычными викидышами [7].
Среди сорбционных методов лечения различают селективное и неселективное удаление из циркуляции патологических белковых структур. К неселективным относится ГС, в основе которой лежат физико-химические свойства активированного угля. Помимо прямого удаления ЦИК, аутоантител и цитокинов, ГС стимулирует антиидиотипическую активность, фагоцитоз и повышает чувствительность клеточных рецепторов к лекарственным препаратам. В лечении больных СКВ ГС имеет те же показания, что и ПФ.
Селективная сорбция осуществляется с помощью селективных иммуносорбентов (биологических или химических), способных целенаправленно удалять РФ, антитела к ДНК и ЦИК. Экспериментальные исследования в этой области свидетельствуют о высокой эффективности иммуносорбентов у больных СКВ с высокой иммунологической активностью. Побочные проявления экстракорпоральной терапии обычно сводятся к транзиторной гиповолемии и ознобу, противопоказанием является язвенная болезнь в стадии обострения, маточное кровотечение, непереносимость гепарина. Несмотря на подчас фантастические результаты в критических ситуациях при СКВ, ПФ и ГС как самостоятельные методы лечения редко находят свое место в плановой терапии. Их применение в значительной степени сдерживается развитием так называемого синдрома рикошета, возникающим непосредственно после процедуры и характеризующимся рецидивом клинической активности и резким повышением уровня антител и ЦИК. Подавление активности антителопродуцирующих b-лимфоцитов и предотвращение синдрома рикошета достигается путем последовательного, синхронного применения ПФ и ПТ МП-ЦФ [2]. Синхронизация интенсивной терапии в виде многомесячной программы, возможно, превосходит по эффективности все известные способы лечения СКВ с неблагоприятным жизненным прогнозом [8]. Существует несколько методик синхронной интенсивной терапии: 1) серия плазмаферезов из 3 – 6 последовательных процедур с дальнейшим коротким курсом мегадоз ЦФ внутривенно; 2) начальная серия процедур ПФ (обычно 3) синхронно с внутривенным введением ЦФ 1 г и МП 3 г и в дальнейшем по 1 процедуре ПФ в 1 – 3 мес в течение года, синхронно с 1 г ЦФ и 1 г МП. Вторая схема синхронной интенсивной терапии представляется более убедительной, так как обеспечивает программный контроль в течение года. Программное назначение комбинации ПФ и ПТ МП и ЦФ показано в первую очередь больным СКВ с неблагоприятным жизненным прогнозом, обусловленным началом заболевания в подростковом и молодом возрасте [9], быстрым развитием нефротического синдрома, быстропрогрессирующим типом нефрита [8], стойкой артериальной гипертензией и с развитием угрожающих жизни состояний (церебральный криз, поперечный миелит, геморрагический пневмонит, тромбоцитопения и др.).
В последние годы агрессивные методы лечения перестают быть “терапией отчаяния”, уделом реанимационных отделений и ургентных ситуаций. Плановое назначение этих методов способно существенно улучшить отдаленный жизненный прогноз у значительной части больных СКВ.
В ближайшей перспективе вполне очевидно появление новых схем и программ интенсивной терапии СКВ, например, синхронизация ВИГ и ПФ, иммуносорбции и ЦФ, ударные дозы препаратов интерферона и антицитокиновых антител.
1. Иванова М. М. Системная красная волчанка. В кн. Ревматические болезни. М., Медицина, 1997;160–72.
2. Cоловьев С.К. В кн. Ревматические болезни. М., Медицина. 1997;106–7;125–7;100–2.
3. Harisdangkul V, Rockhold L, Myers A. Lupus nephritis: efficacy of monthly pulse therapy with intravenous methylprednisolone. South Med J 1989;82(3):321–7.
4. Liebling MR, McLaughlin K, Boonsue S, Kasdin J, Barnett EV. Monthly pulses of methylprednisolone in SLE nephritis. J Rheumatol 1982;9(4):54.
5. Steinberg AD. Cyclophosphamide in lupus nephritis. J Rheumatol 1995;22(10):1812–5.
6. Соловьев С.К., Иванова М.М., Насонов Е.Л. и др. Комбинированное применение ударных доз 6-метилпреднизолона и циклофосфана у больных системной красной волчанкой. Тер. Арх., 1985;8:7–12.
7. Wallace DJ. Plasmapheresis in Lupus. Lupus 1993;2:141–3.
8. Euler HH, Schroeder JO, Harten P, et al. Treatment-free remission in severe systemic lupus erythematosus following synchronization of plasmapheresis with subsequent pulse cyclophosphamide. Arthr Rheum 1994;37(12):1784–94.
9. Соловьев С.К., Шайков А.В., Чикликчи А.С. и др. Программная интенсивная терапия у подростков с неблагоприятным вариантом течения системной красной волчанки. Детск. ревматология. 1995;1:52–8.
Учебная медицинская литература, онлайн-библиотека для учащихся в ВУЗах и для медицинских работников
Системная красная волчанка (СКВ) — системное полисиндромное воспалительное заболевание соединительной ткани, развиваюшееся преимущественно у девушек и молодых женщин на фоне генетически обусловленного дефекта иммунорегуляторных процессов, приводящего к неконтролируемой продукции антител к собственным клеткам и их компонентам.
Лечебная программа при СКВ.
- Режим.
- Диета.
- Лечение гормональными иммунодепрессантами.
- Лечение негормональными иммунодепрессантами.
- Иммунотерапия.
- Интенсивная терапия.
- Лечение аминохинолиновыми соединениями.
- Применение НПВС.
- Лечение антикоагулянтами и антиагрегантами.
- Эфферентная терапия.
- Лечение люпус-нефрита.
- Диспансеризация.
1. Режим
Режим больного СКВ зависит от характера течения, степени активности заболевания, выраженности системных проявлений. Лечение в фазе обострения проводится в стационаре, при тяжелом течении (особенно при развитии диффузного миокардита, эндокардита; люпус-нефрита), высокой активности процесса рекомендуется постельный режим; в случае диффузного миокардита — строгий постельный режим до улучшения состояния, показателей гемодинамики и ликвидации недостаточности кровообращения.
При хроническом течении СКВ и минимальной активности процесса лечение проводится амбулаторно.
2. Лечебное питание
В питании больного следует предусмотреть достаточное количество витамина С, витаминов группы В, ненасыщенных жирных кислот. При развитии недостаточности кровообращения, поражении почек необходимо ограничить потребление поваренной соли, жидкости.
3. Лечение гормональными иммунодепрессантами
Этиологическое лечение СКВ в настоящее время невозможно. Патогенетическая терапия является ведущей и направлена на подавление иммунокомплексной патологии.
Гормональные иммунодепрессанты — глюкокортикоиды — являются лекарствами первого ряда при СКВ.
В. А. Насонова указывает, что обоснована необходимость применения длительной терапии глюкокортикоидами, позволяющей сохранить или продлить жизнь многим больным, значительно улучшить прогноз этого заболевания — от безнадежного до вполне удовлетворительного. Следует учесть, что неадекватное прерывистое лечение глюкокортикоидами сопровождается развитием синдрома отмены с последующими еще более тяжелыми обострениями.
Адекватное лечение глюкокортикоидами в подавляющих дозах, длительное применение их в поддерживающих дозах дает возможность добиться длительной ремиссии. Эффект глюкокортикоидов обусловлен их способностью подавлять иммунокомплексный воспалительный процесс и аутоиммунные реакции.
Абсолютным показанием к назначению глюкокортикоидов является острая, подострая форма СКВ и обострение хронической СКВ. Из всех глюкокортикоидных препаратов наибольшее значение имеет преднизалон, обладающий достаточно высоким терапевтическим эффектом и вызывающий сравнительно нетяжелые побочные реакции при многолетнем приеме. Лучшей переносимостью и хорошим терапевтическим эффектом обладает метилпреднизолон (урбазон). Он значительно реже, чем другие глюкокортикоиды, вызывает поражение ЖКТ (стероидные эрозии и язвы).
Согласно данным В. А. Насоновой, лечение СКВ преднизолоном проводится следующим образом. Доза препарата зависит от остроты течения и активности процесса.
При остром течении с самого начала заболевания, а при подостром и хроническом течении при II и III ст. активности патологического процесса назначаются глюкокортикоиды.
Преднизолон в подавляющей дозе 40-50 мг в сутки назначают при остром и подостром течении (III ст. активности), а при нефротическом синдроме или менингоэнцефалите — в дозе 60 мг в сутки и более.
При подостром течении II ст. активности, а также при хроническом течении II-III ст. активности подавляющая доза может быть меньше 30-40 мг, при I ст. активности — 15-20 мг в сутки. Продолжительность приема преднизолона в подавляющей дозе определяется степенью выраженности клинико-лабораторных признаков (обычно не менее 3 месяцев, а при необходимости — до 6 месяцев и более). В случаях длительной терапии большими дозами глюкокортикоидов можно применять следующую альтернирующую методику приема этих препаратов. При снижении клиниколабораторных признаков активности до II ст. (обязательно исчезновение полиартрита, полисерозита, миокардита) суточную дозу преднизолона можно давать следующим образом: 20 мг утром между 8 и 9 ч после завтрака, два приема по 10 мг в дневные часы (в 12 и 14 ч) после легкого обеда. Достигнув эффекта, дозу преднизолона снижают постепенно: сначала дневную (в 14 ч), затем назначаемую в полдень (в 12 ч), затем утреннюю (после 8 ч утра) (табл. 12).
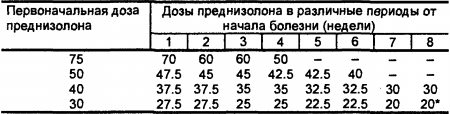
Табл. 12. Примерная схема снижения доз преднизолона (в мг) при достижении терапевтического эффекта. * Далее очень медленно — по 2.5 мг через 1-3 месяца (по показателям общего состояния больного и лабораторных исследований).
Чрезвычайно важен подбор поддерживающей дозы преднизолона, т.е. той наименьшей дозы, которая позволяет поддерживать клинико-лабораторную ремиссию. Преднизолон в поддерживающей дозе 5-10 мг в сутки назначается годами. Для уменьшения побочных явлений преднизолона (кушингоидный синдром, атрофия мышц, артериальная гипертензия, гипокалиемия, остеопороз коры надпочечников) при длительной терапии принимаются удвоенные поддерживающие дозы через день.
Критериями эффективности лечения преднизолоном являются: уменьшение активности патологического процесса, устранение или значительное уменьшение выраженности висцеральных проявлений, особенно со стороны почек, стабилизация течения заболевания.
Величина поддерживающей дозы глюкокортикоидов является одним из критериев глубины клинико-лабораторной ремиссии:
чем меньше поддерживающая доза, тем надежнее ремиссия. Величина поддерживающей дозы 15-20 мг может указывать на активность процесса и на необходимость увеличения дозы, а также, возможно, на целесообразность применения цитостатиков.
Причины неэффективности глюкокортикоидноЙ терапии: нерегулярность приема, неадекватная доза, позднее начало лечения, тяжелая степень иммунокомплексной органной патологии.
При отсутствии преднизолона можно применять триамцинолон, дексаметазон, исходя из паритета : 1 таблетка этих препаратов равна 1 таб летке преднизолона.
О побочных системных действиях глюкокортикоидной терапии см. гл. “Лечение ревматоидного артрита”.
4. Лечение негормональными иммунодепрессантами
Негормональные иммунодепрессанты обладают противовоспалительным эффектом, способностью подавлять иммунокомплексный противовоспалительный процесс и аутоантителообразование.
Показания к назначению цитостатиков:
- высокая активность процесса и быстропрогрессирующее течение;
- активный нефротический и нефритический синдромы;
- генерализованный васкулит (поражение легких, ЦНС, язвенное поражение кожи);
- недостаточная эффективность глюкокортикоидноЙ терапии;
- необходимость быстро уменьшить подавляющую дозу преднизолона из-за плохой переносимости и выраженности побочных действий (подростковый и климактерический возраст больных, значительная и быстрая прибавка в массе тела, тяжелая артериальная гипертензия, стероидный сахарный диабет, психоз, выраженный остеопороз с признаками спондилопатии, аваскулярные некрозы костей);
- необходимость уменьшить поддерживающую дозу преднизолона, если она превышает 15-20 мг в сутки;
- глюкокортикостероидная зависимость.
Наиболее часто применяют азатиоприн (имуран) и циклофосфамид в дозе 1-3 мг на 1 кг массы тела, т.е. от 100 до 200 мг в сутки в сочетании с 30 мг преднизолона. Указанные дозы назначают в течение 2-2.5 месяца (обычно в стационаре), а затем переходят на поддерживающие дозы 50-100 мг в сутки в течение многих месяцев и лет. К этому времени обычно удается снизить дозу глюкокортикоидов.
Критериями эффективности лечения цитостатиками являются:
- исчезновение или уменьшение клинических признаков болезни, в первую очередь нефрита;
- исчезновение или уменьшение кортикостероидной зависимости;
- стойкое снижение активности СКВ и отсутствие в дальнейшем рецидивов;
- предотвращение прогрессирования люпус-нефрита.
Наиболее эффективным цитостатиком при лечении СКВ является циклофосфамид. При высокой активности патологического процесса целесообразно начать лечение с циклофосфамида, но учитывая наибольшую его активность через 4-5 недель следует перейти на азатиоприн или лейкеран для дальнейшего лечения (В. А. Насонова, 1989).
В последние годы стали применять одновременно несколько цитосгатиков: азатиоприн + циклофосфами д (1 мг/кг в д ень внутрь) в сочетании с малыми дозами преднизолона; комбинация азатиоприна внутрь с внутривенным введением циклофосфамида (по 1000 мг/м 2 поверхности тела каждые 3 месяца). При таком комбинированном лечении замедляется прогрессирование люпус-нефрита. Предложена также методика только внутривенного введения циклофосфамида п о 1000 м г/м 2 1 раз в месяц в первые полгода, затем по 1000 мг/м 2 каждые 3 месяца в течение полутора лет на фоне низких доз преднизолона. М. М. Ивановой (1994) установлено, что циклофосфамид более эффективно снижает протеинурию и уменьшает изменения мочевого осадка, синтез антител к ДНК, азатиоприн — наиболее эффективен при диффузном поражении кожи.
О побочных действиях цитостатиков см. в гл. “Лечение ревматоидного артрита”.
5. Иммунотерапия
Разрабатываются следующие методы иммунотерапии СКВ: применение антиидиотипических моноклональных анти-СD4-антител при люпус-нефрите; внутривенное введение иммуноглобулинов (по 0.4 г/кг в сутки в течение 5 дней при выраженных формах СКВ с тромбоцитопенией); лечение любензаритом (подавляет синтез антител к ДНК, ингибирует синтез IgM-ревматоидного фактора); внутривенное введение рекомбинантных препаратов интерферона (а, у) ежедневно в течение 3 недель, а затем дважды в неделю в течен ие 2 м есяцев.
6. Интенсивная терапия
К интенсивной терапии СКВ относятся: пульс-терапия ударными дозами метилпреднизолона, комбинированная пульс-терапия метилпреднизолоном и циклофосфаном.
Показания:
- неэффективность пероральной (даже массивной) глюкокортикоидноЙ терапии, особенно при нефротическом синдроме;
- быстрое прогрессирование болезни и неэффективность обычной терапии СКВ.
Методика пульс-терапии : вводят внутривенно капельно п о 1000 мг метилпреднизолона в 100 м л изотонического раствора натрия хлорида в течение 3 дней подряд. В капельницу добавляют 5000 ЕД гепарина.
Во время пульс-терапии и после нее больные продолжают принимать внутрь ту же дозу преднизолона, что и прежде.
Под влиянием пульс-терапии быстро улучшается функциональное состояние почек, исчезают эритематозная сыпь на лице, капилляриты, полиартрит, в целом наблюдается выраженная положительная клиническая динамика.
Во время пульс-терапии возможны побочные явления: повышение АД, зуд и гиперемия кожи, судорожные подергивания, нарушения ритма сердца, описаны случаи внезапной остановки сердца. Учитывая это, пульс-терапия преднизолоном назначается строго по показаниям и в ходе ее проведения необходимо тщательно контролировать работу сердца.
R. Lugmani (1993) рекомендует после пульс-терапии применять циклофосфамид в дозе 200 мг в неделю в течение 3-6 месяцев в сочетании с преднизолоном в дозе 20-25 мг в сутки.
Этот вид интенсивной терапии применяется при СКВ с тяжелым, торпидным к лечению нефротическим синдромом и генерализованным васкулитом.
Методика: в первый день внутривенно капельно в 100 мл изотонического раствора натрия хлорида в течение 30-40 мин вводя т 1000 мг метилпреднизолона и 1000 мг циклофосфана, в последующие два дня больному вводят капельно по 1000 мг м етилпреднизолона, в капельницу добавляют 5000 ЕД гепарина.
Больным с высоким АД вводят гипотензивные и мочегонные средства. Начиная с четвертого дня, больным назначается преднизолон в той же дозе, что до пульс-терапии, но не ниже 40 мг в сутки в сочетании со средними дозами цитостатиков.
Метод комбинированной пульс-терапии метилпреднизолоном и циклофосфаном высокоэффективен, приводит к значительному клиническому улучшению, особенно это заметно у больных с нефротическим синдромом (снижается или нормализуется АД, повышается диурез, уменьшаются альбуминурия и отеки).
Побочные действия те же, что при пульс-терапии метилпреднизолоном, кроме того, возможны выпадение волос, лейкопения.
7. Лечение аминохинолиновыми соединениями
Механизм действия аминохинолиновых соединений описан в гл. “Лечение ревматоидного артрита”.
Эти препараты назначают больным хронической СКВ прежде всего при поражении кожи, суставов: делагил по 0.25-0.5 г в сутки и плаквенил по 0.2-0.4 г в сутки. Лечение продолжается длительно — месяцы, годы.
Кроме того, аминохинолиновые соединения могут применяться при люпус-нефрите. В. А. Насонова рекомендует в этом случае плаквенил по 0.2 г 4-5 раз в день (всего 0.8-1 г) в течение длительного времени — до года и более.
Аминохинолиновые соединения могут применяться в сочетании с глюкокортикоидами, что позволяет уменьшить дозы препаратов. При лечении аминохинолиновыми соединениями возможны побочные явления: лейкопения, анемия, алопеция, дегенерация сетчатки, диспептические явления. Лечение проводится под контролем анализа крови и исследования состояния глазного дна.
8. Применение НПВС
НПВС обладают выраженным противовоспалительным действием, умеренным иммунодепрессантным эффектом, стабилизируют лизосомальные мембраны.
НПВС назначаются при подостром течении (в ранней стадии) и хроническом течении СКВ, преимущественно при наличии артрита. Эти препараты применяются в обычных терапевтических дозах (как при ревматоидном артрите) длительно, до исчезновения воспаления в суставах и нормализации температуры тела. Однако при лечении НПВС необходимо учитывать нередкое развитие побочных эффектов (см. гл. “Лечение ревматоидного артрита”).
9. Лечение антикоагулянтами и антиагрегантами
Антикоагулянты и антиагреганты в комплексной терапии СКВ применяют при наличии поражения почек, ДВС-синдрома, при нарушениях микроциркуляции.
Из антикоагулянтов рекомендуется гепарин — 10,000-20,000 ЕД в сутки (4 инъекции под кожу живота) в течение нескольких месяцев.
В качестве антиагрегантов используются курантил в суточной дозе 150-200 мг, трентал — 400-600 мг в течение нескольких месяцев.
10. Эфферентная терапия
К эфферентной терапии относятся плазмаферез и гемосорбция.
Плазмаферез — метод эфферентной, экстракорпоральной терапии, направленной на освобождение организма от продуктов метаболизма, циркулирующих иммунных комплексов путем удаления плазмы больного.
Показанием к назначению плазмафереза при СКВ является наиболее тяжелое течение, когда обычная терапия глюкокортикоидами, включая и пульс-терапию метилпреднизолоном, а также применение цитостатиков, оказывается неэффективной.
На курс лечения рекомендуется от 3 до 5 процедур плазмафереза при однократном удалении 800-1000 мл плазмы.
Гемосорбция — экстракорпоральный метод очищения крови путем пропускания ее через колонку с гранулами активированного угля. Метод обладает иммунокорригирующим действием, а также повышает чувствительность клеток крови и тканей к действию глюкокортикоидов.
Показания к гемосорбции при СКВ:
- сохраняющаяся активность СКВ, несмотря на большие дозы глюкокортикоидов и цитостатиков;
- активный люпус-нефрит;
- упорный суставной синдром;
- васкулиты кожи с изъязвлениями;
- невозможность увеличения дозы глюкокортикоидов из-за развившихся осложнений.
М. М. Иванова (1985), учитывая высокую эффективность и хорошую переносимость гемосорбции, рекомендует проводить ее на ранней стадии болезни для более активного воздействия на иммунопатологическую реактивность.
На курс лечения рекомендуется от 3 до 5 процедур гемосорбции, проводимых еженедельно с применением отечественных активированных углей ИГИ, АДБ, ГСУ.
Плазмаферез и гемосорбция проводятся на фоне приема глюкокортикоидов и цитостатиков.
11. Лечение люпус-нефрита
Люпус-нефрит у больных СКВ может принимать тяжелое течение и определять прогноз.
Основными методами лечения люпус-нефрита являются:
- лечение глюкокортикоидами с начальной суточной дозой преднизолона 60-80 мг;
- пульс-терапия метилпреднизолоном;
- комбинированная терапия глюкокортикоидами и цитостатиками;
- пульс-терапия метилпреднизолоном и циклофосфаном;
- лечение аминохинолиновыми соединениями;
- применение гепарина и антиагрегантов;
- плазмаферез, гемосорбция;
- диета № 7 с коррекцией содержания белка в зависимости от уровня его потерь с мочой за сутки при нефротическом синдроме.
М. М. Иванова (1995) предлагает при недостаточной эффективности пульс-терапии проводить лечение метилпреднизолоном внутривенно по 250 мг в сутки в течение еще 2-3 недель.
При развитии у больного ХПН лечение проводится та к, как это описано в гл. “Лечение хронической почечной недостаточности”.
12. Диспансеризация
Диспансеризация больных СКВ осуществляется ревматологом, а при его отсутствии — терапевтом.
Частота наблюдений врачом: при минимальной активности — 2 раза в год, при II ст. активности — 4 раза в год.
ЛОР-врач, стоматолог, гинеколог офтальмолог осматривают больных 2 раза в год; невропатолог, психиатр, нефролог — по показаниям.
Перечень и частота необходимых лабораторных и инструментальных исследований при диспансеризации:
- клинический анализ крови, общий анализ мочи — 4-6 раз в год;
- число тромбоцитов — 2 раз а в год;
- при применении цитостатических препаратов — ежемесячный контроль анализов, рентгенография (флюорография) органов грудной клетк и 2 раза в год;
- рентгенография суставов — по показаниям;
- биохимическое исследование крови (фибриноген, серомукоид, белковые фракции, мочевина) — не реж е 2 раз в год;
- ЭхоКГ и ФКГ — по показаниям;
- исследование крови на содержание волчаночных клеток и антинуклеарного фактора — 2 раза в год.
Основным лечением является применение глюкокортикоидов и цитостатиков в индивидуально подобранных дозах; при III ст. активности — обязательно стационарное лечение.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Читайте также:


