Мрт грыжа передней брюшной стенки
Успешность любого лечения зависит от правильной постановки диагноза. Чем раньше будет обнаружено заболевание, тем выше шанс избавиться от патологии и минимизировать осложнения. Метод, позволяющий вовремя выявить причину беспокоящих симптомов – магнитно-резонансная томография. Суть данного способа визуализации заключается в неинвазивном, безболезненном обследовании органов и систем.
Часто бывает тяжело определить причину неприятных ощущений в области живота. Благодаря МРТ брюшной стенки удается подтвердить или опровергнуть наличие предполагаемого заболевания. Во время процедуры визуализируют состояние мышц, кожного покрова, подкожной жировой клетчатки, сосудов, нервных сплетений, лимфатических узлов и пр. Если пациент жалуется на тянущие боли в области живота (особенно при физической нагрузке), вздутие, постоянные запоры - следует незамедлительно обратиться к врачу для диагностики патологий. В случае присутствия визуальных признаков выпячивания тканей, может быть назначена магнитно-резонансная томография для исключения грыж передней брюшной стенки.
Заболевания мягких тканей живота
Магнитно-резонансная томография лучше компьютерной показывает состояние мягких тканей, выявляет воспалительные процессы, скопления жидкости, опухоли (первичные, вторичные) и другие патологические очаги. Исследование могут проводить с применением контрастного вещества для увеличения четкости изображения.
На снимках МРТ видны следующие заболевания передней стенки живота:
- миозит (воспаление мышц);
- грыжи брюшной стенки (выпячивание сальника или части органа (чаще кишечника) через естественные отверстия живота (пупок, брыжейку и пр.));
- абсцесс, флегмона (гнойные инфекции мягких тканей);
- дегенеративные процессы в мышцах (миопатии, миодистрофии и пр.);
- добро- и злокачественные опухоли и пр.
Магнитно-резонансная томография помогает врачу определить необходимость операции, спланировать ход вмешательства, контролировать результативность проводимой терапии.
МРТ мягких тканей живота, что показывает?
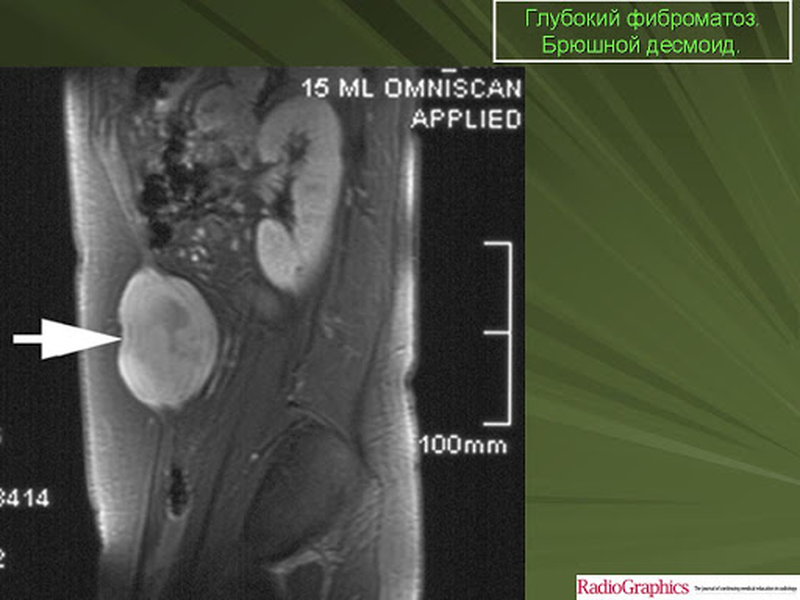
Опухоль передней брюшной стенки
В результате МР-обследования визуализируют патологические процессы мягких тканей передней брюшной стенки. Ранняя стадия заболевания лучше поддается лечению, чем запущенный процесс. Визуализация позволяет определить наличие грыж передней стенки живота. Последние возникают вследствие выпячивания внутренних органов через так называемые “слабые места”, возникающие в зонах травмирования мышц, в том числе в результате оперативного вмешательства, или существующие из-за врожденных дефектов. МРТ брюшной полости позволяет визуализировать осложнения патологии, спланировать ход оперативного удаления грыжи.
При поверхностном абсцессе выявляют ограниченное капсулой скопление гноя в брюшной стенке параллельно с отеком тканей, что свидетельствует о выраженности воспалительной реакции.
Миопатии проявляются перерождением мышц (изменением размера, жировой дегенерацией и пр.)
Опухоли визуально выглядят образованием лимфоидного, жирового или иного характера в брюшной стенке.
Миозит на снимках определяют по отеку мышечной ткани при режиме Т2 ВИ, при контрастировании наблюдают усиление области воспаления.
Как проходит МРТ передней брюшной стенки?
Рекомендована предварительная подготовка, включающая специальную низкоуглеводную диету. Накануне исследования за несколько дней не употребляют продукты, вызывающие вздутие (бобовые, мучное, газированные напитки, капусту и пр.). На сканирование необходимо приходить натощак (за 4-6 часов нельзя принимать пищу), разрешают выпить немного воды.
Процедура проходит в специальном помещении, где установлен магнитно-резонансный томограф. Пациента просят оставить предметы, содержащие металл (украшения, телефон, банковские карты, флеш-носители и пр.), после чего больного располагают в правильном положении на столе аппарата. Во время сканирования медперсонал наблюдает за процессом из соседней комнаты. Исследования передней стенки живота могут проводить с внутривенным введением контрастного вещества. Благодаря индикатору осуществляют дифференциацию патологий, определяют величину опухолей, вовлеченность окружающих тканей и органов, тяжесть заболевания и пр.
Продолжительность диагностики не превышает 30 минут. По окончанию процедуры в течение часа пациенту выдают заключение эксперта.

МР - Холангиография

МРТ брюшной полости цены в СПб

МРТ при раке прямой кишки
Почему возникает
Послеоперационная (вентральная) грыжа – это выход брюшины и внутренних органов за границы брюшной полости в области послеоперационного рубца. Органы выходят не через естественное отверстие, а через послеоперационный дефект передней брюшной стенки.
Это частое осложнение лапаротомических операций – удаления аппендикса, желчного пузыря, матки и других внутренних органов. В большинстве случаев выпячивание формируется в восстановительном периоде после экстренных операций, реже – после плановых.
Единственной причины, которая бы приводила к развитию патологии, не существует. Играет роль комбинация факторов – местных и общих.
Местные факторы связаны с изменениями в области послеоперационной раны:
- нерациональный выбор оперативного доступа (большой разрез);
- некачественное ушивание раны (недостаточное сопоставление краев, избыточное натяжение, неправильный выбор шовного материала);
- постановка дренажей;
- инфицирование раны;
- снижение регенерации.
На развитие болезни влияют и общие факторы, которые связанные с состоянием пациента:
- отягощенная наследственность;
- патологические состояния, которые приводят к повышению внутрибрюшного давления – хронические запоры, длительный кашель, беременность;
- ожирение;
- заболевания, при которых снижаются регенераторные способности тканей (заживление) – сахарный диабет, сердечно-сосудистая патология, авитаминоз, гипопротеинемия, анемия.
На развитие болезни может влиять как один фактор, так и сразу несколько. Причем сочетание нескольких факторов повышает вероятность несостоятельности швов и формирования выпячивания.
Лечение
Если после врачебного обследования диагностирована послеоперационная грыжа брюшной полости что делать? Алгоритм действий зависит от многих факторов – размеров грыжи, наличия ущемления и состояния близлежащих тканей, общего состояния здоровья пациента.
Самым радикальным и эффективным способом лечения послеоперационной грыжи является проведение повторной операции (герниопластики), направленной на укрепление брюшной стенки в области рубца. Подобный способ предотвратит рецидивы и избавит от возможных осложнений в будущем.
Самая простая и быстрая операция для устранения вентральной грыжи – это ушивание дефекта путем наложения внахлест мышц, расположенных по краям отверстия. Перед ушиванием проводят обязательное вправление грыжевого содержимого в брюшную полость. Операция проводится только если размер грыжевых ворот не превышает 5 см, в области раны нет воспалительных и иных патологических изменений. Метод имеет недостаток – возможность повторного возникновения грыжи в том же месте (появление рецидива).
Метод используется в большинстве случаев вентральных грыж. Ткани в области грыжевого отверстия дублируют сетчатым имплантом. Материал не вызывает аллергических реакций. Лоскут импланта необходимого размера, как заплатка, подшивается к тканям вокруг грыжи (мышцам, апоневрозу). Благодаря своей структуре, имплант крепко срастается с окружающими тканями и значительно увеличивает прочность брюшной стенки там, где ранее была грыжа. Применение сетки позволяет избежать излишнего натяжения брюшной стенки в области рубца, что способствует лучшему заживлению и позволяет избежать рецидивов в дальнейшем.
Это операция, при которой хирурги подводят сетчатый имплант к грыжевому дефекту через 2-3 мини-разреза, длиной всего в пару сантиметров. Данная модификация герниопластики обладает всеми преимуществами лапароскопии: быстрое восстановление больного после операции, минимальные рубцы после вмешательства и малая травматичность.
Квалифицированные хирурги нашей клиники всегда правильно и адекватно подберут самые оптимальные способы лечения послеоперационной грыжи или же дадут подробные рекомендации по лечению послеоперационной грыжи без операции. Такие безоперационные способы есть в арсенале врачей и, в ряде случаев, они способны временно улучшить состояние пациента и предотвратить осложнения и прогрессирование заболевания. Но навсегда вылечиться от вентральной грыжи поможет только операция герниопластики.
Если доктор принимает решение по каким-либо причинам отложить операцию герниопластики, для предотвращения увеличения грыжи и появления осложнений пациентам рекомендуются следующие мероприятия:
- Ношение бандажа – это временная мера. Бандаж (широкая лента из эластичной ткани снимет часть нагрузки с мышц брюшного пресса) применим только в начальных стадиях развития грыж.
- Избегать физических нагрузок, так как при них увеличивается внутрибрюшное давление и происходит увеличение грыжевого дефекта и размера выпячивания.
- Следить за функциями кишечника, избегать запоров и метеоризма (вздутия кишечника), так как они тоже увеличивают давление внутри брюшной полости.
Послеоперационная грыжа: диета предусматривает ограничение по количеству одновременно принимаемой пищи (есть нужно малыми порциями, но чаще). Нельзя есть продукты, вызывающие повышенное газообразование – капусту, бобовые, жирную, пряную и острую пищу, газированные и алкогольные напитки. Также следует избегать продуктов, способствующих возникновению запоров – мучных и хлебобулочных изделий из муки высшего сорта, кондитерских изделий, насыщенных мясных бульонов, риса, крепкого чая и кофе, вяжущих фруктов и ягод.
Классификация
Вентральные грыжи характеризуются разнообразными размерами, формой, локализацией. Клиническая картина отличается в зависимости от наличия осложнений, состава грыжевого содержимого. Наличие такого большого разнообразия патологии затрудняет создание единственной классификации. Различают следующие разновидности патологии:
- По локализации: срединные (нижние, верхние) и боковые (правосторонние и левосторонние, нижние и верхние).
- По величине: малые, средние, обширные, гигантские.
- По составу грыжевого мешка: петли тонкого кишечника, большой сальник, желудок, мочевой пузырь.
- По наличию осложнений: ущемленная, перфорирующая, с признаками острой кишечной непроходимости.
- По вправимости: вправимая, невправимая.
Общая информация
Грыжа брюшной стенки – это врожденный или приобретенный дефект мышечно-апоневротической целостности брюшной стенки, который дает возможность для выпячивания через него любого образования, которое в нормальных условиях здесь не происходит.
Название протокола: Вентральная грыжа
Код(ы) по МКБ 10:
| МКБ-10 | |
| Код | Название |
| К43 | Грыжа передней брюшной стенки. Включены: грыжа надчревная, послеоперационная. Исключена: паховая грыжа (40) |
| К43.0 | Грыжа передней брюшной стенки с непроходимостью без гангрены. |
Грыжа передней брюшной стенки: (вызывающая непроходимость, ущемленная, невправимая) без гангрены. Странгуляционная грыжа.
Дата разработки / пересмотра протокола: 2013 год (пересмотр 2020 г.)
Сокращения, используемые в протоколе:
| К43.1 | Грыжа передней брюшной стенки с гангреной. Гангренозная грыжа передней брюшной стенки. |
| К43.9 | Грыжа передней брюшной стенки без непроходимости или гангрены. |
| ВГ | – | вентральная грыжа |
| ГПБС | – | грыжа передней брюшной стенки |
| КТ | – | компьютерная томография |
| МРТ | – | магнитно-резонансная томография |
| ПГ | – | послеоперационная грыжа |
| СИАГ | – | синдром интраабдоминальной гипертензии (компартмент синдром) |
| УЗИ | – | ультразвуковое исследование |
| IPOM | – | intraperitoneal onlay mesh |
| CST | – | component separation technique |
Пользователи протокола: хирурги.
Категория пациентов: взрослые.
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). Результаты, которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
| GPP | Наилучшая клиническая практика. |
Клинические проявления
В большинстве случаев единственный симптом патологии – наличие выпячивания в области послеоперационного рубца на передней стенке живота. Такое образование имеет следующие характеристики:
- локализуется в месте шва;
- увеличивается в положении стоя;
- увеличивается при кашле, натуживании, физической нагрузке;
- уменьшается или исчезает в горизонтальном положении;
- при неосложненном течении легко вправляется обратно.
Второй по частоте встречаемости признак болезни – боль. Поначалу боль имеет ноющий и тянущий характер, усиливается при физической нагрузке. Со временем боль может становиться резкой и постоянной, особенно при невправимости.
Остальные симптомы развиваются реже и зависят от того, какой орган входит в содержимое грыжевого мешка.
| Содержимое грыжевого мешка | Дополнительные симптомы |
| Петли кишечника | Боль носит ограниченный характер, появляется запор и метеоризм. При длительном течении болезни могут развиваться признаки интоксикации. |
| Желудок | Характерно появление изжоги и отрыжки, периодической рвоты, чувства тяжести после еды. |
| Большой сальник | Боль менее интенсивная, распространяется на всю переднюю стенку живота. |
| Мочевой пузырь | Помимо выпячивания появляются дизурические симптомы (учащенное или болезненное мочеиспускание). |
Послеоперационный период
Благодаря современным методам лечения реабилитационный период после лапароскопической операции значительно сокращен, срок пребывания в клинике составляет 1-6 дней. Однако уже в первые сутки пациент может ходить, ему разрешается принимать жидкую пищу. И хотя восстановительный период зависит от множества факторов, пациент, как правило, через неделю может возвратиться к привычному образу жизни. Нужно учесть, что после проведенной операции больной должен носить специальный бандаж, тем более после иссечения послеоперационной грыжи большого размера. Также от пациента требуется неукоснительное соблюдение рекомендаций по питанию, разумная физическая активность, нормализация веса.
Как поставить диагноз
При выявлении выпячивания нужно обратиться к хирургу. Постановка диагноза обычно не вызывает трудностей, учитывается клиническая картина и анамнез (проведенное ранее оперативное вмешательство). При физикальном обследовании врач обращает внимание на следующие изменения:
- послеоперационный рубец;
- выпячивание – его размер, форму, вправимость;
- состояние кожи вокруг рубца (могут быть признаки дерматита);
- консистенция грыжевого содержимого, края грыжевых ворот и размер грыжи (при пальпации);
- симптом кашлевого толчка.
В большинстве случаев этого достаточно для постановки диагноза.
Иногда показано проведение дополнительного обследования – ультразвукового исследования (УЗИ), обзорной и контрастной рентгенографии. Эти методы назначаются не только для подтверждения диагноза, но и для исключения других заболеваний.
Вентральная грыжа: операция лапароскопическим методом
Для проведения вмешательства хирург производит несколько проколов брюшной стенки. Для этого делаются небольшие разрезы, которые не травмируют мышечную часть, а только кожу. Этот факт благоприятно влияет на послеоперационный период, значительно сокращая его, и не доставляет болевых ощущений, что особенно важно для всех пациентов.
Проколы производятся хирургом специальным инструментарием – троакаром. По нему вводится в брюшную полость лапароскоп, к которому подключен источник света и передатчик изображения на монитор. Таким образом, специалист наблюдает за своими движениями изнутри тела.
С помощью дополнительных троакаров вводятся инструменты для выполнения операции. Через один троакар проводится зажим для захвата ткани, которым устанавливается сетчатый имплантат. Другим – закрепляется синтетическая сетка швами или специальными скобками.
Операция длится около 1 часа под общим наркозом. Пациент находится в стационаре 1-2 дня под полным контролем медицинского персонала во избежание непредвиденных осложнений и реакций организма.
Как лечить патологию
Основной метод лечения – оперативное удаление грыжи с последующей пластикой. При наличии противопоказаний к операции применяется консервативное лечение. Оно направлено не столько на излечение от болезни, как на профилактику осложнений.
Консервативное лечение проводится при отказе пациента от операции или наличии противопоказаний. Противопоказанием к хирургическому лечению может быть беременность, тяжелые заболевания сердца, дыхательной системы, нарушение свертывания крови.
В чем заключается консервативное лечение:
- Ношение специального высокого бандажа.
- Укрепление мышц пресса (лечебная физкультура).
- Исключение тяжелой физической нагрузки.
- Нормализация массы тела при ожирении.
- Соблюдение диеты, направленной на предотвращение запоров (употребление клетчатки и злаковых, 1,5 л воды в день).
- Лечение заболеваний, которые проявляются хроническим кашлем.
Консервативное лечение может применяться в качестве подготовки к операции.
Проведение операции по удалению грыжи показано всем пациентам при отсутствии противопоказаний. При неосложненном течении назначается плановое хирургическое вмешательство (через 6–12 месяцев после развития патологии).
При ущемлении грыжи или развитии острой кишечной недостаточности проводится ургентная операция.
Операция может быть открытой или лапароскопической. Выбор тактики зависит от вправимости грыжи, ее размера, наличия воспалительных изменений. В большинстве случаев хирургическое вмешательство проводится под наркозом, редко под местной анестезией (при небольшом размере выпячивания).
Операция состоит из двух этапов:
- Иссечение грыжевого мешка.
- Закрытие дефекта местными тканями или синтетическим протезом.
3Диагностические мероприятия
Диагностирует заболевание хирург, проводится внешний осмотр. Врач осматривает паховую зону. В правой или левой части (реже в обеих) обнаруживается выпячивание. Оно может быть небольшого размера, у детей младенцев обнаружить его не всегда легко из-за маленьких размеров и развитого подкожного жира.
Выпячивание плотное, при пальпации возникают болевые ощущения. При изменении положения или кашле, грыжа не меняет своей формы, кроме того, при поворотах она может уплотняться. В области грыжи могут быть покраснения или припухлость.
Ущемление паховой грыжи не поддается вправлению.
Затруднения диагностирования могут возникнуть, если в грыжевом мешке оказываются яичник или маточная труба (это встречается при ущемлении у женщин и девочек). Эти органы очень быстро поддаются некротизации (в течение нескольких часов). Из-за этого при прикосновении возникает резкая боль. По этой причине представительниц женского пола сразу отправляют на операцию.
Диагностика маленьких детей тоже имеет свои особенности. При осмотре они испытывают резкую боль, вследствии чего громко плачут, могут испытывать болевой шок, сучат ножками. Это происходит из-за особенностей физиологии. У маленьких детей ускоренный кровоток в кишечнике, из-за чего при пальпации болевой синдром сильней, чем у взрослых.
Возможные осложнения и последствия
Наличие послеоперационной грыжи крайне отрицательно сказывается на качестве жизни человека. Эта патология также становится причиной снижения трудовой деятельности. Послеоперационная или парастомальная грыжа представляет собой не только косметический дефект, но и опасную патологию. Без своевременного и грамотного лечения она грозит развитием серьезных осложнений.
- ущемление;
- копростаз – затвердение и скопление каловых масс в кишечнике;
- непроходимость кишечника;
- перфорация – образование отверстий во внутренних органах.
Ущемление грыжевого мешка после оперативного вмешательства, пожалуй, самая опасная и тяжелая патология, которая относится к экстренным случаям и требует немедленной операции. Грыжа, заключенная между воротами, невправимая, в мешке заключены части внутренних органов, которые плохо снабжены кровью.
Клиническая симптоматика
У подавляющего числа пациентов диагностика наружных брюшных грыж не представляет особых трудностей. Основной симптом заболевания - наличие опухолевидного образования, которое изменяет свои размеры под влиянием различных факторов. Оно увеличивается в вертикальном положении пациента, при кашле и натуживании, а в горизонтальном положении уменьшается или даже совсем перестаёт определяться. Быстрое изменение размеров вплоть до полного исчезновения позволяет отличить грыжевое выпячивание от иных опухолевидных образований, размеры которых во время осмотра постоянны.
При пальпации неосложнённая грыжа безболезненна, имеет мягкоэластическую консистенцию и обычно свободно вправляется в брюшную полость в горизонтальном положении пациента. После вправления грыжевого содержимого удаётся определить дефект в брюшной стенке - грыжевые ворота. Классическим признаком любых форм грыж, за исключением ущемлённых, служит положительный симптом кашлевого толчка. При покашливании пациента пальцы врача ощущают толчки органа, выходящего в грыжевой мешок.
Определённые трудности в диагностике возникают в начальной стадии заболевания, когда ещё не образовалось заметное на глаз выпячивание. В этот период пациент ощущает умеренные тянущие боли в области формирующейся грыжи. Боли обычно возникают при поднятии тяжести, кашле или натуживании во время дефекации или мочеиспускания. При пальпации обычно удаётся определить дефект брюшной стенки, через который при покашливании или натуживании пациента выходит небольшое опухолевидное образование. В случае затруднений клинической диагностики используют специальные методы исследования.
Инструментальная диагностика
Современная инструментальная диагностика больных с грыжевыми образованиями включает комплекс рентгенологических, ультразвуковых и эндоскопических методов исследования, а также выполнение ряда функциональных проб. Их проводят как для уточнения диагноза, так и для выявления сочетанной патологии органов брюшной полости и сопутствующей сердечно-лёгочной патологии.
Наиболее информативным методом рентгенологической диагностики грыж передней брюшной стенки - рентгеновская КТ. Её применение позволяет решать различные практические задачи - диагностировать грыжевое выпячивание, оценивать характер грыжевого содержимого и размеры грыжевых ворот, проводить дифференциальную диагностику грыж с другими патологическими образованиями, оценивать состояние тканей передней брюшной стенки. Кроме решения диагностических задач, КТ позволяет определить соотношение объёма грыжевого содержимого к общему объёму брюшной полости пациента, что необходимо учитывать при выборе метода пластики и прогнозирования вероятности развития компартмент-синдрома в раннем послеоперационном периоде.
УЗИ - высокоинформативный метод инструментального обследования пациентов с различными видами грыж. Его проведение по своей информативности во многих клинических ситуациях существенно не уступает КТ и позволяет решать аналогичные диагностические задачи. Кроме того, применение допплеровских режимов ультразвукового сканирования позволяет регистрировать различные функциональные и органические изменения органного кровотока, наличие которых может накладывать свой отпечаток на течение раннего послеоперационного периода, в особенности на фоне повышения внутрибрюшного давления после выполнения пластики передней брюшной стенки.
Из рентгеноконтрастных методов исследования в диагностике грыжевых образований наибольшее распространение получила перитонеорентгенография. При её выполнении водорастворимый рентгеноконтрастный препарат вводят в брюшную полость, после чего с помощью ряда технических приёмов (натуживание, надавливание рукой в гипогастрии) добиваются равномерного распределения препарата в различных отделах паховых и подвздошных областей. Применение перитонеорентгенографии позволяет добиться высокой точности в выявлении грыжевых образований нижней части передней брюшной стенки, в определении вида (бедренная, паховая или запирательного канала) и типа (прямая или косая паховая, скользящая паховая) грыжи, степени разрушения задней стенки пахового канала, а также с высокой точностью диагностировать рецидив заболевания. Кроме того, этот метод даёт возможность дифференциальной диагностики ряда таких чрезвычайно схожих с симптомами паховой грыжи клинико-морфологических синдромов, как пубалгия, спортивные паховые боли и расширение входа в бедренный канал. Основными отрицательными моментами перитонеорентгенографии, ограничивающими её применение, служит инвазивность самой манипуляции и возможные аллергические реакции на введение рентгеноконтрастных препаратов в брюшную полость.
Эндоскопические исследования у пациентов с грыжевыми образованиями в основном применяют для выявления сопутствующей патологии органов брюшной полости, коррекцию которой необходимо проводить при выполнении симультанных хирургических вмешательств. И только в наиболее трудных для диагностики наблюдениях прибегают к выполнению диагностической лапароскопии для дифференцирования грыжи от других заболеваний органов брюшной полости.
Один из обязательных методов инструментальной диагностики больных с грыжевыми образованиями больших размеров - спирометрия, выполнение которой позволяет дать оценку функции внешнего дыхания пациента. Спирометрия позволяет оценить вентиляционную способность лёгких, провести измерение минутного объёма дыхания, выполнить анализ изменений скорости потоков воздуха в различных отделах дыхательных путей при выполнении манёвра форсированного дыхания. Оценка функции внешнего дыхания пациента позволяет дать оценку уровня бронхиальной проходимости и провести индивидуальный подбор наиболее подходящего вида пластики передней брюшной стенки и метода анестезии.
Аннотация научной статьи по клинической медицине, автор научной работы — Мершина Е. А., Васильева Е. С., Синицын В. Е., Лядов В. К., Егиев В. Н.
Целью исследования явилось определить роль магнитно-резонансной томографии в оценке спаечного процесса после пластики передней брюшной стенки. Было обследовано 8 пациентов после лапароскопической интраперитонеальной (5) и открытой (3) пластики передней брюшной стенки. Всем пациентам были проведены диагностическая МРТ и функциональная кино-МРТ с пробой Вальсальвы. У всех лапароскопически прооперированных пациентов четко визуализировались синтетические сетки . После лапаротомических операций синтетическая сетка не определялась, но были обнаружены спайки и послеоперационная грыжа . Наиболее часто определялись спайки с передней брюшной стенкой. Функциональная кино-МРТ подающий надежды метод в оценке спаечного процесса и послеоперационных грыж после пластики передней брюшной стенки.
Похожие темы научных работ по клинической медицине , автор научной работы — Мершина Е. А., Васильева Е. С., Синицын В. Е., Лядов В. К., Егиев В. Н.
Functional cine-MRI in detection of adhesive disease following ventral hernia repair
The aim of this study was to evaluate the role of functional cine-MRI in detection of recurrent hernia and intraabdominal adhesions following ventral hernia repair. 8 patients were examined after intraperitoneal laparoscopic (5 pts) and open sub-lay repair (3 pts). All patients underwent diagnostic and functional cine-MRI with Valsalva test. In all laparoscopy-patients the meshes were identified. After open surgery the mesh was not visualized, but a recurrent hernia and adhesions were found. The most common adhesions were to the ventral abdominal wall. Functional cine-MRI is a reliable technique for detecting adhesions and recurrent hernia after repair.
с данными других авторов [10, 15]. Кроме того, ЭМА не оказывает лечебного эффекта на гиперпласти-ческие процессы эндометрия. Учитывая высокую распространенность сочетанной патологии эндо- и миометрия, большинство пациенток с аденомиозом после ЭМА нуждаются в дополнительной системной гормонотерапии.
Данные работы свидетельствуют о том, что эхографические маркеры (повышение максимальной систолической скорости в восходящих ветвях маточных артерий, усиление васкуляризации миометрия) опережают клинические проявления функциональной активности внутреннего эндометриоза. Учет доппле-рографических данных позволяет прогнозировать рецидивы в течении заболевания и оптимизировать лечебную тактику.
1. Адамян Л. В., Кулаков В. И., Андреева Е. Н. Эндометриозы. Руководство для врачей. - М.: Медицина, 2006. - 416 с.
2. Андреева Е. Н. Контрацепция у больных эндометриозом // Трудный пациент. - 2006. - Т. 4. № 2. - С. 5-9.
3. Демидов В. Н., Гус А. И. Современные принципы ультразвуковой диагностики генитального эндометриоза (в помощь практическому врачу) // Гинекология. - 2002. - Т. 4. № 2. -С. 48-52.
5. Поморцев А. В., Макухина Т. Б., Князев И. О., Платонов В. П. Допплерографические особенности аденомиоза // Ультразвуковая и функциональная диагностика. - 2003. - № 4. - С. 46-50.
6. Chen C. L., Liu P., Zeng B. L., Ma B., Zhang H. Intermediate and long term clinical effects of uterine arterial embolization in treatment of adenomyosis // Zhonghua Fu Chan Ke Za Zhi. - 2006. - Oct., № 41 (10). - P. 660-663.
7. Gaetje R., Scharl A, Kaufmann M., Ahr A. Management of abnormal uterine bleeding. // Zentralbl Gynakol. - 2006. - Aug., № 28 (4). - P. 196-201.
8. Hurskainen R. Managing drug-resistant essential menorrhagia without hysterectomy // Best Pract Res Clin Obstet Gynaecol. - 2006. - May, № 25; Epub ahead of print .
9. Jha R. C., Takahama J., Imaoka I., Korangy S. J., Spies J. B., Cooper C., Ascher S. M. Adenomyosis: MRI of the uterus treated with uterine artery embolization // Am J Roentgenol. - 2003. - Sep, № 181 (3). - P. 851-856.
10. Kim M. D., Kim S., Kim N. K., Lee M. H., Ahn E. H., Kim H. J., Cho J. H., Cha S. H. Long-term results of uterine artery embolization for symptomatic adenomyosis // Am J Roentgenol. - 2007. - Jan., № 188 (1). - P. 176-181.
11. Kim M. D., Won J. W., Lee D. Y., Ahn C. S. Uterine artery embolization for adenomyosis without fibroids // Clin Radiol. - 2004. -Jun., № 59 (6). - P. 520-526.
12. Kitamura Y., Allison S. J., Jha R. C., Spies J. B., Flick P. A., Ascher S. M. MRI of adenomyosis: changes with uterine artery embolization // Am J Roentgenol. - 2006. - Mar., № 186 (3). -P. 855-864.
13. Liu P., Chen C., Liu L., Liu J. Investigation of the hemodynamic changes during uterine arterial embolization in the treatment of adenomyosis // Zhonghua Fu Chan Ke Za Zhi. - 2002. - Sep., № 37 (9). - P. 536-538.
14. Lohle P. N., De Vries J., Klazen C. A., Boekkooi P. F., Vervest
H. A., Smeets A. J., Lampmann L. E., Kroencke T. J. Uterine artery embolization for symptomatic adenomyosis with or without uterine leiomyomas with the use of calibrated tris-acryl gelatin microspheres: midterm clinical and MR imaging follow-up // J Vasc Interv Radiol. -2007. - Jul., № 18 (7). - P. 835-841.
15. Pelage J. P., Jacob D., Fazel A., Namur J., Laurent A, Rymer R., Le Dref O. Midterm results of uterine artery embolization for symptomatic adenomyosis: initial experience // Radiology. - 2005. -Mar., № 234 (3). - P. 948-953. Epub 2005 Jan 28.
16. Rabinovici J., Stewart E. A. New interventional techniques for adenomyosis // Best Pract Res Clin Obstet Gynaecol. - 2006. - Aug., № 20 (4). - P. 617-636. Epub 2006 Aug 24.
17. Ravina J. H., Herbreteau D., Ciraru-Vigneron N., Bouret J. M., Houdart E., Aymard A, Merland J. J. Arterial embolisation to treat uterine myomata // Lancet. - 1995. - Sep 9. № 346 (8976). - P. 671-672.
18. Siskin Gary P., Tublin Mitchell E., Stainken Brian F., Dowling Kyran and Dolen Eric G. Uterine Artery Embolization for the Treatment of Adenomyosis. Clinical Response and Evaluation with MR Imaging // Am J Roentgenol. - 2001. - № 177. P. 297-330.
E. А. МЕРШИНА, E. С. ВАСИЛЬЕВА, В. E. СИНИЦЫН, В. К. ЛЯДОВ, В. Н. ЕГИЕВ
ВОЗМОЖНОСТИ ФУНКЦИОНАЛЬНОМ МРТ В ОЦЕНКЕ СПАЕЧНОЙ БОЛЕЗНИ ПОСЛЕ ПЛАСТИКИ ПЕРЕДНЕЙ БРЮШНОЙ СТЕНКИ
Россия, 125367, г. Москва, Иваньковское ш, 3.
E-mail: elena_mershina@mail.ru, keithy@yandex.ru, vsini@mail.ru, vlyadov@gmail.com
Целью исследования явилось определить роль магнитно-резонансной томографии в оценке спаечного процесса после пластики передней брюшной стенки. Было обследовано 8 пациентов после лапароскопической интраперитонеальной (5) и открытой (3) пластики передней брюшной стенки. Всем пациентам были проведены диагностическая МРТ и функциональная кино-МРТ с пробой Вальсальвы.
У всех лапароскопически прооперированных пациентов четко визуализировались синтетические сетки. После лапаро-томических операций синтетическая сетка не определялась, но были обнаружены спайки и послеоперационная грыжа. Наиболее часто определялись спайки с передней брюшной стенкой. Функциональная кино-МРТ - подающий надежды метод в оценке спаечного процесса и послеоперационных грыж после пластики передней брюшной стенки.
Ключевые слова: МРТ, грыжа, синтетическая сетка, спайки, висцеральное скольжение.
Кубанский научный медицинский вестник № 6 (120) 2010 УДК 616-079.2
Кубанский научный медицинский вестник № 6 (120) 2010
Е. A. MERSHINA, E. S. VASILYEVA, V. E. SINITSYN, V. K. LYADOV, V. N. EGHIEV
FUNCTIONAL CINE-MRI IN DETECTION OF ADHESIVE DISEASE FOLLOWING VENTRAL HERNIA REPAIR
Federal center of medicine and rehabilitation,
Russia, 125367, Moscow, Ivankovskoye highway, 3.
E-mail: elena_mershina@mail.ru, keithy@yandex.ru, vsini@mail.ru, vlyadov@gmail.com
The aim of this study was to evaluate the role of functional cine-MRI in detection of recurrent hernia and intraabdominal adhesions following ventral hernia repair. 8 patients were examined after intraperitoneal laparoscopic (5 pts) and open sub-lay repair (3 pts). All patients underwent diagnostic and functional cine-MRI with Valsalva test.
In all laparoscopy-patients the meshes were identified. After open surgery the mesh was not visualized, but a recurrent hernia and adhesions were found. The most common adhesions were to the ventral abdominal wall. Functional cine-MRI is a reliable technique for detecting adhesions and recurrent hernia after repair.
Key words: MRI, hernia, synthetic mesh, adhesions, visceral slide.
Необходимость укрепления передней брюшной стенки синтетическими материалами при грыжах передней брюшной стенки давно известна [5]. Внутрибрюш-ные спайки являются неспецифическим осложнением, связанным с предыдущими абдоминальными хирургическими вмешательствами. Возможность формирования спаек с синтетическим материалом, установленным во время пластики передней брюшной стенки, остается принципиальным вопросом [5]. Спайки - это основная причина механической кишечной непроходимости у взрослых [6]. Тонкокишечную непроходимость в 75% случаев связывают с наличием спаечного процесса в брюшной полости. Как правило, острые или хронические абдоминальные жалобы являются единственными симптомами, в то время как распространенность спаечного процесса не коррелирует с клиническими данными [1, 4]. Хотя многие пациенты со спаечным процессом в брюшной полости остаются асимптома-тичными [8]. Внутрибрюшные спайки состоят из фиброзных тяжей или фиброзно-жировой ткани. Спайки образуются между петлями кишечника или прикрепляются к париетальной брюшине, как правило к передней брюшной стенке, а также могут вовлекать органы, расположенные забрюшинно [7]. Почти у половины пациентов с жалобами на тазовые боли обнаруживается спаечная болезнь. Бесплодие связано с предыдущими хирургическими вмешательствами в 20-40% случаев. Наибольший уровень спаечного процесса ожидаем при повторных операциях. В случаях повторных оперативных вмешательств более 56% жалоб связано со спайками. Спаечная болезнь является причиной 40-75% повторных операций по поводу кишечной непроходимости. Некоторые авторы утверждают, что наличие спаек является относительным противопоказанием к проведению лапароскопической операции [1, 3]. Следовательно, корректное диагностирование наличия и места расположения спаечного процесса является важным аспектом при установлении показаний, а также в планировании оперативного лечения [3]. Ультразвуковое исследование в реальном времени может использоваться для отображения движения органов брюшной полости относительно передней брюшной стенки. Спайки с передней брюшной стенкой ограничивают скольжение органов, которое можно обнаружить при помощи этой методики [2, 7]. Ультразвуковое исследо-
вание наиболее полезно при сопровождении установки троакаров во время лапароскопических операций [6]. Кроме того, давление от руки оператора на датчик, находящийся на передней брюшной стенке, может помешать разъединению соседних петель кишечника. Хотя ультразвуковое исследование является хорошим методом при оценке спаек с передней брюшной стенкой, на сегодняшний день не существует метода, принятого для оценки спаечного процесса, вовлекающего органы брюшной полости.
Таким образом, целью нашего исследования явилось определить роль функциональной магнитно-резонансной томографии (МРТ) в оценке спаечного процесса после пластики передней брюшной стенки.
Материалы и методы
Было обследовано 8 пациентов (5 мужчин и 3 женщины, возраст 37-72 года, средний возраст - 55,8 года) после лапароскопической интраперитонеальной пластики передней брюшной стенки синтетическими протезами (5 случаев) и после открытой пластики передней брюшной стенки (3 случая). Обследование проводилось через 9-12 месяцев после операции.
МРТ выполнялась на томографе с напряженностью магнитного поля 1,5Т (АуапЬо, Siemens). Всем пациентам были проведены диагностическая МРТ органов брюшной полости и функциональная МРТ в кинорежиме с пробой Вальсальвы. Стандартный протокол диагностического исследования включал получение изображений в режиме ТгиеР^Р (ТКиР1) в корональной плоскости, Т1- и Т2-взвешенные изображения, Т1-взве-шенные изображения с подавлением сигнала от жира в аксиальной плоскости. Для функциональной МРТ была использована односрезовая последовательность ТгиеР^Р (ТКТЕ/РА = 5,8 мсек./2,5 мсек./70°; РоУ -400 мм; толщина среза - 5 мм). Одна кинопетля состояла из 10 последовательно получаемых изображений на одном уровне. Время получения 1 изображения составляло 1,3 сек. Во время исследования пациента просили натуживаться и впоследствии расслабляться, добиваясь таким образом увеличения внутрибрюшного давления. Были получены поперечные (в краниокаудальном направлении) и сагиттальные (слева направо) функциональные МР-изображения всей брюшной полости. Расстояние между срезами (кинопетлями) составило 15 мм. В зависимости от конституционального типа пациента
Рис. 1. Карта брюшной полости, состоящая из 9 сегментов 35%--------------------------33,30%---------------------------
Читайте также:


