Диагностика осложнений клипирования аневризм мозга. Профилактика
Добавил пользователь Дмитрий К. Обновлено: 28.01.2026
Аневризма сосудов головного мозга является локальным выпячиванием артериальных стенок. Заболевание нередко протекает без симптомов. По мере увеличения аневризмы головного мозга происходит значительное истончение стенок образования, что может привести к его разрыву и развитию геморрагического инсульта.
В зависимости от формы аневризма сосудов головного мозга может быть веретенообразной и мешотчатой. Установить точный тип заболевания можно только во время комплексной диагностики. Мешотчатая аневризма встречается намного чаще.
Причины заболевания
Аневризма является опасным состоянием, требующим в первую очередь оперативного лечения. В противном случае не удастся избежать осложнений. Специалисты считают, что болезнь является следствием аномалий развития, которые нарушают строение сосудистой стенки. Нередко аневризма головного мозга сочетается вместе с дисплазией соединительной ткани, поликистозом почек, сосудистыми нарушениями. Приобретенная форма заболевания может стать следствием черепно-мозговой травмы. Также аневризма головного мозга встречается на фоне атеросклероза, гипертонической болезни.
Сам по себе дефект сосудистой стенки возникает постепенно. На фоне дегенеративных процессов, повреждения тканей или их недоразвития участок утрачивает прежнюю эластичность. Под давлением тока крови сосудистая стенка начинает выпячиваться. Так образуется аневризма головного мозга. Чаще всего образование встречается в месте, где разветвляются артерии и наблюдается наиболее сильное давление на стенку сосуда.
Симптомы аневризмы
Можно выделить два варианты течения заболевания: апоплексическое и опухолеподобное. От разновидностей аневризмы зависят особенности клинической картины. Опухолевидная форма заболевания сопровождается активным течением. За короткий срок аневризма увеличивается в размере, сдавливает важные анатомические образования мозга.
Опухолеподобная аневризма чаще всего локализуется в области кавернозного синуса или хиазмы. При поражении хиазмальной области снижается острота зрения. При длительном течении возникает атрофия зрительного нерва. Если аневризма сосудов мозга находится в кавернозном синусе, возникает парез, поражение ветвей тройничного нерва. По мере развития патологии возникают глазодвигательные нарушения, может появляться косоглазие.
Признаки разрыва аневризмы
Резкая головная боль является первым симптомом разрыва аневризмы. Болевой синдром сначала имеет локальный характер. Но очень быстро головная боль распространяется и становится диффузной. При этом пациенты отмечают появление тошноты и повторяющейся рвоты.
В дальнейшем возникают характерные менингеальные симптомы:
- ригидность мышц затылка;
- симптомы Кернига и Брудзинского;
- потеря сознания.
При разрыве аневризмы сосудов головного мозга возникает субарахноидальное кровоизлияние. Она может сопровождаться очаговыми симптомами, которые зависят от места локализации образования. Наиболее тяжелым является кровоизлияние в желудочки, которое часто приводит к смерти больного.
При аневризме передней мозговой артерии развивается парез ног, который нередко сочетается с психическими нарушениями. Поражение средней мозговой артерии приводит к нарушениям речи, развитию гемипареза.
Если патология локализуется в области вертебробазилярной системы, во время разрыва аневризмы возникают нарушения глотания, развивается нистагм в сочетании с центральным парезом лица и тройничного нерва.
При первых признаках возможного появления аневризмы необходимо сразу обращаться за срочной медицинской помощью. Важно сохранять физический покой, избегать перенапряжения. Специалисты проведут осмотр, диагностику, поставят точный диагноз, назначат необходимые препараты для сокращения риска появления опасных для жизни осложнений.
Как диагностируют
Так как аневризма артерии может протекать без выраженных симптомов, необходимо обращать особое внимание на первые признаки у женщин и мужчин. Диагностировать заболевание должен невролог на основании проведенного осмотра, полученных результатов диагностики и изучения цереброспинальной жидкости.
Во время неврологического осмотра выявляют очаговые и менингеальные симптомы. По месту локализации жалоб можно определить предположительно, где находится патологический очаг.
Точную информацию о состоянии пациента невролог получает с помощью следующих исследований:
- Рентгенография черепа. Для аневризмы головного мозга характерны признаки деструкции костных тканей.
- Компьютерная томография, магнитно-резонансная томография головного мозга.
- Ангиография. Можно получить основную информацию о расположении, форме и размере аневризмы мозга.
- Люмбальная пункция. Исследование позволяет обнаружить кровь в цереброспинальной жидкости, что свидетельствует о наличии кровоизлияния.
Специалисты проводят дифференциальную диагностику аневризмы сосудов головного мозга. Важно поставить точный диагноз в короткие сроки. Это позволит избежать неблагоприятных последствий аневризмы мозга. Дифференцировать аневризму необходимо от опухолевидных процессов, кист и абсцессов.
Принципы лечения
Лечение аневризмы проводит невролог. Операцию осуществляет только нейрохирург. Хирургические методы направлены в первую очередь на профилактику разрыва аневризмы, которое может закончиться гибелью пациента. Консервативная терапия при данной патологии используется для замедления развития болезни.
Оперативное лечение аневризмы головного мозга предполагает проведение два типа основных операций: клипирования и эндоваскулярной окклюзии. Хирургическое вмешательство предупреждает разрыв аневризмы. Радикальным методом лечения является удаление артериовенозной мальформации во время проведения микрохирургической операции.
Клипирование аневризмы
Клипирование аневризмы является открытой операцией, во время которой нейрохирург блокирует кровоток в определенном участке сосуда и накладывает клипсу. На этапе подготовки к операции специалисты назначают процедуру, которые позволяют стабилизировать состояние пациента и минимизировать риск появления возможных осложнений. Профилактическое обследование дает возможность выявить возможные нарушения и заболевания, которые могут привести к неблагоприятным последствиям хирургического вмешательства.
Операцию проводят с использованием современной микрохирургической техники, через небольшое трепанационное отверстие. Во время хирургического вмешательства нейрохирург проводит профилактику разрыва стенки мальформации.
После выделения шейки аневризмы специалист накладывает на нее клипсу. Дополнительный контроль допплерографией позволяет оценить состояние кровотока и убедиться в эффективности проводимой операции.
Лечение аневризмы методом клипирования считается достаточно сложным и должно выполняться только опытным нейрохирургом. Квалифицированный специалист сделает все возможное для аккуратного и технически правильного наложения клипсы. В противном случае не избежать опасных осложнений и длительного реабилитационного периода.
Клипсу накладывают на шейку аневризмы сосуда. Точность действий нейрохирурга подтверждается проведением во время процедуры качественной диагностики (допплерография).
Эндоваскулярная окклюзия
Во время эндоваскулярной окклюзии аневризмы нейрохирург проводит блокировку просвета расширенного сосуда специальным имплантом. Операция применяется при невозможности провести клипирование, например, когда аневризма имеет веретенообразную форму. Во время хирургического вмешательства через бедренную артерию потом ангиграфическим контролем специалист вводит баллон-катетер. Он закрывает просвет аневризмы. Также можно использовать микроспираль для проведения тромбирования. Выбор остается за лечащим врачом. Микроспираль в полости пораженного сосудистого участка образует тромбы, которые закупоривают просвет сосуда и выключают аневризмы из кровообращения.
Реабилитация после оперативного лечения аневризмы
Реабилитационный период проходит под контролем специалистов. Профессионалы делают все необходимое для профилактики появления послеоперационных осложнений. В реанимационном отделении пациент находится несколько суток под постоянным контролем специалистов. После больного переводят в общую палату, где некоторое время необходимо соблюдать строгий постельный режим. Возвращение к привычному образу жизни происходит постепенно.
При ухудшении самочувствия больного после хирургического вмешательства возможно назначение транскраниальной допплерографии. Реабилитация направлена в первую очередь на профилактику ангиоспазма и повышения артериального давления. Также специалисты следят за общим состоянием сердечно-сосудистой системы, при необходимости назначают осмодиуретики для устранения отека мозговой ткани. Дополнительно проводится противовоспалительная терапия.
Реабилитация после оперативного лечения аневризмы обязательно включает проведение программы для восстановления нарушенных функций организма и дальнейшей социализации пациента. Срок восстановительного периода продолжается не менее 6 месяцев. С помощью качественной реабилитации можно в том числе устранить неблагоприятные последствия хирургического лечения.
Реабилитационные мероприятия включают проведение физиотерапии, массажа, реализацию индивидуально подобранной восстановительной программы. После проведения клипирования эндоскопическим способом к привычной жизни пациент может вернуться уже через несколько недель.
Возможные осложнения операции
Оперативное лечение аневризмы сосудов мозга является единственным и оправданным методом предупреждения опасных внутричерепных кровоизлияний. При высокой квалификации нейрохирурга риск появления серьезных осложнений достаточно низкий. В 30% случаев остаются умеренные двигательные ограничения, периодически возникающие головные боли, нарушения речи. Восстановить нарушенные функции можно с помощью специальных тренировок, занятий с логопедом, психологом.
Прогноз для жизни
Прогноз заболевания зависит от места локализации сосудистого выпячивания и его размеров. Также огромное влияние оказывает первоначальное состояние пациента. Смертность в случае разрыва аневризмы мозга превышает 30-50%. У выживших пациентов иногда остаются последствия перенесенного состояния в виде ограничений движения, нарушения когнитивных функций и значительного снижения качества жизни. Летальность после повторного кровоизлияния превышает 70%.
Поэтому так важно во время проводить оперативное лечение, обращаясь к квалифицированному нейрохирургу. Операцию откладывают только при наличии определенных медицинских показаний.
Успешные нейрохирургические операции проводят в НИИ Бурденко. Здесь принимают пациентов с признаками аневризмы, подозрением на ее появление. В институте нейрохирургии можно провести комплексную диагностику с использованием новейшей техники и дальнейшее лечение выявленных заболеваний.
Консультация нейрохируга

Гаврилов Антон Григорьевич
Нейрохирург, доктор медицинских наук, профессор
— Нейрохирург 9 отделения НИИ нейрохирургии им. Н.Н.Бурденко (2002 — 2019)
— Ведущий нейрохирург сети клиник «Медси» (2019 — н.в.)
Я не занимаюсь радиохирургией, эндоваскулярной нейрохирургией и лечением аневризмы вены Галена.
Задать вопрос нейрохирургу
По предварительной записи, я могу принять вас на очную консультацию.
Диагностика осложнений клипирования аневризм мозга. Профилактика
Диагностика ретракционных изменений мозга. Профилактика
Диагностика ретракционных изменений возможна при помощи КТ, МРТ, ПЭТ и ЦАТ (при ЦАТ оценивается кровоток в венозной фазе исследования). При верификации ретракционных изменений по данным КТ и МРТ необходима её дифференциация с ишемией мозга в результате ангиоспазма, временное клипирование церебральных артерий и компрессии перфорирующих ветвей. В пользу ретракционных изменений свидетельствуют следующие признаки: очаги отека-ишемии преимущественно имеют геморрагическое пропитывание, располагаются в проекции хирургического доступа и по форме могут соответствовать наконечнику шпателя. По нашим данным, которые согласуются с мнением Е Proust и соавт., спустя 2-3 недели верификация ретракционных изменений при помощи КТ затруднена — в эти сроки очаги ретракционных изменений подвергаются обратному развитию.
R. P. Kivissaari и соавт. (2000 г.) показали, что очаги кистозно-атрофических изменений лобной и височной долей головного мозга в местах давления шпателей выявляются в ряде наблюдений при МРТ в отдаленные сроки после операции спустя 2—6 лет. Авторы обращают внимание, что у этих больных очаги ретракционных изменений не были выявлены при КТ головного мозга, проведенной сразу после хирургического вмешательства и через 3 месяца.
Профилактика ретракционных изменений осуществляется анестезиологическими, хирургическими методами, а также при помощи мониторинга давления шпателей, ЛМК, ДВП и ССВП. Анестезиологические методы, направленные на уменьшение отека мозга и увеличение его толерантности к гипоксии, включают применение маннитола, фармакологический защиты мозга (барбитураты, пропофол, изофлюран, этамидат) и гипотермии. О пользе применения нимодипина и кортикостероидов данные противоречивы. R. J. Andrews и соавт. в качестве меры профилактики ретракционных изменений рассматривают индуцированную артериальную гипертензию во время ретракции мозга, по аналогии со способом профилактики инфаркта мозга во время временного клипирования. Однако и R. P. Kivisaari и соавт. (2000 г.), и мы в собственном исследовании не обнаружили корреляции частоты ретракционных изменений с уровнем АД во время хирургических вмешательств.
Хирургические методы профилактики включают выбор хирургического доступа и объема операции, методики ретракции мозга, и применение методов релаксации мозга. Принцип проведения операций по поводу аневризм с минимальной ретракцией мозга, необходимой только для клипирования аневризмы, является основополагающим.
Уменьшению ретракционного давления способствует выбор хирургического доступа соответственно локализации аневризмы. Учитывая риск ретракционных изменений при подходе к аневризмам базилярной артерии, в качестве альтернативы субфронтального доступа для уменьшения ретракционного давления были предложены транссильвиев, темпорополярный, комбинированный транссильвиев субтемпоральный и краниоорбитальные доступы (В. В. Крылов и соавт., S. Anegawa et al., R. R. Smith et al., R. С Heros, S. H. Lee, T. A. Kopitnik et al.).
При аневризмах средней мозговой артерии (СМА) и длинном М1-сегменте артерии или формировании внутримозговой гематомы для уменьшения ретракционного давления рекомендовано применение транстемпорального доступа. По сравнению с традиционным при данной локализации аневризм транссильвиевым подходом транстемпоральный доступ обеспечивает меньшее ретракционное давление и более легкое выделение аневризм задней стенки СМА (R. С. Heros). При аневризмах М2-МЗ сегментов артерии для профилактики ретракционных изменений предпочтителен ретроградный транссильвиев доступ (S. Nagasawa et al., М. A. Stoodley et al.).
Бифронтальный межполушарный доступ к аневризмам ПСА по сравнению с боковыми доступами позволяет снизить ретракционное давление при подходе к аневризме в 2 раза (Z. Ito). Однако при межполушарном подходе есть риск повреждения соединительных (мостиковых) лобных вен, которое влечет за собой нарушение венозного оттока и в ряде наблюдений ведет к венозному инфаркту мозга, клинически проявляющемуся грубыми неврологическими выпадениями (Y. Kurokawa et al.).
По сравнению с традиционными хирургическими доступами к сосудам основания мозга преимуществом меньшей травматичности и ретракционного воздействия на мозг обладают ограниченные краниобазальные подходы (Т. Fukushima et al., A.J. Keogh et al., K. Kikuchi, K.Watanabe, E. van Lindertetal). Однако, по мнению К. Kikuchi и К. Watanabe, выполнение ограниченных доступов показано только пациентам, находящимся в компенсированном состоянии (I-II степень тяжести по шкале Hunt-Kosnik), при отсутствии у них распространенного субарахноидального кровоизлияния по данным КТ.
Уменьшению ретракции мозга способствует укладка больного с приподнятым концом операционного стола и запрокидыванием головы пациента для дополнительного отведения мозга под действием силы гравитации.
Установка поясничного дренажа, вентрикулярное дренирование либо вентрикулоцистерностомия позволяют уменьшить напряжение мозга и снизить ретракционное давление шпателей на 25—75% (N. Andaluz, М. Zuccarelo). При проведении операции из птерионального доступа на фоне отечного мозга для получения минимально достаточного пространства для подхода к аневризмам переднего отдела артериального круга большого мозга может потребоваться выведение по поясничному дренажу 60—70 мл ЦСЖ, при аневризмах развилки базилярной артерии — 120 мл и более. Необходимо учитывать риск гипердренирования ЦСЖ, которое может приводить к дислокации мозга, натяжению и разрыву парасинусных вен и формированию субдуральных гематом или венозного инфаркта мозга на отдалении от хирургического доступа. Однако следует учитывать, что быстрая релаксация мозга может стать причиной внеконтактного разрыва аневризмы (J. P. Mustaki et al., Е. S. Jr. Connolly et al.).
Успешное применение методов профилактики ретракционных изменений демонстрируют данные А. Р. Lozier и соавт.. Операции по поводу аневризм развилки базилярной артерии были выполнены у 98 больных в условиях умеренной гипотермии, на фоне релаксации мозга путем выведения ЦСЖ через поясничный дренаж и внутривенного введения 20% раствора маннитола. У 18 пациентов во время операции была выполнена остановка кровообращения на фоне нейропротекции барбитуратами. Частота ретракционных изменений составила 2%.
Для ранней диагностики ретракционных изменений рассматривается возможность использования методов регистрации давления шпателя, ЛМК и вызванных потенциалов мозга. А. Ю. Лубниным и соавт. было установлено, что проведение операций с использованием датчика измерения давления, прикрепленного к шпателю, позволяет хирургу контролировать ретракционное давление в безопасных пределах — до 20 мм рт.ст. В этой серии наблюдений РИ удалось избежать у всех больных.
R.J. Andrews и соавт. предполагают эффективным мониторинг ЛМК как одного из ключевых факторов патогенеза ретракционных изменений, определяющих развитие повреждения мозговой ткани. Метод регистрации ССВП и ДВП доказал свою эффективность в диагностике ишемии мозга во время операции по поводу аневризм с применением временного клипирования артерий мозга и, очевидно, может быть также использован для профилактики ишемии мозга во время его ретракции. Высокая чувствительность метода может позволить выявлять признаки ишемии мозга, развивающейся под действием ретракционного давления, на ранних (обратимых) стадиях, и выбирать оптимальную силу и методику ретракции.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Визуальный осмотр аневризмы и окружающих ее сосудов после клипирования через микроскоп и с использованием нейрохирургического зеркальца зачастую не дает надежной информации об отсутствии осложнений клипирования аневризм мозга.
Для интраоперационной диагностики осложнений клипирования аневризм мозга применяют методы ангиографии, контактной допплерографии, эндоскопической ассистенции и регистрации вызванных потенциалов мозга. После операции верифицировать осложнения клипирования аневризм мозга возможно при помощи церебральной ангиографии.
Ангиография признана «золотым стандартом» в диагностике осложнений клипирования аневризм мозга. Существенным недостатком метода является риск тромбоза сосудов и ишемических осложнений, частота которых колеблется от 1,7 до 2,9%. Частота ложноотрицательного результата ангиографии, когда метод не позволяет выявить осложнения клипирования аневризм мозга, достигает 5%.
Контактная допплерография позволяет с высокой чувствительностью выявлять стеноз несущей аневризму артерии, её перфорирующих ветвей и остаточный кровоток в аневризме, свидетельствующий о неполном её клипировании. Преимуществами метода являются быстрота выполнения (3—7 минут) и отсутствие осложнений. К недостаткам допплерографии можно отнести отсутствие возможности диагностировать неклипированную пришеечную часть аневризмы и возможность получения ложноотрицательного результата.
Видеоэндоскопическая ассистенция (ВЭСА) является методом дополнительной визуализации аневризмы и окружающих её структур. G. Profeta и соавт. (2004 г.) и Т. Menovsky и соавт. (1999 г.) считают ВЭСА абсолютно необходимой в хирургии больших и сложных аневризм. Эндоскопическая ассистенция позволяет оперировать на аневризмах, недоступных осмотру в микроскоп, без дополнительной резекции костных образований основания черепа и рассечения намета мозжечка, а также проводить арахноидальную диссекцию в меньшем объеме при меньшей ретракции головного мозга.
Наше мнение совпадает с мнением некоторых авторов, которые признают, что эндоскопический осмотр аневризмы имеет определенные преимущества перед осмотром через микроскоп, так как дает возможность оценить особенности микроанатомии под большим увеличением и при большей интенсивности освещения, особенно если аневризма закрыта стволом несущей ее артерии или костными образованиями основания черепа, либо имеет труднодоступную локализацию (расположена в бассейне БА или в контралатеральном полушарии мозга).
При отсутствии методов интраоперационной диагностики осложнений клипирования аневризм мозга могут быть использованы рекомендации Т.М. Sundt и соавт. (1982 г.), которые считают, что анестезиологическое обеспечение операции должно позволять сразу по окончании операции разбудить больного и произвести оценку неврологических функций.
При наличии неврологического дефицита следует выполнить экстренную церебральную ангиографию и, если выявляются признаки окклюзии крупных ветвей артерий артериального круга большого мозга, — производить экстренную повторную операцию с целью ревизии аневризмы и положения клипса. Эффективность подобной тактики авторы подтверждают на собственных наблюдениях. У двух больных, оперированных по поводу аневризм ВСА, сразу после хирургического вмешательства был выявлен контралатеральный гемипарез, при экстренной ангиографии выявлена окклюзия ПВА.
Хотя этим больным повторные операции и ликвидация окклюзии ПВА были выполнены в течение 12 часов с момента первого вмешательства, неврологические функции в обоих наблюдениях были восстановлены полностью.
Профилактика осложнений клипирования аневризм мозга
Кальцинация шейки аневризмы может быть диагностирована при КТ головного мозга. Однако кальцинированная бляшка может быть затушевана гиперинтенсивными сигналами от крови из окружающих субарахноидальных цистерн. МРТ, при помощи которой часто осуществляется диагностика у больных с неразорвавшимися аневризмами, для верификации кальцинатов на шейке аневризмы неэффективна.
Признаки кальцинации шейки аневризмы часто выявляют у пожилых пациентов. При наличии толстой пришеечной атеросклеротической бляшки М.Т. Lawton и соавт. рекомендуют эндоваскулярное выключение аневризмы.
N. Kodama и соавт. для лучшей сепарации окружающих аневризму артерий и предотвращения их компрессии или повреждения во время клипирования аневризмы использовали фрагменты хирургической оксицеллюлозы, которыми окутывали окружающие сосуды. Недостатком методики являются сокращение пространства между сосудами и аневризмой и затруднение клипирования аневризмы при наличии вокруг нее более чем двух перфорирующих ветвей.
Для тех же целей на этапах выделения и клипирования аневризмы используют небольшого размера кусочки перчаточной резины, которые помещают между стенкой аневризмы и перфорирующими артериями, исключая их слипание и попадание артерий между браншами клипсы. Благодаря этом клипирование аневризмы становится более простой и безопасной процедурой (S. Kashiwagi et al.).
Факторы риска осложнений клипирования аневризм мозга. Частота
К осложнениям, связанным с клипированием аневризмы (ОКА), относят неполное клипирование аневризмы, повреждение и окклюзию магистральных и перфорирующих артерий мозга.
По данным контактной допплерографии, неполное клипирование аневризмы выявляют в 3,7-12,2% случаев, а стеноз сосудов клипсом - в 11,0-31,0%; по данным интра- и послеоперационной ангиографии неполное клипирование аневризмы диагностируют в 1-19% случаев, а стеноз сосудов мозга клипсом — в 5,7-12%. Осложнения клипирования аневризмы при помощи видеоэндоскопической ассистенции диагностируют в 4-12,7% случаев. В наших наблюдениях осложнения клипирования аневризмы при помощи видеоэндоскопической ассистенции были установлены у 5% больных.
Проявления осложнений клипирования аневризм мозга. После неполного клипирования или эмболизации аневризмы в ней сохраняются кровоток и пульсовое АД. Ежегодный риск повторного субарахноидального кровоизлияния из неполностью выключенной из кровотока аневризмы составляет 0,14-0,5%.
Повреждение или компрессия перфорирующих артерий проявляются неврологическим дефицитом, соответствующим бассейну их кровоснабжения. По мнению некоторых авторов, повреждение перфорирующих артерий в хирургии аневризм является наиболее частым интраоперационным осложнением, приводящим к инвалидизации больных.
Факторы риска осложнений клипирования аневризм мозга. Среди факторов риска осложнений клипирования аневризм мозга выделяют размер, локализацию аневризмы, атеросклеротическое поражение стенок артерий и шейки аневризмы и перенесенное субарахноидальное кровоизлияние.
В исследовании Т.М. Jr. Sundt и соавт. было установлено, что операции по поводу аневризм диаметром более 10 мм чаще сопровождаются повреждением и ятрогенной окклюзией магистральных и перфорирующих артерий головного мозга. В наблюдениях S. Kashiwagi и соавт. повреждение перфорирующих артерий происходило исключительно во время операций по поводу гигантских аневризм.
По данным некоторых авторов, осложнения клипирования аневризм мозга наиболее часто встречаются при аневризмах срединной линии — развилки БА, ПСА, офтальмического сегмента ВСА и ЗСА. Частота осложнений клипирования аневризм мозга развилки БА достигает 6—19%. Однако по данным Т. М. Jr. Sundt и соавт. и R. Stendel и соавт., окклюзия магистральных церебральных артерий чаще регистрируется после операций по поводу аневризм СМА из-за особенностей микроанатомии самой артерии, ее ветвей и формы аневризм. После же операций по поводу аневризм ВСА и БА чаще отмечают повреждение перфорирующих артерий мозга.
Среди причин неполного выключения аневризмы из кровотока также выделяют поражение шейки аневризмы кальцинированной атеросклеротической бляшкой и атеросклеро-тические изменения стенки несущей аневризму артерии, препятствующие полному смыканию браншей клипсов.
R. Stendel и соавт. было обнаружено более частое возникновение осложнений клипирования артерий у больных, перенесших субарахноидальное кровоизлияние. Авторы объясняют это трудностями выполнения арахноидальной диссекции после перенесенного кровоизлияния и более частым возникновением у этих больных интраоперационного отека мозга, затрудняющего доступ к аневризме.
Аневризмы сосудов головного мозга ( Церебральная аневризма )
Аневризмы сосудов головного мозга — это патологические локальные выпячивания стенок артериальных сосудов мозга. При опухолеподобном течении аневризма сосудов головного мозга имитирует клинику объемного образования с поражением зрительного, тройничного и глазодвигательных нервов. При апоплексическом течении аневризма сосудов головного мозга проявляется симптомами субарахноидального или внутримозгового кровоизлияния, внезапно возникающими в результате ее разрыва. Аневризма сосудов головного мозга диагностируется на основании данных анамнеза, неврологического осмотра, рентгенографии черепа, исследования цереброспинальной жидкости, КТ, МРТ и МРА головного мозга. При наличии показаний аневризма сосудов головного мозга подлежит хирургическому лечению: эндоваскулярной окклюзии или клипированию.
МКБ-10
Общие сведения
По некоторым данным, аневризма сосудов головного мозга имеется у 5% населения. Однако зачастую она протекает бессимптомно. Увеличение аневризматического расширения сопровождается истончением его стенок и может привести к разрыву аневризмы и геморрагическому инсульту. Аневризма имеет шейку, тело и купол. Шейка подобно стенке сосуда характеризуется трехслойным строением. Купол состоит только из интимы и является наиболее слабым местом, в котором аневризма сосудов головного мозга может разорваться. Наиболее часто разрыв наблюдается у пациентов в возрасте 30-50 лет. По данным статистики именно разорвавшаяся аневризма обуславливает до 85% нетравматических субарахноидальных кровоизлияний (САК).
Причины аневризмы
Врожденное выпячивание сосудов головного мозга является следствием аномалий развития, приводящих к нарушению нормального анатомического строения их стенки. Оно часто сочетается с другой врожденной патологией: поликистозом почек, коарктацией аорты, дисплазией соединительной ткани, артериовенозной мальформацией головного мозга и т. п.
Приобретенная аневризма сосудов головного мозга может развиться в результате изменений, происходящих в стенке сосуда после перенесенной черепно-мозговой травмы, на фоне гипертонической болезни, при атеросклерозе и гиалинозе сосудов. В отдельных случаях она бывает вызвана заносом в мозговые артерии инфекционных эмболов. Такая аневризма в современной неврологии носит название микотической. Формированию патологии способствуют такие гемодинамические факторы, как неравномерность кровотока и артериальная гипертензия.
Патогенез
Аневризма сосудов головного мозга является следствием изменения в строении сосудистой стенки, которая в норме имеет 3 слоя: внутренний — интиму, мышечный слой и наружный — адвентицию. Дегенеративные изменения, недоразвитие или повреждение одного или нескольких слоев сосудистой стенки приводят к истончению и потере эластичности пораженного участка стенки сосуда. В результате в ослабленном месте под давлением тока крови происходит выпячивание сосудистой стенки, образуется аневризма. Наиболее часто выпячивание локализуется в местах разветвления артерий, поскольку там оказываемое на стенку сосуда давление наиболее высоко.
Классификация
По своей форме аневризма сосудов головного мозга бывает мешотчатая и веретенообразная. Причем первые встречаются намного чаще, в соотношении примерно 50:1. В свою очередь мешотчатая форма может быть одно- или многокамерной. По локализации выделяют аневризму передней мозговой артерии, средней мозговой артерии, внутренней сонной артерии и вертебро-базилярной системы. В 13% случаях наблюдаются множественные аневризмы, располагающиеся на нескольких артериях. Существует также классификация по величине. Согласно ей выделяют аневризмы :
- милиарные - размером до 3 мм
- малые — до 10 мм
- средние — 11-15 мм
- большие — 16-25 мм
- гигантские — более 25 мм.

Симптомы церебральной аневризмы
По своим клиническим проявлениям патология может иметь опухолеподобное или апоплексическое течение. При опухолеподобном варианте аневризма сосудов головного мозга прогрессивно увеличивается и, достигая значительных размеров, начинает сдавливать расположенные рядом с ней анатомические образования головного мозга, что приводит к появлению соответствующих клинических симптомов. Опухолеподобная форма характеризуется клинической картиной внутричерепной опухоли. Наиболее часто выявляется в области зрительного перекреста (хиазмы) и в кавернозном синусе.
Аномалия сосудов хиазмальной области сопровождается нарушениями остроты и полей зрения; при длительном существовании может привести к атрофии зрительного нерва. Аневризма сосудов головного мозга, располагающаяся в кавернозном синусе, может сопровождаться одним из трех синдромов кавернозного синуса, представляющих собой сочетание пареза III, IV и VI пары ЧМН с поражением различных ветвей тройничного нерва. Парез III, IV и VI пары клинически проявляется глазодвигательными нарушениями (ослаблением или невозможностью конвергенции, развитием косоглазия); поражение тройничного нерва — симптомами тройничной невралгии. Длительно существующая может сопровождаться деструкцией костей черепа, выявляемой при проведении рентгенографии.
Зачастую заболевание имеет апоплексическое течение с внезапным появлением клинических симптомов в результате разрыва аневризмы. Лишь изредка разрыву аневризмы предшествуют головные боли в лобно-глазничной области.
Разрыв аневризмы
Первым симптомом разрыва является внезапная очень интенсивная головная боль. Вначале она может носить локальный характер, соответствующий месту расположения аневризмы, затем становится диффузной. Головная боль сопровождается тошнотой и многократно повторяющейся рвотой. Возникают менингеальные симптомы: гиперестезия, ригидность затылочных мышц, симптомы Брудзинского и Кернига. Затем происходит потеря сознания, которая может длиться различный период времени. Могут наблюдаться эпилептиформные приступы и психические расстройства от небольшой спутанности сознания до психозов. Субарахноидальное кровоизлияние, возникающее при разрыве аневризматического расширения, сопровождается длительным спазмом расположенных вблизи аневризмы артерий. Примерно в 65% случаев этот сосудистый спазм приводит к поражению вещества головного мозга по типу ишемического инсульта.
Помимо субарахноидального кровоизлияния разорвавшаяся аневризма сосудов головного мозга может вызвать кровоизлияние в вещество или желудочки головного мозга. Внутримозговая гематома наблюдается в 22% случаев разрыва. Кроме общемозговой симптоматики она проявляется нарастающей очаговой симптоматикой, зависящей от локализации гематомы. В 14% случаев разорвавшаяся аневризма становиться причиной кровоизлияния в желудочки. Это наиболее тяжелый вариант развития заболевания, часто приводящий к летальному исходу.
Возникающая при разрыве очаговая симптоматика может носить разнообразный характер и зависит от места локализации аневризмы. При расположеннаи в области бифуркации сонной артерии возникают расстройства зрительной функции. Поражение передней мозговой артерии сопровождается парезами нижних конечностей и психическими нарушениями, средней мозговой — гемипарезом на противоположной стороне и нарушениями речи. Локализующаяся в вертебро-базилярной системе аневризма при разрыве характеризуется дисфагией, дизартрией, нистагмом, атаксией, альтернирующими синдромами, центральным парезом лицевого нерва и поражением тройничного нерва. Выпячивание сосудов головного мозга, расположенное в кавернозном синусе, находится за пределами твердой мозговой оболочки и поэтому ее разрыв не сопровождается кровоизлиянием в полость черепа.
Диагностика
Достаточно часто заболевание характеризуется бессимптомным течением и может быть выявлена случайным образом при обследовании пациента в связи с совершенно другой патологией. При развитии клинических симптомов диагностика осуществляется неврологом на основании данных анамнеза, неврологического осмотра пациента, рентгенологических и томографических обследований, исследования цереброспинальной жидкости.
Неврологический осмотр позволяет выявить менингеальные и очаговые симптомы, на основании которых можно поставить топический диагноз, т. е. определить место локализации патологического процесса. Интсрументальная диагностика включает:
- Рентгенографию. Рентгенография черепа помогает обнаружить петрифицированные аневризмы и деструкцию костей основания черепа. Более точную диагностику дает проведение КТ и МРТ головного мозга.
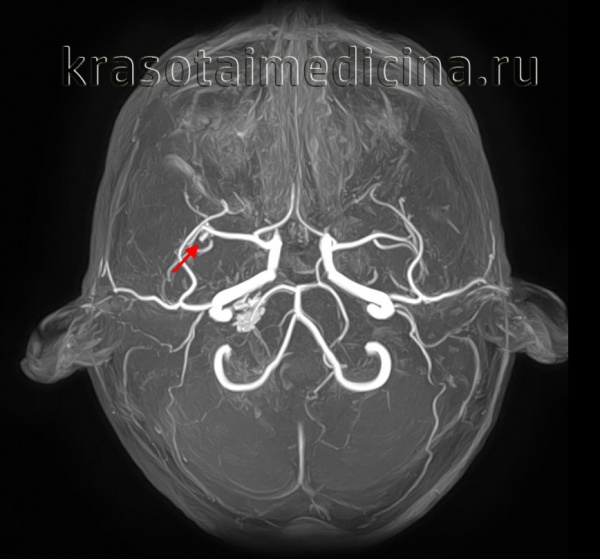
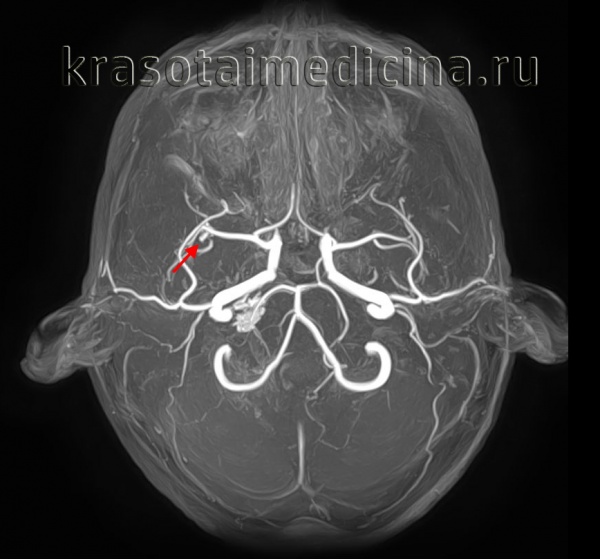
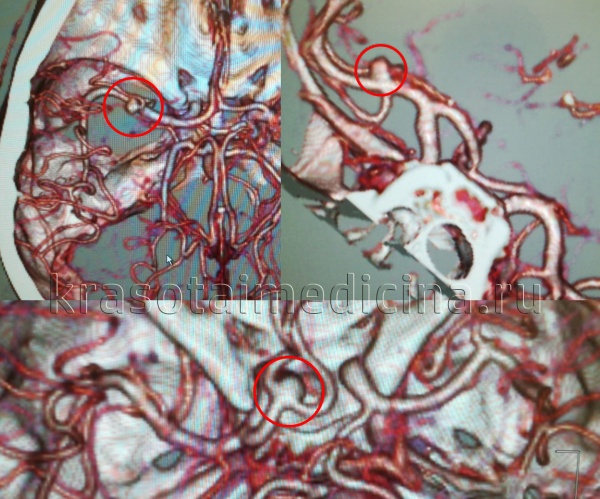
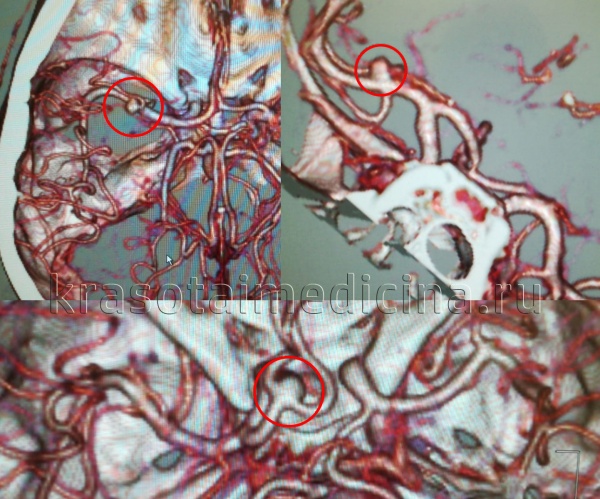
- Ангиографию. Церебральная ангиография позволяет установить расположение, форму и размеры аневризмы. В отличие от рентгенологической ангиографии магнитно-резонансная (МРА) не требует введения контрастных веществ и может проводиться даже в остром периоде разрыва аневризмы сосудов головного мозга. Она дает двухмерное изображение поперечного сечения сосудов или их объемное трехмерное изображение.

КТ-ангиография головного мозга (3D-реконструкция). Аневризматическое расширение левой средней мозговой артерии
- Люмбальную пункцию. При отсутствии более информативных способов диагностики разорвавшаяся аневризма сосудов головного мозга может быть диагностирована путем проведения люмбальной пункции. Обнаружение крови в полученной цереброспинальной жидкости свидетельствует о наличие субарахноидального или внутримозгового кровоизлияния.
В ходе диагностики опухолеподобная аневризма сосудов головного мозга должна быть дифференцирована от опухоли, кисты и абсцесса головного мозга. Апоплексическая аневризма сосудов головного мозга требует дифференцировки от эпилептического приступа, транзиторной ишемической атаки, ишемического инсульта, менингита.
Лечение церебральной аневризмы
Пациенты, у которых аневризма сосудов головного мозга имеет небольшие размеры, должны постоянно наблюдаются у невролога или оперирующего нейрохирурга, поскольку такая аневризма не является показанием для хирургического лечения, но нуждается в контроле за ее размерами и течением. Консервативные терапевтические мероприятия при этом направлены на предупреждение увеличения размеров аневризмы. Они могут включать нормализацию артериального давления или сердечного ритма, коррекцию уровня холестерина крови, лечение последствий ЧМТ или имеющихся инфекционных заболеваний.
Оперативное лечение направлено на предотвращение разрыва аневризмы. Его основными методами являются клипирование шейки аневризмы и эндоваскулярная окклюзия. Может применяться стереотаксическая электрокоагуляция и искусственное тромбирование аневризмы при помощи коагулянтов. В отношении сосудистых мальформаций производят радиохирургическое или транскраниальное удаление АВМ.
Разорвавшаяся аневризма сосудов головного мозга является неотложным состоянием и требует консервативного лечения аналогичного лечению геморрагического инсульта. По показаниям проводят хирургическое лечение: удаление гематомы, ее эндоскопическую эвакуацию или стереотаксическую аспирацию. Если аневризма сосудов головного мозга сопровождается кровоизлиянием в желудочки производят вентрикулярное дренирование.
Прогноз
Прогноз заболевания зависит от места, где располагается сосудистое выпячивание, от его размеров, а также от наличия патологии, ведущей к дегенеративным изменениям сосудистой стенки или гемодинамическим нарушениям. Не увеличивающаяся в размерах церебральная аневризма может существовать в течение всей жизни пациента не вызывая каких-либо клинических изменений. В случае разрыва 30-50% пациентов погибают, у 25-35% остаются стойкие инвалидизирующие последствия. Повторное кровоизлияние наблюдается у 20-25% пациентов, летальность после него составляет достигает 70%.
Читайте также:
- Нарколепсия - клиника, диагностика, лечение
- Порфирийная полиневропатия. Диагностика порфирийной полиневропатии. Лечение порфирийной полиневропатии.
- Кисты и опухоли средостения. Клиника опухолей средостения
- Обеспечение визуализации при витрэктомии. Стабилизация глазного яблока
- Переломы позвоночника, грудной клетки. Механизмы травмы грудной клетки
