Лекарства в интенсивной терапии. Фармакология анестезии и интенсивной терапии
Добавил пользователь Дмитрий К. Обновлено: 08.01.2026
Для общего обезболивания (наркоза, или общей анестезии) в современной анестезиологии применяют различные лекарственные средства. В зависимости от их физико-химических свойств и способов применения их делят на ингаляционные и неингаляционные.
К средствам для ингаляционного наркоза относится ряд легко испаряющихся (летучих) жидкостей (галотан, эфир для наркоза) и газообразных веществ (главным образом закись азота). В связи с хорошими наркотизирующими свойствами и безопасностью (не воспламеняются и не взрывоопасны) фторированные углеводороды, особенно галотан, нашли широкое применение в анестезиологической практике, вытеснив ранее применявшийся Циклопропан и ограничив применение эфира для наркоза. Потерял значение как средство для наркоза хлороформ.
К средствам для неингаляционного наркоза относят барбитураты (тиопентал натрий) и небарбитуровые препараты (кетамин и др.).
Для введения в наркоз (индукции) чаще применяют неингаляционные наркотические средства (барбитураты и др.), вводимые внутривенно или внутримышечно, а основной наркоз проводят ингаляционными или неингаляционными средствами для наркоза. Основной наркоз может быть однокомпонентным — простым (мононаркоз) или многокомпонентным — комбинированным. Вводный наркоз может осуществляться также соответствующими концентрациями средств для ингаляционного наркоза (азота закись в смеси с кислородом и др.).
В процессе подготовки к операции проводится премедикация, включающая назначение больному успокаивающих, анальгетических, холинолитических, сердечно-сосудистых и других препаратов. Эти средства применяют с целью ослабить отрицательное влияние на организм эмоционального стресса, предшествующего операции, и предупредить возможные побочные явления, связанные с наркозом и оперативным вмешательством (рефлекторные реакции, нарушения гемодинамики, усиление секреции желез дыхательных путей и др.). Премедикация облегчает проведение наркоза: возможно уменьшение концентрации или дозы применяемого для наркоза средства, менее выражена фаза возбуждения и др.
Во время наркоза и при выходе из него также используют анальгетики, миорелаксанты (или декураризирующие средства), сердечно-сосудистые препараты и др., способствующие сохранению функций организма на физиологическом уровне.
В последние годы для общего обезболивания широко пользуются внутривенным введением различных сочетаний нейротропных средств, стремясь получить так называемую сбалансированную анестезию без использования традиционных ингаляционных средств для наркоза. Одним из методов такого вида общего обезболивания, основанным на применении нейролептиков (дроперидол) в сочетании с анальгетиками (фентанил, тримеперидин и др.), является нейролептанальгезия (НЛА). Другой многокомпонентный метод — атаральгезия, или транквиланальгезия, также предусматривает использование анальгетиков (фентанил, тримеперидин и др.) в сочетании с транквилизаторами (диазепам, феназепам или др.), натрия оксибатом, холинолитиками (атропин, метациния йодид) и другими препаратами.
Одним из методов общего обезболивания является введение наркотических анальгетиков (морфин или др.) в спинномозговой канал.
Лекарства в интенсивной терапии. Фармакология анестезии и интенсивной терапии
Внутривенные препараты для общей анестезии - наркоза
Вещества разных химических классов отключают сознание при в/в введении и могут использоваться как общие инъекционные анестетики. Как и ингаляционные препараты, большинство этих лекарственных средств влияет только на сознание и не оказывает обезболивающего действия (исключение: кетамин).
Эффект, вероятно, развивается в результате взаимодействия слигандзависимыми ионными каналами. Каналы, вызывающие возбуждение нейронов (NMDA-рецептор), блокируются, в то время как функция каналов, тормозящих возбуждение (ГАМКБA-рецептор, у трех препаратов дополнительно рецептор глицина), аллостерически усиливается.
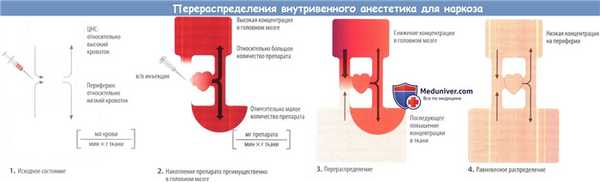
Большинство инъекционных анестетиков характеризуется коротким периодом действия. Быстрое прекращение действия обусловлено в основном перераспределением: после в/в инъекции концентрация в головном мозге быстро увеличивается до эффективного обезболивающего уровня из-за высокого мозгового кровотока.
Далее лекарственное средство равномерно перераспределяется в организме, т. е. концентрация повышается на периферии и падает в головном мозге — перераспределение и уменьшение анестезии. Следовательно, интенсивность эффекта снижается еще до того, как лекарственное средство покинет организм. При второй инъекции этот же препарат попадает в «преднасыщенные» отделы организма, поэтому интенсивность эффекта трудно предсказать.
Только этомидат и пропофол можно вводить в виде инфузии в течение длительного периода для поддержания бессознательного состояния. При использовании дополнительного ингаляционного средства вся процедура будет называться общей внутривенной анестезией.
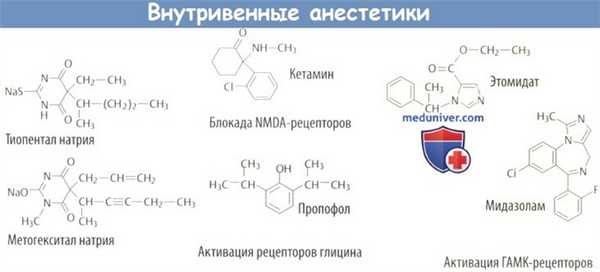
Тиопентал и метогекситал принадлежат к барбитуратам, которые в зависимости от дозы вызывают седацию, сонливость или анестезию. Барбитураты снижают болевой порог, что приводит к ослаблению защитных рефлекторных движений; они также подавляют активность дыхательного центра. Барбитураты часто используются для вводного наркоза.
Кетамин оказывает обезболивающее действие, которое сохраняется до 1 ч после инъекции, что значительно превышает начальный период бессознательного состояния (только 15 мин). При возвращении сознания пациент может ощущать диссоциацию психических процессов [диссоциативная анестезия]. Часто отмечается потеря памяти в течение восстановительного периода.
Вместе с тем взрослые пациенты, в частности, жалуются на тревожные фантастические видения. Их можно предупредить путем введения бензодиазепина (мидазолам). Влияние кетамина на ЦНС отчасти повышается за счет действия на глутаматергическую передачу возбуждения через лигандзависимые катионные каналы NMDA-подтипа на которые кетамин действует как блокатор канала. Искусственная возбуждающая аминокислота N-метил-О-аспартат (NMDA) является селективным агонистом этого рецептора. Кетамин вызывает высвобождение катехоламинов с соответствующим повышением ЧСС и АД.
У пропофола достаточно простая структура, похожая на фенольные дезинфицирующие средства. Поскольку он нерастворим в воде, инъекционную эмульсию готовят с помощью соевого масла, фосфатида и глицерина. Препарат быстро начинает и быстро прекращает действовать, что удобно для пациентов. Интенсивность действия хорошо контролируется во время длительного введения. К возможным нежелательным реакциям относятся артериальная гипотензия и угнетение дыхания, а также смертельно опасный синдром, включающий бронхоспазм, гипотензию и эритему.
Анестезирующее действие (+)этомидата уменьшается в течение нескольких минут благодаря перераспределению препарата. Этомидат стимулирует миоклонические движения, которые можно предупредить премедикацией бензодиазепином или опиоидным препаратом. Из-за слабого влияния на ВНС он подходитдля вводного наркоза при комбинированной анестезии. Этомидат ингибирует синтез кортизола в субанестетических дозах и поэтому может использоваться при длительном лечении избыточной активности мозгового и коркового вещества (синдром Кушинга).
Мидазолам — быстро метаболизируемый бензодиазепин, используется в качестве вводной анестезии.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Глава 5. Основные фармакологические средства, применяемые во время анестезии, реанимации и интенсивной терапии
Холинолитические (или антихолинергические) средства включают большую группу препаратов, блокирующих преимущественно холинорецепторы (м- и н-холинергические структуры). В анестезиологии и реаниматологии наиболее часто используют м-холинолитики группы атропина (атропин, скополамин), а также синтетический холинолитик метацин.
Атропин (ампулы по 1 мл 0,1% раствора) блокирует м-холинорецепторы, в результате чего они становятся нечувствительными к ацетилхолину, выделяющемуся в зоне окончаний постганглионарных парасимпатических волокон. В связи с этим действие атропина проявляется эффектами, противоположными наблюдаемым при возбуждении холинэргической (парасимпатической) нервной системы. Оно сопровождается учащением сердечных сокращений, подавлением секреции слюнных, бронхиальных, желудочных, потовых желез, поджелудочной железы, снижением тонуса гладкой мускулатуры внутренних органов, в том числе бронхов. Действие атропина проявляется в большей степени при повышенном тонусе парасимпатического отдела вегетативной нервной системы. Кроме того, после введения атропина расширяются зрачки, в связи с затруднением оттока жидкости из камер глаза повышается внутриглазное давление. Атропин проникает через гемато-энцефалический барьер. При передозировке вызывает психомоторное возбуждение, судороги и галлюцинации. Следует иметь в виду, что атропин в малых дозах (до 5 мкг/кг) может вызывать парадоксальный эффект за счет центрального вагусного стимулирующего действия.
Среди побочных эффектов атропина наиболее неблагоприятными являются:
- повышение потребления миокардом кислорода на фоне тахикардии, что крайне нежелательно у больных ИБС и пороками сердца. Атропин может провоцировать развитие пароксизма мерцательной или другой наджелудочковой тахиаритмии у лиц, имеющих в анамнезе нарушения ритма сердца, повышать внутриглазное давление (противопоказан при любой форме глаукомы), приводит к сгущению бронхиальной слизи, накоплению в бронхах вязкой трудноотделяемой мокроты, что особенно неблагоприятно у лиц с хроническими заболеваниями органов дыхательной системы.
После его введения возможно повышение температуры тела в связи с блокадой м-холинорецепторов потовых желез, что приводит к уменьшению теплоотдачи испарением и нарушению функции центра терморегуляции. Это имеет существенное значение у больных с лихорадкой и особенно опасно для пострадавших от теплового удара. Следует помнить также о вероятности развития задержки мочеиспускания у пожилых пациентов с аденомой простаты.
В анестезиологической и реаниматологической практике атропин применяют в составе премедикации для профилактики осложнений, возникающих в результате повышения тонуса блуждающего нерва («вагусная» брадикардия), подавления избыточной секреции слюнных и бронхиальных желез, предупреждения ларинго- и бронхоспазма, уменьшения потока афферентных импульсов в ЦНС из зоны операции по парасимпатическим нервным волокнам. С этой же целью его используют во время операции, вводя при необходимости повторно, а также во время реанимации при выраженной брадикардии и остановке сердца, возникшей на фоне ваготонии. Обязательно атропин применяют при проведении декураризации прозерином.
Для премедикации атропин вводят внутривенно из расчета 0,01 мг/кг массы тела, с осторожностью применяя у детей (склонность к гипертермии) и стариков. Период полувыведения атропина 2 ч, поэтому после введения он быстро исчезает из крови. До 60% препарата выводится с мочой в неизмененном виде.
Скополамин близок по своему действию к атропину и вызывает в основном такие же эффекты со стороны периферических холинореактивных систем. У него более выражено центральное действие, что проявляется седативным эффектом (общее успокоение, сонливость), иногда амнезией. Однако в ряде случаев в результате индивидуальной чувствительности к скополамину он может вызывать не успокоение, а возбуждение и галлюцинации. Показания и противопоказания такие же, как и для атропина. Взрослым обычно вводят 0,004 - 0,007 мг/кг (0,5 - 1 мл 0,05% раствора).
Метацин является избирательно действующим периферическим холинолитиком, так как плохо проникает через гемато-энцефалический барьер. По своему антихолинергическому действию превосходит атропин. Сильнее подавляет секрецию слюнных и бронхиальных желез, более активно, чем атропин, расслабляет гладкую мускулатуру бронхов и полых органов. Значительно меньше по сравнению с атропином расширяет зрачок, потому более удобен в анестезиологической практике. Противопоказания такие же, как и к применению атропина. Выпускается метацин в виде 0,1% раствора по 1 мл в ампуле. Применяют у взрослых в дозе 0,007 – 0,015 мг/кг внутривенно, можно подкожно и внутримышечно.
Глава 25. Анестетики и другие лекарственные средства, применяемые в анестезиологии и интенсивной терапии
Закись азота (N2O) - бесцветный газ, тяжелее воздуха, без запаха. Выпускается в 10-литровых баллонах серого цвета в нашей стране и голубого за рубежом с надписью черными буквами. Газ в баллоне находится в сжатом состоянии в виде жидкости и небольшой газообразной фракции. Из 1 литра жидкой закиси азота образуется 500 л газа. Не воспламеняется, но поддерживает горение. Применяется в смеси с кислородом при помощи специальных аппаратов для ингаляционного наркоза, причем, концентрация кислорода в смеси с N2O не должна быть менее 30 об. %. Закись азота слабый анестетик и несколько более сильный анальгетик. Обычно используется в сочетании с другими ингаляционными и неингаляционными анестетиками, анальгетиками, нейролептиками, атарактиками, мышечными релаксантами.
Плохая растворимость закиси азота в крови обуславливает быстрый ввод в наркоз (через 5 минут после начала ингаляции газа). В свою очередь, слабая тропность к тканям человеческого организма является причиной быстрого выхода из анестезии (через 10-15 минут). Таким образом, наркоз закисью азота легко управляем. Выводится N2O из организма в основном в неизмененном виде через легкие. Причем, в течение первых 5-10 минут по окончании анестезии большое количество поступающей из крови закиси азота может привести к вытеснению из альвеол кислорода и, как следствие, к диффузионной гипоксии. Поэтому, после прекращение подачи закиси азота больному необходимо ингалировать 100% кислород минимум в течение 5 минут.
Помимо легких закись азота может выводиться (в очень небольшом количестве) почками и через желудочно-кишечный тракт. В кишечнике под воздействием анаэробной флоры она распадается с образованием свободных радикалов, которые в конечном итоге могут служить помехой для нормального синтеза ДНК. Это в свою очередь (при ингаляции высоких концентраций закиси азота) может провоцировать спонтанные аборты, развитие врожденной патологии, нарушение функции красного костного мозга, полинейропатии.
Закись азота, обладая в 34 раза большей растворимостью, чем азот, легко диффундирует в содержащие воздух полости и может привести к резкому повышению давления в них. Именно этим обуславливается опасность применения N2O при наличии кист, пневмоторакса и т.д.
При концентрации закиси азота во вдыхаемой смеси выше 50% проявляется ее угнетающее действие на дыхательный центр и нарушается работа межреберных мышц, что вызывает закономерное угнетение дыхания. Также этот анестетик способен снижать функциональную остаточную емкость легких и тонус бронхиальной гладкой мускулатуры.
В концентрации выше 40% закись азота оказывает прямое угнетающее действие на миокард, что может проявиться гитотензией и снижением сердечного выброса (особенно у пациентов с заболеваниями сердечно-сосудистой системы).Как и многие другие ингаляционные анестетики, закись азота вызывает расширение сосудов головного мозга с повышением мозгового кровотока и внутричерепного давления.
Эфир для наркоза(диэтиловый эфир) - бесцветная, прозрачная, легковоспламеняющаяся жидкость, летучая (точка кипения 35 С о ), с резким запахом, 1 мл жидкого эфира дает при испарении 230 мл пара. В смеси с кислородом и воздухом пары эфира образуют взрывчатую смесь. Под влиянием света и воздуха эфир разлагается на токсичные вещества, поэтому должен храниться в темной, плотно закупоренной посуде. Выпускается во флаконах из темного стекла емкостью 150 мл.
Эфир имеет высокую наркотическую активность. Положительным свойством препарата является большая широта терапевтического действия. Он обладает выраженным наркотическим, анальгетическим и миорелаксирующим эффектами.
Хорошая растворимость эфира в крови и тканях человеческого организма обуславливает медленный ввод в наркоз (в среднем 20 минут после начала ингаляции анестетика) и выход из анестезии (около 30 минут с последующей сонливостью и депрессией).
Данный анестетик обладает выраженным стимулирующим действием на симпато-адреналовую систему, что сопровождается периферической сосудистой вазоконстрикцией с артериальной гипертензией, тахикардией, гипергликемией, повышением в крови концентрации кортизола. Таким образом, в умеренных концентрациях эфир способствует увеличению производительности сердца. Однако, в высоких концентрациях, он способен понизить сердечный выброс за счет прямого депрессивного действия на миокард.
Индукция в наркоз при применении диэтилового эфира сопровождается выраженной стадией двигательного и речевого возбуждения, характеризующейся резким напряжением всей мускулатуры (особенно жевательной - тризм), усилением кашлевого и рвотного рефлексов, значительной артериальной гипертензией и тахикардией с возможными сердечными аритмиями вплоть до фибрилляции желудочков. Длительность стадии возбуждения около 5 минут.
Эфир обладает раздражающим действием на слизистые оболочки дыхательных путей и ЖКТ, что и является причиной частого развития кашля, ляринго- и бронхоспазма, а также тошноты и рвоты на этапах вводной анестезии и выхода из наркоза.
Под влиянием эфира увеличивается секреция слюнных и бронхиальных желез, снижается тонус бронхиальной мускулатуры. Угнетение перистальтики под влиянием анестетика способствует развитию пареза кишечника в послеоперационном периоде. Имеются наблюдения, свидетельствующие об изменении волемических показателей, сопровождающихся уменьшением объема плазмы, сгущением крови, снижением диуреза на фоне увеличения секреции антидиуретического гормона. При глубоком уровне общей анестезии отмечаются нарушения функции печени.
В современной анестезиологической практике эфир для вводного наркоза практически не используется. Чаще с его помощью осуществляют поддержание анестезии. Более популярной, чем чистый эфир, является азеотропная смесь (2 части фторотана + 1 часть эфира).
Фторотан (галотан, флюотан, наркотан) - прозрачная, бесцветная жидкость, со своеобразным сладковатым запахом, летучая (точка кипения 50,2 С о ), не воспламеняется. Выпускается во флаконах из темного стекла емкостью 50, 125 и 250 мл, так как на свету способен спонтанно разлагаться. По этой же причине в качестве стабилизатора в анестетик добавляют тимол для предотвращения его окисления.
Умеренная растворимость фторотана в крови и его высокая наркотическая активность обеспечивают быстрый ввод в наркоз (5 минут с начала ингаляции анестетика). Средний уровень растворимости в тканях и высокая скорость метаболизма обуславливают относительно быстрый выход из фторотановой анестезии (около 10 минут, с постнаркозной депрессией до 1 часа). Индукция в анестезию и выход из нее длятся несколько дольше у полных пациентов, так как фторотан является липофильным агентом.
Данный анестетик по своей наркотической мощности превосходит эфир и закись азота. Анальгетический эффект у него несколько слабее. В отличие от эфира фторотан не раздражает слизистых оболочек, и у него гораздо менее выражена и менее длительна стадия возбуждения. Фторотан обладает непосредственным умереннымм миорелаксирующим эффектом и может потенцировать действие мышечных релаксантов.
Депрессия дыхания при фторотановом наркозе вызвана прямым воздействием на дыхательный центр и ослаблением тонуса межреберной мускулатуры. Анестетик также способствует расслаблению бронхиальных мышц и способен купировать бронхиолоконстрикцию. В высоких концентрациях (3 об.% и выше) фторотан может ликвидировать гипоксическую легочную гипертензию.
При фторотановом наркозе наблюдается дозозависимая артериальная гипотензия, вызванная как непосредственным влиянием на гладкую мускулатуру сосудов, так снижением миокардиальной сократимости с уменьшением сердечного выброса.
Часто фторотан вызывает брадикардию, купирующуюся введением атропина. Также анестетик способен нарушать проводимость электрических импульсов в сердце на уровне атриовентикулярного узла и волокон Пуркинье, что увеличивает риск возникновения сердечных аритмий по механизму “re-entry”. Как и закись азота, фторотан подавляет барорефлекс и вазомоторный рефлекторный ответ на гиповолемию.
Применение данного ингаляционного анестетика сопровождается сенисибилизацией миокарда к катехоламинам (адреналин, норадреналин, допамин). Их сочетанное применение часто вызывает серьезные нарушения сердечного ритма опасные для жизни пациента.
В гораздо большей степени, чем иные ингаляционные анестетики, фторотан вызывает вазодилятацию мозговых сосудов с последующим увеличением церебрального кровотока и повышением внутричерепного давления. Кроме того, он снижает скорость синтеза цереброспинальной жидкости, но при этом уменьшает и ее реабсорбцию.
Хорошо известно дозозависимое снижение почечного кровотока при фторотановом наркозе в результате снижения перфузионного давления из-за вазодилятации. Нередка и печеночная дисфункция при применении данного анестетика (15—20% фторотана метаболизируются в печени). Она может проявляться в двух формах: при одной наблюдается лишь транзиторное повышение концентрации печеночных ферментов в крови, а вторая представляет собой молниеносную форму печеночной недостаточности.
Фторотан является одним из веществ, наиболее часто вызывающих злокачественную гипертермию.
Энфлюран (этран) - галогенсодержащий ингаляционный анестетик, впервые внедренный в практику в 1966 году. Представляет собой прозрачную, бесцветную жидкость с цветочным запахом, летучую (точка кипения 56,5 С о ). Не горюч. Выпускается в темных стеклянных флаконах по 125 и 250 мл.
Умеренная растворимость анестетика в крови и тканях обеспечивает быстрый ввод в наркоз (в течение 2-5 минут) и выход из анестезии (7-10 минут).
2,4% поступившего в организм энфлюрана метаболизируются оксидазными системами печени, при этом образуются потенциально нефротоксичные вещества. Однако, гепатотоксичность энфлюрана гораздо ниже, чем у фторотана.
В начале анестезии энфлюран, как и большинство ингаляционных анестетиков, приводит к респираторному ацидозу, что клинически проявляется учащением спонтанного дыхания на фоне сниженного дыхательного объема. В дальнейшем, по мере углубления наркоза происходит депрессия спонтанной вентиляции за счет угнетения дыхательного центра и расслабления межреберной мускулатуры.
Так же, как и фторотан, энфлюран, вызывает дозозависимое угнетение гипоксического вазоконстрикторного легочного рефлекса. Однако, он практически не влияет на гладкую мускулатуру сосудов легочного круга кровообращения. Энфлюран способен вызвать (хотя и в меньшей степени, чем фторотан) дозозависимую артериальную гипотензию, снижение миокардиальной сократимости с уменьшением сердечного выброса. При проведении энфлюрановой анестезии не наблюдается сенсибилизации миокарда к катехоламинам. Энфлуран не вызывает коронарной вазодилятации, что, при определенных условиях, может привести к так называемому «феномену обкрадывания» сердечной мышцы.
Гипервентиляция с сопутствующей гипокапнией на фоне энфлюрановой анестезии может привести к появлению судорожной активности головного мозга и даже развитию эпилептиформного приступа. Как и фторотан, энфлюран вызывает церебральную вазодилятацию с повышением мозгового кровотока и внутричерепного давления. Однако, эти явления невозможно купировать увеличением минутного объема вентиляции. Повышение внутричерепного давления при энфлюрановом наркозе возможно и по другой причине. Данный анестетик увеличивает синтез цереброспинальной жидкости и при этом нарушает ее реабсорбцию.
Энфлюран потенцирует действие мышечных релаксантов, так как сам обладает миорелаксирующим эффектом. Применение энфлюрана, как и любого галогенсодержащего препарата, способно вызвать развитие злокачественной гипертермии.
Изофлюран (форан, аэрран) - впервые применен на практике в 1981 году. Представляет собой бесцветную, прозрачную, не воспламеняющуюся жидкость (точка кипения 48,5 С о ) с резким, острым, слегка похожим на эфир запахом. Выпускается во флаконах из темного стекла емкостью 100 мл.
Растворимость паров изофлюрана в крови и тканях человеческого организма гораздо ниже, чем у фторотана и энфлюрана, что обеспечивает, соответственно, более быструю индукцию в анестезию (2-3 минуты) и выход из нее (5-7 минут).
В начальных стадиях изофлюранового наркоза не отмечается характерного для вышеперечисленных галогенсодержащих анестетиков тахипноэ. При более глубокой анестезии имеет место депрессия дыхания по тем же причинам.
Влияние изофлюрана на сосуды легочной артерии аналогично энфлюрану. Однако, при изофлюрановой анестезии имеют место более выраженная гипотензия (из-за расслабления гладкой мускулатуры сосудов) и тахикардия, чем при применении всех выше названных анестетиков этого ряда. Следствием развивающейся тахикардии (до +20% к исходной ЧСС) является сниженный ударный объем на фоне стабильного сердечного выброса.
Изофлюран, в отличие от фторотана и энфолюрана, способен вызывать вазодилятацию коронарных сосудов.
Низкий метаболизмм (0,17% от поступившего в организм) изофлюрана и его малая раствориммость в тканях определяют его меньшую, чем у предшествовавших анестетиков, нефро- и гепатотоксичность.
В обычно применяемых дозах изофлюран практически не влияет на тонус церебральных сосудов, а соответственно и на величину мозгового кровотока. Продукция цереброспинальной жидкости также не меняется под влиянием данного анестетика, хотя реабсорбция ее несколько снижается. Возникающее при этом повышение интракраниального давления незначительно.
Изофлюран обладает миорелаксирующим эффектом и увеличивает кровоток в мышцах. Причем, эффект потенцирования миорелаксантов у него выражен больше, чем у закиси азота и фторотана, и практически такой же, как у энфлюрана.
Использование изофлюрана может являться триггером для запуска процесса злокачественной гипертермии.
Дезфлюран (супран) - как и другие галогенсодержащие анестетика, является бесцветной, прозрачной жидкостью с резким запахом и точкой кипения 22,8 С о . Не взрывоопасен.
Являясь веществом, еще менее раствориммым в крови и других тканях человеческого организма, обеспечивает более быстрое введение в наркоз и выход из него, чем изофлюран. Иными словами, анестезия дезфлюраном самая управляемая из всех, вызываемых ингаляционными анестетиками.
Из всего поступившего в организм дезфлюрана метаболизму подвергаются лишь 0,02%. Данный факт, а также слабая растворимость препарата в тканях обуславливают его крайне низкую (или полное отсутствие) нефро- и гепатотоксичность.
По сравнению с фторотаном, дезфлюран гораздо чаще во время вводной анестезии вызывает кашель, повышение бронхиальной секреции, ларингоспазм (особенно у детей). При углублении анестезии наблюдается угнетение спонтанного дыхания, как и при наркозе другими галогенсодержащими анестетиками.
Обладая вазодилятирующим эффектом, дезфлюран, однако, в меньшей степени, чем изофлюран снижает артериальное давление. Он практически не вызывает изменений частоты сердечного ритма. Депрессивное действие дезфлюрана на сердечную мышцу меньше, чем у других ингаляционных анестетиков. Данный препарат также не сенсибилизирует миокард к действию катехоламинов.
Расширяя церебральные сосуды, дезфлюран может вызвать увеличение мозгового кровотока и повышение интракраниального давления, купирующиеся гипервентиляцией. Воздействие дезфлюрана на синтез и реабсорбцию ликвора до конца не выяснены.
Препарат может служить причиной развития злокачественной гипертермии.
Севофлюран - бесцветная, прозрачная жидкость с точкой кипения 58,5 С о . Не взрывоопасен. Обладает менее мощным наркотическим эффектом, чем изофлюран.
Плохо растворим в крови и тканях, что обуславливает наступление анестезии через 1-1,5 минуты после начала ингаляции препарата и быстрый выход из наркоза.
Менее, чем дезфлюран раздражает слизистую верхних дыхательных путей, поэтому практически никогда не вызывает кашля и ларингоспазма.
Севофлюран разлагается натронной известью, поэтому не может использоваться в реверсивных системах.
Влияние его на спонтанное дыхание и гладкую мускулатуру бронхиального дерева такое же, как и у дезфлюрана.
Практически не изменяет частоту сердечных сокращений. Депрессивное действие на миокард такое же, как и у изфолюрана. Севофлюран способен вызвать умеренную артериальную гипотензию, дилятируя периферические сосуды. Однако расширения коронарных сосудов он не вызывает. Данный препарат не способствует сенсибилизации сердца к катехоламинам, а его собственный аритмогенный эффект является средним между энфлюраном и изофлюраном.
Около 3% севофлюрана метаболизируется печенью, таким образом, его гепатотоксичный эффект слабо выражен.
Умеренно увеличивает мозговой кровоток и повышает внутричерепне давление. Как правило, это купируется гипервентиляцией, и приходит в норму по окончании наркоза.
Так же, как и остальные анестетики данной группы, севофлюран потенцирует действие миорелаксантов и может вызвать развитие злокачественной гипертермии.
Необходимо отметить, что все ингаляционные анестетики свободно проходят через маточно-плацентарный барьер и способны вызвать дозозависимую депрессию плода.
Анестезиология и интенсивная терапия (Гельфанд Б.Р
Б.Р. Гельфанд, П.А. Кириенко, Т.Ф. Гриненко, В.А. Гурьянов, С.Л. Нистратов, О.А. Мамонтова, Б.З. Белоцерковский, Е.Б. Гельфанд, А.Н. Мартынов, Д.Н. Проценко, Ю.Я. Романовский, А.И. Ярошецкий, О.В. Игнатенко, И.И. Яковлева
Автор предисловия академик В.С. Савельев
Г32 Анестезиология и интенсивная терапия: Практическое руководство / Б.Р. Гельфанд, П.А. Кириенко, Т.Ф. Гриненко, В.А. Гурьянов и др.; Под общ. ред. Б.Р. Гельфанда. — М.: Литтерра, 2006. — 576 с.
ISBN 5 98216 026 1
Книга является практическим руководством, в котором в сжатой форме представлены вопросы клинической физиологии и фармаколо гии, общей и частной анестезиологии. Большое внимание уделено выбо ру анестезии в зависимости от сопутствующих заболеваний, осложнени ям анестезии — их профилактике и лечению. Кроме того, в руководстве представлены важные для практической деятельности анестезиолога реа ниматолога сведения об интегральных шкалах оценки состояния боль ных, послеоперационной аналгезии, профилактике тромбоэмболических осложнений и стресс поражений желудочно кишечного тракта. Отдель ные разделы руководства посвящены сепсису и синдрому острого по вреждения легких.
Книга предназначена для врачей анестезиологов реаниматологов, хирургов, преподавателей, научных работников, студентов медиков.
УДК [617 089.5 + 616 036.882] (035)
©Гельфанд Б.Р., Кириенко П.А.,
Гриненко Т.Ф., Гурьянов В.А.
© Оформление, оригинал макет.
ЗАО «Издательство «Литтерра», 2006
Памяти нашего учителя члена корреспондента РАМН профессора Виктора Адольфовича Гологорского посвящается
Б.Р. Гельфанд — чл. корр. РАМН, доктор медицинских на ук, профессор, кафедра факультетской хирургии с кур сом анестезиологии реаниматологии и антимикробной химиотерапии и курсом сердечно сосудистой хирургии и хирургической флебологии ФУВ РГМУ, заведующий курсом анестезиологии реаниматологии и антимикроб ной химиотерапии
П.А. Кириенко — кандидат медицинских наук, доцент, ка федра факультетской хирургии с курсом анестезиоло гии реаниматологии и антимикробной химиотерапии и курсом сердечно сосудистой хирургии и хирургической флебологии ФУВ РГМУ
Т.Ф. Гриненко — кандидат медицинских наук, ведущий научный сотрудник, ПНИЛ ангиологии РГМУ
В.А. Гурьянов — доктор медицинских наук, профессор, ка федра анестезиологии реаниматологии ФППОВ Мос ковской медицинской академии им. И.М. Сеченова
С.Л. Нистратов — кандидат медицинских наук, доцент, заве дующий отделением анестезиологии и реаниматологии Спасо Перовского госпиталя Мира и Милосердия
В подготовке ряда разделов руководства участвовали
Б.З. Белоцерковский — кандидат медицинских наук, ассис тент, кафедра факультетской хирургии с курсом анесте зиологии реаниматологии и антимикробной химиоте рапии и курсом сердечно сосудистой хирургии и хирур гической флебологии ФУВ РГМУ («Нозокомиальная пневмония в хирургии и травмотологии»)
Е.Б. Гельфанд — кандидат медицинских наук, доцент, ка федра факультетской хирургии с курсом анестезиоло гии реаниматологии и антимикробной химиотерапии и курсом сердечно сосудистой хирургии и хирургической флебологии ФУВ РГМУ («Профилактика инфекцион ных осложнений в хирургии», «Сепсис»)
О.В. Игнатенко — врач реаниматолог, Городская клиниче ская больница №7, г. Москва («Нозокомиальная пнев мония в хирургии и травматологии»)
Анестезиология и интенсивная терапия
О.А. Мамонтова — кандидат медицинских наук, доцент, кафедра факультетской хирургии с курсом анестези ологии реаниматологии и антимикробной химиотера пии и курсом сердечно сосудистой хирургии и хирурги ческой флебологии ФУВ РГМУ («Метаболизм и нутри тивная поддержка»)
А.Н. Мартынов — кандидат медицинских наук, ассистент, кафедра факультетской хирургии с курсом анестезиоло гии реаниматологии и антимикробной химиотерапии и курсом сердечно сосудистой хирургии и хирургической флебологии ФУВ РГМУ («Послеоперационная тошно та и рвота», «Профилактика стресс повреждений верх него отдела ЖКТ»)
Д.Н. Проценко — кандидат медицинских наук, ассистент, кафедра факультетской хирургии с курсом анестезиоло гии реаниматологии и антимикробной химиотерапии и курсом сердечно сосудистой хирургии и хирургической флебологии ФУВ РГМУ, врач реаниматолог, Городская клиническая больница № 7, г. Москва («Сепсис», «Синд ром острого повреждения легких и острый респиратор ный дистресс синдром»)
Ю.Я. Романовский — заведующий отделением реанимации и интенсивной терапии, Городская клиническая боль ница № 7, г. Москва («Синдром острого повреждения легких и острый респираторный дистресс синдром»)
И.И. Яковлева — доктор медицинских наук, заведующая отделением реанимации и интенсивной терапии, Город ская клиническая больница № 1 им. Н.И. Пирогова, («Экстракорпоральное очищение крови в интенсивной терапии»)
А.И. Ярошецкий — врач реаниматолог, Городская клини ческая больница № 7, г. Москва («Сепсис», «Синдром острого повреждения легких и острый респираторный дистресс синдром»)
Авторы с благодарностью примут все замечания и предложения по поводу содержания книги
и просят направлять их на адрес Издательства или Кафедры факультетской хирургии РГМУ.
Читайте также:
- Психопатологическая продукция при алкоголизме и наркомании. Отрицание болезни и деменция
- Предоперационная подготовка при ранениях: катетеризация мочевого пузыря
- Прионопатия с изменчивой чувствительностью к действию протеаз
- Лучевая диагностика инфаркта печени
- Методика моноаурального исследования. Ускорение нарастания громкости
