Лобэктомия на рентгенограмме, КТ
Добавил пользователь Алексей Ф. Обновлено: 30.01.2026
Особенности изменения органов грудной клетки после лечения на КТ, ПЭТ
Одной из наиболее распространенных трудностей, с которыми сталкиваются врачи лучевой диагностики, является оценка диагностических изображений пациентов после проведения терапии по поводу первичных и вторичных новообразований органов грудной клетки. Для выбора соответствующей тактики ведения пациента приходится дифференцировать изменения после лечения с резидуальными или рецидивирующими опухолями и осложнениями терапии.
Поэтому важно, чтобы врачи лучевой диагностики имели представление о том, с какими изменениями в органах грудной клетки они могут встретиться после проведенных хирургических вмешательств, лучевой терапии, системной терапии (химиотерапии, иммунотерапии) и абляции.
а) Хирургические вмешательства. Для лечения пациентов с новообразованиями органов грудной клетки разработан целый ряд хирургических процедур, выбор которых в каждом случае зависит от типа опухоли и ее локализации. Например, при наличии в легких новообразования или ограниченного количества метастазов злокачественных новообразований внегрудной локализации могут выполняться пневмонэктомия, лобэктомия или субдолевая резекция в зависимости от расположения опухоли, ее протяженности, возраста пациента и сопутствующих заболеваний.
Пневмонэктомия, или удаление хирургическим путем всего легкого и висцерального листка плевры, представляет собой наиболее обширную операцию, которая обычно проводится при наличии опухолей большого размера или образований, характеризующихся местнодеструирующим ростом. В послеоперационном периоде в ложе удаленного легкого некоторое время сохраняется воздух, который постепенно замещается жидкостью, что хорошо видно при КТ. При наличии в позднем периоде после пневмонэктомии в остаточной полости воздуха следует заподозрить бронхоплевральный свищ.
Лобэктомия и субдолевая резекция (объединяет клиновидную резекцию и сегментэктомию) являются менее масштабными процедурами, которые могут быть идентифицированы по объемному уменьшению легкого и наличию хирургических скоб.
Большинство новообразований пищевода, подлежащих хирургическому лечению, удаляют посредством эзофагэктомии, в том числе с использованием модифицированного доступа по Ivor-Lewis. Однако в некоторых случаях пациентам с опухолью на ранней стадии может быть выполнено менее инвазивное вмешательство, известное как эндоскопическая резекция слизистой оболочки пищевода. После эзофагэктомии могут возникнуть осложнения со стороны легких и кондуита. К осложнениям со стороны легких относят пневмонию, бронхоспазм, острый респираторный дистресс-синдром (ОРДС) и дыхательную недостаточность, обусловливающую необходимость в постоянном использовании аппарата искусственной вентиляции легких.
К осложнениям со стороны кондуита относят несостоятельность анастомоза, его стриктуру, ишемию и функциональные нарушения. При эпителиальных опухолях тимуса (тимома, рак) и герминативноклеточных новообразованиях средостения может выполняться резекция.
В большинстве случаев злокачественную мезотелиому плевры (ЗМП) выявляют на поздних стадиях, вследствие чего такие пациенты не подлежат хирургическому лечению. Однако в некоторых случаях на ранней стадии заболевания могут быть выполнены экстраплевральная пневмонэктомия или плеврэктомия и декортикация легкого. Часто операцию сочетают с химиотерапией, а в некоторых случаях дополнительно проводят еще и лучевую терапию. Другие новообразования плевры, например локализованную фиброзную опухоль плевры, обычно резецируют, если отсутствуют метастазы. При рецидивирующем пневмотораксе и рефрактерном плевральном выпоте может выполняться плевродез-метод склерозирования плевральной полости.
Для данной процедуры могут быть использованы различные химические вещества, но обычно применяется тальк. После плевродеза тальком при КТ вдоль плевры чаще всего выявляются линейные или узловые участки повышенной плотности. При ПЭТ/КТ плевра после данной процедуры, как правило, характеризуется повышенным уровнем поглощения ФДБ который может сохраняться в течение нескольких лет.
Основным методом лечения пациентов со злокачественными опухолями грудной стенки является резекция, поскольку она позволяет повысить выживаемость и уменьшить выраженность симптомов. В случае поражения грудной стенки крупными первичными новообразованиями или метастазами, например немелкоклеточного рака легкого, может быть выполнена резекция грудной стенки единым блоком. Глубина резекции зависит в том числе и от гистологического типа опухолей, а необходимость реконструкции грудной стенки во многом определяется их размером и локализацией.
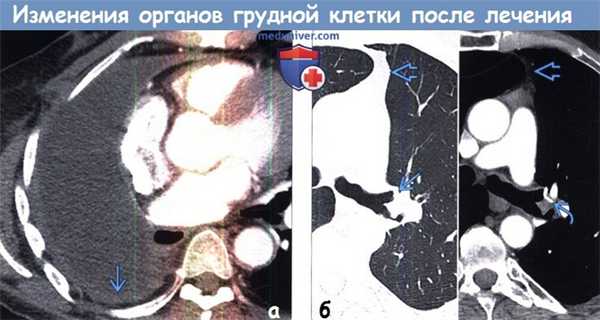
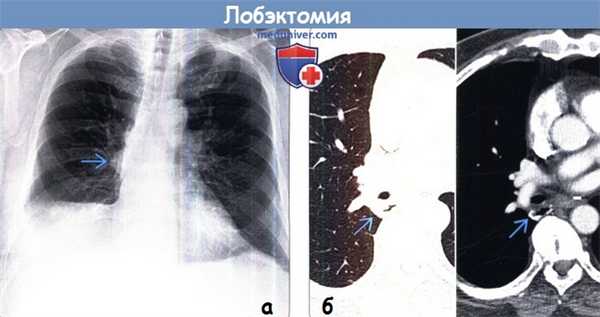
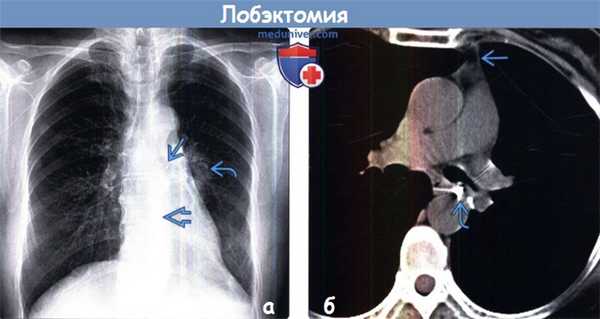
(а) Мужчина 58 лет, перенесший пневмонэктомию справа по поводу рака легкого. При КТ с контрастным усилением всю правую половину грудной полости занимает жидкость. Следует отметить доброкачественное утолщение париетального листка плевры справа.
(б) Пациент, перенесший верхнедолевую лобэктомию слева. На совмещенных изображениях при КТ с контрастным усилением в легочном (слева) и мягкотканном (справа) режимах визуализируются культя левого верхнедолевого бронха >i и хирургические скобы. Следует отметить смещение влево переднего средостения вследствие объемного уменьшения левой половины грудной полости.
б) Постлучевые изменения. Благодаря возникновению новых и безопасных технологий возросла роль лучевой терапии в лечении злокачественных опухолей органов грудной клетки: рака легких, метастазов в легких, рака пищевода, лимфомы средостения и злокачественной мезотелиомы плевры. Могут применяться различные методики дистанционной лучевой терапии (ДЛТ), например 3D конформная лучевая терапия (3D-KЛT), лучевая терапия с модулированной интенсивностью (ЛТМИ), стереотаксическая лучевая терапия (СЛТ) и стереотаксическая радиохирургия (СРХ), а также брахитерапия.
Постлучевые изменения локализуются главным образом в зоне облучения, характеристики которой зависят от локализации и размера злокачественной опухоли. Так, после лечения рака легких в последних выявляются наиболее выраженные постлучевые изменения. При этом в случае рака пищевода и лимфомы средостения наиболее выраженные изменения после облучения грудной клетки будут наблюдаться в средостении, хотя некоторые изменения можно будет выявить и в легких. На степень поражения тканей при лучевой терапии влияет несколько факторов: суммарная доза, доза на фракцию, количество рассеянного излучения, особенности зоны облучения и коллимации, а также параллельное проведение химиотерапии.
Постлучевые изменения в легких встречаются достаточно часто. В течение первых шести месяцев после лечения обнаруживают пневмонит, который при КТ чаще всего проявляется наличием зон уплотнения по типу «матового стекла» и участков консолидации легочной ткани. Через 6-12 месяцев после облучения обычно формируется лучевой фиброз, выраженность которого на протяжении следующих двух лет может уменьшаться. К характерным особенностям лучевого фиброза при КТ относят объемное уменьшение легкого, рубцевание, хроническую консолидацию, нарушение архитектоники легкого и формирование бронхоэктазов/бронхиолоэктазов. Симптомы лучевого эзофагита обычно возникают через 2-4 недели после начала лучевой терапии.
Вероятность его развития выше при использовании более высоких доз облучения и при сочетании лучевой терапии с химиотерапией. При остром эзофагите наблюдается отечность слизистой оболочки вследствие воспаления, границы которого соответствуют краям зоны облучения. При КТ обнаруживают циркулярное утолщение стенки пищевода на относительно большом протяжении. Контрастирование слизистой оболочки в сочетании с гиподенсной подслизистой оболочкой проявляется симптомом «мишени». При ПЭТ/КТ эзофагиту соответствует повышенный уровень накопления ФДГ протяженным сегментом пищевода, что не следует расценивать как опухолевое поражение. В большинстве случаев лучевые эзофагиты купируются самостоятельно, однако они могут осложняться развитием стриктур, некроза и свищей между пищеводом и дыхательными путями, а также между пищеводом и плевральной полостью.
Поражение органов сердечно-сосудистой системы встречается реже и характеризуется различной степенью выраженности. Так, постлучевые изменения могут проявляться только клинически (перикардит, изменения при электрокардиографии и аритмии), но могут обнаруживаться и лучевыми методами диагностики. В последнем случае могут быть выявлены признаки перикардиального выпота, констриктивного перикардита и кардиомиопатии.
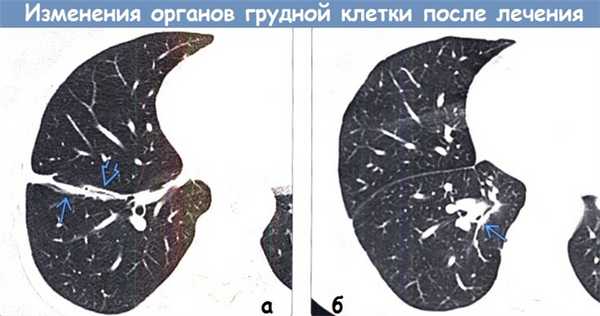
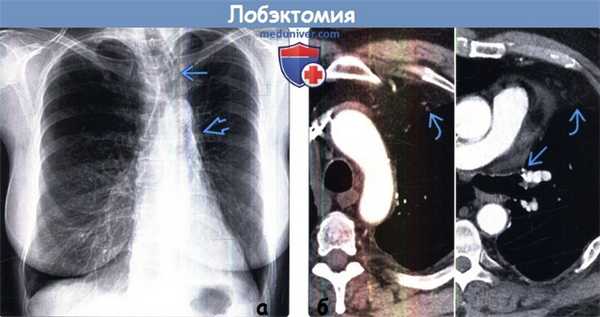
(а) Женщина 57 лет с метастазами рака толстой кишки. При КТ с контрастным усилением определяются последствия клиновидной резекции нижней доли правого легкого. Следует отметить наличие хирургических скоб и прилежащего к ним рубца.
(б) Женщина 32 лет с метастазами меланомы. При КТ с контрастным усилением в нижней доле правого легкого визуализируются хирургические скобы после удаления заднего сегмента. Сегментэктомия является видом субдолевой резекции.
в) Лекарственно-индуцированные изменения в легких. Лекарственно-индуцированное поражение легких является частым следствием химиотерапии пациентов с онкологическими заболеваниями, которое встречается в 10-20% случаев после применения цитотоксических и цитостатических препаратов. Описано три патофизиологических механизма поражения легких: 1) прямое повреждение пневмоцитов из-за высвобождения свободных радикалов кислорода, 2) прямое повреждение эндотелия сосудов легких и 3) гиперчувствительность немедленного или замедленного типа, обусловленная высвобождением цитокинов. Также описано несколько механизмов повреждения легких вследствие применения таргетной терапии и иммунотерапии, используемых в последнее время все чаще. Так, ингибирование иммунной системы может приводить к развитию реакций гиперчувствительности и аутоиммунного клеточного ответа вследствие продукции скрытых антигенов.
К наиболее распространенным патоморфологическим типам лекарственно-индуцированного поражения легких относят: диффузное повреждение альвеол (ДПА), неспецифическую интерстициальную пневмонию (НСИП), организующуюся пневмонию, эозинофильную пневмонию и диффузное альвеолярное кровотечение. По возможностям выявления патологических изменений в легких, обусловленных лекарственной токсичностью, КТ высокого разрешения (КТВР) превосходит рентгенографию органов грудной клетки. Многие типы лекарственно-индуцированного поражения легких характеризуются наличием острой и хронической фаз. На ранних этапах ДАП и НСИП при КТ чаще всего обнаруживают рассеянные или диффузные участки уплотнения легочной ткани по типу «матового стекла».
Организующаяся пневмония проявляется периферическими или перилобулярными участками уплотнения легочной ткани по типу «матового стекла» или участками консолидации, часто имеющими треугольную форму и характеризующимися наличием умеренно выраженных тракционных бронхоэктазов. Кроме того, могут выявляться центрилобулярные узелки и уплотнения по типу «дерева в почках». Эозинофильная пневмония при КТ проявляется однородными уплотнениями легочной ткани, расположенными преимущественно в периферических и верхних отделах легких. Наиболее частым признаком диффузного альвеолярного кровотечения при КТ является наличие рассеянных или диффузных участков уплотнения по типу «матового стекла» в обоих легких.
Поставить диагноз чаще всего удается на основании соответствующей клинической картины и результатов исследования методами лучевой диагностики. Несмотря на то что поставить точный диагноз можно посредством патоморфологического анализа, в клинической практике биопсию выполняют редко. В пользу предполагаемого лекарственно-индуцированного поражения легких говорит уменьшение выраженности симптомов и патологических изменений с течением времени и под воздействием лечения.
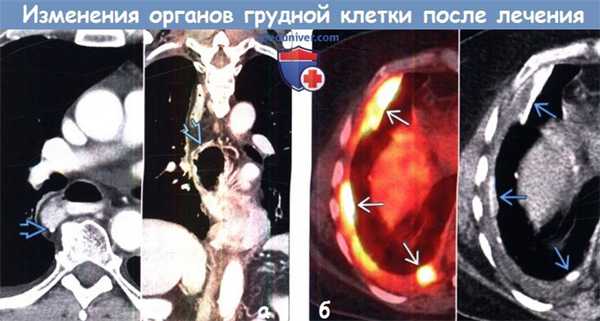
(а) Пациент, перенесший эзофагэктомию по Ivor-Lewis. На совмещенных изображениях при КТ с контрастным усилением в аксиальной (слева) и коронарной (справа) плоскостях в области анастомоза с проксимальными отделами пищевода определяются хирургические скобы.
(б) Женщина 51 года со злокачественной мезотелиомой плевры. На совмещенных изображениях при ФДГ-ПЭТ/КТ (слева) и нативной КТ (справа) в правой половине грудной полости визуализируются линейные и узловые участки повышенного накопления ФДГ. Данные участки при КТ соответствуют гиперденсным очагам в плевре, возникшим в результате плевродеза тальком.
г) Абляция. Для лечения пациентов с неоперабельными первичными и вторичными злокачественными опухолями легких может быть использован целый ряд абляционных процедур. К термической абляции относят радиочастотную абляцию (РЧА), в основе которой лежит использование электрического тока для индуцирования коагуляционного некроза, микроволновую абляцию (MBA), при которой электромагнитные волны высокой частоты вследствие трения вызывают нагрев и коагуляционный некроз, и криоабляцию, или чрескожную криотерапию (ЧККТ), при которой сжатый аргон индуцирует формирование льда внутри клетки и ее некроз. Возможность выполнения и выбор метода абляции в первую очередь зависят от локализации и размера опухоли.
Абляции предпочтительнее подвергать опухоли, расположенные на периферии, поскольку в этом случае риск повреждения жизненно важных структур ниже. Эффективность абляции новообразований, прилежащих к крупным сосудам, может снижаться вследствие отведения сосудами тепла. Кроме того, доступ к опухолям центральной локализации может быть затруднен из-за близости жизненно важных органов. Эффективность этого метода лечения в отношении небольших узелков в легких (
После термической абляции динамический контроль обычно проводят с помощью КТ и ПЭТ/КТ. Некоторые авторы предлагают выполнять КТ через один месяц и через три месяца после терапии, спустя шесть месяцев после лечения проводить ПЭТ/КТ, а затем в течение первых двух лет после терапии чередовать КТ и ПЭТ/КТ каждые три месяца, однако в каждом конкретном случае алгоритм обследования может быть изменен. По прошествии двух лет считается целесообразным выполнять КТ или ПЭТ/КТ с интервалом в шесть месяцев.
Для того чтобы избежать диагностических ошибок, следует знать, как выглядят изменения, возникшие в результате проведения абляции. Непосредственно после выполнения данной процедуры вокруг легочного узелка ожидают увидеть ореол изменений по типу «матового стекла» размером не менее 5 мм. Обычно ореол подвергается обратному развитию в течение одного месяца. Также вокруг узелка могут выявляться концентрические кольца, соответствующие симптому «кокарды». После лечения при ПЭТ/КТ может наблюдаться увеличение регионарных лимфатических узлов и накопление ими ФДГ Однако сохранение лимфаденопатии на протяжении более шести месяцев указывает на наличие в лимфатических узлах метастазов.
В случае паренхиматозных образований в течение трех месяцев в зоне абляции могут выявляться полости и утолщение прилежащих отделов плевры. В то же время наличие полостей через три месяца после проведения MBA считается благоприятным прогностическим показателем. Узелки в легких, подвергшиеся абляции, в течение первых шести месяцев могут увеличиваться в размере, однако увеличение размеров в более поздние сроки следует расценивать, как признак возможного прогрессирования заболевания. После абляции в случае выявления при КТ узлового накопления контрастного вещества следует заподозрить рецидивирование злокачественной опухоли.
д) Список литературы:
1. Carter BW et al: Acute Thoracic Findings in Oncologic Patients. J Thorac Imaging. ePub, 2015
2. Alpert JB et al: Imaging the post-thoracotomy patient: anatomic changes and postoperative complications. Radiol Clin North Am. 52(1):85-103, 2014
5. Narsule CK et al: Sublobar versus lobar resection: current status. Cancer J. 17(1):23-7, 2011
7. Nguyen NC et al: F-1 8 FDG PET/СТ characterization of talc pleurodesisinduced pleural changes overtime: a retrospective study. Clin Nucl Med. 34(12):886-90, 2009
8. Wolf FJ et al: Microwave ablation of lung malignancies: effectiveness, CT findings, and safety in 50 patients. Radiology. 247(3):871-9, 2008
9. Bojarski JD et al: CT imaging findings of pulmonary neoplasms after treatment with radiofrequency ablation: results in 32 tumors. AJR Am J Roentgenol. 185(2):466-71,2005
10. Kim EA et al: Radiographic and CT Findings in Complications Following Pulmonary Resection. Radiographics. 22(1):67-86, 2002
11. Rossi SE et al: Pulmonary drug toxicity: Radiologic and pathologic manifestations. Radiographs 20:1245-59, 2000
Рак легких
Рак легкого – это злокачественная опухоль, источником которой являются клетки бронхиального и альвеолярного эпителия. Это опасное заболевание характеризуется неконтролируемым ростом клеток в тканях лёгкого, склонностью к метастазированию. При отсутствии лечения опухолевый процесс может распространиться за пределы легкого в близлежащие или отдаленные органы. В зависимости от характеристик опухолеобразующих клеток, основными типами рака легких являются мелкоклеточный рак легкого (МРЛ) и немелкоклеточный рак лёгкого (НМРЛ).
По данным ВОЗ эта болезнь занимает одну из лидирующих позиций неинфекционных заболеваний, ставших причиной смерти до 70 лет.
Классификация
По месту первичного очага классифицируют виды опухоли легкого.
Центральный рак локализирован в проксимальных (центральных) отделах бронхиального дерева. Первые признаки рака легких (симптомы), которые должны насторожить, в этом случае выражены ярко:
- сухой продолжительный кашель, не поддающийся лечению.
- начинается кровохарканье с присоединением мокроты.
- закупорка просвета бронха опухолевыми массами приводит к одышке даже в состоянии покоя. В некоторых случаях возможно повышение температуры.
Фото 1 — Центральный рак правого нижнедолевого бронха (1) с обтурацией и метастазами (2) в бифуркационные лимфатические узлы
Периферический рак постепенно сформировывается в боковых отделах легких, медленно прорастая и ничем себя не обнаруживая. Данная опухоль легкого симптомы долгое время может не давать, они появляются при значительном местном распространении, вовлечении соседних органов и структур, прорастания бронхов. Диагностика рака легких этого типа локализации чаще всего возможна при профилактическом обследовании (рентгенографии или компьютерной томографии).
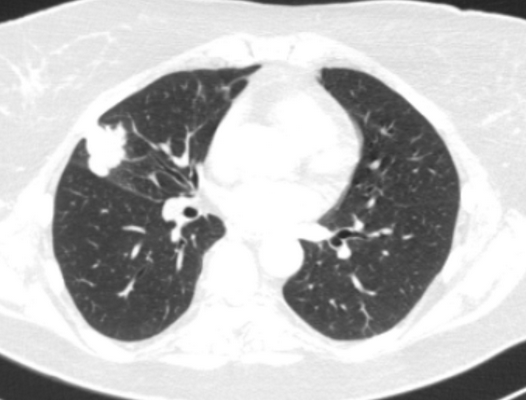
Фото 2 — Периферический рак (1) верхней доли правого легкого
Причины
Причиной рака легких, в подавляющем большинстве случаев (до 85%), становится долгосрочное табакокурение. В 10-15-процентной вероятностью заболевание проявляется у людей, которые не имеют этой вредной привычки. В этом случае можно отметить сочетание генетических факторов и воздействие радона, асбеста, вторичного табачного дыма или других форм загрязнения воздуха.
Диагностика
Онкология легких обычно выявляется при рентгенографическом исследовании грудной клетки и компьютерно-томографическом сканировании (КТ). Диагноз подтверждается биопсией, которая обычно выполняется при трахеобронхоскопии или под КТ контролем.
Профилактика
Профилактикой рака легкого является снижение влияния факторов риска:
- отказ от курения, в том числе и «пассивного» (вдыхание табачного дыма от находящегося рядом курящего человека),
- применение средств индивидуальной защиты (маски, респираторы) при работе с вредными материалами.
Лечение
Лечение онкологии легких и отдаленные результаты зависят от типа рака, степени распространения (стадии), а также общего состояния здоровья человека. При немелкоклеточном раке легкого применяют:
- хирургический
- химиотерапевтический
- лучевой методы лечения
Для мелкоклеточного рака легкого характерна лучшая чувствительность к медикаментозной и лучевой терапии.
Хирургический метод лечения рака легкого
— основной радикальный способ при 1-3 стадии болезни. Операции, выполняемые при данном заболевании классифицируются:
- по объему резекции (лобэктомии (удаление доли легкого), билобэктомии (удаление двух долей легкого), пневмонэктомии (удаление целого легкого)),
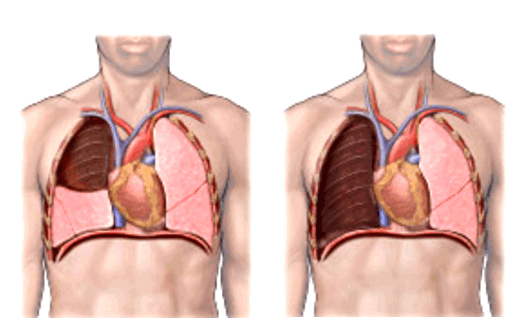
Фото 3 — Лобэктомия
Фото 4 — Пневмонэктомия
- по объему удаления лимфатических узлов грудной полости (стандартные, расширенные, сверхрасширенные),
- по наличию резекции соседних органов и структур (комбинированные операции проводятся при прорастании опухоли в перикард, трахею, верхнюю полую вену, пищевод, аорту, предсердие, грудную стенку, позвоночник). Помимо оперативного лечения возможно применение комплексного подхода, включающего лучевую и химиотерпию.
При лечении местнораспространенного злокачественного образования с переходом на главный бронх и лёгочную артерию, в тех случаях, где раньше единственным вариантом оперативного лечения являлась пневмонэктомия, сейчас возможно выполнение органосохранных операций. В этом случае иссекается пораженный участок главного бронха с последующим восстановлением непрерывности (бронхопластические и ангиопластические лобэктомии)

Фото 5 — Схема верхней бронхопластической лобэктомии
Лучевая терапия рака лёгкого
На сегодняшний день активное внедрение получают такие современные методы радиотерапии, как IMRT (радиационная терапия с возможностью изменения дозы излучения), 3Д конформная лучевая терапия (трехмерное компьютерное планирование избирательного облучения) стереотаксическая (точно сфокусированная) лучевая терапия. В проведении этих манипуляций, помимо онкологов, участвуют медицинские физики, врачи-радиологи, физики-дозиметристы и др. специалисты.
- пациентам с резектабельной опухолью лёгкого, которым оперативное лечение выполнить невозможно ввиду противопоказаний со стороны сердечно-сосудистой системы или по другим причинам;
- как альтернатива хирургическому вмешательству;
- для снижения риска рецидива при поражении лимфаузлов средостения, положительном крае резекции по данным гистологического исследования.
Химиотерапия
Планирование курса лечения немелкоклеточного рака лёгкого включает в себя использование фармакологических средств. Применяется в целях профилактики: адъювантная (вспомогательная), послеоперационная химиотерапия при 2-3 стадии заболевания и в терапевтическом курсе.
В зависимости от гистологического типа опухоли, стадии заболевания и предполагаемой чувствительности к воздействию, разработаны различные схемы применения химиопрепаратов.
Таргетная терапия (англ. target – мишень, цель)
Отдельный вид фармакологического лечения, заключающийся в назначении препаратов-ингибиторов, действующих только на опухолевые клетки, в которых выделены различные нарушения, задерживающих или даже блокирующих дальнейший рост.
- ингибиторы тирозинкиназы (гефитиниб, эрлотиниб, афатиниб) используются в лечении больных, в опухолевой ткани которых выявлены мутации в гене EGFR.
- При отрицательном статусе EGFR-мутации — ингибиторы ALK (кризотиниб, алектиниб).
Существуют таргетные препараты, для назначения которых не требуется выявление каких-либо нарушений в опухолевых клетках. К ним относятся бевацизумаб (ингибитор VEGF), ниволюмаб и пембролизумаб (анти PDL1 антитела).
Прогноз жизни
Прогноз онкологии легких при НМРЛ включает симптоматику, размер опухоли (> 3 см), неплоскоклеточный гистологический вариант, степень распространения (стадию), метастазирование в лимфаузлы и сосудистую инвазию. Неоперабельность заболевания, выраженная клиника и потеря веса более, чем на 10% — дают более низкие результаты. Прогностические факторы при мелкоклеточном раке легкого включают в себя статус состояния, пол, стадию заболевания и вовлеченность центральной нервной системы или печени во время диагностики.
Для немелкоклеточного рака легкого прогноз жизни, при полной хирургической резекции стадии IA (ранняя стадия заболевания) — 70% пятилетняя выживаемость.
Лобэктомия на рентгенограмме, КТ
Признаки субдолевой резекции легкого на рентгене, КТ
а) Терминология:
1. Синонимы:
• Клиновидная резекция (неанатомическая субдолевая резекция)
• Сегментэктомия (анатомическая субдолевая резекция)
2. Определение:
• Анатомическая субдолевая резекция (сегментэктомия): удаление одного и более сегментов; требует диссекции соответствующих артерии, вены и бронхов
• Неанатомическая субдолевая резекция (клиновидная): удаление периферической части легкого, содержащей патологическое образование, без удаления структур корня легкого
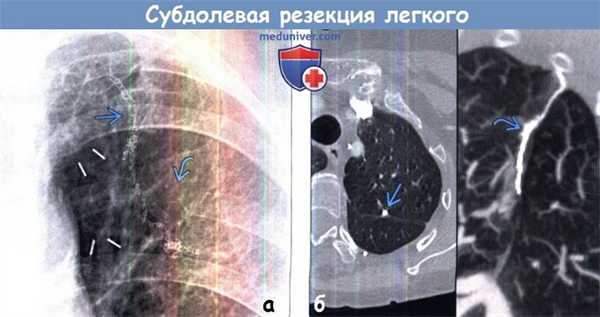
(а) Пациент, перенесший субдолевую резекцию по поводу периферического рака легкого на ранней стадии. При прицельной рентгенографии органов грудной клетки в ПП проекции определяются вертикально ориентированные металлические скобы. Также выявляются изменения в заднем отрезке ребра слева, обусловленные торакотомией.
(б) У этого же пациента на совмещенных изображениях при КТ с контрастным усилением в аксиальной плоскости (слева)и на реконструкции в кососагиттальной плоскости в режиме MIP (справа) хирургическая скоба выглядит соответственно в виде небольшого плотного узелка и в виде линейной структуры Хирургическая скоба в аксиальной плоскости может имитировать кальцифицированный узелок.
б) Лучевые признаки:
1. Рентгенография после субдолевой резекции легкого:
о Хирургические скобы:
- Рентгеноплотная линия шва (металлической плотности)
- Может имитировать кальцифицированные гранулемы
о Признаки объемного уменьшения легкого (например, высокое стояние купола диафрагмы, смещение средостения)
о Признаки торакотомии (например, переломы или деформация ребер)
2. КТ после субдолевой резекции легкого:
• Хирургические скобы:
о В аксиальной плоскости могут имитировать кальцифицированные гранулемы
о При мультипланарной реконструкции (т.е. в сагиттальной и коронарной плоскостях) характеризуются линейной формой; режим MIP позволяет более детально разглядеть структуру хирургического шва
о Утолщение прилежащих отделов плевры (послеоперационные изменения)
• Визуализация мягких тканей вблизи хирургических скоб (часто):
о Обычно вследствие ателектаза или рубцевания
о При узловом или массивном характере изменений следует заподозрить местное рецидивирование:
- Динамический контроль при КТ позволяет выявить изменения в размере
- При ФДГ-ПЭТ/КТ определяется повышенный уровень поглощения ФДГ
в) Дифференциальный ряд заболеваний:
1. Кальцифицированные гранулемы:
• Имеют узловую структуру в аксиальной плоскости и при мультипланарной реконструкции
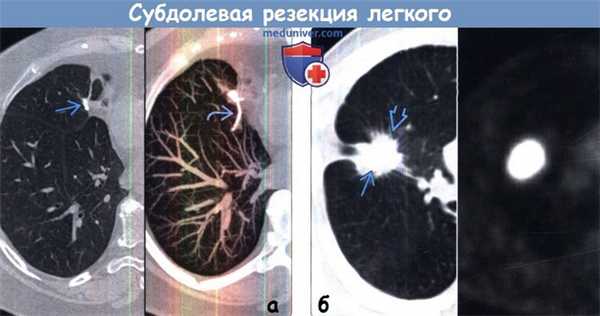
(а) Пациент, перенесший субдолевую резекцию. На совмещенных изображениях при КТ с контрастным усилением (слева) и в режиме MIP (справа) в средней доле определяется небольшое узловое образование металлической плотности. Е Я в режиме MIP видна линейная структура данного образования.
(б) Пациент, перенесший субдолевую резекцию. На совмещенных изображениях при нативной КТ (слева) и ФДГ-ПЭТ (справа) вокруг хирургических скоб визуализируется мягкотканный компонент со спикулообраз-ным контуром, который интенсивно накапливает ФДГ. Картина соответствует местному рецидивированию.
д) Список литературы:
1. Asamura Н: Role of limited sublobar resection for early-stage lung cancer: steady progress. J Clin Oncol. 32(23):2403-4, 2014
2. Cao C et al: Meta-analysis of intentional sublobar resections versus lobectomy for early stage non-small cell lung cancer. Ann Cardiothorac Surg. 3(2): 134-41, 2014
3. Fox M et al: Surgical management of pulmonary carcinoid tumors: sublobar resection versus lobectomy. Am J Surg. 205(2):200-8, 2013
4. Kaifi JT et al: Indications and approach to surgical resection of lung metastases. J Surg Oncol. 102(2):187-95, 2010
ОФЭКТ-КТ исследование в онкологии
ОФЭКТ-КТ – это эффективный метод диагностики злокачественных опухолевых заболеваний молочных желез, легких, органов брюшной полости и малого таза, а также их метастазов в лимфатических узлах и костях. О возможностях, области применения и достоинствах этого метода рассказывает Павел Иванович Крживицкий, кандидат медицинских наук, заведующий отделением радионуклидной диагностики НМИЦ онкологии им. Н.Н. Петрова.
Радионуклидная диагностика – раздел ядерной медицины, основанный на выявлении болезней с помощью радиоактивных меток или радиофармпрепаратов. Метод основан на принципе меченых атомов, согласно которому, радиоактивные вещества принимают такое же участие в процессах жизни клетки, как и не радиоактивные. Поэтому изучая распределение радиоактивной метки в организме больного с помощью специальных детектирующих аппаратов, например таких как ОФЭКТ-КТ и ПЭТ-КТ , врач получает возможность увидеть самые начальные проявления опухоли
Как проходит исследование? Пациенту внутривенно вводят радиоактивный препарат, и врач через определенное время с помощью современного оборудования (ОФЭКТ-КТ или ПЭТ-КТ) видит его пространственное распределение в клетках, тканях или органах у обследуемого человека. С помощью современных компьютерных систем формируется изображение, которое анализируют обычно не менее 2 специалистов.

По данным Европейского общества ядерной медицины, треть всех ОФЭКТ-КТ исследований производится в онкологии.
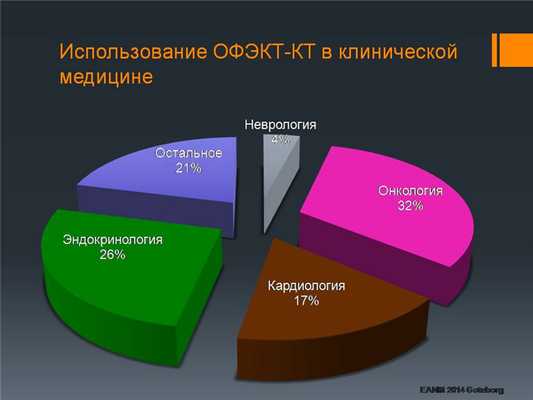
С помощью ОФЭКТ-КТ исследования мы можем определить аномально протекающие биохимические процессы в опухолевых клетках, когда анатомические и морфологические изменения еще не видны и не могут быть выявлены с помощью методов классической лучевой диагностики, таких, как рентгенография или КТ. С помощью методов радионуклидной диагностики сегодня мы можем диагностировать опухоли размерами менее 1 сантиметра.
Главная задача радионуклидных исследований в онкологии – оценка распространенности опухолевого процесса и оценка эффективности лечения.
Основные методы лучевой и радионуклидной диагностики разделяют на две категории
- Рентгенография
- Компьютерная томография (КТ)
- Магнитно-резонансная томография (МРТ)
- Сцинтиграфия
- Однофотонная эмиссионная компьютерная томография (ОФЭКТ)
- Позитронно-эмиссионная томография (ПЭТ)
Гибридные методы сочетают в себе анатомические и функциональные. К ним относится ОФЭКТ-КТ и ПЭТ-КТ. В отделении радионуклидной диагностики НМИЦ онкологии им. Н.Н. Петрова установлен гибридный аппарат «SiemensSymbiaT16». Этот прибор сочетает в себе двухдетекторную гамма-камеру и 16-срезовый компьютерный томограф. В целом информативность ОФЭКТ-КТ выше, чем КТ + ОФЭКТ отдельно. Исследования достаточно безопасны для пациентов.

За одно обследование получается максимум диагностической информации. Например, при раке молочной железы на ОФЭКТ-КТ томографе Siemens за одно исследование мы можем оценить состояние молочной железы, регионарных лимфатических узлов, органов грудной и брюшной полостей. В результате, пациент может начать специфическое противоопухолевое лечение максимально быстро.
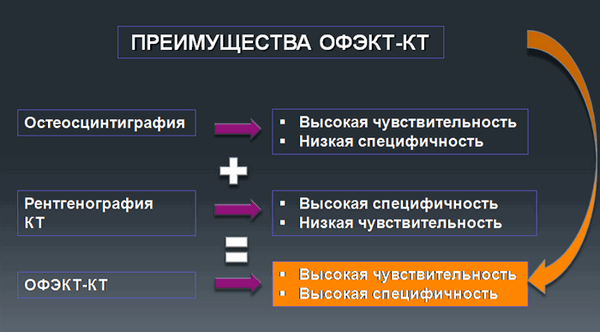
Преимущества ОФЭКТ-КТ
- Позволяет получить трехмерное функциональное изображение
- Высокое качество изображения
- Возможность точной анатомической локализации выявленный патофизиологических процессов
- Возможность одновременной совместной оценки выявленных функциональных и структурных нарушений
Диагностика метастатического поражения скелета
Наибольшее распространение этот метод получил в исследовании костей. ОФЭКТ-КТ исследование объединяет преимущества остеосцинтиграфии – высокую чувствительность и рентгенографии – высокую специфичность.
В результате ОФЭКТ-КТдиагностики могут быть выявлены новые уточняющие данные и даже может измениться диагноз. По опыту отделения радионуклидной диагностики НМИЦ онкологии им. Н.Н. Петрова: после рутинной остеосцинтиграфии в 40% случаев изменялся диагноз.
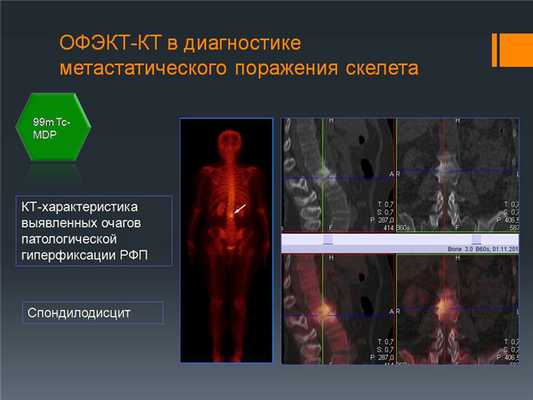
Пример уточняющей диагностики: При КТ-исследовании выявлен очаг, подозрительный на метастазы в 3 поясничном позвонке. После выполнения ОФЭКТ-КТ видно, что это спондилодисцит позвоночника, не онкологическое заболевание.
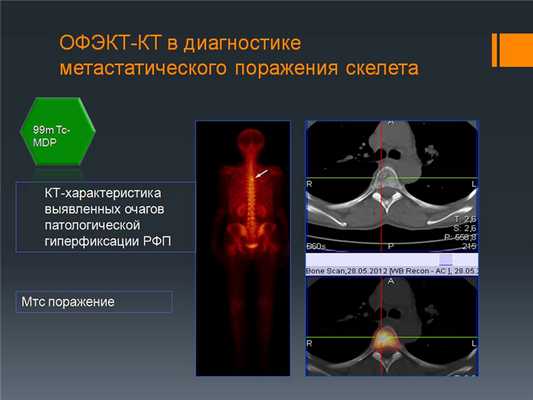
Пример уточняющей диагностики: Выявлен очаг гиперфиксации подозрительный на мтс. На снимке ОФЭКТ-КТ подтверждается, что это метастазы.
Диагностика метастатического поражения регионарных лимфоузлов у больных РМЖ
Статус регионарных лимфатических узлов влияет не только на прогноз, но и на выбор лечебной тактики, на объем лучевой терапии. При поражении лимфоузлов лучевая терапия может проводиться в над- и подключичной области. А при отсутствии метастазов облучается только грудная стенка и даже возможно полное отсутствие лучевой терапии.
Биопсия сигнальных лимфоузлов у больных РМЖ
Современное лечение РМЖ немыслимо без методов радионуклидной диаг ностики. Известно, что состояние сигнального лимфоузла определяет состояние всех остальных лимфоузлов. При помощи ОФЭКТ-КТ можно анатомически точно определить сигнальный лимфоузел. Во-первых, это помощь для хирурга: точная локализация позволяет ему быстрее обнаружить нужный лимфоузел. Во-вторых, результат исследования облегчает навигацию при последующей лучевой терапии.
ОФЭКТ-КТ также успешно применяется в диагностике нейроэндокринных новообразований, в диагностике метастазов при раке предстательной железы.

Авторская публикация:
Крживицкий Павел Иванович
врач-рентгенолог, врач-радиолог, кандидат медицинских наук.
Заведующий отделением радионуклидной диагностики, cтарший научный сотрудник отдела ядерной медицины и радиационной онкологии
Что вам необходимо сделать
Если вы хотите узнать побольше о бесплатных возможностях ФБГУ НМИЦ онкологии им. Н.Н. Петрова Минздрава России, получить очную или заочную консультацию по диагностике и лечению, записаться на приём, ознакомьтесь с информацией на официальном сайте.
Если вы хотите общаться с нами через социальные сети, обратите внимание на аккаунты в ВКонтакте и Одноклассники.
а) Определение:
• Лобэктомия:
о Полная резекция анатомической доли легкого
о Обычно включает в себя резекцию регионарных лимфатических узлов
• Рукавная лобэктомия:
о Резекция доли легкого и части главного бронха
1. Основные особенности лобэктомии:
• Оптимальный диагностический ориентир:
о Визуализация при КТ культи бронха, отсутствие резецированных доли и ветвей бронха
2. Рентгенография лобэктомии:
о Основные признаки:
- Наличие новообразованной междолевой щели:
Формируется между поверхностями оставшихся долей, покрытыми висцеральным листком плевры
- Признаки объемного уменьшения легкого
- Гипервентиляция оставшихся долей легкого о Прочие признаки:
- Хирургические скобы, изменения после торакотомии о Правосторонняя верхнедолевая лобэктомия:
- Объемное уменьшение правого легкого
- Новообразованная междолевая щель:
Формируется между средней долей правого легкого (СДПЛ) и нижней долей правого легкого (НДПЛ)
Лучше визуализируется при рентгенографии органов грудной клетки в боковой проекции
Повторяет ожидаемый ход главной междолевой щели
Смещена вперед и вверх
- Угол бифуркации трахеи уменьшен
- Выявляется юкстадиафрагмальный пик в правом куполе диафрагмы
- Высокое расположение корня правого легкого:
Правый главный бронх и промежуточный бронх смещены вверх и латерально
Проксимальные отделы правой нижнедолевой артерии смещены вверх и латерально
о Правосторонняя среднедолевая лобэктомия:
- Новообразованная междолевая щель:
Формируется между верхней долей правого легкого (ВДПЛ) и НДПЛ
Лучше визуализируется при рентгенографии органов грудной клетки в боковой проекции
Повторяет ожидаемый ход главной междолевой щели
- Смещение правого главного бронха и правой промежуточной легочной артерии
о Правосторонняя нижнедолевая лобэктомия:
- Объемное уменьшение правого легкого
- Смещение корня правого легкого вниз
- Реориентация 1 типа:
Новообразованная междолевая щель: между ВДПЛ и СДПЛ
Рентгенография органов грудной клетки во фронтальной проекции: косой ход новообразованной междолевой щели, при котором латеральные ее отделы расположены ниже медиальных
Рентгенография органов грудной клетки в боковой проекции: горизонтальный ход верхнезадних отделов новообразованной междолевой щели
Задние отделы новообразованной междолевой щели расположены выше передних
Смещение правого главного бронха вниз
ВДПЛ расположена сверху и спереди от новообразованной междолевой щели
СДПЛ расположена снизу и сзади от новообразованной междолевой щели
СДПЛ увеличена в объеме и занимает большую часть базальных отделов правой половины грудной полости
- Реориентация 2 типа:
Новообразованная междолевая щель: между ВДПЛ и СДПЛ
Лучше визуализируется при рентгенографии органов грудной клетки во фронтальной проекции
Рентгенография органов грудной клетки во фронтальной проекции: нижние отделы новообразованной междолевой щели справа располагаются ниже, чем при реориентации 1 типа
ВДПЛ занимает задненижние отделы правой половины грудной полости
СДПЛ остается спереди
о Левосторонняя верхнедолевая лобэктомия:
- Объемное уменьшение левого легкого
- Новообразованная междолевая щель отсутствует
- Высокое расположение корня левого легкого
- Угол бифуркации трахеи уменьшен
- Переднее средостение смещено влево
- Выявляется юкстадиафрагмальный пик в левом куполе диафрагмы
- Гипервентиляция нижней доли левого легкого (НДЛЛ)
о Левосторонняя нижнедолевая лобэктомия:
- Объемное уменьшение левого легкого
- Новообразованная междолевая щель отсутствует
- Корень левого легкого смещен вниз
- Переднее средостение смещено влево
- Высокое стояние левого купола диафрагмы
- Гипервентиляция верхней доли левого легкого (ВДЛГ1)
(а) Пациент, перенесший правостороннюю нижнедолевую лобэктомию. При рентгенографии органов грудной клетки в /7/7 проекции определяются объемное уменьшение правого легкого и смещение корня правого легкого вниз.
(б) У этого же пациента на совмещенных изображениях при КТ с контрастным усилением в легочном (слева) и мягкотканном (справа) режимах визуализируются объемное уменьшение правого легкого и хирургические скобы в области резекции. Оптимальным диагностическим ориентиром выполненной лобэктомии является выявление культи бронха и отсутствие резецированной доли легкого.
3. КТ после лобэктомии:
• КТ с контрастным усилением:
о Основные признаки:
- Визуализация культи бронха, отсутствие резецированных доли и ветвей бронха:
Ход бронхов можно проследить от уровня бифуркации трахеи
Метод позволяет обнаружить культю бронха
- Объемное уменьшение оперированного легкого
- Гипервентиляция оставшихся долей
о Прочие признаки:
- Хирургические скобы, изменения после торакотомии
о Правосторонняя верхнедолевая лобэктомия:
- Новообразованная междолевая щель:
При КТ выявляется тонкая линия или полоса
Имеет изгиб по часовой стрелке
На уровне дуги аорты ориентирована в коронарной плоскости
На уровне бифуркации трахеи ориентирована в косокоронарной плоскости
На уровне нижней легочной вены ориентирована в коронарной или сагиттальной плоскостях, располагается спереди от вены
- Правый главный бронх и промежуточный бронх смещены вверх и латерально
- Проксимальные отделы правой нижнедолевой артерии смещены вверх и латерально
о Правосторонняя среднедолевая лобэктомия:
- Новообразованная междолевая щель:
При КТ выявляется тонкая линия или полоса
На всех уровнях ориентирована в коронарной плоскости
Ориентирована менее вертикально, чем главная междолевая щель слева
Нижние отделы щели расположены ближе к передней поверхности тела, чем верхние
На уровне нижней легочной вены щель расположена ближе к передней поверхности тела, чем главная междолевая щель слева
- Правая промежуточная артерия смещена латерально
- Правый верхнедолевой бронх смещен вниз
о Правосторонняя нижнедолевая лобэктомия:
- Реориентация 1 типа:
Новообразованная междолевая щель: при КТ выявляется тонкая линия или полоса
Отсутствие бронха и артерии НДПЛ
Правый верхнедолевой бронх смещен вниз
- Реориентация 2 типа:
Новообразованная междолевая щель: при КТ выявляется тонкая линия или полоса
На уровне бифуркации трахеи новообразованная междолевая щель расположена впереди, ее задние отделы расположены ниже
Отсутствие бронха и артерии НДПЛ
Правый верхнедолевой бронх смещен вниз и кзади
Гипервентиляция ВДПЛ
СДПЛ имеет меньшие размеры, чем при реориентации 1 типа
о Левосторонняя верхнедолевая лобэктомия:
- Новообразованная междолевая щель отсутствует
- Отсутствуют артерия и бронх ВДЛЛ
- Гипервентиляция НДЛЛ
о Левосторонняя нижнедолевая лобэктомия:
- Новообразованная междолевая щель отсутствует
- Отсутствуют артерия и бронх НДЛЛ
- Гипервентиляция ВДЛЛ
(а) Пациент, перенесший левостороннюю верхнедолевую лобэктомию. При рентгенографии органов грудной клетки в /7/7 проекции определяются объемное уменьшение левого легкого, высокое расположение корня левого легкого и смещение влево верхних отделов средостения.
(б) У этого же пациента на совмещенных изображениях при КТ с контрастным усилением визуализируются смещение влево переднего средостения и хирургические скобы в культе верхнедолевого бронха.. При левосторонней лобэктомии междолевая щель не формируется.
4. Рекомендации к проведению лучевых исследований:
• Оптимальный метод лучевой диагностики:
о КТ позволяет выявить культю бронха и отсутствие резецированных доли легкого и ветвей бронха
• Рекомендации по выбору протокола:
о Облегчает диагностику мультипланарная реконструкция изображений
в) Дифференциальная диагностика лобэктомии:
1. Долевой ателектаз:
• Новообразованная междолевая щель и послеоперационные изменения отсутствуют
• Сохранение эластических свойств легких ограничивает перераспределение легочной ткани
• По сравнению с лобэктомией объемное уменьшение легкого выражено в меньшей степени
2. Субдолевая резекция:
• Сегментэктомия и клиновидная резекция
• Небольшие новообразования периферической локализации без признаков инвазии
• По сравнению с лобэктомией объемное уменьшение легкого выражено в меньшей степени
3. Пневмонэктомия:
• Удаление всего легкого; тотальное затемнение половины грудной полости
• Крупные опухоли с местнодеструирующим характером роста
• По сравнению с лобэктомией объемное уменьшение легкого выражено в большей степени
(а) Пациент, перенесший левостороннюю нижнедолевую лобэктомию. При рентгенографии органов грудной клетки в /7/7 проекции определяются смещение вниз корня левого легкого и смещение влево азигоэзофагеального кармана. Следует отметить наличие хирургических скоб в области резекции.
(б) У этого же пациента при нативной КТ визуализируется небольшое смещение влево жировой клетчатки переднего средостения. Также выявляются хирургические скобы в культе левого нижнедолевого бронха.
г) Патоморфология лобэктомии:
1. Основные особенности:
• Этиология:
о Рак легких:
- Ведущая причина в структуре смертности от онкологических заболеваний в США
- Показатель пятилетней выживаемости: 15,7%:
В значительной мере варьируется в зависимости от стадии опухоли на момент ее выявления
о Метастазы о Бронхоэктазы
о Абсцесс легкого
2. Макроскопические патоморфологические и хирургические особенности:
• Основные:
о Торакотомия:
- Предпочтительнее выполнять торакотомию через заднелатеральный доступ
- Переднелатеральный доступ и латеральный доступ, который позволяет избежать повреждения мышц
о Видеоторакоскопия:
- Выполняется все чаще
- Вероятность развития осложнений ниже
- Показатели выживаемости соответствуют таковым при открытой торакотомии
- Меньшая длительность госпитализации
• Рукавная лобэктомия:
о Является альтернативой пневмонэктомии
о Выполняется при поражении патологическими образованиями главных или долевых бронхов:
- Доброкачественные и высокодифференцированные злокачественные новообразования
- Стеноз дыхательных путей
- < 10% операбельных новообразований легкого
о Нарушение функции сердца и легких:
- ОФВ1 < 50%
- Максимальная произвольная вентиляция < 50%
о Правосторонняя верхнедолевая лобэктомия выполняется чаще, чем левосторонняя верхнедолевая лобэктомия
г) Клинические аспекты лобэктомии:
1. Проявления:
• Наиболее частые признаки:
о Осложнения:
- Ранние (1-30 день после операции):
Кровотечение, пневмония, отек легких, эмпиема, формирование бронхоплеврального свища, несостоятельность швов, формирование грыжи легкого и перекрут доли легкого
- Поздние (> 30 дней после операции):
Формирование бронхоплеврального свища, эмпиема, пневмония, рецидивирование новообразования и стриктура анастомоза
2. Естественное течение заболевания и прогноз:
• Лобэктомия:
о Торакотомия:
- Вероятность развития осложнений: 49%; смертность: 2,9%
о Видеоторакоскопия:
- Вероятность развития осложнений: 31%; смертность: 0-2%
- По сравнению с торакотомией вероятность развития рецидива варьируется в зависимости от источника данных
• Рукавная лобэктомия:
о 1-30 день после операции: показатель смертности составляет 5%
о Вероятность местно-регионарного рецидивирования: 4-22%
• Прогнозирование функциональных характеристик оперированного легкого:
о Динамическая перфузионная МРТ, количественная КТ, перфу-зионная ОФЭКТ
3. Лечение:
• Бронхоплевральный свищ:
о Пневмонэктомия
о Закрытие культи бронха васкуляризированным лоскутом
• Стриктура анастомоза:
о Пневмонэктомия
Читайте также:
- Комбинированная психофармакотерапия - принципы, возможности
- Стоматологические устройства
- Клиника полиомиелита. Диагностика полиомиелита. Лечение полиомиелита. Профилактика полиомиелита.
- КТ, МРТ при гемифациальной микросомии
- Проницаемость кишечника при хронических воспалительных заболеваниях кишечника - болезни Крона
