Моторная функция желудка. Двигательная функция желудка.
Добавил пользователь Alex Обновлено: 29.01.2026
В статье рассматриваются механизмы влияния некоторых нейрогуморальных веществ на моторику желудочно-кишечного тракта, в том числе на кишечные сокращения. Основная часть работы посвящена роли серотонина на двигательную активность пищеварительной трубки. Пр
Mechanisms of the effect of some neurohumoral agents on alimentary canal motor activity including intestinal abridgement are discussed in the article. Major part of the work is dedicated to serotonin effect on motor activity of digestive tube. The authors also provide comparative analysis of serotonergic preparations that affects motor activity of esophagus, stomach and bowels. Clinical manifestations of deficit and excess of serotonin and the ways of its corrections are described.
Основными классами рецепторов, участвующих в регуляции моторно-эвакуаторной функции желудочно-кишечного тракта (ЖКТ), являются холинергические, адренергические, допаминергические, серотониновые, мотилиновые и холецистокининовые. Препараты, применяемые при депрессивных и тревожных расстройствах, панических атаках и других вегетативных дисфункциях, действуют на те же рецепторы, которые отвечают за моторно-эвакуаторную функцию желудочно-кишечной трубки. Регулирование деятельности гладкой мускулатуры и подвижности кишечника происходит на нескольких уровнях. Гормоны и нейротрансмиттеры являются доминирующими компонентами, которые прямо или косвенно воздействуют на гладкомышечные клетки. Постпрандиальный эндокринный ответ включает в себя выработку инсулина, нейротензина, холецистокинина (ХХК), гастрина, глюкагоноподобных пептидов (ГПП-1 и ГПП-2), глюкозозависимый инсулинотропный полипептид (ГИП, ранее известный как желудочный ингибиторный пептид) [1], данные об эффектах нейромедиаторов и гормонов представлены в табл. 1. Например, ХХК выделяется в проксимальных отделах тонкой кишки и непосредственно влияет на сокращение мышечных клеток желчного пузыря и нейромедиированную релаксацию мышц клеток сфинктера Одди, которая опосредуется через ГИП нервно-мышечные соединения.
В настоящей статье особое внимание уделено серотонинергическим рецепторам, которые являются одними из важных регуляторов кишечной перистальтики. Серотонин, или 5-гидрокситриптамин (5-HT), — моноаминовый нейромедиатор, который является главным посредником в физиологии психологического состояния и настроения человека, а также одним из регуляторов функции сосудов и желудочно-кишечной моторики. 5-HT, как известно, представлен в тромбоцитах, ЖКТ и центральной нервной системе человека и животных [2–5]. Серотонин вырабатывается в организме человека из поступившей с пищей аминокислоты триптофана — так как именно она нужна для непосредственного синтеза серотонина в синапсах; второй путь выработки серотонина связан с поступлением глюкозы с углеводной пищей, которая стимулирует выброс инсулина в кровь, далее происходит катаболизм белка в тканях, что также приводит к повышению уровня триптофана в крови.
На основе биохимических и фармакологических критериев 5-HT-рецепторы подразделяются на семь основных подтипов, пять из которых находятся в кишечных нейронах, энтерохромаффинных (ЭХ) клетках и в гладкой мускулатуре ЖКТ — это 5-HT1, 5-HT2, 5-HT3, 5-НТ4 и 5-HT7 [6, 7]. Около 80% от общего количества 5-НТ-рецепторов находятся в ЭХ-клетках кишечника, где они принимают участие в кишечной перистальтике через несколько подтипов 5-HT-рецепторов [8, 9]. За исключением 5-HT3-рецепторов, лиганда закрытого ионного канала, все 5-HT-рецепторы связываются с рецепторами G-белка, которые активируют внутриклеточные реакции второго каскада, стимулируя возбуждающие или тормозные реакции в ЖКТ [10]. Серотонин обладает хорошо изученным воздействием на кишечную моторику, секрецию и сенситивность через центральные и периферические нейромедиаторные пути, что делает его ключевым фармакологическим средством, применяемым в лечении моторных нарушений ЖКТ [11]. Серотонин высвобождается из ЭХ-клеток в ответ на химическое или механическое раздражение слизистой оболочки [12] или в ответ при экспериментальных моделях стресса [13]. Серотонин синтезируется и хранится не только в ЭХ-клетках (90%), но и в нейронах кишечника (10%). Как говорилось выше, 5-HT выделяется в кровь после приема пищи и в ответ на изменения давления в кишечной стенке, а также при воздействии вредных раздражителей [13], а затем поступает в просвет кишечника и далее в его стенки из базолатерального депо ЭХ-клеток [14]. 5-HT стимулирует круговые и продольные мышцы желудка, двенадцатиперстной кишки и тощей кишки [15]. Важно стратегическое расположение ЭХ-клеток в непосредственной близости от сенсорных нервных окончаний слизистой оболочки кишечника, интерганглионарных нейронов и синапсов двигательных возбуждающих и тормозных нейронов. Серотонин увеличивает сокращение амплитуды мышц желудка, двенадцатиперстной кишки, тощей кишки и подвздошной кишки [16]. В тонкой кишке 5-HT стимулируют круговые сокращения мышц в течение первой манометрической фазы, вызываемые сокращения распространяются, становятся более частыми и активируют быстрые моторные комплексы [17]. В толстой кишке серотонин стимулирует подвижность на протяжении всей длины, вызывая фазовые сокращения, но не гигантские двигательные комплексы [18]. Кишечные гладкомышечные ритмические колебания определяются спонтанной активностью интерстициальных клеток Кахаля, которые работают как кардиостимулятор для клеток в ЖКТ [19–22]. Кишечная нервная система (КНС) состоит из полуавтономных эффекторных систем, которые связаны с центральной вегетативной системой. При освобождении серотонина из энтерохромаффинных клеток происходит инициация вагусных рефлексов — перистальтических, выделительных, сосудорасширяющих, ноцицептивных. Парасимпатический и симпатический отделы вегетативной нервной системы образуют КНС через афферентные и эфферентные связи. Текущие двунаправленные отношения рефлекторной дуги «мозг–кишка» с участием 5-HT оказывают существенное влияние на эффекторные системы. Нарушенная 5-HT-трансмиссия может привести к возникновению как кишечных, так и внекишечных проявлений синдрома раздраженного кишечника (СРК) [23].
Степень участия в функциональной перистальтической активности ЖКТ различных 5-HT подразделяется следующим образом — 5-HT3 — 65%, 5-НТ4 — 85% и 5-HT7 — 40%. В сочетании антагонисты этих рецепторов, приведенные в парах, способны уменьшить перистальтическую активность кишечника примерно на 16% (5-HT3 + 5-HT4), на 70% (5-HT3 + 5-HT7) и на 87% (5-HT4 + 5-HT7), а одновременное введение всех трех антагонистов неизбежно блокирует всю перистальтическую активности. Таким образом, 5-HT-рецепторы играют ключевую роль в модуляции кишечной перистальтики с одновременной блокадой трех рецепторов и подавляют перистальтическую активность. Среди 5-HT-рецепторов ЖКТ подтип 5-HT4 наиболее функционально важен для перистальтики, а 5-HT3- и 5-HT7-рецепторы играют несколько менее активную роль в этом процессе, что отражено в табл. 2 и на рис. 1 [24].
5-HT4-агонисты были доступны с введением в клиническую практику метоклопрамида в 1964 г. Этот препарат является антагонистом дофаминовых D2- и 5-HT3-рецепторов, а также агонистом 5-HT4-рецепторов и до сих пор широко используется во всем мира. Его успех привел к разработке альтернативных молекул, которые не влияют на D2-рецепторы, устраняя тем самым такие неблагоприятные события, как акатизия и экстрапирамидные двигательные расстройства.
Серотониновые рецепторы, в частности, 5-HT3 и 5-НТ4, участвуют в сенсорных и рефлекторных реакциях на раздражители при гастроинтестинальных расстройствах, обусловливая такие проявления, как рвота, запор или диарея, нарушения пищевого поведения, боли в животе, измененные сенсомоторные рефлексы [25]. Было высказано предположение, что селективные ингибиторы обратного захвата серотонина (СИОЗС) могут влиять на функцию 5-HT3-рецепторов, а также могут улучшить симптоматику СРК и сопутствующей депрессии у пациентов. Согласно ряду исследований и обзоров [26–29], трициклические антидепрессанты (амитриптилин, Мелипрамин), антидепрессанты ряда СИОЗС, такие как флуоксетин, пароксетин, циталопрам, кломипрамин, литоксетин, тразодон, и ряда селективных ингибиторов обратного захвата серотонина и норадреналина (СИОЗСиН) (дулоксетин) улучшают симптомы СРК. Долгосрочные побочные эффекты данной терапии являются общими для лечения антидепрессантами и связаны с антихолинергическим, серотонинергическим, седативным, антигистаминым и альфа-адренергическим эффектами. Эти эффекты необходимо учитывать при выборе подхода к лечению, поскольку описанные выше препараты влияют на моторику кишечника, функция кишечника пациента также должна учитываться при выборе серотонинергических препаратов (рис. 2) [30].
Как указывалось ранее, 5-HT1-, 5-HT3- и 5-НТ4-подтипы рецепторов играют важную роль в двигательных, чувствительных и секреторных функциях ЖКТ. Препараты, непосредственно влияющие на 5-HT-рецепторы, в отличие от трициклических антидепрессантов и СИОЗС, модулируют 5-гидрокситриптамин (5-HT) путем связывания с 5-HT-рецепторами, их характеристики отражены в табл. 3. Кишечные функции 5-HT-рецепторов связаны с гладкими мышцами, увеличением количества дефекаций, а также со снижением кишечного транзитного времени [31, 32]. Блокада 5-НТ3-рецепторов, в частности противорвотными средствами типа ондансетрона, приводит к запорам [33]. В течение последнего десятилетия были разработаны и испытаны блокаторы 5-НТ3-рецепторов — алосетрон и силансетрон при СРК-Д (СРК с диареей). Недавний систематический обзор и метаанализ 11 рандомизированных контролируемых исследований (РКИ) сравнения этих двух 5-НТ3-антагонистов с плацебо выявили положительный эффект препаратов [34]. Тем не менее, ряд редких побочных эффектов, включая ишемический колит и тяжелые запоры, привел к тому, что производство алосетрона и исследования по силансетрону были приостановлены [35]. Алосетрон сегодня доступен только по строгим показаниям (в США) для пациенток с тяжелым резистентным СРК с диареей, которые не ответили на первую или вторую линии терапии.
5-HT4-агонисты доказали свой терапевтический потенциал для лечения больных с нарушениями моторики ЖКТ. Препараты, у которых отсутствует селективность к 5-HT4-рецепторам, имеют ограниченный клинический успех в гастроэнтерологической практике. Например, наряду со сродством к 5-HT4-рецепторам, такие препараты, как цизаприд и тегасерод, имеют заметное сродство и к другим рецепторам, каналам или белкам-трансмиттерам. Неблагоприятные кардиоваскулярные события, наблюдаемые при применении этих средств, связаны с их неселективностью и перекрестными эффектами. Систематический обзор и метаанализ показали, что тегасерод превосходит плацебо при лечении запоров, в том числе и при СРК. Большинство исследований, относящихся к тегасероду, проводились с участием женщин, и в результате препарат первоначально был одобрен для лечения СРК-З (СРК с запором) только у женщин. Тем не менее, маркетинг тегасерода был также приостановлен, когда стали сообщаться данные о возможном росте сердечно-сосудистых и цереброваскулярных событий на фоне приема препарата [6].
Важным событием в клинической фармакологии стало открытие селективного лиганда (лиганд, от лат. ligare — связывать, атом, ион или молекула, связанные с неким центром (акцептором), термин применяется в биохимии для обозначения агентов, соединяющихся с биологическими акцепторами — рецепторами, иммуноглобулинами и др.) к 5-HT4-рецептору — прукалоприда (prucalopride). Избирательность этого нового препарата значительно отличает его от старших поколений альтернативных препаратов благодаря сведению к минимуму возможностей побочных эффектов. Кроме того, концепция поиска аналогичных лигандов открывает широкие возможности для дальнейшей разработки лекарственных препаратов и создания агонист-специфических эффектов в различных типах клеток, тканей или органов. Селективный агонист 5-HT4-рецепторов прукалоприд является инновационным препаратом с привлекательным профилем безопасности для лечения пациентов, страдающих гипомоторными расстройствами ЖКТ [36]. Прукалоприд имеет высокое сродство и избирательность к 5-HT4-рецепторам ЖКТ. За время существования препарата прукалоприд было проведено несколько крупных и долгосрочных исследований, которые позволили в полной мере оценить риски и преимущества использования прукалоприда при хронических запорах [36–38]. В целом прием прукалоприда был связан с последовательным и значительным улучшением удовлетворенности пациентов в их лечении, по оценке опросника качества жизни при запорах (Patient Assessment of Constipation Quality of Life questionnaire — PAC-QOL). Доля участников, получавших прукалоприд в дозе 2 мг в сутки, которые отметили улучшение ≥ 1 пункт по 5-балльной подшкале PAC-QOL, составила 45,3%, по сравнению с 21,3% среди тех больных, кто получал плацебо (р ≤ 0,001), но число ответчиков почти во всех исследованиях было менее 50%. В ходе других испытаний — PRU-США-11 и PRU-США-13 — не было выявлено никакого существенного различия между прукалопридом и плацебо во всех суррогатных точках. Общая частота нежелательных явлений была статистически достоверно чаще у пациентов, получавших прукалоприд (72%), по сравнению с пациентами, принимавшими плацебо (59%) (отношение рисков (ОР) 1,21, 95% доверительный интервал (ДИ): 1,06, 1,38). Неблагоприятные события, которые наиболее часто сообщали пациенты, получавшие прукалоприд, были головная боль (до 30%), тошнота (до 24%), диарея (до 5%), боли в животе и метеоризм (до 23%), головокружение (до 5%) и инфекции верхних дыхательных путей [39]. R. Cinca и соавт. сравнили эффективность, безопасность и влияние на качество жизни макрогола и прукалоприда у 240 женщин с хроническими запорами, которым другие слабительные не обеспечивали адекватную помощь. В этом исследовании макрогол оказался более эффективным для лечения хронического запора, чем прукалоприд, и лучше переносился [40]. В итоге можно сделать вывод, что прукалоприд может назначать врач, имеющий опыт в лечении хронических запоров, женщинам от 18 до 75 лет в том случае, если в их лечении не были эффективны другие слабительные средства.
Важно знать, что не всегда у пациентов бывает дефицит серотонина, в ряде случаев врач может сталкиваться с его избытком. У беспокойных гастроэнтерологических пациентов, которые имеют повышенное содержание серотонина, развивается аэрофагия, что вызывает увеличение воздушного пузыря в желудке и приводит к раздражению рецепторного аппарата [41]. Повышенный уровень серотонина обуславливает частую тошноту и рвоту вследствие активации блуждающего нерва, диарею или спастический запор, гастроинтестинальные панические атаки, головную боль, тремор, гипергидроз, волнение и тревогу, сердцебиение, нестабильное артериальное давление, бессонницу.
Серотонин играет важную роль не только в регуляции моторики и секреции в ЖКТ, усиливая его перистальтику и секреторную активность, но и является фактором роста для некоторых видов симбиотических микроорганизмов, усиливает бактериальный метаболизм в толстой кишке. Сами бактерии толстой кишки также вносят некоторый вклад в секрецию серотонина кишечником, поскольку многие виды симбиотических бактерий обладают способностью декарбоксилировать триптофан. При дисбиозе и ряде других заболеваний толстой кишки продукция серотонина кишечником значительно снижается. Массивное высвобождение серотонина из погибающих клеток слизистой желудка и кишечника при воздействии цитотоксических химиопрепаратов является одной из причин возникновения тошноты и рвоты, а также диареи при химиотерапии злокачественных опухолей [42, 43].
Трудно переоценить роль серотонина в организме человека. В передней части мозга под воздействием серотонина стимулируются области, ответственные за процесс познавательной активности, а повышение серотонинергической активности создает в коре головного мозга ощущение подъема настроения. Поступающий в спинной мозг серотонин положительно влияет на двигательную активность и тонус мышц, это состояние можно охарактеризовать фразой «горы сверну». Кроме настроения, серотонин «отвечает» за самообладание или эмоциональную устойчивость. Серотонин контролирует восприимчивость мозговых рецепторов к стрессовым гормонам адреналину и норадреналину. У людей с пониженным уровнем серотонина малейшие поводы вызывают обильную стрессовую реакцию. Отдельные исследователи считают, что доминирование особи в социальной иерархии обусловлено именно высоким уровнем серотонина [42, 43].
Заключение
Когда в организм поступает пища, в том числе содержащая триптофан, увеличивается выработка серотонина, что повышает настроение. Мозг быстро улавливает связь между этими явлениями и, в случае депрессии (серотонинового голодания), незамедлительно «требует» дополнительного поступления пищи с триптофаном или глюкозой. Наиболее богаты триптофаном продукты, которые почти целиком состоят из углеводов, например, хлеб, бананы, шоколад, инжир, курага, финики, изюм, арбузы и т. п. Перечисленные продукты давно известны и как регуляторы кишечной перистальтики. Их дефицит в питании приводит к депрессиям и проблемам ЖКТ, что можно часто наблюдать у людей, соблюдающих строгую низкокалорийную диету. По этой причине прежде чем назначать пациенту лекарственные препараты, повышающие уровень серотонина, необходимо уточнить причину его дефицита. Знание о деталях строения серотониновых рецепторов, несомненно, найдет применение в лечении пациентов некардиотоксичными аналогами серотонина или препаратами, повышающими уровень серотонина, которые будут выполнять свою целебную функцию и окажутся приятны во всех отношениях, например, такие как шоколад [44]. Препараты, повышающие уровень серотонина в синаптической щели и способствующие усилению его эффектов, относятся к группе антидепрессантов. Сегодня они являются одними из самых назначаемых лекарств врачами общей медицинской практики многих стран мира, в том числе Европы и Северной Америки. Своевременное назначение антидепрессантов как в монотерапии, так и в схемах лечения различных заболеваний, позволяет повысить эффективность лечения основного заболевания и улучшить качество жизни пациентов, особенно у пациентов гастроэнтерологического профиля.
Литература
Е. Ю. Плотникова 1 , доктор медицинских наук, профессор
О. А. Краснов, доктор медицинских наук, профессор
Моторная функция желудка. Двигательная функция желудка.
Депонирование пищи и ее гидролитическое расщепление происходят в основном в теле и дне желудка, эвакуация химуса из желудка осуществляется за счет двигательной активности его антральной части.
В желудке принято выделять три различных мышечных образования, функционирование которых происходит в определенной последовательности:
- дно — резервуар, который способен к расслаблению и сокращению;
- антрум — отдел, в котором происходит большая часть переваривания пищи и превращение ее в химус;
- пилорус — расположен у перехода желудка в двенадцатиперствую кишку. Стенка дна желудка состоит из трех слоев мышц:
- внутренний — циркулярный слой;
- средний — слой мышц, который является общим для всех отделов желудочно-кишечного тракта (по всей его длине) и расположен продольно;
- наружный — косые мышцы желудка, которые переходят с кардии на большую кривизну в виде «капюшона».
Натощак:
- сокращения мышц желудка слабые;
- величина внутриполостного (внутрижелудочного) давления близка к таковой внутрибрюшного;
- периодически внутрижелудочное давление увеличивается, и развиваются так называемые голодные сокращения.
Голодные сокращения обусловлены наличием мигрирующего моторного комплекса. В состоянии покоя (без стимуляции приемом пищи) в нервных ганглиях желудка и тонкого кишечника возникают так называемые медленные волны с пиками, которые вызывают их перистальтические сокращения, распространяемые по направлению к дистальным отделам тонкой кишки. Эти волны получили название мигрирующего моторного комплекса
Также существует мнение, что регуляция мигрирующих моторных комплексов осуществляется при участии собственного нервного аппарата и его нейротрансмитера — оксида азота (NO-радикал). Продолжительность мигрирующего моторного комплекса в норме составляет 93— 151 минут, и в нем выделяют три фазы:
- I фаза — фаза двигательного покоя, во время которой генерируются медленные волны, которые не сопровождаются пиковыми потенциалами (потенциалами действия) и изменениями сократительной активности;
- II фаза характеризуется нерегулярным появлением пиковых потенциалов (потенциалов действия), медленных волнах с частотой примерно 1 в минуту, что приводит к повышению тонуса мышц и появлению их сокращений;
- III фаза — потенциалы действия возникают регулярно, сокращения антральной части желудка происходят около 2,5—3,5 раза в минуту и распространяются из гастродуоденальной области к дистальным отделам тонкой кишки;
- IV фаза — наступает не всегда и характеризуется коротким промежутком времени снижения двигательной активности желудка.
Прием пищи, акт глотания и прохождение пищи по пищеводу вызывают расслабление дна желудка (рецептивная пищевая реакция) в результате повышения активности эфферентных неадренергических, нехолинергических волокон блуждающего нерва, из окончаний которых высвобождается, например, вазоактивный интестинальный пептид (VIP), который снижает тонус гладкой мускулатуры. Сокращения стенок желудка в этот момент очень слабые и напоминают пульсацию. После прохождения пищи в полость желудка тонус мышц дна сразу же повышается.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Моторная функция желудочно-кишечного тракта. Гладкая мускулатура пищеварительного тракта. Cфинктеры жкт. Сократительная деятельность кишечника.
Процесс пищеварения во всех отделах пищеварительного тракта осуществляется при участии двигательной активности его мускулатуры. Сокращения мышц обеспечивают: прием и измельчение пищи в процессе жевания в ротовой полости, глотание и продвижение порции пищи по пищеводу, накопление ее в желудке и эвакуацию его содержимого в кишечник, сокращение и расслабление желчного пузыря, перемешивание и продвижение кишечного содержимого, движение ворсинок, переход химуса из тонкой кишки в толстую, его перемещение по толстой кишке, сокращение и расслабление сфинктеров, перистальтику выводных протоков пищеварительных желез и выведение экскрементов.
Гладкая мускулатура пищеварительного тракта состоит из гладкомы-шечных клеток (миоцитов). Они собраны в пучки и соединены друг с другом нексусами. Пучок получает нервные терминали, артериолу и выполняет роль функциональной единицы гладкой мышцы. Миоциты обладают способностью к спонтанному ритмическому возбуждению за счет периодической деполяризации их мембраны. Это возбуждение распространяется благодаря нексусам от клетки к клетке (как по синцитию). Пучки миоцитов образуют гладкомышечные слои пищеварительной трубки — циркулярный (внутренний), продольный (наружный) и подслизистый (косой).
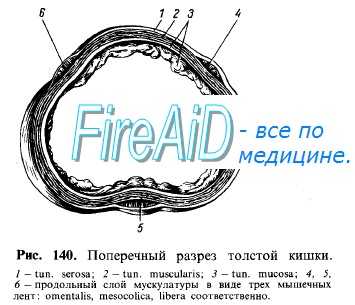
Растяжение мышц содержимым желудочно-кишечного тракта является для них адекватным раздражителем, вызывающим деполяризацию мембран их клеток и сокращение мышечных волокон. Частота и сила сокращений миоцитов изменяются в широком диапазоне под влиянием нервных импульсов эфферентных терминалей вегетативных нервных волокон, гормонов и гастроинтестинальных регуляторных пептидов. Комплексная нервно-гуморальная регуляция миоцитов обеспечивает соответствие уровня активности мускулатуры объему и составу содержимого желудка и кишечника.
Характер сократительной деятельности мускулатуры пищеварительного тракта зависит от активности водителей ритма, расположенных в желудке и кишечнике. Они представляют собой гладкомышечные клетки, более чувствительные к биологически активным веществам и имеющие более обильную иннервацию, чем другие пучки миоцитов.
На протяжении пищеварительного тракта у человека имеется около 35 сфинктеров. Они состоят из мышечных пучков, расположенных циркулярно (в основном), спирально и продольно. Сокращение циркулярных пучков приводит к смыканию сфинктера, а сокращение спиральных и продольных пучков увеличивает его просвет, что способствует переходу содержимого пищеварительного тракта в нижележащий отдел. Сфинктеры обеспечивают движение содержимого пищеварительной трубки в каудальном направлении и временное разобщение функционально различных частей пищеварительного тракта. Основные из них — кардиальный (на входе в желудок), пилорический (на выходе из желудка), в основании баугиниевои заслонки (на входе в слепую кишку), внутренний и наружный анальный (на выходе из прямой кишки).
Желудок. Функции и строение желудка. Ферменты желудка.
Желудок — орган, который полностью расположен в брюшной полости, представляет собой мешкообразное расширение пищеварительного тракта. В желудок пережеванная и смоченная слюной пища попадает из пищевода, где начинается очередной этап пищеварения. Выделяют следующие части желудка:
- малая и большая кривизна;
- кардия — часть желудка, прилежащая к пищеводу;
- пилорус (привратник) — место непосредственно перед переходом желудка в двенадцатиперстную кишку;
- дно (фундус), или свод, — часть желудка, которая располагается левее и выше кардии;
- пилорический сфинктер — мышечное образование, препятствующее забросу содержимого двенадцатиперстной кишки в желудок в норме;
- тело желудка — от дна до пилорического сфинктера. В желудке происходит всасывание некоторых продуктов (глюкозы, этилового спирта, соли, воды) и второй этап переваривания пищи.
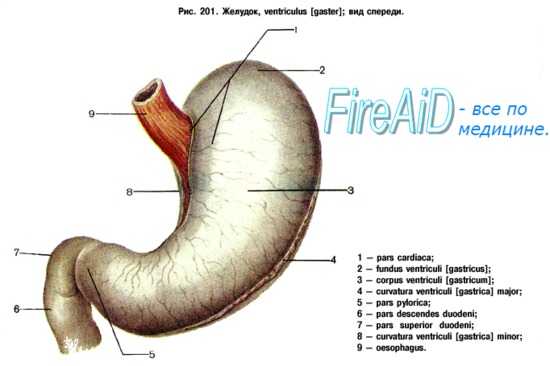
Внутренняя поверхность желудка представлена слизистой оболочкой, которая образует продольные складки. Слизистая покрыта слизью, которая защищает ее от действия соляной кислоты и ферментов. В слизистой оболочке расположены специфические железы, участвующие в синтезе соляной кислоты, пищеварительных ферментов, слизи и других биологически активных соединений. Вся совокупность этих соединений называется желудочным соком. Причем состав желудочного сока при каждом приеме пищи определяется ее составом. И это еще одна из причин, почету надо хорошо пережевывать пищу, — сигнал, поступивший из ротовой полости, должен быть получен головным мозгом, который, в свою очередь, определенным образом реагирует на него, регулируя выделение желудочного сока определенного состава и количества для обеспечения адекватного расщепления ингредиентов пищи. Важную роль в регуляции пищеварения играет центральная нервная система, которая была доказана академиком И. П. Павловым. Даже при виде определенной пищи или мысли о ней образуется желудочный сок определенного состава.
Основным ферментом желудочного сока является пепсин, под действием которого происходит расщепление белков на более мелкие фрагменты.
Натощак желудок периодически сокращается (перистальтика, моторная функция желудка), что может вызвать так называемые голодные спазмы. При попадании первой порции пищи в желудок на определенный промежуток времени перистальтика прекращается, и начинается процесс переваривания. По мере переваривания пищи сокращения возобновляются и она начинает продвигаться к выходу из желудка — к привратнику. К этому моменту перистальтика желудка активируется, что способствует перемешиванию пищи с желудочным соком и ее лучшему перевариванию.
Необходимо подчеркнуть, что в процессе продвижения пищи из желудка в кишечник активное участие принимают мышцы передней брюшной стенки — прямые и косые мышцы передней брюшной стенки (брюшной пресс), а также мышцы желудка, которые имеют автономную иннервацию. В положении стоя или при ходьбе мышцы сокращаются и стимулируют перистальтику кишечника, тогда как в положениях сидя или лежа они расслаблены, и нормальная перистальтика желудка практически прекращается.
На границе между желудком и двенадцатиперстной кишкой также находится сфинктер, затрудняющий попадание содержимого кишечника обратно в желудок.
В результате действия ферментов желудочного сока и моторной функции желудка в двенадцатиперстную кишку поступает более однородный пищевой комок, по консистенции напоминающий кашицу.
После желудка начинается кишечник, в котором выделяют тонкую и толстую кишки, имеющие отличительные черты строения и физиологические функции. В этих отделах ЖКТ выделяют также отдельные части.
В состав тонкого кишечника входит двенадцатиперстная, тощая и подвздошная кишки. По тонкому кишечнику пища продвигается в течение 7—8 часов.
Последние трансляциивсе записи
Недиабетические гипогликемии в практике интерниста. О чем подумать?
Бариатрическая хирургия — современные возможности или новые проблемы? В чем нуждается пациент после операции
Новые подходы и фундаментальные основы антитромботической терапии в лечении пациентов с ИБС
Хронический коронарный синдром: сложности диагностики и лечения
Медицина и политическая теория: «Этический реализм и идеализм в политической теории»
лекторывсе лекторы
Уникальные интерактивные лекции ведущих специалистов мира по внутренним болезням: нашими лекторами уже стали более 1000 экспертов
Профессор, доктор медицинских наук, заведующий кафедрой внутренних болезней педиатрического факультета РНИМУ имени.
Заслуженный врач РФ, директор Московского Научно-исследовательского онкологического института им. П.А. Герцена, главный онколог МЗ.
Профессор, доктор медицинских наук, генеральный директор ФГБУ «НМИЦ кардиологии» Минздрава России
Профессор, доктор медицинских наук,
директор ФГБУ "НМИЦ ССХ им. А.Н. Бакулева" Минздрава России,
СТАТЬИвсе статьи
Вашему вниманию представлены самые актуальные материалы по наиболее острым вопросам современной медицины
Сравнение пероральных и инъекционных нейролептиков у пациентов с шизофренией
Исследований, сравнивающих короткодействующие пероральные и длительнодействующие инъекционные антипсихотики, выполнено мало и большинство и них проведено среди пожилых лиц или употребляющих наркотики или начавших рано инъекционную терапию.
Можно ли назвать паратиреоидэктомию панацеей нефролитиаза при первичном гиперпаратиреозе?
Нефролитиаз является классическим показанием к паратиреоидэктомии при первичном гиперпаратиреозе. Однако эффективность операции в профилактике рецидива нефролитиаза не до конца ясна.
Эффективность дулаглутида у молодых пациентов с диабетом
Целью исследования было оценить эффективность дулаглутида, агониста рецептора глюкагон-подобного пептида-1, среди молодых взрослых.
Эпидемиология внебольничной остановки сердца, вызванной анафилаксией, и факторы, связанные с ее исходами
Анафилаксия возникает как в больничных, так и во внебольничных условиях, и имеется мало информации о факторах, связанных с эпидемиологией анафилаксии или ее исходами. Ещё меньше данных по внебольничной остановки сердца, вызванной анафилаксией (ВОС). Авторы работы описали особенности эпидемиологии ВОС, вызванной анафилаксией и определить факторы, связанные с исходами.
ЦИКЛЫ ПЕРЕДАЧвсе циклы
29 Российский национальный конгресс "Человек и лекарство"
4 - 7 апреля 2022 года
Медицинский детектив
Поставить правильный диагноз и назначить адекватное лечение может быть очень сложно. Приглашаем вас почувствовать себя настоящими детективами в серии авторских программ «Медицинский детектив» с профессором Драпкиной Оксаной Михайловной
Медицина и политическая теория
Целью проекта является ознакомление врачей с основными категориями гуманизма, проблемами и теоретическими подходами современной политологии, этики и деонтологии, заложить основу для дальнейшего изучения взаимосвязи политологических дисциплин и практической медицины. Программа предполагает как ряд широких, так и узкоспециальных отсылок, необходимых для профессионального выстраивания цивилизованных взаимоотношений между индустрией, государственными структурами и профессиональным медицинским сообществом.
X Международный интернет конгресс специалистов по внутренним болезням.
Российская академия наук
ФГБУ "НМИЦ ТПМ" Минздрава России
приурочен ко Дню российской науки
Всероссийская Образовательная Интернет-Сессия
Информация и материалы, представленные на настоящем сайте, носят научный, справочно-информационный и аналитический характер, предназначены исключительно для специалистов здравоохранения, не направлены на продвижение товаров на рынке и не могут быть использованы в качестве советов или рекомендаций пациенту к применению лекарственных средств и методов лечения без консультации с лечащим врачом.
Лекарственные препараты, информация о которых содержится на настоящем сайте, имеют противопоказания, перед их применением необходимо ознакомиться с инструкцией и проконсультироваться со специалистом.
Мнение Администрации может не совпадать с мнением авторов и лекторов. Администрация не дает каких-либо гарантий в отношении cайта и его cодержимого, в том числе, без ограничения, в отношении научной ценности, актуальности, точности, полноты, достоверности научных данных представляемых лекторами или соответствия содержимого международным стандартам надлежащей клинической практики и/или медицины основанной на доказательствах. Сайт не несет никакой ответственности за любые рекомендации или мнения, которые могут содержаться, ни за применимость материалов сайта к конкретным клиническим ситуациям. Вся научная информация предоставляется в исходном виде, без гарантий полноты или своевременности. Администрация прикладывает все усилия, чтобы обеспечить пользователей точной и достоверной информацией, но в то же время не исключает возможности возникновения ошибок.
Читайте также:
