Мышечный лоскут при трахеопищеводном свище.
Добавил пользователь Дмитрий К. Обновлено: 29.01.2026
Изобретение относится к медицине, а именно к хирургии. Целью изобретения является улучшение результатов хирургического лечения несформированных смешанных неполных свищей путем этапной мышечной пластики частями лоскута, образованного из прямой мышцы живота.
Несформированные свищи желудочно-кишечного тракта являются сложной и нерешенной проблемой абдоминальной хирургии. Они возникают вследствие несостоятельности желудочного и кишечного шва и перфорации стенки полого органа, не имеют канала и открываются в брюшную полость или рану стенки живота. Возникновение несформированного свища обуславливает появление опасных для жизни осложнений: выраженных нарушений гомеостаза, местного и распространенного перитонита, аррозионных кровотечений, множественных новых свищей и сепсиса (Каншин Н.Н., 1998; Григорьев Е.Г., Коган А.С., 2000). В области желудочного, дуоденального и тощекишечного несформированных свищей преобладают процессы альтерации, и нормальная регенерация тканей отсутствует. Спонтанное заживление таких свищей наблюдается редко, а консервативное лечение требует изобретательности, терпения, продолжается длительно и не гарантирует успеха (Ханевич М.Д., Долгий Р.Н., 2003; Каншин Н.Н., 2004; Саенко В.Ф. и соавт., 2004). Длительное стационарное лечение, значительная потребность в дорогостоящих лекарственных препаратах и инфузионно-трансфузионных средах ведут к большим финансовым затратам.
Рекомендации по лечению несформированных свищей, прежде всего двенадцатиперстной кишки, несостоятельности швов пищеводно-кишечного и желудочно-кишечного анастомозов противоречивы. Каншин Н.Н. (1999, 2004) отдает предпочтение дренажному способу с аспирацией в «струе воздуха» через двухканальные силиконовые трубки ТММК и формированием компрессионной подвесной еюностомы по авторской методике. Применение обтуратора при неполном тонкокишечном свище на эвентрированной кишечной петле может привести к образованию полного свища и необходимости срочного выключения кишечной петли, несущей свищ, через хирургический доступ за пределами гнойной раны (Макаренко Т.П., Богданов А.В., 1986; Каншин Н.Н., 2004). Летальность при хирургическом лечении несформированных кишечных свищей достигает 44-50% (Рузин Э.П. и соавт., 1991; Максимов A.M., Пакин В.П., 2004).
На XXV Всесоюзном съезде хирургов (Москва, 1.-8.10.1946 г.), посвященном хирургическому лечению огнестрельных ранений в период Великой Отечественной войны, Вазин Н.А. привел данные о мышечной пластике свищей толстой кишки. Толстокишечные пристеночные свищи автор устранял ушиванием с последующим укрытием линии швов мышечным лоскутом из наружной косой мышцы живота. Мышечная пластика несвободным лоскутом из большой ягодичной мышцы использована при лечении свищей типа anus sacralis. По мнению Вазина Н.А., мышечная пластика позволяет устранить морфологический дефект и «мертвое» пространство около кишки, несущей свищ, исключает расположение хирургических швов в одной плоскости.
Петров В.П. и соавт. (2003 г.) сообщили о 3 наблюдениях успешного закрытия обширного огнестрельного дефекта прямой кишки большой ягодичной мышцей у 2 и нежной мышцей бедра у 1 больного.
Нами разработан способ этапного закрытия смешанных свищей желудочно-кишечного тракта одним расщепленным лоскутом, образованным из прямой мышцы живота. В качестве аналога использован способ пластики дуоденальных свищей лоскутом из прямой мышцы живота, описанный Гриневым М.В. (1992). Автор осуществляет мышечную пластику следующим способом. Одиночный дефект стенки двенадцатиперстной кишки зашивают кисетным швом. Мобилизованную и пересеченную прямую мышцу живота на питающей верхней надчревной артерии перемещают из ее влагалища в брюшную полость и подшивают к двенадцатиперстной кишке по окружности ранее наложенного кисетного шва непрерывным кетгутовым швом. Гринев М.В. (1992) привел 5 клинических наблюдений применения описанной методики.
В отличие от аналога мы последовательно, в два этапа, закрываем несколько несформированных свищей желудочно-кишечного тракта одним лоскутом, образованным из прямой мышцы живота, путем парциального его пересечения и расщепления (расслоения) с перемещением вновь образованного дочернего мышечного лоскута на кишечный свищ, расположенный в стороне от оси основного лоскута.
Описание техники выполнения разработанного нами способа пластики. На первом этапе по известным правилам формируется лоскут из прямой мышцы живота. После продольного рассечения передней стенки фасциального влагалища прямой мышцы живота мышца выделяется острым и тупым путем на протяжении, достаточном для укрытия наиболее удаленного несформированного свища. Прямая мышца после мобилизации поперечно пересекается, и образованный мышечный лоскут выводится за пределы фасциального влагалища. Фасциальное влагалище дренируют силиконовой трубкой и зашивают. Мышечным лоскутом в первую очередь укрывают наиболее удаленный свищ и фиксируют его к стенке органа вокруг свища (Фиг.1).
Второй этап операции выполняется не ранее чем через 16 суток после первого этапа. К этому времени свищ, закрытый мышечным лоскутом, заживает, и образуются кровеносные сосуды между дистальной частью мышечного лоскута и окружающими тканями. При выполнении второго этапа мышечный лоскут тупым путем частично отделяют от подлежащих тканей, пересекают на половину ширины, расслаивают вдоль волокон по направлению к основанию. Сосудистая сеть обеспечивает кровоснабжение обеих половин лоскута. Вновь образованный дочерний лоскут перемещают на второй свищ (Фиг.2). Интервал между первым и вторым этапами операции необходим для сохранения жизнеспособности дистальной части основного лоскута после расщепления за счет новых дополнительных источников кровоснабжения от соседних тканей и органов.
Приводим клиническое наблюдение.
Ш., 33 лет, история болезни 8291. Госпитализирован в городскую больницу 23.10.1999 г. по поводу профузного кровотечения из множественных острых и хронических желудочных язв. На протяжении полутора месяцев ему выполнено 9 операций по поводу основного заболевания и многочисленных послеоперационных осложнений: 24.10. и 26.10. - экстренная лапаротомия и релапаротомия-1, гастротомия, прошивание кровоточащих сосудов в язвах тела и кардиального отдела; 29.10. - релапаротомия-2, субтотальная резекция желудка на высоте очередного обильного кровотечения, дренирование левостороннего поддиафрагмального абсцесса; 2.11. - релапаротомия-3, гастротомия, прошивание кровоточащих сосудов культи желудка, санация и дренирование брюшной полости по поводу разлитого гнойного перитонита; 3.11. - релапаротомия-4, экстирпация культи желудка на высоте очередного желудочного кровотечения в условиях разлитого гнойного перитонита. Патогистологическое исследование препарата 5611-5620: множественные хронические и острые язвы с фибриноидным некрозом тканей краев и дна, аррозия кровеносных сосудов; 8.11., 12.11. и 18.11. проведены программированные релапаротомии 5, 6 и 7 по поводу продолжавшегося разлитого перитонита с формированием межкишечных, подпеченочного и тазового абсцессов; 29.11. - релапаротомия-8, ушивание дефекта пищеводно-тощекишечного анастомоза, проведение интестинального зонда для питания. Через 5 суток несостоятельность анастомоза рецидивировала. Кроме того, в гнойной срединной ране образовались 2 несформированных свища на эвентрированной поперечной ободочной кишке. Левосторонняя нижнедолевая пневмония осложнилась эмпиемой плевры. Развились сепсис и полиорганная недостаточность. Состояние пациента крайне тяжелое. Гнойная рана с тусклыми грануляциями переднебоковой стенки живота имела размеры 23×15 см. В рану открывались 2 свища поперечной ободочной кишки диаметром 2 и 0,8 см, расположенные на расстоянии 6 см друг от друга. На дне щелевидного пространства под левой долей печени и диафрагмой глубиной 14 см пальпаторно определялся дефект пищеводно-тощекишечного анастомоза, занимавший треть его окружности. Пальпировался «оголенный» назоинтестинальный зонд, находившийся в отводящей петле тощей кишки. Через свищ вытекали желчь, слюна, слизь и введенная через зонд питательная смесь. Утрата массы тела к этому моменту составила 26 кг (30% от исходной величины). Осмотреть дефект анастомоза и наложить швы со стороны раны стенки живота невозможно. Выполнена 10-я операция. Лоскут длиной 18 см, образованный из правой прямой мышцы живота и кровоснабжаемый верхней надчревной артерией, был погружен до дна поддиафрагмального щелевидного пространства до несостоятельного пищеводно-тощекишечного анастомоза (Фиг.1). Мышечным лоскутом тампонированы отверстия пищеводного и тощекишечного свищей. В поддиафрагмальное пространство рядом с мышечным лоскутом плотно введен марлевый тампон, пропитанный мазью «Левосин». Левая плевральная полость дренирована силиконовой трубкой. После операции продолжена интенсивная многокомпонентная терапия в реанимационном отделении городской больницы. Состояние больного постепенно улучшилось. Выделения содержимого орального отдела пищеварительного тракта в поддиафрагмальное пространство прекратилось через неделю, дренаж удален. 23.12. выполнен 2-й этап пластики свищей: проведено расщепление мышечного лоскута по описанной методике и образованным «дочерним» лоскутом 7×3 см закрыт большой свищ поперечной ободочной кишки, свищ зажил под мышечным лоскутом (Фиг.2). Второй ободочный свищ диаметром 0,8 см зажил самостоятельно в результате активных репаративных процессов в ране. При рентгенологическом исследовании 27.12.1999 г. констатированы свободная проходимость пищевода и пищеводно-кишечного соустья, отсутствие затеков контрастной массы за пределы анастомоза. Дефектов слизистой оболочки и сужения в зоне анастомоза при эзофагоскопии не обнаружено, имели место умеренный отек и гиперемия слизистой оболочки. Кишечный зонд удален, начато кормление больного через рот. За время стационарного лечения длительностью 76 дней пациенту перелито 11,5 л эритроцитной массы, 37 л свежезамороженной плазмы, 14 л аминоплазмаля.
Пациент обследован в клинике через 2 года. Состояние удовлетворительное. Дисфагии и кишечных свищей нет. Дефицит массы тела составляет 10%. Работает официантом. Выполнено грыжесечение по поводу послеоперационной вентральной грыжи. Послеоперационный период протекал без осложнений. Пациент демонстрирован на заседании Архангельского областного научного общества хирургов им. Н.И.Пирогова 29.02.2002 г.
Краткое описание чертежей
На фиг.1 схематически представлен первый этап хирургического лечения несформированных смешанных свищей мышечным лоскутом на питающей верхней надчревной артерии. Цифрой 1 обозначен пищеводно-тощекишечный свищ, возникший после гастрэктомии, цифрой 2 - лоскут из правой прямой мышцы живота, перемещенный из ее фасциального влагалища к пищеводно-тощекишечному свищу, цифрой 3 - функционирующий несформированный свищ поперечной ободочной кишки и цифрой 4 - трубчатый дренаж в фасциальном влагалище правой прямой мышцы живота.
На фиг.2 схематически представлен второй этап хирургического лечения несформированных смешанных свищей мышечным лоскутом на сосудистой ножке. Цифрой 1 обозначен заживший пищеводно-тощекишечный свищ, цифрой 2 - расщепленный лоскут из правой прямой мышцы живота, цифрой 3 - несформированный свищ поперечной ободочной кишки, укрытый вновь образованным мышечным лоскутом. Трубчатый дренаж из фасциального влагалища правой прямой мышцы живота удален.
Похожие патенты RU2338468C1
- Быков Виталий Петрович
- Баранов Сергей Николаевич
- Бенсман Владимир Михайлович
- Сидоренко Олег Васильевич
- Гучетль Александр Якубович
- Белоконев Владимир Иванович
- Пушкин Сергей Юрьевич
- Харин Игорь Вячеславлвич
- Гуляев Максим Геннадьевич
- Дамбаев Георгий Цыренович
- Скиданенко Василий Васильевич
- Попов Алексей Михайлович
- Шведова Мария Витальевна
- Вусик Александр Николаевич
- Расулов Родион Исмагилович
- Хаматов Рафаил Камильевич
- Чикинев Юрий Владимирович
- Дробязгин Евгений Александрович
- Исраелян Армен Исраелович
- Коробейников Александр Владимирович
- Фокеев Сергей Дмитриевич
- Шойхет Яков Наумович
- Казанцева Елена Сергеевна
- Кравцов Сергей Анатольевич
- Решетов Игорь Владимирович
- Чиссов Валерий Иванович
- Белоконев В.И.
- Измайлов Е.П.
- Иштуков Роберт Ризович
- Нартайлаков Мажит Ахметович
- Пантелеев Владимир Сергеевич
- Дорофеев Вадим Давидович
Иллюстрации к изобретению RU 2 338 468 C1
Реферат патента 2008 года СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ НЕСФОРМИРОВАННЫХ СМЕШАННЫХ НЕПОЛНЫХ СВИЩЕЙ ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА РАСЩЕПЛЕННЫМ МЫШЕЧНЫМ ЛОСКУТОМ НА СОСУДИСТОЙ НОЖКЕ
Использование: в медицине, а именно в абдоминальной хирургии. Формируют мышечный лоскут на сосудистой ножке из прямой мышцы живота. Закрытие свищей осуществляют в два этапа. На первом этапе мышечным лоскутом закрывают свищ, наиболее удаленный от основания лоскута. После заживления этого свища на втором этапе закрывают второй свищ, расположенный в стороне от мышечного лоскута. При этом парциально пересекают и расщепляют мышечный лоскут. Перемещают на свищ вновь образованный дочерний мышечный лоскут. Способ позволяет надежно закрыть множественные желудочно-кишечные свищи. 2 ил.
Формула изобретения RU 2 338 468 C1
Способ хирургического лечения несформированных смешанных неполных свищей желудочно-кишечного тракта, включающий формирование мышечного лоскута на сосудистой ножке из прямой мышцы живота, в котором закрытие свищей осуществляют в два этапа, при этом на первом этапе мышечным лоскутом закрывают свищ, наиболее удаленный от основания лоскута; после заживления этого свища, на втором этапе, закрывают второй свищ, расположенный в стороне от мышечного лоскута, путем парциального пересечения и расщепления последнего, а также перемещения на свищ вновь образованного дочернего мышечного лоскута.
Мышечный лоскут при трахеопищеводном свище.
Первый Московский государственный медицинский университет им. И.М. Сеченова, Москва, Россия
Российский научный центр хирургии им. акад. Б.В. Петровского, РАМН, Москва
Первый Московский государственный медицинский университет им. И.М. Сеченова, Москва, Россия
Российский научный центр хирургии им. акад. Б.В. Петровского РАМН, Москва
Транстрахеальный доступ при мультифокальном трахеопищеводном свище
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2013;(7): 55‑57
Паршин В.Д., Вишневская Г.А., Паршин В.В., Шарипжанова Р.Д. Транстрахеальный доступ при мультифокальном трахеопищеводном свище. Хирургия. Журнал им. Н.И. Пирогова. 2013;(7):55‑57.
Parshin VD, Vishnevskaia GA, Parshin VV, Sharipzhanova RD. The transtracheal access by multifocal tracheoesophageal fistula. Pirogov Russian Journal of Surgery = Khirurgiya. Zurnal im. N.I. Pirogova. 2013;(7):55‑57. (In Russ.).
Первый Московский государственный медицинский университет им. И.М. Сеченова, Москва, Россия
Первый Московский государственный медицинский университет им. И.М. Сеченова, Москва, Россия
Российский научный центр хирургии им. акад. Б.В. Петровского, РАМН, Москва
Первый Московский государственный медицинский университет им. И.М. Сеченова, Москва, Россия
Российский научный центр хирургии им. акад. Б.В. Петровского РАМН, Москва
Хирургия трахеопищеводного свища (ТПС) в настоящее время остается уделом ограниченного круга специализированных медицинских учреждений. Это связано не только с редкостью данного заболевания, но и со сложностью лечения подобных больных. Результаты этого лечения в руках опытных специалистов представляются вполне приемлемыми. Разработанные в последние десятилетия лечебная тактика и хирургические приемы позволили практически полностью отказаться от паллиативных вариантов лечения, излечивать больных за одну операцию, даже при ТПС в сочетании со стенозом трахеи. Осложненные формы ТПС, обусловленные рубцовым процессом в трахее или пищеводе, а также дегенеративными изменениями пищеводной стенки из-за ее чрезмерного постоянного расширения воздухом, существенно затрудняют лечение. Эти состояния являются основными причинами рецидива свища, неоправданного удаления пищевода, требующего последующей сложной реконструкции пищеварительного тракта, а также других осложнений, в том числе двустороннего паралича гортани.
Истончение стенки пищевода при больших размерах ТПС, массивном поступлении воздуха в пищеварительный тракт существенно затрудняет операцию. Во время операции пищевод легко травмируется при его мобилизации. Дефект пищевода трудно ушить, особенно когда он был увеличен в результате операционной травмы. В этих ситуациях актуальность приобретает адекватный доступ к свищу. В большинстве наблюдений к ТПС удается подойти через трахеопищеводную борозду, наиболее часто с левой стороны. Манипуляции в этой зоне всегда опасны из-за возможности повреждения нижнего возвратного гортанного нерва, особенно слева. Травма данного нерва с одной стороны не приводит к нарушению дыхания и глотания. Двусторонний приводящий паралич голосовых складок в послеоперационном периоде является грозным осложнением. Возникает потребность в трахеостомии для обеспечения дыхания пациента. Длительное нахождение инородного тела (трахеостомической трубки) в области недавно наложенных швов трахеи является основной причиной рецидива ТПС в ближайшем послеоперационном периоде. Кроме того, стеноз гортани, обусловленный приводящим параличом, в дальнейшем потребует нескольких операций со сложной функциональной реабилитацией. При двустороннем повреждении нижних гортанных возвратных нервов возможно возникновение и отводящего паралича без нарушения дыхания. Это не должно обнадеживать хирурга. Данная ситуация имеет временный характер. В дальнейшем возникнет приводящий паралич и появится клиническая картина стридора. Предрасполагающими факторами для двустороннего повреждения нижних возвратных гортанных нервов являются ТПС больших размеров с вовлечением в патологический процесс всей ширины мембранозной стенки трахеи. Чрезмерно большой диаметр пищевода обусловливает технические трудности выделения свища, смещение органов средостения в латеральных направлениях.
Для хирургического доступа в зависимости от локализации ТПС производят цервикотомию, стернотомию либо правостороннюю боковую торакотомию. Однако у некоторых больных приходится избирать нетрадиционный доступ. Примером подобной ситуации является следующее клиническое наблюдение.
Больная К., 19 лет, поступила в отделение хирургии легких и средостения с жалобами на кашель с выделением слизистой мокроты, поперхивание при приеме пищи, одышку при физической нагрузке. С детского возраста состояла на учете у педиатра по поводу врожденной аномалии развития легких. В 1994 г. ей выполнили нижнюю лобэктомию слева с резекцией язычковых сегментов по поводу бронхоэктазов. В период с 1994 по 2007 г. возникали частые обострения воспалительного процесса в легких, по поводу чего неоднократно лечилась в стационаре по месту жительства. При обследовании высказывалось предположение о наличии ТПС, однако при ФЭГДС диагноз не был подтвержден. В 2007 г. состояние больной ухудшилось, усилился кашель, увеличилось количество слизисто-гнойной мокроты. При повторной операции выполнена верхняя лобэктомия слева по типу пневмонэктомии. В сентябре 2011 г. больная вновь отметила ухудшение состояния, прогрессирование одышки, появление кашля с мокротой гнойного характера, поперхивание при приеме пищи. При обследовании по месту жительства был диагностирован ТПС.
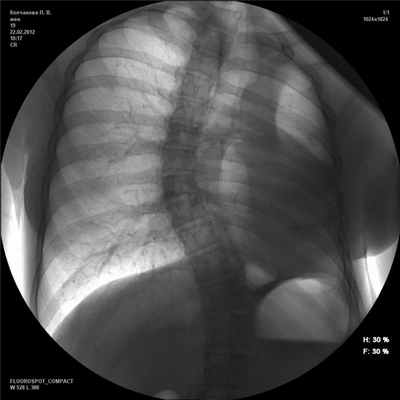
При поступлении общее состояние больной относительно удовлетворительное. Подкожный жировой слой плохо развит. Аускультативно справа выслушивалось жесткое дыхание, хрипов не было. Тоны сердца ясные и ритмичные. Пульс 75 в 1 мин, удовлетворительного наполнения и напряжения. АД 110/70 мм рт.ст. Язык чистый. Живот мягкий, безболезненный. При полипозиционной рентгеноскопии и рентгенографии органов грудной клетки левая половина грудной клетки деформирована и затемнена (рис. 1). Рисунок 1. Рентгенограмма грудной клетки в прямой проекции. Смещение органов средостения влево, легочная грыжа, искривление позвоночника. Отсутствие левого легкого после пневмонэктомии. Тень средостения определялась слева от средней линии. Правое легочное поле было прозрачное, без очаговых и инфильтративных теней. В переднем средостении определялась легочная грыжа. При приеме водорастворимого контрастного вещества в положении больной на правом боку отмечался заброс препарата в трахею на уровне ключиц. Диаметр свищевого хода 5 мм.
При компьютерной томографии (рис. 2) Рисунок 2. Компьютерные томограммы. В шейно-грудном отделе трахеи трахеопищеводный свищ, резкое расширение пищевода, стенка которого истончена (а). Рисунок 2. Компьютерные томограммы. Органы средостения смещены влево после пневмонэктомии (б). диагностирован фиброторакс слева после пневмонэктомии, средостение значительно смещено влево. Определялось трахеопищеводное соустье. На значительном протяжении стенка между трахеей и пищеводом была крайне истончена.
При эндоскопическом исследовании голосовые складки подвижны. Слизистая трахеи и бронхов незначительно отечна и гиперемирована. Культя левого главного бронха была длиной около 3 см без видимых дефектов. В мембранозной части трахеи на расстоянии приблизительно 6 см от голосовых складок и 5 см от карины трахеи имеется отверстие размером 3×5 мм с гладкими краями. Через него эндоскоп свободно проходит в просвет пищевода. Последний не изменен, слизистая гладкая, розовая, блестящая. На расстоянии 20 см от резцов по передней стенке определяется свищевое отверстие диаметром около 3-4 мм, слизистая краев отверстия гладкая, розовая.
Таким образом, диагностирован ТПС с локализацией его устья в шейно-грудном отделе. Неблагоприятными моментами для хирургического лечения были смещение трахеи и пищевода вместе с органами средостения влево, резкое увеличение размеров пищевода с истончением его стенки в результате большого сброса воздуха из дыхательного пути через ТПС, тонкая прослойка тканей между трахеей и пищеводом, что повышало риск их повреждения при выделении соустья. От правосторонней боковой торакотомии отказались из-за высокого расположения ТПС, смещения средостения влево, необходимости выполнения операции через плевральную полость единственного легкого, что могло повлечь нарушение газообмена, а в послеоперационном периоде развитие пневмонии травматического генеза. Подойти к трахее и пищеводу через стернотомию для разделения свища было также затруднительно, так как пришлось бы значительно ротировать трахею для доступа к ее мембранозной стенке. Увеличенный и истонченный пищевод при этом могли легко травмировать. Кроме того, имелся крайне высокий риск повреждения нижних гортанных возвратных нервов. С учетом всего изложенного выше было принято решение в качестве нетрадиционного доступа избрать стернотомию с последующим поперечным пересечением трахеи и мобилизацией пищевода с разобщением свища.
01.03.12 - операция. Произведена цервикотомия по нижней кожной складке, частичная продольно-поперечная стернотомия до уровня третьего межреберья. В рану прилежала большая легочная грыжа. При ее отделении и смещении содержимого в правую плевральную полость медиастинальная плевра была повреждена и произошел пневмоторакс справа. При дальнейшей ревизии установлено, что структуры средостения несколько смещены влево. Выделены и взяты на держалки левая плечеголовная вена и артериальный брахицефальный ствол. Остро и тупо мобилизованы трахея и грудной отдел пищевода, которые были интимно спаяны друг с другом. Стенка пищевода резко истончена, его диаметр превышал размеры трахеи и соответствовал диаметру позвонков, к которым он был интимно припаян. С учетом сложившейся ситуации разделение трахеи и пищевода через трахеопищеводную борозду было сопряжено с риском повреждения пищевода, увеличением размеров свища, повреждением возвратных нервов. В связи с этим принято решение пересечь трахею в поперечном направлении с последующим отделением мембранозной стенки под визуальным контролем. Трахея взята на держалку. С помощью трансиллюминации установлен уровень ТПС. Трахея поперечно пересечена с оставлением участка мембранозной стенки у устья ТПС (рис. 3, а, б). Рисунок 3. Этапы операции. а — трахея пересечена с оставлением участка мембранозной стенки вокруг свища. Рисунок 3. Этапы операции. б — определяется 2 трахеопищеводных свища. В них введен зажим.
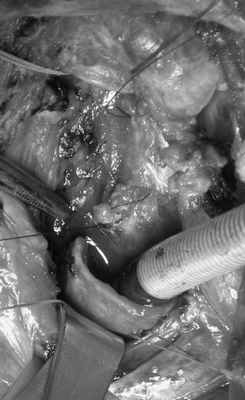
Краниальная культя трахеи отделена от пищевода острым путем. При этом диагностировано второе устье ТПС, которое располагалось на 2-3 см краниальнее первого. Оно было хорошо эпителизировано, без признаков воспаления. В этой зоне трахея и пищевод разделены аналогичным способом с оставлением участка мембранозной стенки трахеи вокруг устья свища. Оба свища ушиты двухрядным швом: первый - с использованием участка мембранозной части трахеи, второй - мышечной оболочки пищевода с погружением в нее первого шва (рис. 3, в). Рисунок 3. Этапы операции. в — дефекты пищевода ушиты двухрядным швом. Интубационная трубка через операционную рану установлена в каудальном отделе трахеи по типу шунт—дыхание.
Для наложения швов использована викриловая нить 3/0 на атравматической игле. После ушивания дефектов пищевода выкроен лоскут из мышц шеи, который отсечен в его краниальной части и ротирован в средостение путем фиксации к передней стенке пищевода отдельными узловыми швами для изоляции его швов. Ввиду образовавшихся дефектов в мембранозной стенке трахеи выполнена ее циркулярная резекция на протяжении около 3,5 см. Целостность дыхательного пути восстановленна с помощью межтрахеального анастомоза по типу конец в конец (рис. 3, г, д). Рисунок 3. Этапы операции. г — целостность мембранозной стенки восстановлена обвивным швом. Рисунок 3. Этапы операции. д — окончательный вид трахеального анастомоза. Мембранозная стенка ушита обвивным викриловым швом, хрящевая - узловыми викриловыми швами. Трахеальный анастомоз изолирован от брахицефального артериального ствола участком вилочковой железы на ножке. Правая плевральная полость дренирована двумя дренажами, средостение - одним дренажем. Грудина фиксирована узловыми стальными швами. После послойного ушивания раны голова больной фиксирована в положении приведения к передней стенке грудной клетки с помощью двух кожных швов.
Послеоперационный период протекал без осложнений. Питание через рот восстановлено на 5-е сутки. Дыхание полностью компенсировано. По данным эндоскопии, трахеальный анастомоз зажил первичным натяжением без признаков стенозирования.
Таким образом, индивидуальный подход в выборе тактики лечения больной с длительно существующим мультифокальным ТПС на фоне дегенеративных изменений пищевода, связанных с его перераздуванием воздухом, после левосторонней пневмонэктомии и смещением органов средостения, позволил выполнить радикальную органосохраняющую операцию с хорошим результатом. Прецизионный транстрахеальный доступ к пищеводу в области локализации ТПС дал возможность минимизировать риск повреждения истонченного пищевода и нижних возвратных гортанных нервов, обеспечить надежное ушивание дефекта пищевода за счет участка мембранозной стенки трахеи и хорошую изоляцию пищеводных швов мышечным лоскутом на питающей ножке. Восстановление целостности дыхательного пути с помощью формирования межтрахеального анастомоза конец в конец в условиях отсутствия натяжения тканей и при соответствующем опыте оперирующего хирурга надежно и минимально рискованно. Представляется, что подобный транстрахеальный доступ также показан при сочетании ТПС и стеноза трахеи, когда патологическое соустье располагается на уровне стенозированного фрагмента дыхательного пути. В таких ситуациях резекция суженного отдела трахеи позволяет подойти к пищеводу спереди, хорошо визуализировать и ушить свищевое отверстие, тем самым излечить больного от сочетанных заболеваний за одну операцию. Приведенное наблюдение показывает, что хирургическое лечение трахеопищеводного свища требует серьезного практического опыта и неклассического мышления оперирующего хирурга.
Мышечный лоскут при трахеопищеводном свище.
Государственное бюджетное учреждение здравоохранения
Тюменской области "Областная клиническая больница №1"
Нам доверяют самое ценное!
К врачам «ОКБ № 1» за помощью едут со всей страны! Торакальные хирурги провели сложнейшую операцию на трахее жительнице Свердловской области.
К врачам «ОКБ № 1» за помощью едут со всей страны! Торакальные хирурги провели сложнейшую операцию на трахее жительнице Свердловской области.
30 Марта 2018
Центр торакальной хирургии «Областной клинической больницы № 1» Тюменской области является одним из ведущих в Российской Федерации с широким спектром лечебных и диагностических хирургических вмешательств. Специалисты - торкальные хирурги Центра успешно оперируют пациентов с заболеваниями органов грудной клетки как «открытым» способом, так и «миниинвазивно» - с применением видеоторакоскопической техники.
В январе 2018 года за помощью к тюменским специалистам обратилась жительница Свердловской области по поводу ухудшения состояния своей матери на фоне трахеопищеводного свища. Восстановительные операции на трахее и пищеводе относятся к категории сложных вмешательств и только несколько клиник нашей страны владеют этой технологией. Специалисты «ОКБ № 1» и медицинской организации Свердловской области на онлайн консилиуме определили показания к хирургическому лечению и 80- летняя пациентка была оперативно доставлена в Тюмень.
Реконструктивную операцию с использованием современного эндоскопического оборудования выполнил Игорь Аркадьевич Бродер, торакальный хирург, заместитель главного врача «ОКБ № 1» по медицинской части. Во время операции необходимо тщательно, не повредив стенки, разделить трахею и пищевод, а затем восстановить их целостность. Важно для профилактики рецидива свища места пластики трахеи и пищевода укрепить мышечным лоскутом на сосудистой ножке. Также важно не допустить ранения сосудов, идентифицировать и сохранить возвратный нерв, обеспечивающий функционирование дыхательной системы, речевого аппарата и акта глотания. Кроме этого, важным является обеспечить стабильное состояние больного во время операции, учитывая возраст и сопутствующую патологию, организовать раннюю послеоперационную реабилитацию. Благодаря опыту многопрофильной бригады врачей операция прошла успешно!
«В декабре прошлого года, у мамы после трахеостомы ухудшилось состояние. Она не могла ни есть, ни дышать нормально. Человек просто тихонько умирал. Врачи нашей больницы подсказали обратиться в Тюмень. Я очень благодарна хирургам и всем врачам «ОКБ № 1» за то, что спасли мою маму, за внимание и отношение к ней!», - написала дочь.
«Трахеопищеводные свищи – это довольно редкая патология. Лечение их исключительно хирургическое, поскольку консервативная тактика абсолютно бесперспективна. Проведение реконструктивных операций на трахее и пищеводе возможно только в многопрофильной клинике, обладающей современным оборудованием, в составе которой есть опытная команда торакальных хирургов, анестезиологов-реаниматологов, диагностов. Именно такой клиникой является «Областная клиническая больница № 1», - рассказал Сергей Евгеньевич Ярцев, главный врач ГБУЗ ТО «ОКБ № 1».
RU2269956C2 - Способ ушивания свища культи главного бронха и бифуркации трахеи - Google Patents
Publication number RU2269956C2 RU2269956C2 RU2003135839/14A RU2003135839A RU2269956C2 RU 2269956 C2 RU2269956 C2 RU 2269956C2 RU 2003135839/14 A RU2003135839/14 A RU 2003135839/14A RU 2003135839 A RU2003135839 A RU 2003135839A RU 2269956 C2 RU2269956 C2 RU 2269956C2 Authority RU Russia Prior art keywords stump flap bronchus main bronchus pleuro Prior art date 2003-12-10 Application number RU2003135839/14A Other languages English ( en ) Other versions RU2003135839A ( ru Inventor с Николай Владимирович Л (RU) Николай Владимирович Ляс Сергей Васильевич Козлов (RU) Сергей Васильевич Козлов Владимир Николаевич Хурнин (RU) Владимир Николаевич Хурнин Олег Борисович Ермаков (RU) Олег Борисович Ермаков Original Assignee Государственное учреждение Самарский государственный медицинский университет Priority date (The priority date is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the date listed.) 2003-12-10 Filing date 2003-12-10 Publication date 2006-02-20 2003-12-10 Application filed by Государственное учреждение Самарский государственный медицинский университет filed Critical Государственное учреждение Самарский государственный медицинский университет 2003-12-10 Priority to RU2003135839/14A priority Critical patent/RU2269956C2/ru 2005-05-20 Publication of RU2003135839A publication Critical patent/RU2003135839A/ru 2006-02-20 Application granted granted Critical 2006-02-20 Publication of RU2269956C2 publication Critical patent/RU2269956C2/ru
Links
- Espacenet
- Global Dossier
- Discuss
- 210000000621 Bronchi Anatomy 0.000 title claims abstract description 20
- 206010016717 Fistula Diseases 0.000 title claims description 3
- 230000003890 fistula Effects 0.000 title claims description 3
- 210000003437 Trachea Anatomy 0.000 claims description 11
- 238000002271 resection Methods 0.000 claims description 5
- 238000001356 surgical procedure Methods 0.000 abstract description 5
- 239000003814 drug Substances 0.000 abstract description 3
- 230000000694 effects Effects 0.000 abstract description 2
- 239000000126 substance Substances 0.000 abstract 1
- 210000003205 Muscles Anatomy 0.000 description 5
- 210000004224 Pleura Anatomy 0.000 description 4
- 208000007026 Bronchial Fistula Diseases 0.000 description 3
- 210000003516 Pericardium Anatomy 0.000 description 3
- 210000003281 Pleural Cavity Anatomy 0.000 description 3
- 210000000683 Abdominal Cavity Anatomy 0.000 description 2
- 210000001367 Arteries Anatomy 0.000 description 2
- 210000004072 Lung Anatomy 0.000 description 2
- 206010037844 Rash Diseases 0.000 description 2
- 230000002980 postoperative Effects 0.000 description 2
- 206010061218 Inflammation Diseases 0.000 description 1
- 206010056720 Muscle mass Diseases 0.000 description 1
- 210000002747 Omentum Anatomy 0.000 description 1
- 210000000062 Pectoralis major Anatomy 0.000 description 1
- 210000003105 Phrenic Nerve Anatomy 0.000 description 1
- 210000000614 Ribs Anatomy 0.000 description 1
- 206010043183 Teething Diseases 0.000 description 1
- 210000003462 Veins Anatomy 0.000 description 1
- 230000002421 anti-septic Effects 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- 238000003745 diagnosis Methods 0.000 description 1
- 238000007865 diluting Methods 0.000 description 1
- 238000002224 dissection Methods 0.000 description 1
- 229940079593 drugs Drugs 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 230000023597 hemostasis Effects 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 230000001483 mobilizing Effects 0.000 description 1
- 210000001519 tissues Anatomy 0.000 description 1
- 230000036346 tooth eruption Effects 0.000 description 1
Abstract
Изобретение относится к медицине, а именно к хирургии, и может быть применимо для ушивания свища культи главного бронха и бифуркации трахеи. Производят торакотомию. Мобилизуют культю главного бронха. Производят ререзекцию культи. Выкраивают плевроперикардиальный лоскут на питающей ножке П-образной формы, основанием обращенный краниально. Укладывают лоскут плевральной стороной к бронху. Фиксируют лоскут перикардо-плевро-бронхо-бронхо-плевро-перикардиальными швами. Способ позволяет предотвратить несостоятельность швов.
Description
Известен способ закрытия бронхиальных свищей после пульмонэктомии мышечным лоскутом на ножке с использованием широчайшей мышцы спины, большой грудной мышцы, ромбовидной мышцы и других мышц (1).
Недостатком данного способа является травматичность операции, так как способ сопровождается рассечением больших мышечных массивов, отслоением мышц, резекцией ребер.
Недостатком способа является необходимость одновременного вскрытия брюшной полости и инфицированной плевральной полости.
Известен способ ушивания свища культи главного бронха и бифуркации трахеи путем торакотомии, мобилизации культи главного бронха, ререзекции культи, закрытия дефекта в бронхе или в шве бифуркации трахеи сшиванием медиастинальной плевры над культей реампутированного бронха (3).
Недостатком данного способа является высокая вероятность прорезывания швов на измененной вследствие воспаления стенке бронха или трахеи, что является причиной низкой эффективности лечения.
Эта цель достигается тем, что в качестве аутоткани используют плевроперикардиальный лоскут на питающей "ножке", а укрытие дефекта в бронхе или в бифуркации трахеи производят перикардо-плевро-бронхо-бронхо-плевро-перикардиальными швами.
Выполняют реторакотомию путем снятия послеоперационных швов и разведения раны реберным ранорасширителем.
Мобилизуют культю главного бронха, бифуркацию трахеи, противоположный главный бронх и нижнюю часть трахеи.
На перикарде намечают линию разреза с учетом хода перикардиально-диафрагмальной артерии и ее ветвей (сохраняют на лоскуте питающие сосуды).
На уровне дистальной границы лоскута на зажимах рассекают и дважды перевязывают сосудисто-нервный пучок (перикардиально-диафрагмальные артерия, вена и диафрагмальный нерв).
По намеченной линии ножницами на всю толщину (медиастинальная плевра с сосудами и перикард) выкраивают П-образный лоскут, основанием обращенный краниально.
Атравматической иглой накладывают провизорные швы через всю толщину бронха, отступя от края дефекта по 4-5 мм. Расстояние между стежками около 6 мм. Дополнительно по одному - два шва накладывают в пределах здоровых тканей. Нити берут на зажимы.
Швы последовательно завязывают, закрывая плевроперикардиальным лоскутом культю главного бронха или линию шва бифуркации трахеи.
Больной Е. 56 лет поступил в торакальное отделение Самарского областного онкологического диспансера 05.06.2002 г. с диагнозом: Центральный рак левого легкого с поражением главного бронха. 18.06.2002 г. Операция: Расширенная комбинированная пульмонэктомия с клиновидной резекцией бифуркации трахеи. 19.06.2002 г. у больного клинико-рентгенологическая картина несостоятельности шва трахеи. Экстренно взят в операционную. При реторакотомии и ревизии выявлено прорезывание двух швов трахеи - дефект до 6 мм в диаметре. Выполнено ушивание дефекта плевроперикардиальным лоскутом на питающей ножке перикардо-плевро-бронхо-бронхо-плевро-перикардиальными швами. Послеоперационный период без особенностей. Выписан 12.07.2002 г. в удовлетворительном состоянии.
Положительный эффект от использования предложенного способа выражается в возможности лечения таких осложнений пульмонэктомии, как несостоятельность шва культи главного бронха или несостоятельность шва бифуркации трахеи.
Способ целесообразно использовать в торакальных отделениях при развитии таких осложнений пульмонэктомии, как несостоятельность шва культи главного бронха или несостоятельность шва бифуркации трахеи.
1. Хирургия легких и плевры. Под редакцией И.С.Колесникова и М.И.Лыткина - Ленинград, Медицина, 1988, 224 с.
2. Хирургическое лечение бронхиальных свищей после пневмонэктомии. А.А.Полежаев, А.Ф.Малышев, В.В.Кулик, О.Н.Булатова. - Хирургия. Журнал им. Н.И.Пирогова №11, 1999, 38 с.
3. Трахеобронхиальная хирургия. Б.В.Петровский, М.И.Перельман, Н.С.Королева - М., Медицина, 1978, 263 с., 267 с.
Claims ( 1 )
Способ ушивания свища культи главного бронха и бифуркации трахеи, включающий торакотомию, мобилизацию культи главного бронха, ререзекцию культи, выкраивание плевроперикардиального лоскута на питающей ножке, закрытие дефекта лоскутом и ушивание раны, отличающийся тем, что выкраивают лоскут П-образной формы, основанием обращенный краниально, укладывают лоскут плевральной стороной к бронху, фиксируют лоскут перикардо-плевро-бронхо-бронхо-плевро-перикардиальными швами.
RU2003135839/14A 2003-12-10 2003-12-10 Способ ушивания свища культи главного бронха и бифуркации трахеи RU2269956C2 ( ru )
СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ТРАХЕОПИЩЕВОДНЫХ СВИЩЕЙ НЕОПУХОЛЕВОГО ГЕНЕЗА
Изобретение относится к области медицины, а именно к хирургии, и может быть использовано при лечении трахеопищеводных свищей неопухолевого генеза.
Наиболее близким к предлагаемому (прототипом) является способ радикальной операции по поводу свища пищевода и дыхательных путей, включающий выделение, иссечение или рассечение свищевого хода, раздельное ушивание отверстий трахеи и пищевода [2]. Недостатки способа связаны с риском несостоятельности швов на пищеводе и трахее в ранние сроки после операции с развитием медиастинита или рецидива свища. К этому предрасполагает неизбежное инфицирование области вмешательства в результате вскрытия просвета трахеи и пищевода, нарушение кровоснабжения разобщенных трахеи и пищевода, техническая сложность ушивания образующихся дефектов, а также неравномерная компрессия тканей по линии шва, проникновение швов через слизистую оболочку в просвет трахеи и пищевода, что нарушает биологическую герметичность шва и условия для первичного заживления. Кроме того, вследствие выраженных воспалительных изменений в области шва существует риск развития стеноза трахеи и пищевода в отдаленном периоде. Для предупреждения несостоятельности швов на трахее и пищеводе в дополнение к способу рекомендовано разобщение линии швов этих органов путем ротирования пищевода вокруг своей оси или укрытие швов ауто-, ксено- или аллотрансплантатом и их обязательное подшивание по линии шва и вокруг них. В качестве пластического укрывающего материала применяются мышечный лоскут на питающей ножке (лоскут грудино-щитовидной, грудино-подъязычной, большой грудной, межреберных, грудино-ключично-сосцевидной мышцы, лоскут диафрагмы и др.) [2, 3, 4], бычий перикард, политетрафторэтилен («Gore-Тех») [5].
Новая техническая задача - упрощение действий хирурга и сокращение продолжительности операции, повышение ее состоятельности.
Отсутствие в мировой литературе и в патентно-информационных источниках решений со сходной совокупностью существенных признаков свидетельствует о соответствии предложения авторами критериям «новизна» и «изобретательский уровень». Изобретение иллюстрируется схемами выполнения конкретных приемов и примерами отдельных операций в эксперименте.
На иллюстрациях представлено:
Фиг.1. Формирование и перемещение лоскута большого сальника на питающей ножке в грудную полость: 1 - лоскут большого сальника со свободным краем U-образной формы, 2 - тракционные лигатуры, 3 - трахея, 4 - пищевод, 5 - диафрагма.
Фиг.2. Подведение при помощи двух лигатур жирового лоскута на питающей ножке со свободным краем U-образной формы к свищу: 2 - тракционные лигатуры, 6 - трахеопищеводный свищ.
Фиг.3. Фиксирование лигатурами жирового лоскута на уровне свища. Схема поперечного среза на уровне свища.
Фиг.4. Установка компрессионной клипсы (7). Схема поперечного среза на уровне свища.
Фиг.5. Вид клипсы, укрытого жировым лоскутом трахеопищеводного свища, дренажа: 7 - бранши клипсы, 8 - дренажная трубка.
Проверочным тестом достижимости технического результата является экспериментальная апробация предлагаемого способа хирургического лечения трахеопищеводных свищей неопухолевого генеза, смоделированных на 8 беспородных собаках массой тела 10-16 кг. Эксперименты на животных выполнены в отделе экспериментальной хирургии Центральной научно-исследовательской лаборатории СибГМУ. Исследование проводили согласно этическим принципам, изложенным в "Европейской конвенции по защите позвоночных животных, используемых для экспериментальных и других научных целей", все манипуляции и выведение животных из опытов проводили под общей анестезией. В послеоперационном периоде проводилось клиническое наблюдение, рентгенологический, эндоскопический контроль, гистологическое исследование препаратов.
Пример 1 (беспородная собака массой тела 16 кг с предварительно сформированным трахеопищеводным свищом на уровне шеи). После обработки операционного поля йодом и спиртом под общей анестезией с управляемым дыханием выполнили цервикотомию, осуществили доступ к сформированному трахеопищеводному свищу, разделили трахею и пищевод на уровне свища, выделили свищ, сформировали лоскут из жировой клетчатки переднего средостения на питающей ножке со свободным краем U-образной формы. После формирования лоскута необходимой длины его прошили за свободные края двумя обвивными лигатурами и тракцией за них подвели лоскут в боковое пространство между трахеей и пищеводом на уровне трахеопищеводного свища (фиг.2), осуществили укрытие свищевого хода и фиксацию лоскута, связывая лигатуры между собой (фиг.3), свободные концы лигатур срезали. Развели бранши предварительно охлажденной клипсы из никелида титана с эффектом памяти формы и сверхэластичности, выполненной в виде двухвитковой продолговатой проволочной спирали, сомкнутой по всей длине, с симметричным расположением свободных концов проволоки у первого конца спирали, причем обе ветви каждого витка спирали на преобладающей длине в сторону второго конца спирали спрямлены и сближены до взаимного касания для образования линейных бранш [5], прикрепленной дистальным концом к тракционной нити, и установили клипсу на жировой лоскут в проекции свищевого хода (фиг.4). После нагревания от окружающих тканей и смыкания бранш клипсы произошло пережатие свища и фиксация лоскута жировой клетчатки. Свободный конец тракционной нити провели наружу через просвет дренажной трубки (фиг.5). Установили дренажную трубку к области вмешательства и вывели через отдельный разрез на шею. Операционную рану послойно ушили. Удаление клипсы произвели через 8 суток после оперативного вмешательства тракцией за нить. Дренажную трубку удалили через сутки после извлечения клипсы.
Пример 2 (беспородная собака массой тела 14 кг с предварительно сформированным трахеопищеводным свищом на уровне шеи). После обработки операционного поля йодом и спиртом под общей анестезией с управляемым дыханием выполнили цервикотомию, осуществили доступ к сформированному трахеопищеводному свищу, разделили трахею и пищевод на уровне свища, выделили свищ. Выполнили лапаротомию, сформировали дефект в диафрагме и лоскут большого сальника на питающей ножке со свободным краем U-образной формы (фиг.1). После формирования лоскута необходимой длины его прошили за свободные края двумя обвивными лигатурами и тракцией за них через сформированное отверстие в диафрагме, переместили в переднее средостение и далее на шею, уложили лоскут в боковое пространство между трахеей и пищеводом на уровне трахеопищеводного свища (фиг.2), осуществили укрытие свищевого хода и фиксацию лоскута, связывая лигатуры между собой (фиг.3), свободные концы лигатур срезали. Развели бранши предварительно охлажденной клипсы из никелида титана с эффектом памяти формы и сверхэластичности, выполненной в виде двухвитковой продолговатой проволочной спирали, сомкнутой по всей длине, с симметричным расположением свободных концов проволоки у первого конца спирали, причем обе ветви каждого витка спирали на преобладающей длине в сторону второго конца спирали спрямлены и сближены до взаимного касания для образования линейных бранш [5], прикрепленной дистальным концом к тракционной нити, и установили клипсу на лоскут жировой клетчатки в проекции свищевого хода (фиг.4). После нагревания от окружающих тканей и смыкания бранш клипсы произошло пережатие свища и фиксация лоскута жировой клетчатки. Свободный конец тракционной нити провели наружу через просвет дренажной трубки (фиг.5). Установили дренажную трубку к области вмешательства и вывели через отдельный разрез на шею. Операционные раны послойно ушили. Удаление клипсы произвели через 10 суток после оперативного вмешательства тракцией за нить. Дренажную трубку удалили через сутки после извлечения клипсы.
Результаты экспериментальной апробации подтверждают работоспособность предлагаемого способа и достижимость технического результата. Готовность операции к клиническому применению свидетельствует о соответствии предложения критерию «промышленно применимо».
Таким образом, предлагаемый способ позволяет упростить и сократить продолжительность операции, повысить ее состоятельность.
1. Пат. 2202961, МПК 7 А61В 17/00. Способ хирургического лечения приобретенных трахеопищеводных свищей / М.Б.Скворцов, Е.В.Нечаев, В.В.Дроков. №2000116538; Заявлено 21.06.2000; Опубл. 27.04.2003, Бюл. №18, Приоритет 21.06.2000 (Россия). 6 с.
2. Трахео-бронхиальная хирургия / Б.В.Петровский, М.И.Перельман, Н.С.Королева. М.: 1978. - С.254-257.
3. Sokolov V.V., Bagirov M.M. Reconstructive surgery for combined tracheoesophageal injuries and their sequelae // Eur. J.Cardiothorac. Surg. 2001; 20: 1025-1029.
4. Bardini R., Radicchi V., Parimbelli P. et al. Repair of a recurrent bening tracheoesophageal fistula with a Gore-tex membrane // Ann. Thorac. Surg. 2003; 76: 304-6.
5. Пат. 2285468, МПК 7 A61B 17/11, A61B 17/122. Клипса для анастомоза полых органов / Г.Ц.Дамбаев, В.Э.Гюнтер, М.М.Соловьев и др. №2005103056; Заявлено 07.02.2005; Опубл. 20.10.2006, Бюл. №29, Приоритет 07.02.2005 (Россия). 8 с.
Читайте также:
