Показания для портокавального шунтирования при портальной гипертензии
Добавил пользователь Alex Обновлено: 29.01.2026
Цель: оптимизировать тактику ведения пациентов с циррозом печени, подвергшихся трансъюгулярному внутрипеченочному портосистемному шунтированию, на основании анализа собственного опыта и сведений из литературы.
Материал и методы. С 2014 по 2019 г. выполнено 51 трансъюгулярное внутрипеченочное портосистемное шунтирование.
Результаты. Уточнены показания к оперативному вмешательству, тактика ведения пациентов в периоперационном периоде, рассмотрены ранние и отдаленные результаты оперативного лечения, в том числе у лиц, включенных в лист ожидания трансплантации печени.
Заключение. Миниинвазивная операция позволяет добиться стойкой декомпрессии в системе воротной вены, уменьшить частоту рецидивов кровотечения из варикозно расширенных вен пищевода и желудка и летальность, помогает ряду больных дождаться трансплантации печени.
Ключевые слова
Об авторах
ФГБОУ ВО “Кубанский государственный медицинский университет” МЗ РФ, кафедра хирургии №3, факультет повышения квалификации и профессиональной переподготовки специалистов; ГБУЗ “Краевая клиническая больница №2” МЗ Краснодарского края
Россия
Дурлештер Владимир Моисеевич – доктор мед. наук, профессор, заведующий кафедрой хирургии №3 ФГБОУ ВО КубГМУ;
заместитель главного врача по хирургии ГБУЗ ККБ №2
350063, Краснодар, ул. Седина, д. 4;
350012, Краснодар, ул. Красных Партизан, д. 6/2
ФГБОУ ВО “Кубанский государственный медицинский университет” МЗ РФ, кафедра хирургии №3, факультет повышения квалификации и профессиональной переподготовки специалистов; ГБУЗ “Краевая клиническая больница №2” МЗ Краснодарского края
Россия
Габриэль Сергей Александрович – доктор мед. наук, главный врач ГБУЗ ККБ №2;
профессор кафедры хирургии №3 ФГБОУ ВО КубГМУ;
350063, Краснодар, ул. Седина, д. 4;
350012, Краснодар, ул. Красных Партизан, д. 6/2
ФГБОУ ВО “Кубанский государственный медицинский университет” МЗ РФ, кафедра хирургии №3, факультет повышения квалификации и профессиональной переподготовки специалистов; ГБУЗ “Краевая клиническая больница №2” МЗ Краснодарского края
Россия
Корочанская Наталья Всеволодовна – доктор мед. наук, руководитель гастроэнтерологического центра ГБУЗ ККБ №2;
профессор кафедры хирургии №3 ФГБОУ ВО КубГМУ
350063, Краснодар, ул. Седина, д. 4;
Бухтояров Артем Юрьевич – заведующий отделением рентгенохирургических методов диагностики и лечения №2
350012, Краснодар, ул. Красных Партизан, д. 6/2
ФГБОУ ВО “Кубанский государственный медицинский университет” МЗ РФ, кафедра хирургии №3, факультет повышения квалификации и профессиональной переподготовки специалистов; ГБУЗ “Краевая клиническая больница №2” МЗ Краснодарского края
Россия
Марков Павел Викторович – доктор мед. наук, заведующий хирургическим отделением №5 ГБУЗ ККБ №2;
профессор кафедры хирургии №3 ФГБОУ ВО КубГМУ
350063, Краснодар, ул. Седина, д. 4;
350012, Краснодар, ул. Красных Партизан, д. 6/2
ФГБОУ ВО “Кубанский государственный медицинский университет” МЗ РФ, кафедра хирургии №3, факультет повышения квалификации и профессиональной переподготовки специалистов; ГБУЗ “Краевая клиническая больница №2” МЗ Краснодарского края
Россия
Мурашко Дмитрий Сергеевич – канд. мед. наук, врач-хирург хирургического отделения №5 ГБУЗ ККБ №2;
ассистент кафедры хирургии №3 ФГБОУ ВО КубГМУ
350063, Краснодар, ул. Седина, д. 4;
350012, Краснодар, ул. Красных Партизан, д. 6/2
Оганесян Оганес Арамович – врач отделения рентгенохирургических методов диагностики и лечения №2
350012, Краснодар, ул. Красных Партизан, д. 6/2
Измайлова Лаура Геннадьевна – канд. мед. наук, врач ультразвуковой диагностики отделения рентгенохирургических методов диагностики и лечения №1
350012, Краснодар, ул. Красных Партизан, д. 6/2
ФГБОУ ВО “Кубанский государственный медицинский университет” МЗ РФ, кафедра хирургии №3, факультет повышения квалификации и профессиональной переподготовки специалистов
Россия
Басенко Михаил Андреевич – клинический ординатор кафедры хирургии №3
350063, Краснодар, ул. Седина, д. 4
Хоронько Юрий Владиленович – доктор мед. наук, профессор, заведующий кафедрой оперативной хирургии и топографической анатомии, врач-хирург
344022, Ростов-на-Дону, Нахичеванский пер., д. 29
Список литературы
2. Анисимов А.Ю., Верткин А.Л., Девятов А.В., Дзидзава И.И., Жигалова С.Б., Затевахин И.И., Ивашкин В.Т., Киценко Е.А., Котив Б.Н., Лебезев В.М., Лопаткина Т.Н., Маевская М.В., Манукьян Г.В., Монахов Д.В., Назыров Ф.Г., Огурцов П.П., Павлов Ч.С., Прудков М.И., Хоронько Ю.В., Цициашвили М.Ш., Чжао А.В., Шерцингер А.Г., Шиповский В.Н. Клинические рекомендации по лечению кровотечений из варикозно расширенных вен пищевода и желудка (приняты на Общероссийской согласительной конференции по принятию Национальных клинических рекомендаций “Кровотечение из верхних отделов желудочно-кишечного тракта”, г. Воронеж, 5–6 июня 2014 г. Российское общество хирургов, Ассоциация гепатопанкреатобилираных хирургов стран СНГ). М. – Воронеж, 2014. 46 с.
4. Киценко Е.А., Анисимов А.Ю., Андреев А.И. Современное состояние проблемы кровотечений из варикозно расширенных вен пищевода и желудка. Вестник современной клинической медицины. 2014; 7 (5): 89–98.
8. Дурлештер В.М., Бухтояров А.Ю., Чехоев С.В., Лясковский К.О., Никитин С.П. Использование коронарной техники при операциях трансъюгулярного внутрипеченочного портосистемного шунтирования. Научный вестник здравоохранения Кубани. 2016; 48 (6): 36–43.
21. Dunne P., Sinha R., Stanley A., Lachlan N., Ireland H., Shams A., Hayes P. OTU-09 use of early-TIPSS in patients with oesophageal variceal bleeding, a UK dual-centre randomised control trial. Gut. 2019; 68 (Suppl 2): A106–107.
26. Stefánková J., Hulek P., Babu A., Cermáková E., Safka V., Stefanek J., Fejfar T., Krajina A. Hepatic encephalopathy due to TIPS-retrospective study. Hepatogastroenterology. 2007; 54 (74): 480–484.
31. ter Borg P.C., Hollemans M., Van Buuren H.R., Vleggaar F.P., Groeneweg M., Hop W.C., Laméris J.S. Transjugular intrahepatic portosystemic shunts: long-term patency and clinical results in a patient cohort observed for 3–9 years. Radiology. 2004; 231 (3): 537–545.
Показания для портокавального шунтирования при портальной гипертензии
Показания для портокавального шунтирования при портальной гипертензии
В наше время большинство больных с заболеванием печени, портальной гипертензией и кровотечением из варикозных вен пищевода лечат без операции: склеротерапией или перевязкой варикозных узлов. Другим пациентам, с далеко зашедшим поражением печени и отсутствием резервов у этого органа, производят его трансплантацию.
Кроме того, внедрение трансъюгулярного внутрипечёночного портосистемного шунтирования искоренило необходимость в экстренных хирургических вмешательствах при кровотечениях из варикозных вен пищевода, не поддающихся склеротерапии и перевязке варикозных узлов. Несмотря на то, что трансъюгулярное внутрипечёночное портосистемное шунтирование не предназначено для создания длительно проходимых портосистемных шунтов, у многих больных эта процедура позволяет немедленно взять под контроль портальную гипертензию, а эффект её сохраняется длительное время.
Всё же остаётся небольшая группа больных с портальной гипертензией и кровотечениями из вен пищевода, периодически повторяющимися, несмотря напроведение склеротерапии и перевязку узлов, печень которых ещё сохранила резервы, потому им не показана пересадка печени. Эти больные — кандидаты для мезентерико-системного венозного шунтирования. Кроме того, редкую форму портальной гипертензии — синдром Бадда-Киари — в некоторых случаях считают показанием для мезентерико-системного венозного шунтирования.
Несмотря на то, что мезентерико-системное шунтирование выполняют уже несколько десятилетий и его результаты давно обсуждают исследователи, не существует единого мнения о том, какой вид анастомоза оптимален. Первыми из успешно выполняемых были портокавальные анастомозы «конец в бок» и «бок в бок». Редко применяемые в наши дни, они, тем не менее, имеют своих приверженцев.
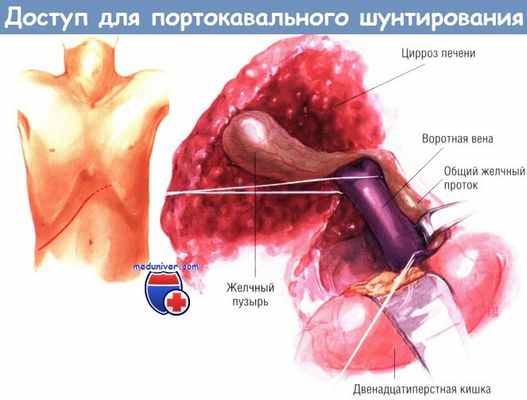
Портокавальный шунт «конец в бок» можно сформировать достаточно быстро и с небольшой кровопотерей. Этот шунт противопоказан больным с асцитом, резистентным к терапии, поскольку такая операция не снижает давление в синусоидах. Однако если у больного нет асцита, а по данным ангиографии у него обнаружен ретроградный кровоток по воротной вене, такой шунт теоретически имеет преимущества. Частота энцефалопатии после портокавального шунтирования «конец в бок» значительна, однако, скорее всего, она возникает реже, чем при шунтировании «бок в бок».
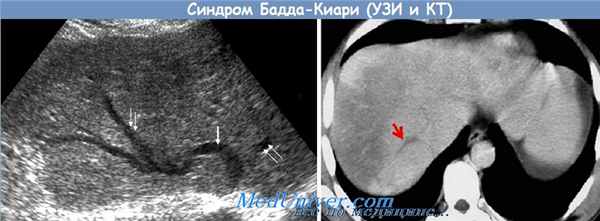
Хотя приток крови к печени по воротной вене после шунтирования «конец в бок» нарушается, всё же ретроградного кровообращения по воротной вене не возникает. Многие хирурги считают, что портокавальный шунт «конец в бок» вызывает энцефалопатию реже, чем анастомоз «бок в бок», и что существуют теоретические предпосылки для его выполнения у больных, имевших ретроградный кровоток по воротной вене до операции.
Портокавальный шунт «бок в бок» можно применить при асците, не поддающемся иной терапии. Он не только снижает давление в брыжеечных венах, но и превращает воротную вену в путь для оттока крови от печени, в результате чего снижается давление в синусоидах и прекращается выделение асцитической жидкости. Техника его наложения более сложна; нередко для сопоставления воротной вены и нижней полой вены необходима частичная резекция хвостатой доли печени. Некоторые хирурги также считают, что портокавальный шунт «бок в бок» — операция выбора при синдроме Бадда-Киари — редкой форме портальной гипертензии, возникающей при тромбозе печёночных вен.
Однако, поскольку при синдроме Бадда-Киари хвостатая доля обычно гипертрофирована, создание такого шунта может быть технически сложным, потому при шунтировании нередко необходима частичная резекция этой доли печени.
Самый современный из портокавальных анастомозов — Н-образный шунт, его создают путём интерпозиции сосудистого протеза между воротной и нижней полой венами. Приверженцы этой операции утверждают, что при достаточно малом диаметре протеза шунт работает селективно, сохраняя центробежный кровоток по воротной вене в сторону печени. Если протез, соединяющий воротную и нижнюю полую вену, имеет малый диаметр, тогда давление в портальной системе снижается умеренно, однако в большинстве случаев этого достаточно для предупреждения кровотечений из варикозных вен пищевода.
Возможны ранние тромбозы Н-образных шунтов, однако при таких осложнениях возможно успешное проведение тромболитической терапии через катетеры, установленные рентген-хирургами в нижнюю полую или воротную вену (чрескожным чреспечёночным доступом), обеспечивающее длительную проходимость анастомоза.
Важно подчеркнуть, что существование любого портокавального шунта значительно увеличивает трудности при трансплантации печени. Исключение составляет мезокавальный шунт, находящийся на достаточном удалении от ворот печени и потому легко лигируемый во время трансплантации печени. Независимо от того, какой шунт предполагают создать, больным до операции необходимо выполнить катетеризацию печёночных вен, поскольку давление в воротной вене можно высчитать по давлению заклинивания в печёночных венах. В прошлом также выполняли ангиографию брыжеечных вен, однако после внедрения MPT-ангиографии и трёхмерной РКТ изображения вен брыжейки стали получать неинвазивным путём.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Трансъюгулярное внутрипеченочное портосистемное шунтирование (TIPS)
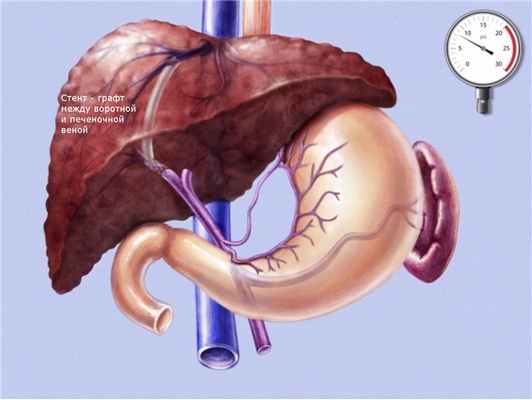
Трансюгулярное внутрипеченочное портосистемное стентирование (TIPS) представляет собой эндоваскулярную операцию по созданию искусственного канала в печени, который обеспечивает отток крови из воротной вены в нижнюю полую вену, минуя пораженную печеночную ткань.
Операция эффективно останавливает кровотечения из варикозных вен пищевода и уменьшает асцит, за счет снижения давления в воротной вене, которое всегда повышено при циррозе печени.
Операция проводится в рентгеноперационной под контролем ангиографии. Во время вмшетельства используются контрастные вещества и ультразвуковое сканирование печени. Средняя продолжительность вмешательства около 2 часов.
Подготовка и обследование для TIPS
Для определения вида портальной гипертензии необходимо выполнить визуализацию структуры печени, проходимость вен воротной системы и определить степень портальной гипертензии и ее риски.
Необходимые методы диагностики:
- УЗИ внутренних органов живота (печени, селезенки, поджелудочной железы) - дают возможность оценить степень поражения печени, выявить опухоли печени и поджелудочной железы, увеличение селезенки.
- УЗИ воротной вены позволяет получить общую информацию о размере и проходимости воротной вены.
- МРТ внутренних органов и вен брюшной полости - в сосудистом режиме позволяет оценить проходимость воротной вены
- Компьютерная томография с ангиографией аорты и венозной фазы - позволяет получить общую оценку воротной системы и варикозных вен в брюшной полости
- Прямая портография (чрезпеченочное введение катетера и контрастирование воротной системы) - заключительный метод диагностики перед вмешательством.
Анестезиологическая поддержка
- За неделю до операции мы переводим пациентов на диету с ограничением белковых продуктов. Это делается для того, чтобы избежать развития энцефалопатии в раннем послеоперационном периоде.
- Накануне вмешательства даются слабительные препараты и ставится очистительная клизма, дается легкий ужин.
- Операция проводится под местной анестезией мест проколов. Анестезиолог присутствует в операционной, для контроля за жизненно-важными функциями организма.
- Пациенту устанавливается мочевой катетер и монитор для измерения артериального давления и снятия ЭКГ.
Как проходит операция
Трансюгулярное внутрипеченочное портосистемное шунтирование проводится под рентгеноскопическим контролем с использованием ультразвукового сканирования для контроля доступов к сосудам.
Доступ к печеночной вене осуществляется через внутреннюю яремную вену на шее. Для облегчения доступа используется ультразвуковой контроль. После пункции устанавливается проводник и интродьюсер. Проводник с катетером проводятся в нижнюю полую и печеночную вену. После установки катетера в печеночной вене измеряется давление прямым методом, чтобы рассчитать в последующем градиент.
Для поиска ветви воротной вены может использоваться УЗИ навигация, либо проводится пункция печени под УЗИ контролем и проводится контрастное исследование портальной системы с использованием функции roadmap.
После определения целевой воротной вены через катетер в печеночной вене проводится пункция специальной иглой. Проведя последнюю в воротную вену через нее устанавливают проводник и проводят катетер. Проводится контрастирование воротной системы через яремный катетер и замеряется давление в воротной системе.
Через паренхиму печени по проводнику проводится баллон, который затем раздувается создавая канал в печеночной ткани. После извлечения баллона по проводнику проводится специальный стент-графт, представляющий собой трубчатую металлическую сетку покрытую внутри специальным герметичным пластиком.
Таким образом, мы соединяем прямым шунтом воротную и печеночную вену, что способствует снижению давления в воротной системе и предупреждает рецидивы кровотечения.
После измерения давления в воротной системе все инструменты удаляются, а пациент помещается в палату наблюдения.
Возможные осложнения
В руках опытного хирурга частота опасных осложнений составляет менее 1%. Очень редко может развиться внутрибрюшное кровотечение или абсцесс печени.
Чаще встречаются осложнения, связанные с успехом процедуры. Прямой поток крови из кишечника может привести к увеличению поступления в системный кровоток азотистых шлаков и развитие энцефалопатии. Проявления энцефалопатии (тремор, бессоница, спутанность сознания) наблюдаются у 25% прооперированных пациентов, однако у большинства пациентов эти симптомы проходят в течение недели после операции. Для предупреждения энцефалопатии необходимо уменьшить потребление белковой пищи.
Недостаточность кровоснабжения печени - ишемический гепатит является более редким осложнением, так как при портальной гипертензии основное кровообращение печень получает за счет печеночной артерии. Однако в некоторых случаях, создание шунта может вызвать ишемическое повреждение печени с острой печеночной недостаточностью, что может потребовать срочного закрытия шунта.
Редким, но серьезным осложнением является развитие инфекционного процесса в зоне вмешательства, то есть нагноения стент-графта. Для предупреждения подобного осложнения в послеоперационном периоде применяются сильные антибиотики.
Прогноз после TIPS
Важно понимать, что портокавальные анастомозы не лечат цирроз печени, но устраняют опасные для жизни осложнения. Пациенты с функционирующим шунтом имеют меньший риск умереть от желудочно-кишечного кровотечения, однако сохраняется риски связанные с печеночной недостаточности.
В целом TIPS позволяет избежать преждевременного неблагоприятного исхода связанного с кровотечениеми и часто применяется как предварительное вмешательство перед пересадкой печени.
Наблюдение после операции
Контроль за функцией шунта осуществляется как с помощью прямых методов визуализации, так и косвенных.
Из косвенных признаков важным является уменьшение диаметра вен в подслизистом слое перехода из пищевода в желудок. Это позволяет иметь уверенность, что рецидива кровотечения не будет. ЭГДС мы рекомендуем выполнять через неделю и через месяц после вмешательства, а затем раз в 6 месяцев.
При ультразвуковом сканировании отмечается кровоток по шунту и определяется его скорость. Оценивается диаметр воротной вены и размеры селезенки. Так же можно отметить уменьшение асцита. УЗИ рекомендуем выполнять каждые 3 месяца у нашего специалиста.
Через год после вмешательства мы рекомендуем выполнить МСКТ ангиографию брюшной полости с оценкой венозной фазы. При этом хорошо выявляется функционирующий стент.
Метод TIPS в Инновационном сосудистом центре
Сосудистые хирурги Инновационного сосудистого центра с 2004 года занимались проблемой лечения осложнений портальной гипертензии, выполняя открытые портокавальные вмешательства. С 2011 года в нашей клинике появилась возможность выполнять эндоваскулярные операции взамен более опасных открытых вмешательств.
Для операций TIPS мы берем пациентов с печеночной формой портальной гипертензии и осложненной тяжелым варикозным расширением вен пищевода, либо уже после состоявшегося пищеводного кровотечения. После обследования мы принимаем решение о виде оперативного вмешательства.
Трансъюгулярное внутрипеченочное портосистемное шунтирование (TIPS)
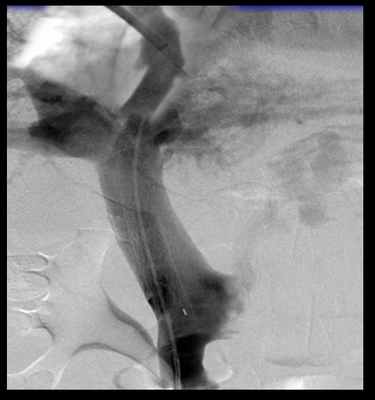
Одним из грозных осложнений цирроза печени является развитие синдрома портальной гипертензии, характеризующегося повышением давления в системе воротной вены.
При декомпенсированной форме портальной гипертензии развиваются варикозное расширение вен пищевода, желудка, спленомегалия и асцит.
Одной из последних новаторских технологий в лечении портальной гипертензии, асцитического синдрома, кровотечения из варикозных вен нижней трети пищевода и желудка, внедренных в отделении рентгенхирургических методов диагностики и лечения ФГБУ «Клиническая больница № 1» явилась эндоваскулярная операция - трансъюгулярное интрапеченочное портокавальное шунтирование (TIPSS).
Данная операция позволяет выполнить эффективную декомпрессию портальной системы, профилактику развития рецидивирующих кровотечений из варикозно расширенных вен пищевода и желудка, асцитический синдром, и значительно улучшает качество жизни пациентов. ТИПС является альтернативой хирургическим методам лечения портальной гипертензии и имеет ряд преимуществ перед достаточно травматичными хирургическими шунтирующими операциями.
Операцию ТИПС часто применяют как поддерживающую, восстанавливающую перед пересадкой печени пациентам с циррозом печени в стадии C. С ростом опыта, развитием рентгенэндоваскулярной хирургии, рефрактерный асцит (асцит неподдающийся медикаментозной терапии) становится ведущим показанием к ТИПС во многих медицинских клиниках. Если, больному поставлен диагноз рефрактерный асцит, больной имеет плохой прогноз – 50% смертность в течение 12 месяцев без соответствующего лечения. После выполнения ТИПС асцит уменьшается в 58% случаев (при выполнении лапароцентеза эта цифра составляет 19%).
Лучший способ описать ТИПС – объяснить, что значит каждая буква:
Т (трансъюгулярное) – термин обозначающий, что рентгенэндоваскулярный хирург, выполнив местное обезболивание, начинает операцию с пункции иглой яремной вены, расположенной на шее. Через иглу проводится тонкий проводник до момента попадания кончика проводника в печеночную вену. Далее по проводнику проводится специальный катетер.
И (интрапеченочное) – термин обозначающий, что катетер проводится через печеночную вену в саму печень. Затем вводится длинная изогнутая игла.
П (порто-системное) – термин обозначающий, что игла введенная через печеночную вену, проткнув ткань печени, попадет в воротную вену, расположенную так же в самой печени.
Стент растягивает печеночную паренхиму создав канал между ветвью воротной и печеночной вены.
После стентирования кровь дренируется из воротной вену с повышенным давлением в печеночную вену со сниженным давлением, что приводит к устранению портальной гипертензии, спаданию расширенных вен пищевода. Давление в воротной вене снижается до нормальных величин, что приводит к резкому улучшению клинического состояния больного.
Для TIPSS существуют строго определенные показания:
- портальная гипертензия;
- острое кровотечение из варикозно расширенных вен пищевода и желудка;
- повторное пищеводно-желудочное кровотечение;
- рефрактерный асцит (асцит неподдающийся медикаментозной терапии);
- печеночный гидроторакс (скопление асцитической жидкости в плевральной полости);
- синдром Бадда-Киари (сдавление нижней полой вены в инфраренальном отделе узлами регенератами).
Клиническую эффективность мы оцениваем по прекращению или уменьшению проявлений портальной гипертензии - прекращение пищеводно-желудочного кровотечения, уменьшение количества асцитической жидкости, спадание варикозно расширенных вен передней брюшной стенки. В послеоперационном периоде больным проводится стандартный курс инфузионной, гемостатической и диуретической терапии.
При необходимости, ТИПС может быть дополнен эндоваскулярной эмболизацией варикозно расширенных вен пищевода и желудка.
В настоящее время существует возможность выполнения данной операции бесплатно, по федеральной квоте. Можно получить квоту на высокотехнологичное лечение как по месту жительства, так и через комиссию при нашей клинике. Пациент собирает необходимый пакет документов и ждет получения квоты. Для более полной информации – звоните по тел.:
Ординаторская 8 (495) 441-92-11
Хирурги:
8 (916) 490-84-89 Алексей Сергеевич
TIPS. Когда? Кому? Зачем?
Статья представляет собой обзор современных данных о применении трансъюгулярного внутрипеченочного портосистемного шунтирования (TIPS) у больных циррозом печени. Дана историческая справка о становлении метода и теоретическое обоснование его применения. Основное внимание уделено показаниям и противопоказаниям к проведению TIPS, названы наиболее частые осложнения после его проведения. Представлены данные об эффективности TIPS в зависимости от исходного состояния на основании результатов рандомизированных клинических исследований.
- КЛЮЧЕВЫЕ СЛОВА: цирроз печени, асцит, энцефалопатия
Статья представляет собой обзор современных данных о применении трансъюгулярного внутрипеченочного портосистемного шунтирования (TIPS) у больных циррозом печени. Дана историческая справка о становлении метода и теоретическое обоснование его применения. Основное внимание уделено показаниям и противопоказаниям к проведению TIPS, названы наиболее частые осложнения после его проведения. Представлены данные об эффективности TIPS в зависимости от исходного состояния на основании результатов рандомизированных клинических исследований.
Общие положения
Единственным радикальным методом лечения цирроза печени (ЦП) и его осложнений является трансплантация печени. Существуют противопоказания к выполнению пересадки печени при ЦП, но развитие этого направления во всем мире в наибольшей степени сдерживает ограниченная доступность донорских органов.
Как правило, пациенты с ЦП умирают от осложнений. Поэтому от комплекса мер, направленных на профилактику прогрессирования ЦП, а также профилактику и лечение осложнений, следует ожидать продления жизни у многих пациентов.
Большинство осложнений (самые грозные из них кровотечение из варикозно расширенных вен пищевода (ВРВП) и желудка, рефрактерный асцит и гепаторенальный синдром (ГРС)) развивается вследствие прогрессирующей печеночной недостаточности и портальной гипертензии. Несмотря на возможность медикаментозной коррекции портального давления, наиболее продолжительный и надежный эффект достигается хирургическими методами.
Длительная история хирургии портальной гипертензии привела к селекции небольшого числа наиболее эффективных и безопасных шунтирующих операций, различные модификации которых используются в настоящее время.
С начала 1990-х гг. увеличилось число публикаций, посвященных результатам применения метода малоинвазивного портокавального шунтирования. Это так называемые операции трансъюгулярного внутрипеченочного портосистемного шунтирования, или TIPS (transjugular intrahepatic portosystemic shunt). Эта аббревиатура широко используется в англоязычной литературе. В русскоязычной медицинской литературе кроме этой аббревиатуры встречается ТИПС – трансъюгулярное интрапеченочное портосистемное стентирование.
Изначально методика была предложена для малоинвазивного лечения и профилактики осложнений портальной гипертензии, связанной с ЦП.
Метод основан на принципе равенства давления в синусоидах и давления заклинивания в печеночных венах (ДЗПВ), а также устойчивой прямой корреляции между давлением в системе воротной вены и давлением в синусоидах. Под давлением заклинивания подразумевается давление, достигаемое в крупном притоке одной из печеночных вен при раздувании баллончика на рабочей части катетера, который проводится пункционно через яремную вену, верхнюю полую вену, правое предсердие и нижнюю полу вену в устье одной из печеночных вен. Создаваемая таким образом окклюзия для кровотока в печеночной вене позволяет определить давление ниже уровня окклюзии и получить информацию о давлении в синусоидах. В здоровой печени механизм компенсации повышения давления в синусоидах функционирует благодаря перераспределению тока крови между синусоидами. Поэтому значение давления заклинивания несколько меньше. Подобный механизм перераспределения практически отсутствует в цирротически измененной печени вследствие нарушения архитектоники долек постнекротическими изменениями. ДЗПВ отражает давление в системе воротной вены только при отсутствии подпеченочного блока.
Для диагностических целей не используются собственно значения ДЗПВ, а также свободного давления в печеночных венах (СДПВ). Диагностическое значение имеет разница этих показателей, называемая градиентом давления в печеночных венах (ГДПВ). Как правило, для получения более точного значения ГДПВ проводится трехкратное измерение ДЗПВ. В норме ГДПВ составляет 3–5 мм рт. ст. Более высокие значения ГДПВ расцениваются как показатель портальной гипертензии независимо от наличия или отсутствия клинических проявлений [1].
Измерение ДЗПВ – эффективный метод оценки давления в системе воротной вены, особенно для пациентов с алкогольным ЦП и ЦП вирусной этиологии (в том числе вирус гепатита C) [2].
Тем не менее в ряде исследований, посвященных сравнению эффективности измерения ДЗПВ с прямыми методами измерения величины портального давления, показано расхождение полученных данных у больных ЦП в исходе хронического гепатита С [3].
В настоящее время считается доказанным, что превышение пороговых значений ГДПВ служит прогностическим показателем для развития ВРВП и кровотечения [4].
ГДПВ > 5 мм рт. ст. в отсутствие клинических проявлений соответствует субклинической портальной гипертензии. ГДПВ ≥ 10 мм рт. ст. считается показателем клинически значимой портальной гипертензии и служит предиктором развития осложнений ЦП, в том числе летального исхода [5]. ГДПВ > 12 мм рт. ст. является пороговым для разрыва ВРВП [4, 6].
Впервые давление в воротной системе было измерено в 1896 г. у собаки посредством канюли, установленной в брыжеечную вену и соединенной с водным манометром [7]. Тем не менее методика прямого измерения портального давления не получила клинического применения из-за инвазивности и неудобства использования на практике.
В 1951 г. J.D. Myers и W.J. Taylor впервые описали измерение давления заклинивания в печеночных венах, которое отражало давление в синусоидах, как первый метод непрямой оценки портального давления [8]. Впоследствии было доказано, что давление заклинивания строго коррелирует с давлением в системе воротной вены. Однако на практике стали использовать разницу давления заклинивания и свободного давления в печеночных венах. Экспериментальное изучение TIPS началось в 1970-х гг. Первые публикации о клиническом применении методики появились в начале 1990-х гг. В настоящее время опыт применения TIPS, согласно данным литературы, исчисляется тысячами пациентов.
Первые рекомендации были разработаны после конференции, проведенной под эгидой национальных институтов здоровья в 1995 г. Было показано, что методика TIPS эффективна как для купирования острого кровотечения из ВРВП, так и для профилактики рецидива кровотечения из ВРВП. Однако оставалось неясным, насколько TIPS по эффективности превосходит медикаментозную терапию и хирургию в лечении осложнений портальной гипертензии. Не было полного представления и о возможностях TIPS в лечении рефрактерного асцита и синдрома Бадда – Киари.
Операции TIPS внедрены в ограниченном числе российских клиник [9–11]. В проекте клинических рекомендаций по лечению кровотечений из ВРВП и желудка, разработанных в 2013 г. специалистами ведущих центров СНГ, занимающихся лечением больных портальной гипертензией, сказано, что применение TIPS должно быть ограничено случаями профузных кровотечений из ВРВП и желудка у больных ЦП и портальной гипертензией, которым планируется трансплантация печени [12].
При выполнении TIPS крайне важны правильная регистрация и интерпретация показателей венозного давления. Измерение ГДПВ обычно проводится под седацией и местной анестезией. Интродьюсер устанавливается обычно в правую яремную вену пункционно по методике Сельдингера. Реже используются бедренный или кубитальный доступы. Катетер с баллончиком на рабочей части (Swan-Ganz или Goodale Lubin) диаметром 7-Fr под рентген-телевизионным контролем проводится и «заякоривается» в печеночной вене на глубине 3–4 см от устья печеночной вены. Измеряется СДПВ. После стабилизации показателей СДПВ и подтверждения герметичности окклюзии просвета печеночной вены баллоном трехкратно регистрируются показатели ДЗПВ. Учитывается их среднее значение, причем разница всех трех измерений не должна превышать 1 мм рт. ст. При наличии показаний к шунтированию проводник из печеночных вен через паренхиму печени низводится в одну из ветвей воротной вены. Проводятся канюляция воротной вены и портография. Устанавливается саморасширяющийся стент.
Показания к TIPS
Согласно рекомендациям Американской ассоциации по изучению заболеваний печени (American Association for the Study of Liver Diseases – AASLD) показания к TIPS условно разделены на две группы – подтвержденные и не подтвержденные контролируемыми исследованиями [13].
К первой группе показаний эксперты относят прежде всего профилактику повторных кровотечений из ВРВП и рефрактерный асцит на фоне ЦП. Вторую группу показаний, в отношении которых эффективность оценивалась в неконтролируемых исследованиях, составляют острое кровотечение из варикозно расширенных вен (ВРВ) при неэффективности эндоскопических методов гемостаза, портальная гастропатия, кровотечение из ВРВ желудка, желудочная антральная сосудистая эктазия, гидроторакс на фоне портальной гипертензии, рефрактерный к другим методам лечения, гепаторенальный синдром 1-го и 2-го типов, синдром Бадда – Киари, веноокклюзионная болезнь, гепатопульмональный синдром.
Основной задачей TIPS является снижение давления в системе воротной вены. При этом достигается доказанная в рандомизированных клинических исследованиях профилактика рецидива кровотечения из ВРВП и купирование или уменьшение проявлений рефрактерного асцита.
Критериями эффективности TIPS в профилактике рецидива кровотечения служат снижение ГДПВ 20 мм рт. ст. показано TIPS (летальность 11% против 38% в группе без TIPS) [18]. В отсутствие эффективных методов прогнозирования риска рецидива кровотечения TIPS не должно использоваться в профилактике рецидива кровотечения у пациентов только с одним эпизодом кровотечения из ВРВП. Показания к TIPS должны быть ограничены неэффективностью медикаментозной терапии или эндоскопического лечения.
Методика TIPS эффективна в профилактике кровотечения из ВРВ желудка и эктопических ВРВ (включая ВРВ кишечника, кишечных стом, аноректальные) и предпочтительна в профилактике рецидива кровотечения в этой группе пациентов. Показано, что для профилактики рецидива кровотечения из ВРВ желудка можно достичь меньшего ГДПВ, чем для ВРВП, хотя не исключена необходимость эмболизации ВРВ [19].
Еще одно показание к TIPS, целесообразность которого доказана в рандомизированных клинических исследованиях, – рефрактерный асцит. Это асцит, не поддающийся курации при ограничении поваренной соли и назначении высоких доз диуретиков (спиронолактон 400 мг/сут, фуросемид 160 мг/сут), а также асцит у пациентов, не толерантных к диуретикам [20, 21]. Развитие рефрактерного асцита усугубляет прогноз заболевания, повышая годичную летальность до 50% [21, 22].
Из многих методов лечения рефрактерного асцита в настоящее время обсуждаются только TIPS и парацентез большими объемами. Методы перитонеовенозного шунтирования не рассматриваются из-за высокого риска осложнений. Вместе с тем по сравнению с профилактикой кровотечений из ВРВП эффективность TIPS в купировании или уменьшении рецидивов рефрактерного асцита определена в меньшей степени. Трудная объективизация прогноза связана с тем, что причиной рефрактерного асцита является не только нарушение кровотока в системе воротной вены, но и нарушение почечного кровотока. Поэтому снижение портального давления может быть недостаточным для увеличения диуреза и уменьшения продукции асцита. Одним из способов повышения эффективности TIPS в такой ситуации стало более выраженное снижение ГДПВ по сравнению с профилактикой рецидивов кровотечения из ВРВП 45 мм рт. ст.).
Относительными противопоказаниями считаются гепатоцеллюлярная карцинома (ГЦК), особенно центральной локализации, обструкция всех печеночных вен, тромбоз воротной вены, тяжелая коагулопатия (международное нормализованное отношение > 5), тромбоцитопения 3 , легочная гипертензия средней тяжести [13].
При высоком риске летального исхода в течение 30 дней (MELD > 15–18 или уровень общего билирубина > 70 мкмоль/л) пациент должен быть информирован о прогнозе. TIPS возможно только при отсутствии других вариантов лечения (метод выбора – трансплантация).
В связи с изложенным выше особое значение имеет правильный отбор кандидатов для проведения TIPS.
Читайте также:
