Утилизация энергии при сердечной недостаточности. Электролиты при сердечной недостаточности
Добавил пользователь Валентин П. Обновлено: 27.01.2026
Инфаркт миокарда – это заболевание, сопровождающееся некрозом одного или нескольких участков сердечной мышцы в результате острого нарушения кровотока в коронарных артериях, питающих миокард. Острый инфаркт миокарда без подъема сегмента ST и инфаркт миокарда с подъемом сегмента ST являются разновидностями острого коронарного синдрома, который включает также нестабильную стенокардию.
Риск инфаркта миокарда повышается с возрастом – чаще заболевают люди старше 60 лет. Однако в последнее время увеличилось количество ранних инфарктов миокарда – у людей моложе 40 лет. Среди пациентов младше 70 лет преобладают мужчины, однако после 70 количество мужчин и женщин с инфарктом миокарда становится одинаковым. Это может быть связано с защищающим действием эстрогенов (женских половых гормонов), которые снижают вероятность атеросклероза – главного фактора риска развития сердечного приступа.
Прогноз инфаркта миокарда зависит от обширности поражения сердечной мышцы, наличия сопутствующих заболеваний, времени обращения за медицинской помощью и возраста пациента. Смертность при остром инфаркте миокарда достигает 30 %.
Синонимы русские
Сердечный приступ, ИМ.
Синонимы английские
Heart attack, acute myocardial infarction, MI, myocardial infarction.
Симптомы
Основным симптомом острого инфаркта миокарда является резкая боль в груди, которая чаще всего ощущается как резкое сдавливание. Она продолжается обычно дольше 15 минут и не купируется приемом нитроглицерина. Боль может распространяться на левое плечо, лопатку, шею, нижнюю челюсть, может сопровождаться холодным потом, тошнотой и рвотой, потерей сознания. В некоторых случаях боль имеет нетипичную локализацию – в животе, в позвоночнике, левой или даже правой руке.
Иногда инфаркту предшествуют неспецифические симптомы: в течение нескольких дней до сердечного приступа человек может ощущать слабость, недомогание, дискомфорт в области груди.
Инфаркт может не сопровождаться характерным болевым синдромом и проявляться лишь такими признаками, как одышка, учащенное сердцебиение, слабость, тошнота. Неявная симптоматика инфаркта миокарда особенно характерна для женщин.
Таким образом, основными симптомами острого инфаркта миокарда являются:
- боль в груди,
- одышка,
- холодный пот,
- чувство страха,
- потеря сознания,
- тошнота, рвота.
Общая информация о заболевании
Инфаркт миокарда развивается в результате нарушения кровоснабжения сердечной мышцы, что приводит к недостатку кислорода и питательных веществ и некрозу (омертвению) участка миокарда. Основной причиной нарушения кровотока в сосудах, питающих миокард, является атеросклероз коронарных артерий – отложение атеросклеротических бляшек, состоящих в основном из холестерина, на внутренней поверхности сосудов. Затем происходит разрастание соединительной ткани (склероз) стенки сосуда и формирование отложений кальция (кальциноз) с дальнейшей деформацией и сужением просвета сосуда вплоть до полной закупорки. Впоследствии в атеросклеротической бляшке может развиваться так называемое асептическое воспаление, которое при воздействии провоцирующих факторов (физической нагрузке, повышении артериального давления и др.) способно приводить к надрыву бляшки. В области повреждения скапливаются тромбоциты, выделяются биологически активные вещества, которые еще больше усиливают адгезию (слипание) форменных элементов крови, и в итоге образуется тромб, закупоривающий просвет коронарной артерии. Возникновению тромба также способствует повышенная свертываемость крови. В случае, если кровоток в сосудах не восстанавливается в ближайшие шесть часов, происходят необратимые изменения в тканях миокарда.
Редко инфаркт миокарда случается при резком спазме или тромбоэмболии патологически неизмененных коронарных артерий, однако это наблюдается лишь в 5 % случаев.
Чаще всего инфаркт миокарда локализуется в передней стенке левого желудочка, реже – в задней стенке левого желудочка и межжелудочковой перегородки. Инфаркт в области правого желудочка возникает редко. Выделяют трансмуральный и субэндокардиальный инфаркт миокарда. При трансмуральном патологические изменения затрагивают всю стенку сердца, при субэндокардиальном – от ? до ½ толщины стенки. Существует также деление на инфаркт миокарда без подъема сегмента ST и инфаркт миокарда с подъемом сегмента ST. Наличие изменений сегмента S-T на электрокардиограмме позволяет заподозрить полную закупорку коронарной артерии и обширное повреждение миокарда с более высоким риском развития необратимого некроза тканей. Подъем сегмента S-T не наблюдается при частичной закупорке артерии – это может говорить об инфаркте миокарда без подъема сегмента S-T или нестабильной стенокардии. Однако лишь при инфаркте миокарда изменяется активность кардиальных энзимов.
При нарушении кровоснабжения миокарда гибель клеток начинается, прежде всего, в области эндокарда, а затем зона повреждения распространяется по направлению к перикарду. Обширность поражения зависит от степени закупорки артерии, ее длительности, системы коллатерального кровообращения.
Некроз в тканях сердечной мышцы вызывает острую боль. Обширное повреждение миокарда может приводить к нарушению сократительной функции сердца, что проявляется острой левожелудочковой недостаточностью с развитием отека легких и кардиогенного шока. Кардиогенный шок, в свою очередь, усугубляет течение инфаркта миокарда за счет ухудшения коронарного кровообращения. В результате возникают тяжелые нарушения ритма сердца, в том числе фибрилляция предсердий.
Трансмуральный инфаркт в некоторых случаях может приводить к разрыву стенки сердца или к аневризме – локальному истончению и выпячиванию участка миокарда.
Кто в группе риска?
Основной причиной развития инфаркта миокарда (до 90 % всех случаев) является атеросклероз. Поэтому факторы риска развития атеросклероза увеличивают и вероятность развития сердечного приступа. В группу риска входят:
- мужчины старше 45 лет и женщины старше 65 лет,
- страдающие ожирением, дислипидемией, артериальной гипертензией, сахарным диабетом,
- люди, родственники которых страдают сердечно-сосудистыми заболеваниями и/или перенесли инфаркт миокарда,
- курильщики,
- ведущие малоподвижный образ жизни,
- употребляющие наркотики (кокаин, амфетамины могут спровоцировать спазм коронарных артерий),
- испытывающие сильный стресс.
Диагностика
Острый инфаркт миокарда во многих случаях протекает малосимптомно или атипично, что затрудняет его диагностику. Существует ряд заболеваний, проявления которых зачастую могут быть схожи с проявлениями сердечного приступа: аневризма аорты, стенокардия, заболевания печени и желчевыводящих путей, депрессия, эзофагит и другие. Поэтому при подозрении на инфаркт миокарда необходимо провести ряд лабораторных и инструментальных исследований, позволяющих отличить инфаркт миокарда от другой патологии и выявить обширность и локализацию повреждения, продолжительность ишемии, постинфарктные осложнения. Кроме того, важно распознать признаки сопутствующих заболеваний: патологии почек и дыхательной системы, сахарного диабета, анемии. Все это определяет дальнейшую схему лечения и прогноз заболевания.
- Общий анализ крови. При остром инфаркте миокарда может наблюдаться лейкоцитоз. Количество лейкоцитов увеличивается со второго часа после возникновения нарушений кровообращения и достигает пика на 2-4-е сутки. Важно обратить внимание и на количество эритроцитов, так как анемия усугубляет кислородное голодание сердечной мышцы.
- Лейкоцитарная формула. Возможен лейкоцитоз со сдвигом лейкоцитарной формулы влево и анэозинофилией.
- Скорость оседания эритроцитов (СОЭ). Повышение СОЭ свидетельствует об остром воспалительном процессе.
- Тропонин I (количественно) – белок, который участвует в мышечном сокращении. При сердечном приступе его уровень обычно повышается начиная с 4-6-го часа, максимум на 2-е сутки и нормализуется в течение 6-8 дней от начала заболевания.
- Миоглобин. Это белок, который содержится в мышечной ткани, в том числе в миокарде. При инфаркте миокарда уровень миоглобина увеличивается в течение 4-6 часов.
- Аланинаминотрансфераза (АЛТ) и аспартатаминотрансфераза (АСТ). При инфаркте миокарда уровень этих ферментов является показателем обширности повреждения сердечной мышцы.
- Креатинкиназа MB. Увеличение ее концентрации специфично для повреждения сердечной мышцы. Ее уровень возрастает с первых часов и сохраняется повышенным в течение 2-3 суток.
- Лактатдегидрогеназа (ЛДГ) общая – фермент, который содержится практически во всех клетках организма и участвует в утилизации глюкозы. Уровень ЛДГ повышается при инфаркте миокарда, патологии печени, крови, почек. При инфаркте миокарда остается повышенным в течение 10-14 дней.
- Лактатдегидрогеназа 1, 2 (ЛДГ, 1, 2 фракции). Формы фермента лактатдегидрогеназы, которые содержатся в основном в клетках сердца, коркового вещества почек, печени. Эти показатели могут быть использованы для оценки обширности поражения при инфаркте миокарда.
- Антитромбин III. Синтезируется в клетках эндотелия сосудов и клетках печени, участвует в инактивации ряда факторов свертывания крови. Уменьшение количества антитромбина III говорит о повышенном риске тромбоза. Понижен его уровень при тромбоэмболии, атеросклерозе.
- Волчаночный антикоагулянт, скрининговый тест (LA1). Волчаночный антикоагулянт представляет собой комплекс антител против фосфолипидов. Их наличие может свидетельствовать об аутоиммунных заболеваниях, а также является признаком повышенного риска тромбообразования.
- Протромбиновый индекс (ПИ), международное нормализованное отношение – МНО). Анализ используется для оценки внешнего пути свертывания крови и активности I, II, V, VII, X факторов свертывания. Гиперкоагуляция увеличивает риск образования тромбов. При инфаркте миокарда протромбиновый индекс может быть повышен.
- Гликированный гемоглобин (HbA 1c, гликозилированный гемоглобин, гликогемоглобин). Образуется при присоединении глюкозы к гемоглобину. Данный показатель позволяет оценить количество глюкозы в крови на протяжении последних 120 дней – это средняя продолжительность жизни эритроцита. Высокий уровень гликированного гемоглобина говорит о высокой концентрации глюкозы за последние три месяца и свидетельствует о большой вероятности осложнений сахарного диабета, который, в свою очередь, увеличивает риск инфаркта миокарда. Тест на гликированный гемоглобин используется для оценки эффективности лечения и прогноза инфаркта миокарда у пациентов с сахарным диабетом.
- Глюкоза в плазме. Также используется для диагностики сахарного диабета.
- Железо в сыворотке. Железо входит в состав цитохромов и участвует в клеточном дыхании. При инфаркте миокарда уровень железа может быть повышен.
- Электролиты сыворотки. При остром инфаркте миокарда может меняться уровень натрия, калия, магния, кальция, хлора. Однако это происходит не всегда, при неосложненном течении инфаркта миокарда уровень электролитов может быть не изменен.
- Мочевая кислота в сыворотке. При нарушении кровоснабжения миокарда происходит некроз клеток сердечной мышцы с распадом органических веществ и выделением продуктов распада, в том числе мочевой кислоты. Это, в свою очередь, провоцирует развитие воспаления в зоне повреждения миокарда. Таким образом, уровень мочевой кислоты при обширном инфаркте миокарда может быть повышен.
- С-реактивный белок, количественно. При инфаркте миокарда бывает повышен за счет воспалительной реакции.
- Триглицериды. Образуются в кишечнике из жиров пищи. Депонируются в жировой ткани и расходуются клетками по мере необходимости для получения энергии. Повышенный уровень триглицеридов может свидетельствовать о высоком риске атеросклероза.
- Холестерол общий. Это соединения, которые участвуют в формировании атеросклеротических бляшек. Его концентрация может быть увеличена при инфаркте миокарда, возникшем в результате атеросклероза коронарных артерий.
- Холестерол – липопротеины высокой плотности (ЛПВП) – фракция общего холестерина, которая препятствует формированию атеросклеротических бляшек.
- Холестерол – липопротеины низкой плотности (ЛПНП) – фракция холестерола, участвующая в формировании атеросклеротических бляшек.
- Холестерол – липопротеины очень низкой плотности (ЛПОНП). Это липопротеины, которые образуются в печени. Являются переносчиками фосфолипидов, триглицеридов, холестерола. При попадании из печени в кровь подвергаются химическим превращениям с образованием липопротеинов низкой плотности
- Коэффициент атерогенности. Это соотношение "вредных" (ЛПНП, ЛПОНП, триглицеридов) и "полезных" липопротеинов (ЛПВП). Повышение коэффициента атерогенности говорит о высоком риске развития атеросклероза.
Другие методы исследования
- Электрокадиография (ЭКГ). Позволяет подтвердить диагноз "инфаркт миокарда", определить локализацию и степень повреждения сердечной мышцы, выявить признаки нарушения сердечного ритма.
- Рентгенография органов грудной клетки. Используется для выявления аневризмы сердца.
- Ультразвуковое исследование сердца. Позволяет выявить участок поражения миокарда, оценить сократительную способность сердца.
Лечение
Терапия назначается индивидуально в зависимости от возраста пациента, тяжести состояния и обширности поражения сердечной мышцы. Огромное значение имеет восстановление кровоснабжения миокарда в течение первых 12 часов после появления первых признаков инфаркта миокарда. Это может предотвратить или уменьшить степень некроза тканей. Основными направлениями терапии при остром инфаркте миокарда являются купирование болевого синдрома, тромболитическая и антикоагулянтная терапия, снижение нагрузки на миокард, предупреждение и лечение возникших осложнений.
Профилактика
Здоровое питание с низким содержанием насыщенных жиров и большим количеством овощей и фруктов.
Достаточная физическая активность.
Отказ от алкоголя и курения.
Своевременное прохождение профилактических медицинских осмотров для выявления заболеваний, повышающих риск развития инфаркта миокарда.
Утилизация энергии при сердечной недостаточности. Электролиты при сердечной недостаточности
Утилизация энергии при сердечной недостаточности. Электролиты при сердечной недостаточности
Большинство авторов приходит к заключению, что при сердечной недостаточности метаболические дефекты касаются преимущественно утилизации энергии (Bing, Benson и др.). Поскольку ведущую роль в освобождении кинетической энергии играют митохондрии, Schwartz и Kwang-Soo-Lee (1962) изучали активность обменных процессов в изолированных митохондриях сердечной мышцы у животных с хронической сердечной недостаточностью и нашли, что процесс окислительного фосфорилирования был резко угнетен.
Изолированные митохондрии сердечной мышцы животных с сердечной недостаточностью потребляли значительно меньше кислорода, чем в контрольных опытах. Так же резко понижено было и поглощение митохондриями глюкозы у подопытных животных.
Для нормального протекания обменных процессов в сердечной мышце необходим достаточный подвоз кислорода, а гипертрофированная сердечная мышца относительно хуже васкуляризирована и недостаточно снабжается кислородом и питательными веществами. Так же неполноценно удаляются и продукты обмена из миокарда.
Ф. З. Меерсон считает, что хроническая сердечная недостаточность развивается в результате нарушения ферментативных процессов, участвующих в ресинтезе контрактильных белков. При сердечной недостаточности наблюдается дефицит сульфгидрильных (SH) групп, играющих основную роль в процессе восстановления контрактильных белков.
Таким образом, изучение биохимических изменений в миокарде, лежащих в основе сердечной недостаточности, еще далеко до окончательного разрешения. Hochrein (1959) пишет, что большое увлечение гемодинамическими методами исследования сердечной недостаточности шло в ущерб изучению нарушения биохимических процессов.

Большое значение в развитии сердечной недостаточности имеет также и нарушение обмена электролитов. Сердечная мышца точно удерживает свой электролитный состав и колебания, которые происходят в течение фаз сокращения, быстро восстанавливаются в период диастолы.
Изменения электролитного обмена, который приводит к обеднению мышечных клеток калием и увеличению содержания в них натрия, влекут за собой понижение АТФ-активности и затрудняют сокращения миофибрилл. Изменения электролитного обмена в миокарде чаще наблюдаются как вторичный процесс при гемодинамических нарушениях; реже эти изменения могут носить первичный характер.
Ведущую роль в регуляции электролитного обмена играют минералокортикоиды, поэтому понятен и вполне оправдан тот интерес, который проявляют клиницисты и экспериментаторы в отношении изучения секреции и выделения минералокортикоидов при сердечной недостаточности.
Много работ за последнее время посвящено изучению нарушений секреции кортикостероидов и провоцирующей роли этих нарушений в развитии сердечной недостаточности при кардиальной патологии. Рядом авторов установлено повышенное выделение кортикостероидов при этом состоянии, но большинство расценивает это как вторичное явление.
Pekkarinen (1960) не нашел изменений в содержании 17-гидрокортикостероидов в крови у больных с сердечной недостаточностью. Lasche, Perloff и Durant (1951) установили у больных с явлениями сердечной недостаточности значительное снижение выделения 11-оксикортикостероидов и 17-кетостероидов. Дача ртутных мочегонных, согласно их данным, повышает выделение 11-оксистероидов почти в 10 раз.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Кардиоцеребральная дисфункция: факторы риска и возможности цитопротективной терапии
Метаболическая терапия, целью которой является улучшение эффективности утилизации кислорода миокардом и головным мозгом в условиях развивающейся ишемии, находит все большее применение в комплексном лечении сердечно-сосудистых заболеваний (ССЗ), в частности цереброваскулярной болезни, основной причиной развития которой являются сердечно-сосудистые нарушения.
Целесообразно назначение препаратов, обладающих антиоксидантным и антигипоксическим эффектами. Благодаря многоплановому действию, а именно органонезависимому влиянию на метаболизм клеток и мощному антиоксидантному эффекту, в стандарты ведения больных с цереброваскулярной болезнью может быть включен Актовегин.
- КЛЮЧЕВЫЕ СЛОВА: кардиология, ангиология, сердечно-сосудистые заболевания, кардиоцеребральная дисфункция, цитопротективная терапия
Метаболическая терапия, целью которой является улучшение эффективности утилизации кислорода миокардом и головным мозгом в условиях развивающейся ишемии, находит все большее применение в комплексном лечении сердечно-сосудистых заболеваний (ССЗ), в частности цереброваскулярной болезни, основной причиной развития которой являются сердечно-сосудистые нарушения.
Целесообразно назначение препаратов, обладающих антиоксидантным и антигипоксическим эффектами. Благодаря многоплановому действию, а именно органонезависимому влиянию на метаболизм клеток и мощному антиоксидантному эффекту, в стандарты ведения больных с цереброваскулярной болезнью может быть включен Актовегин.
Болезни сердечно-сосудистой системы, в том числе инфаркт миокарда (ИМ) и мозговой инсульт (МИ), занимают лидирующие позиции в структуре общей смертности и обеспечивают высокий процент инвалидизации работоспособного населения. В основе острых и хронических поражений головного мозга лежит целый ряд сердечно-сосудистых заболеваний (ССЗ). Ведущими ССЗ являются ишемическая болезнь сердца (ИБС), артериальная гипертония (АГ), хроническая сердечная недостаточность (ХСН), нарушения ритма (чаще – фибрилляция предсердий), приобретенные пороки сердца и осложнения после протезирования клапанов сердца.
Роль сердечно-сосудистых заболеваний в развитии цереброваскулярных нарушений
В последнее десятилетие выявление взаимосвязи между кардиальными и церебральными нарушениями привело к возникновению такого междисциплинарного направления в медицине, как кардионеврология. Одним из важных направлений кардионеврологии является изучение неврологических расстройств у больных с болезнями сердца [1]. В современной литературе появились термины «кардиогенная энцефалопатия», «кардиогенная деменция», «кардиоцеребральный континуум» и др. [1, 2]. Своевременное выявление хронических кардиальных заболеваний, приводящих к прогрессированию цереброваскулярных нарушений, а также уточнение их патогенетических механизмов позволит оптимизировать профилактику и лечение больных с указанными коморбидными состояниями, что является не только медицинской, но и очень важной социальной проблемой.
- ИБС (инфаркт миокарда, связанные с ишемией миокарда нарушения ритма сердца и ХСН со сниженной фракцией выброса левого желудочка (ЛЖ));
- АГ, в том числе гипертонические кризы;
- кардиогенные эмболии церебральных сосудов;
- кардиогенные синкопальные состояния с развитием постишемической энцефалопатии;
- гиперхолестеринемия и ДЛП;
- атеросклероз экстра- и интракраниальных сосудов;
- неврологические осложнения бактериального эндокардита.
- нарушение ауторегуляции мозгового кровотока;
- ухудшение реологических свойств крови;
- эндотелиальная дисфункция;
- ДЛП;
- внутрисосудистая активация гемостатического потенциала.
- снижение кровотока и содержания кислорода;
- образование циклических нуклеотидов и утилизация кислорода;
- выброс эйкозаноидов, накопление кальция, активация протеаз;
- развитие окислительного стресса;
- возникновение местных воспалительных реакций;
- нарушение функционирования эндотелиоцитов и развитие блока микроциркуляции.
Возможности применения метаболической терапии в кардионеврологии
В последнее время в кардионеврологии особое внимание специалистов привлекает метаболическая терапия, которая нацелена на повышение эффективности утилизации кислорода миокардом и головным мозгом в условиях развивающейся ишемии. В физиологических условиях СРО необходимо для нормального функционирования организма. Однако в случае патологического усиления окислительного стресса развивается эндотелиальная дисфункция, повреждаются клетки и разобщаются процессы окислительного фосфорилирования и тканевого дыхания, ингибируются ферментативные системы, деполяризуется дезоксирибонуклеиновая кислота (ДНК), повреждаются мембраны клеток и нарушается их проницаемость, наблюдается потеря эластических свойств, вплоть до разрыва и гибели клетки. Окислительный стресс играет важную роль в патогенезе атеросклероза, ИБС, ХСН, ишемических и геморрагических инсультов и других ССЗ [3–5].
Первопричиной многих нарушений, обусловленных повышением активности перекисного окисления липидов (ПОЛ), при многих ССЗ является гипоксия, поэтому в комплексной терапии желательно назначать препараты, обладающие не только антиоксидантным, но и антигипоксическим эффектом. Например, таким препаратом является Актовегин («Никомед/Такеда»), который входит в стандарты ведения больных с ЦВБ, оказывает многоплановое действие, обусловленное органонезависимыми влияниями на метаболизм клеток, обладает мощным антиоксидантным эффектом, приводя к повышению потребления и использования кислорода, а также усилению поступления в клетку глюкозы, благодаря чему активируется клеточный метаболизм, улучшается функционирование микроциркуляторного русла [4–6].
Фармакологическая характеристика и механизм действия Актовегина
Актовегин представляет собой высокоочищенный депротеинизированный гемодериват, не содержащий эндотоксинов и антигенов; состоит из более чем 200 биологически активных субстанций с молекулярной массой менее 5000 дальтон, получаемый методами ультрафильтрации и диализа из крови телят. Препарат содержит исключительно физиологические компоненты: аминокислоты, олигопептиды, нуклеотиды, промежуточные продукты метаболизма жирных кислот и углеводов, низкомолекулярные компоненты клеточных мембран, а также неорганические электролиты и важные микроэлементы. Актовегин состоит из молекул, которые содержатся в организме в физиологических условиях, поэтому проведение фармакокинетических и фармакодинамических исследований с определением его активных молекул не представляется возможным.
- повышается обмен высокоэнергетических фосфатов (аденозинтрифосфатов (АТФ));
- активируются ферменты окислительного фосфорилирования (пируват- и сукцинатдегидрогеназы, цитохром С-оксидазы);
- повышается активность кислой фосфатазы и лизосомальная активность клетки;
- повышается активность щелочной фосфатазы, ускоряется синтез углеводов и белков;
- увеличивается приток ионов калия в клетку, происходит активация калийзависимых ферментов: каталаз, сахараз, глюкозидаз;
- ускоряется распад продуктов анаэробного гликолиза – лактата и бета-гидроксибутирата.
Особенности применения Актовегина в неврологии
- ишемический мозговой инсульт;
- восстановительный период после перенесенного острого нарушения мозгового кровообращения;
- дисциркуляторная и постгипоксическая энцефалопатия;
- черепно-мозговая травма;
- коматозные состояния различной этиологии;
- диабетическая полинейропатия;
- дискогенная радикулопатия.
- при хронической ишемии мозга: по 200 мг (1 драже) 3 раза в день в течение 30 дней или по 200–800 мг внутримышечно или внутривенно капельно в течение 10–14 дней;
- при остром инсульте: 800–2000 мг в сутки в течение 10 дней, далее по 1–2 таблетки в течение 4–5 месяцев;
- при постгипоксической энцефалопатии: 800–2000 мг в сутки внутривенно капельно в течение 5 суток;
- диабетическая полинейропатия: 2000 мг внутривенно капельно в сутки в течение 3 недель, далее по 2–3 драже 3 раза в день в течение не менее 4–5 месяцев.
Применение Актовегина в кардиологии
В 1980-е гг. ряд исследователей впервые выявили позитивное влияние препарата Актовегин на метаболизм не только головного мозга, но и миокарда. Было показано, что препарат усиливает окислительное фосфорилирование в митохондриях, тем самым повышая уровень АТФ; ускоряет не только энергетический, но и резервный метаболизм; может способствовать усиленному накоплению гликогена и калия. Препарат вызывает дозозависимое повышение потребления кислорода по сравнению с контролем [1].
Актовегин в качестве биологического агента обладает плейотропными, нейропротективными и метаболическими эффектами и по механизмам действия соответствует концепции интегрального терапевтического подхода, что делает актуальной возможность его применения у кардиологических больных. Кроме того, в последние годы уделяется большое внимание церебральным нарушениями при ИБС. Доказано, что ИБС является независимым фактором риска деменции, выявлена связь между атеросклерозом/кальцинозом коронарных артерий сердца и повышением риска когнитивных нарушений [1]. Снижение сердечного выброса, особенно у пожилых людей, приводит к гипоперфузии головного мозга с развитием неврологической симптоматики. Подходы к профилактике и терапии цереброваскулярных нарушений у больных с хронической кардиальной патологией достаточно четко представлены в работах российских ученых [1, 3, 4, 5, 7]. Особое место в качестве цитопротективной терапии занимает препарат Актовегин.
Применение Актовегина при ишемической болезни сердца
Очень важным моментом при ведении пациента с кардиальной патологией является возможность усилить энергетические процессы метаболизма в миокарде именно с помощью лекарственных препаратов, существенно не влияющих на гемодинамику, не обладающих отрицательным хроно- и инотропным действием. Такой подход может быть особенно эффективен у больных ИБС, когда возможности увеличения доз антиишемических средств, обладающих влиянием на гемодинамику, уже исчерпаны, а положительный клинический эффект еще не достигнут. Основными энергетическими субстратами в сердце являются глюкоза и свободные жирные кислоты (СЖК), конечным продуктом их распада – ацетилкоэнзим-А, вступающий в цикл Кребса в митохондриях с образованием АТФ. В норме при достаточном поступлении кислорода основным энергетическим субстратом в миокарде являются СЖК, которые служат источником 60–80% АТФ.
В случае умеренной ишемии аэробное окисление СЖК и глюкозы снижается. Анаэробный гликолиз становится основным источником АТФ. В этих условиях запасы гликогена мобилизуются на поддержку гликолиза. Следует отметить, что при полной окклюзии сосуда анаэробный гликолиз остается единственным источником образования энергии. Таким образом, при угнетении аэробной энергопродукции наиболее адаптивную роль играет анаэробный гликолиз, что обусловливает целесообразность назначения цитопротективных препаратов с антиоксидантным эффектом уже на ранних этапах развития ишемии миокарда.
- отсутствие эффекта от традиционной терапии;
- возникновение нарушений ритма и проводимости, развитие сердечной недостаточности;
- ухудшение течения ИБС (медленно прогрессирующая стенокардия);
- сочетание ИБС с АГ, СД, хронической обструктивной болезнью легких, хроническими заболеваниями печени.
- ОИМ после проведения тромболизиса или баллонной ангиопластики, для профилактики синдрома реперфузии;
- ОИМ с нарушениями ритма и проводимости, развитием недостаточности кровообращения (НК);
- нестабильная стенокардия (НС), особенно при невозможности назначения максимальных целевых доз антиангинальных препаратов (бета-адреноблокаторов, нитратов, антагонистов кальция);
- различные виды шока;
- после остановки кровообращения и асфиксии;
- тяжелое течение ХСН (IIБ–III степени)/ХСН III–IV функционального класса (ФК) по классификации Нью-Йоркской ассоциации кардиологов (NYHA, New York Heart Association);
- кардиальный синдром Х.
Подобные результаты были получены и в других исследованиях [2, 3, 5]. В работе В.В. Никонова и соавт. (2008) [4] изучали применение Актовегина у 102 больных НС. У 80% больных было продемонстрировано положительное влияние препарата на клиническое состояние в виде уменьшения приступов стенокардии, на дозы принимаемых нитратов и восстановление их эффективности, на повышение толерантности к физической нагрузке по данным ВЭМ и отдельные показатели внутрисердечной гемодинамики (снижение КДР ЛЖ и повышение ФВ ЛЖ). Полученные положительные результаты были более выраженными у лиц с исходно низкой ФВ ЛЖ. Одновременно с уменьшением клинических проявлений нестабильности коронарного кровотока больные, получавшие Актовегин в дозе 400 мг в сутки (в виде внутривенной инфузии на физиологическом растворе 200,0 мл со скоростью 2 мл в минуту) в течение 10–12 дней, отмечали улучшение церебральных проявлений ишемической болезни, свойственные больным ИБС: уменьшались головные боли, шум в ушах, головокружения. У 40% больных отмечено уменьшение тревожности, беспокойства, нормализация сна, улучшение настроения. Вместе с тем на фоне приема Актовегина не наблюдался синдром обкрадывания в связи с отсутствием у препарата вазодилатирующего эффекта, что является особенно важным у больных с сопутствующим заболеванием головного мозга [4].
В настоящее время нет четких данных по применению оптимальных доз Актовегина у больных ОКС. Считается, что цитопротективный эффект препарата проявляется при использовании высоких доз (1000 мг и выше в сутки) [2]. В основном в клинической практике при ОКС чаще всего применяют умеренные дозы препарата – 400 мг в сутки [12, 13]. При ОКС имеет место развитие микроциркуляторных нарушений. Применение Актовегина способствует улучшению микроциркуляции, по-видимому, за счет улучшения аэробного обмена сосудистого эндотелия. Это сопровождается высвобождением мощных вазодилататоров – оксида азота и простациклина, что приводит к улучшению перфузии органов и тканей, уменьшению общего периферического сосудистого сопротивления, и создаются условия для снижения сопротивления сердечного выброса и уменьшения потребности миокарда в кислороде [14].
Наибольшие положительные эффекты были получены при применении Актовегина у больных ОИМ с признаками НК и высокими градациями желудочковых нарушений ритма сердца (ЖНРС). Современное лечение ОИМ включает реканализацию тромбированных коронарных артерий с помощью тромболитической терапии и/или чрескожной транслюминальной баллонной ангиопластики с установкой стента или без него. Однако восстановление коронарного кровотока приводит в 30% случаев и более к развитию синдрома реперфузии, который обусловлен резким возрастанием поступления кислорода и неспособностью кардимиоцитов утилизировать его. В результате увеличивается СРО, способствующее повреждению липидов мембран, дополнительному повреждению функционально важных белков, в частности цитохромной дыхательной цепи и миоглобина, нуклеиновых кислот и других структур кардиомиоцитов [2, 7].
- способностью воздействовать на сохранение энергетического потенциала кардиомиоцитов в условиях ишемии, препятствуя развитию нарушений ритма и проводимости;
- снабжение поврежденной клетки глюкозой, нормализация метаболизма и, как следствие, купирование и предотвращение нарушений ритма (это обусловлено тем, что, поскольку Актовегин обладает инсулиноподобным действием, можно предположить, что он улучшает проникновение ионов калия в клетки миокарда);
- положительное влияние на ЖНРС путем улучшения ФВ и структурно-функционального состояния миокарда ЛЖ.
Теоретические предпосылки и клинический опыт свидетельствуют о том, что применение Актовегина в составе стандартной терапии у больных ИБС является высокоэффективным и безопасным методом лечения, которое улучшает клинический статус пациентов, структурно-функциональное состояние ЛЖ, повышает ФВЛЖ, нормализует исходно нарушенную ВРС, уменьшает тяжесть ЖНРС, уменьшает выраженность эпизодов ишемии, повышает толерантность к физической нагрузке. При ведении больных с заболеваниями сердца назначение Актовегина не только оптимизирует сердечную деятельность и предупреждает сердечно-сосудистые катастрофы, но и обеспечивает метаболические потребности головного мозга и профилактику цереброваскулярных расстройств.
Электролитные нарушения и их коррекция

Notice: Trying to get property of non-object in /var/www/agent3/data/www/pan.admins24.online/wp-content/themes/scooter/single-specialistam.php on line 52
Препараты калия и магния в кардиологической практике
Во всем мире препараты калия и магния приобретают все большее значение в качестве терапевтического средства, поскольку они эффективны, практически лишены побочных действий и экономически доступны. Панангин – лекарственный препарат, содержащий калий и магний, позволяет быстро восстановить содержание этих важных элементов в крови, оказывает защитное действие на сердце и сосуды, предупреждая развитие жизнеопасных аритмий, уменьшая токсическое влияние некоторых лекарственных препаратов, улучшая диастолическую функцию сердца, восстанавливая функцию эндотелия, замедляя развитие атеросклероза и снижая риск тромбообразования [16].
Панангин в лечении суправентрикулярных тахиаритмий у больных урологического профиля.
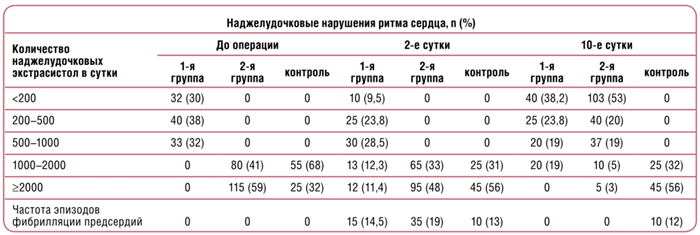
Пониженное поступление с пищей калия и магния, а также избыточное употребление солей натрия – отличительная черта современной цивилизации, что является одним из факторов, способствующих распространенности сердечно-сосудистых заболеваний [8]. Низкое содержание калия и магния повышает риск развития опасных нарушений сердечного ритма и обусловливает неблагоприятный прогноз при сердечной недостаточности [17, 18]. Клинические исследования показали, что аритмии у больных инфарктом миокарда с уровнем калия в крови >4,6 ммоль/л развивались намного реже [19, 20]. Дефицит магния в крови также обусловливает опасные нарушения сердечного ритма. Наиболее типичный вариант аритмии при дефиците магния – желудочковая тахикардия под названием пируэт – грозное состояние, переходящее в фибрилляцию желудочков и при отсутствии лечения приводящее к смертельному исходу [17, 21]. За урологической помощью обращаются преимущественно мужчины пожилого возраста, страдающие заболеваниями как органов мочеполовой системы, так и сердечно-сосудистыми. Нередко у данной категории больных в послеоперационном периоде развиваются суправентрикулярные нарушения ритма сердца. Нами оценена эффективность препарата Панангин в комплексной терапии для лечения и профилактики аритмий у 300 мужчин в возрасте старше 40 лет, страдающих заболеваниями мочеполовой и сердечно-сосудистой систем и находившихся на лечении в городской клинической урологической больнице № 47 Департамента здравоохранения г. Москвы. При этом больных с сочетанием ИБС и гипертонической болезни было 60%, с гипертонической болезнью – 20%, с ИБС и стенокардией I и II ФК – 20%. В зависимости от основного диагноза больным были произведены: трансуретральная резекция предстательной железы, дистанционная литотрипсия, нефрэктомия, радикальная простатэктомия и некоторые другие оперативные вмешательства. Все больные на предоперационном этапе прошли холтеровское мониторирование (ХМЭКГ) и были проконсультированы кардиологом. Впослеоперационном периоде, на 2‑е и 10‑е сутки, проводили повторный осмотр кардиологом и ХМ-ЭКГ; при необходимости корректировали кардиотропную терапию.
ELECTROLYTE DISORDERS AND THEIR CORRECTION S. Davydova, Candidate of Medical Sciences; I. Komissarenko, MD City Clinical Urology Hospital Forty-Seven, Central Gastroenterology Research Institute, Moscow The paper considers electrolyte disorders in gastroenterology and gives the results of using panangin and the β-adrenoblocker metoprolol in the prevention and treatment of supraventricular tachyarrhythmia after operations on the urinary system in patients with concomitant cardiac and urologic problems. Key words: potassium, magnesium, panangin, supraventricular tachycardia, premature supraventricular contractions, urologic surgical interventions
Определение электролитов в крови (натрий, калий, кальций ионизированный в комплексе)
Краткое описание:
Натрий, калий и кальций ионизированный являются основными электролитами организма.Электролиты–это минеральные соединения, которые способны проводить электрический заряд. Находясь в тканях и крови в виде растворов солей, они помогают перемещению питательных веществ в клетки и выводу продуктов обмена веществ из клеток, поддерживают в них водный баланс и необходимый уровень кислотности.
Синонимы (rus): Электролиты в сыворотке.
Синонимы (eng): Electrolyte Panel, Sodium, Potassium, Chloride, CMP, BMP.
Метод: ионселективные электроды.
Единицы измерения: ммоль/л (миллимоль на литр)
Подготовка к исследованию:
• Не принимать пищу в течение 12 часов перед исследованием.
• Исключить физическое и эмоциональное перенапряжение за 30 минут до исследования.
• Не курить в течение 30 минут до сдачи крови.
Тип биоматериала: Венозная кровь.
Тип пробирки: вакуумная пробирка с литий гепарином ( с зеленой крышкой).
Цена услуги: 458 руб.
Сроки выполнения: один рабочий день.
Электролит Референсные значения
Калий (К+) 3,4 – 5.1 ммоль/л
Натрий (NA+) 136 - 146 ммоль/л
Кальций ионизированный (Ca+) 1,15-1,29 ммоль/л
Повышение уровня калия (гиперкалиемия):
• избыточное поступление калия в организм: быстрое вливание растворов калия;
• выход К+ из клеток во внеклеточную жидкость: при массивном гемолизе, рабдомиолизе, распаде опухолей, тяжелых повреждениях тканей, глубоких ожогах, злокачественной гиперпирексии, ацидозе;
• сниженное выделение К+ почками: острая почечная недостаточность с олиго- и анурией, ацидозом, терминальная стадия хронической почечной недостаточности с олигурией, болезнь Аддисона, псевдогипоальдостеронизм, гипофункция ренин-ангиотензин-альдостероновой системы, шоковые состояния, ишемия тканей;
• уменьшение объема внеклеточной жидкости - дегидратация;
• приём таких лекарственных средств, как амилорид, спиронолактон, триамтерен, аминокапроновая кислота, противоопухолевые средства, дигоксин, нестероидные противовоспалительные препараты, триметоприм-сульфаметоксазол.
Понижение уровня калия (гипокалиемия):
• недостаточное поступление калия в организм: при хроническом голодании, диете, бедной калием;
• потеря калия организмом с кишечными секретами при частой рвоте, профузном поносе, аденоме ворсинок кишечника, кишечных свищах, отсасывании содержимого желудка через назогастральный зонд;
• потеря калия с мочой при почечном канальцевом ацидозе, почечной канальцевой недостаточности, синдроме Фанкони, синдроме Конна (первичном альдостеронизме), вторичном альдостеронизме, синдроме Кушинга, осмотическом диурезе (при сахарном диабете), алкалозе, введении АКТГ, кортизона, альдостерона;
• перераспределение калия в организме (усиленное поступление калия внутрь клеток): при лечении глюкозой и инсулином, семейном периодическом параличе, алкалозе;
• потеря с потом при муковисцидозе;
• лечение мегалобластической анемии витамином В12 или фолиевой кислотой;
• гипотермия;
• прием кортикостероидов, диуретиков (кроме калийсберегающих), бета-адреноблокаторов, антибиотиков;
• введение большого количества жидкости с низким содержанием калия;
• ВИПома (опухоль островковых клеток поджелудочной железы, секретирующая вазоактивный интестинальный полипептид - ВИП);
• Дефицит магния.
Повышение уровня натрия (гипернатриемия):
• гипертоническая дегидратация:
а) потеря жидкости через кожу при сильной потливости;
б) потеря жидкости через легкие при длительной одышке;
в) потеря жидкости через ЖКТ при частой рвоте и тяжелой диарее11356433
г) при высокой лихорадке (брюшной тиф, паратиф, сыпной тиф и т. п.);
• недостаточное поступление воды в организм;
• задержка натрия в почках (снижение выведения с мочой) при первичном и вторичном гиперальдостеронизме, синдроме Кушинга (избытке кортикостероидов);
• избыточное введение солей натрия, например, гипертонического раствора натрия хлорида;
• прием таких препаратов, как АКТГ, анаболические стероиды, андрогены, кортикостероиды, эстрогены, метилдопа, оральные контрацептивы, бикарбогат натрия.
Понижение уровня натрия (гипонатриемия):
• недостаточное поступление натрия в организм;
• потеря натрия при рвоте, диарее, сильной потливости при адекватном водном и неадекватном солевом замещении;
• передозировка диуретиков;
• недостаточность надпочечников;
• острая почечная недостаточность (полиурическая стадия);
• осмотический диурез;
• гипотоническая гипергидратация:
а) избыточное парентеральное введение жидкости;
б) сниженное выведение воды при почечной недостаточности, повышенной секреции вазопрессина, дефиците кортикостероидов;
• гипонатриемия разведения с отеками и асцитом при хронической сердечной недостаточности, циррозе печени, циррозе печени, печеночной недостаточности, нефротическом синдроме;
• приём таких препаратов, как фуросемид, аминогликозиды, гипертонический раствор глюкозы, нестероидные противовоспалительные препараты, амитриптилин, галоперидол;
• гипотиреоз.
Повышение уровня кальция (гиперкальциемия):
• Первичный гиперпаратиреоидизм;
• Эктопические опухоли, вырабатывающие паратгормон;
• Избыточное потребление витамина Д.
• Злокачественные опухоли (повышение ионизированного кальция может быть при нормальных величинах общего кальция) и метастазы;
• Ацидоз;
• Прием лекарственных препаратов : гидрохлортиазид (длительный прием), литий, андрогены.
Понижение уровня кальция(гипокальциемия):
• Первичный гипопаратиреоидизм,
• псевдогипопаратиреоидизм;
• Дефицит витамина Д;
• Сепсис;
• Острый панкреатит;
• Почечная недостаточность;
• Тяжелые поражения скелетных мышц;
• Гемодиализ при низкой концентрации кальция в диализате;
• После переливаний крови, содержащей комплексирующие кальций анионы (цитрат);
• После обширных травм, хирургических вмешательств;
• Ожоги;
• Полиорганная недостаточность;
• Дефицит магния;
• Алкалоз;
• Гипернатриемия;
• Атрофический гастрит;
• Вещества, связывающие кальций (цитрат, оксалат, ЭДТА, гепарин);
• Лекарственные препараты (противосудорожные средства, даназол, фоскарнет, фуросемид первоначальное действие),
• алкоголь.
Читайте также:
