Аномалии, болезни зрачка и радужки у ребенка
Добавил пользователь Владимир З. Обновлено: 21.01.2026
Иркутский филиал ФГАУ «НМИЦ «МНТК «Микрохирургия глаза» им. акад. С.Н. Федорова» Минздрава России, Иркутск, Россия
Цель работы: представить тактику лечения персистирующей зрачковой мембраны (ПЗМ) с использованием коагулирующего лазера.
Материалы и методы: в статье представлен метод лазерного лечения васкуляризированной ПЗМ коагулирующим лазером у пациента с темной радужкой.
Результаты: в послеоперационном периоде наблюдалось ареактивное течение. Уже в 1-е сут после операции пациент отметил субъективно повышение остроты зрения.
Заключение: лазеркоагуляция васкуляризированной ПЗМ у пациентов с темной радужкой и отсутствием помутнений в хрусталике является наиболее предпочтительным и безопасным методом лечения.
Ключевые слова: персистирующая зрачковая мембрана, лазерное лечение.
Для цитирования: Щуко А.Г., Букина В.В., Борисова А.В., Юрьева Т.Н. Персистирующая зрачковая мембрана. Лазерное лечение // РМЖ. Клиническая офтальмология. 2015. № 4. С. 183-186.
Persistent pupillary membrane. Laser treatment.
Schuko A.G.1,2, Bulina V.V.1, Borisova A.V.1, Yur'eva N.N.1,3
1 Irkutsk Department of FGMU MNTK Eye Microsurgery named after acad. Fedorov S.N. of the Ministry of Health of the Russian Federation
2 Irkutsk Academy of Postdiploma Education
3 Irkutsk State Medical University
Purpose: to present the tactics of treatment of persistent pupillary membrane using laser coagulation.
Materials and methods: the paper presents a method of laser treatment of vascularized persistent pupillary membrane by laser coagulation in patient with dark iris.
Results: in the postoperative period complications were not registered. On the first day after surgery, the patient noted a subjective improvement in visual acuity.
Conclusion: laser coagulation of vascularized persistent pupillary membrane in patients with dark iris and the lack of opacity in the lens is the most preferred and safe treatment.
Key words: persistent pupillary membrane, laser treatment.
For citation: Schuko A.G., Bulina V.V., Borisova A.V., Yur'eva N.N. Persistent pupillary membrane. Laser treatment // RMJ. Clinical ophthalomology. 2015. № 4. P. 183-186.
Для цитирования: Персистирующая зрачковая мембрана. Лазерное лечение. Клиническая офтальмология. 2015;16(4):183-186.
В статье рассмотрена проблема персистирующей зрачковой мембраны и ее лазерного лечения
Введение
Персистирующая зрачковая мембрана (ПЗМ) является врожденной аномалией развития мезодермальной ткани радужки и встречается в 30-95% случаев у здоровых новорожденных [1, 2, 4-6]. Она представляет собой остатки передней части хрусталиковой сумки, которая питает хрусталик во время внутриутробного развития [1].
Впервые о врожденной зрачковой мембране в 1707 г. сообщил Litfre [2]. Е.С. Вельховер с соавт. (1992) называют ее остаточной зрачковой мембраной Вахедорфа [3]. ПЗМ нередко наблюдается у недоношенных детей, и это может быть использовано для идентификации гестационного возраста новорожденного (между 27 и 34 нед.) [5]. По данным М.Д. Вершининой (1989), Н.Ф. Бобровой (2013), чаще зрачковая мембрана встречается у пациентов с миопической рефракцией и в 80% случаев наблюдается у лиц с темными радужками.
Известно, что для адекватного стимулирования сетчатки и развития зрительной коры зрачковая диафрагма должна превышать диаметр 1,5 мм. В противном случае существенно возрастает риск развития обскурационной амблиопии [5, 6]. Таким образом, показаниями к лечению ПЗМ являются снижение корригированной остроты зрения, а также риск развития обскурационной амблиопии.
Определенной стандартизированной тактики ведения пациентов с наличием остаточной зрачковой мембраны нет. Как правило, в каждом случае принимается индивидуальное решение о необходимости лазерного или хирургического вмешательства у пациентов с данной патологией.
Цель работы: представить тактику лечения ПЗМ с использованием коагулирующего лазера.
Материалы и методы
Под нашим наблюдением находился пациент Е., 14 лет, который обратился с жалобами на низкую остроту зрения правого глаза, пятно перед правым глазом в виде «жука». Из анамнеза выяснено, что низкое зрение обнаружили в 4 года, наблюдался у окулиста по месту жительства, лечение не получал. Острота зрения на момент диагностики правого глаза снижена до 0,35, не корригируется, острота зрения левого глаза - 1,0. При биомикроскопии правого глаза в проекции зрачка определяется плотная остаточная мембрана из мезодермальной ткани радужной оболочки, ножки которой фиксированы к воротничку радужки и обильно васкуляризированы. На передней капсуле хрусталика имеются отложения пигмента (рис. 1 А и Б). На левом глазу визуализируется мембрана, идентичная мембране правого глаза, но с преимущественным расположением в параоптической зоне зрачка, что объясняет сохранение у пациента высоких зрительных функций (рис. 1 В).
Изменения в глубжележащих отделах и на глазном дне обоих глаз не выявлены.
На основании полученных данных поставлен диагноз: ПЗМ обоих глаз. Обскурационная амблиопия II степени правого глаза.
Вследствие того, что ПЗМ на правом глазу препятствует светопроведению и, соответственно, световосприятию, являясь причиной развития обскурационной амблиопии, пациенту была запланирована лазерная коагуляция зрачковой мембраны. В отличие от описанных в литературе лазерных [4, 5, 7-9] и хирургических методов [1, 6] удаления мембраны в нашем случае лазерное лечение было проведено методом лазеркоагуляции мембраны на установке Visual-YAG-Argon фирмы Carl Zeiss. Такой подход был обусловлен наличием достаточно крупных сосудов в ножках мембраны, травматизация которых могла вызвать серьезные геморрагические осложнения. При использовании метки 50 мкм и мощности 0,24 Вт с нанесением коагулятов от периферии к центру ножки зрачковой мембраны были пересечены, за счет чего ее центральная часть сместилась к краю зрачка, освободив оптическую зону (рис. 1).
Результаты
В послеоперационном периоде наблюдалось ареактивное течение. Противовоспалительная поддержка включала в себя назначение препарата из группы НПВС в течение 2 нед. Уже в 1-е сут после операции пациент отметил субъективно повышение остроты зрения и, что немаловажно, впервые за 14 лет отсутствие пятна, напоминавшего подростку «жука», перед правым глазом (рис. 2).
Пациент выписан для проведения амбулаторного лечения с остротой зрения 0,5 и рекомендациями провести курсовое плеоптическое лечение.
Дискутабельным остается вопрос о лечении ПЗМ. Первым этапом, как правило, проводится консервативное лечение с применением мидриатиков, использование которых приводит к расширению зрачка и может способствовать разрыву нитей мембраны [4, 6]. Если консервативное лечение не дает нужного результата, возможно хирургическое вмешательство, которое заключается в отсечении тяжей мембраны от зрачкового края, аккуратном отделении ее от хрусталика вискодиссекцией либо при помощи микрошпателя и витреальных микроножниц с возможным сохранением целостности передней капсулы хрусталика и его прозрачности [1]. Показаниями к хирургии являются сращение ПЗМ с передней капсулой хрусталика, а также мембраны, сопровождающиеся помутнением хрусталика, случаи, отличающиеся большой площадью и плотностью нерассосавшейся ткани, полностью закрывающей просвет зрачка и приводящей к развитию обскурационной амблиопии. Однако хирургическое лечение сопряжено с риском развития осложнений, cвязанных с применением анестезии, а также кровоизлияний, инфекций, повреждением хрусталика.
В последние десятилетия в лечении ПЗМ наиболее часто стали использоваться лазерные технологии. Большинство авторов считают, что лазерная хирургия во многих случаях является более щадящей и обоснованной, чем оперативное лечение. Лазерные методы предполагают дисцизию ПЗМ или формирование отверстия в оптической зоне мембраны. В литературе описаны 2 метода лазерного воздействия: YAG-лазерная дисцизия и комбинированный метод аргон-YAG-лазерного лечения [4, 7-9].
YAG-лазерная дисцизия заключается в иссечении «ножек» мембраны при помощи Neodymium-YAG Laser, сама мембрана при этом остается в передней камере глаза [9]. Метод является предпочтительным у пациентов со светлыми радужками и наличием аваскулярных персистирующих мембран.
В МНИИ ГБ им. Гельмгольца (Москва) разработан и применяется комбинированный метод устранения врожденной остаточной зрачковой мембраны с иссечением верхнего отдела мембраны и аргон-коагуляцией ее к передней поверхности радужки [7]. По данным Н.Н. Арестовой (2004), метод используется при наличии аваскулярных мембран, не сращенных с передней капсулой хрусталика. В зарубежной литературе описано применение аргон-коагуляции мембраны [8] и Neodymium-YAG-лазерной дисцизии врожденной зрачковой мембраны [4] первым этапом перед факоэмульсификацией. Однако YAG-лазерная дисцизия ПЗМ может вызвать такие осложнения, как синдром пигментной дисперсии и геморрагии, риск возникновения которых значительно снижается при лазеркоагуляции мембраны.
Заключение
Таким образом, лазеркоагуляция васкуляризированной ПЗМ у пациентов с темной радужкой и отсутствием помутнений в хрусталике является наиболее предпочтительным и безопасным методом лечения. Также преимуществами данного вида лечения являются короткий период реабилитации и возможность лечения обскурационной амблиопии в ранние сроки после операции.
Поликория
Поликория - это офтальмопатология, при которой в радужной оболочке расположено два и более зрачка. Клинические проявления включают зрительный дискомфорт, снижение остроты зрения, появление «тумана» перед глазами, фотофобию. Для постановки диагноза достаточно физикального обследования. С целью уточнения формы заболевания проводят пробу с мидриатиками, УЗИ глаза, визометрию, периметрию, биомикроскопию глаз, изучают реакцию зрачков на свет. Рекомендовано применение оперативной тактики (иридопластики). При наличии противопоказаний к хирургическому лечению используют контактные линзы для устранения косметического дефекта и коррекции зрительной дисфункции.

Общие сведения
Поликория - врожденный порок развития радужной оболочки, который выявляют на первом году жизни ребенка. Описаны единичные случаи приобретенной формы патологии у лиц зрелого возраста. Статистические данные об общей распространенности заболевания отсутствуют. В качестве одного из проявлений синдрома Аксенфельда-Ригера дырчатые дефекты радужки диагностируют с частотой 1:200 000. В мире насчитывается около 35 000 человек с данной нозологией. Поликория с одинаковой частотой встречается среди лиц мужского и женского пола. Географических особенностей распространения болезни не наблюдается.

Причины поликории
Этиология заболевания до конца не изучена. Генетическая теория возникновения патологии базируется на выявлении мутации гена РАХ6. Основные причины поликории:
- Действие тератогенных факторов. Аномалии радужной оболочки часто связаны с воздействием ионизирующего излучения, употреблением матерью алкоголя и наркотических средств в период беременности.
- Колобома радужки. Образование дополнительных отверстий провоцирует частичное закрытие колобомы тканью мезо- или эктодермы на этапе эмбрионального развития.
- Внутриутробные инфекции. Поражение радужной оболочки вызывает инфицирование вирусом краснухи и опоясывающего герпеса или токсоплазмой, которые обладают способностью нарушать дифференциацию внутриглазных структур и вызвать множественные пороки развития плода.
- Иридокорнеальный эндотелиальный синдром. В основе этой патологии лежит эссенциально-мезодермальная дистрофия или частичная атрофия оболочки. На тех участках, где выраженное истончение оболочки сменяется атрофическими изменениями, образуется ложная поликория.
- Ятрогенное воздействие. Псевдополикория возникает вторично в послеоперационном периоде у пациентов, которым были проведены операции на радужке, из-за превышения мощности лазерного излучения при выполнении иридопластики.
- Травматическое повреждение. Образование нескольких зрачков часто обусловлено травмами или ожогами органа зрения. При этом наблюдается ложная форма заболевания.
- Синдром Аксенфельда-Ригера. Развитие поликории при данной нозологии связано с врожденной гипоплазией радужки и эктопией зрачка.
Патогенез
Истинная поликория возникает из-за нарушения эмбрионального развития глазного бокала. Наружный пигментный слой - это структура нейроэктодермального происхождения, из которой в норме образуется эпителиальный слой радужной оболочки, сфинктер и дилятатор зрачка. Стромальная ткань развивается из переднего сегмента мезенхимальной ткани. При действии тератогенных факторов или инфекционных агентов на 4-6 неделе внутриутробного развития плода нарушается процесс дифференциации двухслойного зрительного бокала и формирование ретинального пигментного эпителия. Из-за этого при рождении ребенка в области радужки наблюдаются множественные дырчатые дефекты.
Ложная поликория развивается, если зрачковая мембрана не поддается своевременному редуцированию. В основе формирования псевдополикории часто лежит явление мезодермального дисгенеза или нейротрофические нарушения, что приводит к формированию аномалий строения радужки. Доказана роль адгезии хрусталика к роговице на этапе разделения листков экто- и мезодермы в возникновении данной патологии. Из-за того, что в оболочке образуется несколько отверстий, сфинктер зрачка не может полноценно функционировать. Это приводит к спазму аккомодации и зрительной дисфункции. Изучается влияние генетической мутации на развитие поликории у скомпрометированных лиц.
Классификация
Поликория относится к числу врожденных пороков развития. Однако доказано, что возможен приобретенный вариант у пациентов с патологией радужки в анамнезе. Заболевание может симметрично поражать оба глаза или иметь одностороннее течение. С клинической точки зрения в офтальмологии выделяют следующие формы поликории:
- Истинная. Характеризуется наличием более одного зрачка при условии сохраненной реакции на свет.
- Ложная (псевдополикория). При этом варианте заболевания зрачок имеет форму песочных часов, т. к. зачатки мембраны, сформированной в эмбриональном периоде, соединяют края зрачка, которые расположены параллельно друг другу.
Симптомы поликории
Пациенты с поликорией отмечают выраженный дискомфорт в области глазницы при выполнении зрительной работы. В раннем возрасте возникают астенопические жалобы, вызванные образованием дырчатых дефектов радужки. Попадание большого количества света на сетчатку приводит к фотофобии. Возможны затруднения при работе за компьютером из-за яркого свечения монитора, при просмотре телевизора. Острота зрения снижается только на стороне поражения. Частые симптомы - затуманивание зрения, диплопия. Родители отмечают, что ребенок часто зажмуривает глаз, пытаясь ограничить его участие в зрении. Появление дефектов зрительного поля в виде скотом и фотопсий связано с общей аурой мигрени. Косметический дефект часто приводит к сложностям в социальной адаптации.
Осложнения
Распространенное осложнение поликории - амблиопия, возникновение которой обусловлено нарушением аккомодационной способности глазного яблока. При размере зрачков менее 1,5 мм зрительные функции не удается восстановить путем применения контактных линз. Пациенты подвержены риску развития инфекционных и воспалительных реакций (кератит, конъюнктивит, пан- и эндофтальмит). В редких случаях поликория осложняется глазной мигренью, вторичной открытоугольной глаукомой. У больных чаще выявляются дегенеративно-дистрофические и эрозивные изменения радужки, что обусловлено особенностями строения и применением контактных линз.
Диагностика
Для верификации диагноза офтальмологу достаточно провести наружный осмотр. В большинстве случае визуализируется 2-3 зрачка, один из которых больше по размеру. Отверстия в радужке округлые, реже неправильной формы. Специальное офтальмологическое обследование включает:
- Исследование зрачковой реакции. При истинной поликории реакция зрачков на яркий свет сохранена, вялая. Размеры отверстий в радужке уменьшены (менее 2,5 мм), положение эксцентричное, контур неровный. Нарушена конвергенция и аккомодация. При ложной форме реакция зрачков не возникает.
- УЗИ глаза. Ультразвуковое исследование дает возможность визуализировать зрачковый сфинктер при истинном варианте и его отсутствие в области дополнительных отверстий при псевдополикории. Также методика используется для выявления сопутствующих клинических проявлений при развитии поликории на фоне патологии Аксенфельда-Ригера.
- Проба с мидриатиками. Инстилляции М-холиноблокаторов вызывает стойкое расширение зрачков при истинной форме. Применение пробы при ложном варианте не потенцирует мидриаз.
- Биомикроскопия глаза. Позволяет обнаружить дегенеративно-дистрофические изменения радужки, детально изучить характеристики зрачковых отверстий, диагностировать признаки воспалительных и инфекционных заболеваний переднего отдела глазного яблока.
- Периметрия. При локализации дополнительных зрачков на периферии радужки диагностируют сужение зрительного поля.
- Тонометрия. Измерение внутриглазного давления проводится для выявления признаков повышения офтальмотонуса, проведения дифференциальной диагностики между глазной мигренью и истинной офтальмогипертензией.
- Визометрия. Исследование позволяет оценить степень снижения остроты зрения. Дополнительно может осуществляться рефрактометрия для изучения типа клинической рефракции у пациента.
Лечение поликории
Тактика ведения определяется выраженностью симптоматики, размерами и количеством зрачков, возрастом пациента. Раннее устранение дефекта дает возможность профилактировать развитие спазма аккомодации и амблиопии. В лечении поликории применяется:
- Пластика радужки. Оперативное вмешательство осуществляется закрытым способом после предварительного проведения парацентеза. При обширном поражении радужной оболочки или множественных дефектах органа зрения на одном из этапов операции показана имплантация иридохрусталиковой диафрагмы.
- Хирургическая коррекция. При выявлении патологии в период новорожденности и диаметре зрачков более 2 мм накладываются швы с формированием единого зрачкового отверстия. Данная методика применима, если у ребенка имеется не менее трех зрачков в одном глазу.
- Симптоматическая терапия. Используется только при наличии абсолютных противопоказаний к оперативному лечению. Сводится к применению косметических линз для устранения визуального дефекта. Коррекция остроты зрения проводится при помощи контактных линз или очков.
Прогноз и профилактика
Прогноз для жизни и трудоспособности при поликории благоприятный. При своевременном устранении порока развития возможно полное восстановление зрительных функций. Специфическая профилактика заболевания не разработана. Неспецифические превентивные меры сводятся к исключению воздействия тератогенных факторов и предупреждению внутриутробного инфицирования плода патогенными агентами, способными проникать через гематоплацентарный барьер. Для предотвращения возникновения приобретенной формы рекомендовано применять средства индивидуальной защиты (очки, каска) в условиях работы на производстве.
Аномалии развития глаза
Аномалии развития глаза - это наследственные или врожденные пороки развития органа зрения, приводящие к неправильной закладке отдельных структур и глазного яблока в целом. Характерно изменение размеров глазного яблока вплоть до его полного отсутствия, недоразвитие роговицы, радужной оболочки, стекловидного тела, хрусталика и других отделов глаза. Патология сопровождается снижением зрения, часто сочетается с другими пороками развития. Диагностируется на основании клинических признаков, офтальмоскопии и биомикроскопии глаза. Лечение аномалий развития глаза направлено на коррекцию зрения и возможное сохранение пораженных частей глаза. Также проводится терапия основного заболевания.
МКБ-10


Аномалии развития глаза в совокупности встречаются достаточно часто. Многие системные пороки развития клинически проявляются различными дефектами органа зрения. Высокая актуальность данной группы патологий в практической педиатрии связана с огромной ролью зрения в повседневной жизни, особенно с рождения. В то же время, основная часть аномалий развития глаза требует длительной и сложной коррекции, которая нередко приводит лишь к частичному восстановлению зрительной функции. Кроме того, при большинстве пороков необходимо применение высокотехнологичных дорогостоящих методов хирургического лечения. В дальнейшем такие дети практически всегда имеют группу инвалидности и показания для специального обучения на дому.

Причины
Возможно наследование по аутосомно-доминантному, аутосомно-рецессивному типу, X-сцепленное наследование. Также встречаются врожденные аномалии развития глаза, возникающие под влиянием тератогенных факторов в первом триместре беременности. На 2-5 неделях эмбриогенеза происходит закладка органа зрения, воздействие радиации, алкоголя, никотина, наркотиков и запрещенных медикаментов именно в этот период приводит к нарушению правильного формирования глаза. Внутриутробные инфекции также становятся причиной врожденных пороков органа зрения. Реже аномалии формируются в составе хромосомных синдромов, например, при синдроме Дауна.
Симптомы
Патология может затрагивать глаз в целом, а может представлять собой нарушение закладки отдельных оболочек и структур органа зрения. Аномалии развития глаза в целом проявляются изменением его размеров. Чаще всего речь идет о микрофтальме различной степени вплоть до полного отсутствия глазного яблока (анофтальм). Пораженный глаз визуально меньших размеров, возможен двусторонний микрофтальм. Также встречается криптофтальм, представляющий собой недоразвитие век, которые частично или полностью срастаются с роговицей. Такие грубые аномалии развития глаза заметны сразу после рождения.
Порок может затрагивать отдельно роговицу, радужную оболочку, хрусталик иди другие отделы глазного яблока. Заметить аномалию развития может педиатр и детский офтальмолог. Врожденные патологии радужки характеризуются ее недоразвитием или отсутствием (аниридия), наличием колобом или округлых дефектов, напоминающих зрачки (поликория). Аномалии хрусталика и сетчатки могут визуально не проявляться и диагностируются только в момент осмотра.
Для всех аномалий развития глаза характерно снижение зрения различной степени выраженности. По этой причине малыш может не реагировать на свет и на окружающих. Пороки часто сочетаются с другими дефектами лицевого черепа, а также с дисплазией костной ткани, умственной отсталостью и другими заболеваниями.

Первичная диагностика возможна уже в роддоме. Грубые аномалии развития глаза, как уже было сказано, заметны при первом осмотре, диагноз не вызывает сомнения. Осмотр офтальмолога в роддоме также является обязательным для всех новорожденных. Офтальмоскопия позволяет выявить аномалии развития радужной оболочки, хрусталика. Для подтверждения диагноза часто требуется биомикроскопия глаза - осмотр при помощи щелевой лампы. Исследование дает возможность обнаружить мелкие дефекты, которые можно пропустить при обычной офтальмоскопии. Например, так можно заметить вывихи и подвывихи хрусталика, обычно связанные с заболеваниями соединительной ткани (синдром Марфана), вследствие чего мышцы хрусталика не могут держать его в правильном положении.
Лечение аномалий развития глаза
Тактика ведения пациентов зависит от вида порока, возможности восстановления утраченной функции зрения, а также от возраста ребенка и других факторов. При аномалиях глазного яблока показана стимуляция роста орбиты при помощи специальных имплантатов. В дальнейшем может быть выполнена операция по имплантации искусственного глаза. С целью улучшения зрения всем пациентам проводится плеоптическая терапия, способствующая стимуляции развития пораженного участка. В целом терапия направлена на улучшение адаптации пациентов, поскольку зрительный анализатор считается основным источником информации из внешнего мира.
Хирургическое лечение включает операции, например, по замене хрусталиков в случае врожденной катаракты, вмешательства на роговице и другие микрохирургические манипуляции. Коррекция зрения также проводится с помощью очков и контактных линз. При недоразвитии радужной оболочки или полном ее отсутствии показаны специальные линзы, выполняющие функции радужки.
Поскольку аномалии развития глаза часто сочетаются с другими пороками, необходима их хирургическая коррекция, а также лечение основного заболевания. Многие врожденные обменные нарушения, например, мукополисахаридозы, являются причиной глазных аномалий, лечение ферментами в подобных случаях также улучшает прогноз для органа зрения.
Грубые пороки плохо поддаются коррекции. При одностороннем анофтальме зрение на втором глазу обычно снижено. Методы плеоптической терапии имеют лишь незначительный эффект, качество жизни улучшается только после имплантации глаза. Однако даже в этом случае инвалидность неизбежна. Кроме того, аномалии развития глаза редко встречаются изолированно, что также оказывает негативное влияние на прогноз. Профилактика заключается в исключении воздействия тератогенных факторов на ранних сроках гестации. Необходимо планирование беременности и генетическая консультация в случае наследственных заболеваний у родителей и других родственников.
1. Большие и малые аномалии развития органа зрения при хромосомной патологии/ Шерстнев Г. Е.// Вестник Совета молодых учёных и специалистов Челябинской области. - 2017.
2. Морфологические особенности клинических проявлений некоторых видов врожденных аномалий хрусталика и стекловидного тела/ Харлап С. И., Салихова А. Р., Аветисов К. С., Аветисов С. Э. // Вестник офтальмологии. - 2017. - 133(2).
Аниридия ( Иридеремия )
Аниридия - это редкое, в большинстве случае генетически детерминированное заболевание глаз, для которого характерно полное или частичное отсутствие радужной оболочки. Клинически проявляется снижением остроты зрения, горизонтальным нистагмом и светобоязнью. Для диагностики заболевания необходимо провести осмотр переднего отдела глазного яблока, офтальмоскопию, тонометрию, гониоскопию, ультразвуковую биомикроскопию, исследовать клиническую рефракцию. Установить этиологию аниридии можно при помощи генетического тестирования. Специфическое лечение аниридии основывается на трансплантации искусственной радужки.



Аниридия (иридеремия) относится к ряду орфанных (редких) заболеваний, характеризующихся гипоплазией радужной оболочки глаз. Частота распространения заболевания в среднем составляет 1:70000. К ассоциированным с аниридией заболеваниям относят синдром Гиллеспи и WAGR-синдром. Пациенты с иридеремией входят в группу риска развития катаракты, глаукомы, помутнения роговицы. В связи с наличием генетической мутации гена PAX6 высока вероятность возникновения патологий других органов и систем организма.
Наследственная предрасположенность наблюдается у 65% больных аниридией, поскольку заболевание может передаваться, как по аутосомно-доминантному, так и по аутосомно-рецессивному типу. В 35% случаев патология носит спорадический характер, вызванный впервые проявившейся мутацией. Заболевание в равной степени распространено среди мужского и женского пола, не имеет расовых отличий и особенностей в географическом распространении.

Причины аниридии
Этиологическим фактором развития врожденной аниридии является мутация гена PAX6, что локализуется на 11 хромосоме. Данный ген кодирует факторы транскрипции, которые на этапе эмбриогенеза индуцируют развитие глазного яблока, а также регулируют процессы дифференциации органов центральной нервной системы, носа, поджелудочной железы. В случае патологии экспрессии гена PAX6 нарушается формирование анатомических структур глазного яблока, которое происходит на 12-14 неделе гестации. Причиной развития аниридии может выступать травматическое повреждение глаз, сопровождающееся отрывом радужки у корня.
Патогенез данного заболевания напрямую зависит от степени функциональной активности аллелей гена PAX6. На протяжении дифференциации радужки снижается степень экспрессии белковых структур цитокератинов и факторов адгезии. В свою очередь, теряется способность клеток к миграции из нервного гребня к месту формирования стромы радужной оболочки.
При низкой степени экспрессии гена не происходит на должном уровне дифференциация хрусталика и пигментного эпителия сетчатки, что является предпосылкой к комбинации врожденной катаракты и аниридии. При вовлечении в патологический процесс угла передней камеры глаза и трабекулярного аппарата развивается врожденная глаукома. В более зрелом возрасте глаукома возникает из-за образования синехий. Также в роли фактора, играющего роль в развитии аниридии, выступает дефицит лимбальных стволовых клеток.

Симптомы аниридии
По происхождению в современной офтальмологии выделяют врожденную и приобретенную (травматическую) формы аниридии. Симптомы травматической иридеремии зависят от степени повреждения радужной оболочки. С клинической точки зрения выделяют полную, частичную и сочетанную с Гиллеспи и WARG-синдромом аниридию.
Полная форма заболевания характеризуется наличием небольших остатков корня радужки. Клинически заболевание проявляется снижением остроты зрения, что связано с недоразвитием структур глазного яблока. Степень снижения остроты зрения напрямую зависит от наличия в анамнезе катаракты, глаукомы и кератопатии. Отсутствие радужной оболочки приводит к повышенной светочувствительности. Одним из симптомов полной аниридии является горизонтальный нистагм в сочетании с косоглазием.
Для частичной аниридии свойственна та же симптоматика, что и для полной формы патологии. Но в связи с тем, что для заболевания характерна легкая степень гипоплазии стромы радужной оболочки, клинические проявления слабо выражены.
WARG-синдром, помимо аниридии, включает в себя опухоль Вильмса (злокачественная нефробластома), заболевания мочеполовой системы и задержку психического развития. Часто в данный симптомокомплекс входит панкреатит и хроническая почечная недостаточность. Внешний вид пациентов может сопровождаться гемигипертрофией (гипертрофией мышечного аппарата одной из половин тела). На ранних этапах развития синдром может не иметь выраженных клинических проявлений, что является причиной гиподиагностики.
Синдром Гиллеспи характеризуется сочетанием аниридии с клинической картиной мозжечковой атаксии и умственной отсталости. У ряда пациентов отмечают птоз, снижение слуха и стеноз клапана легочной артерии.
В комплекс диагностических мероприятий при аниридии включают визуальный осмотр передних отделов глаз, офтальмоскопию, тонометрию, гониоскопию, исследование клинической рефракции и ультразвуковую биомикроскопию. Генетический анализ позволяет определить причину развития аниридии. Его проводят только в случае врожденных форм заболевания.
- Осмотр глаза. При осмотре передних отделов глаз не удается визуализировать радужную оболочку. В частных случаях наблюдаются небольшие скопления радужки, что наиболее характерно для травматической или частичной аниридии. Методом офтальмоскопии удается выявить гипоплазию центральной части сетчатки и зрительного нерва, что свойственно для полной формы аниридии.
- Тонометрия. Позволяет измерить внутриглазное давление (ВГД). Повышение ВГД выше толерантных значений является фактором риска глаукомы. Пациентам с аниридией рекомендовано измерять ВДГ при помощи прибора ICare, что позволяет провести манипуляцию без анестетиков. С целью профилактики развития глаукомы необходимо проводить тонометрию и офтальмоскопию в динамике. Гониоскопия требуется пациентам с повышенным ВДГ для дополнительного осмотра передней камеры глаза.
- Исследование клинической рефракции. Проводится методом скиаскопии, прямой офтальмоскопии или рефрактометрии. В зависимости от сопутствующей патологии может выявляться эмметропическая, гиперметропическая и миопическая рефракция.
- УЗ-биомикроскопия. Метод ультразвуковой биомикроскопии позволяет оценить остаточную ткань радужной оболочки и исследовать глазное дно у больных катарактой или кератопатией.
- Генетические анализы. Для подтверждения наследственной аниридии выполняется FISH-тест и исследования на определения типа дефекта гена PAX6. Проведение FISH-теста необходимо для исключения WARG-синдрома. До момента проведения генетического анализа необходимо 1 раз в 3 месяца проводить УЗИ почек и органов малого таза.
- Другие исследования. В качестве дополнительных методов исследования применяется оптическая когерентная томография, зрительные вызванные потенциалы и топография роговицы.

Лечение аниридии
Специфическое лечение аниридии основывается на имплантации искусственной радужки. Протез состоит из специального гидрогеля с отверстием, соответствующим зрачку. Цвет искусственной радужки подбирают в соответствии с цветом глаз пациента. Оперативное вмешательство проводится при помощи транссклерального хирургического доступа.
Имплантация искусственной радужки показана пациентам с травматической аниридией. При врожденных формах заболевания оперативное вмешательство проводится только в том случае, если риск повреждения роговицы является минимальным. При сочетании аниридии с катарактой тактика операции сводится к имплантации протеза, замещающего, как радужку, так и хрусталик.
Симптоматическое лечение включает в себя использование косметических контактных линз для скрытия дефекта радужной оболочки. При повышении внутриглазного давления рекомендовано использовать капли из группы ингибиторов карбоангидразы, простагландинов и бета-блокаторов. Для профилактики развития кератопатии необходимо использовать увлажняющие капли и гели. Всем пациентам необходимо носить солнцезащитные очки, которые обеспечивают 100% блокировку ультрафиолетовых лучей.
Специфические меры по профилактике аниридии не разработаны, т. к. заболевание связано с генетической мутацией. Семье, в которой один из родителей болен аниридией, перед планированием беременности необходимо проконсультироваться у генетика и врача-офтальмолога. Профилактика травматической аниридии сводится к соблюдению техники личной безопасности, т. к. сильный удар может стать причиной отрыва радужной оболочки.
При соблюдении всех рекомендаций прогноз при врожденной аниридии для жизни благоприятный. Развитие глаукомы или ассоциация аниридии с Гиллеспи и WARG-синдромом может стать причиной ранней инвалидизации пациента.
2. Генетические аспекты врожденной аниридии/ Васильева Т.А.,Поздеева Н.А.,Воскресенская А.А. и др.// Практическая медицина. - 2015.
3. Клинические особенности врожденной аниридии в детском возрасте/ Воскресенская А.А., Поздеева Н.А.,Васильева Т.А. и др.// Российская педиатрическая офтальмология. - 2016.
Наследственные заболевания глаз. Какие же они?
Глаза - один из самых важных органов для человека, связанный с головным мозгом, и другими органами. На основе информации, которую дают глаза, человек выполняет те или иные действия, ориентируется в пространстве, формирует восприятие действий и предметов.
Некоторые люди через наследственность не могут пользоваться зрением в полной мере. Врожденные аномалии глаз встречаются у 1 - 2% случаев всех новорождённый детей. Современная медицина нашла более 1200 генов, отвечающих за возможность возникновения определенных заболеваний.
Многие из наследственных заболеваний глаз протекают бессимптомно, не меняют остроту зрения, поэтому человек, длительное вовремя может не замечать некоторые небольшие изменения, и тем самым теряет драгоценное время.
Виды наследственных заболеваний глаз
Офтальмологи разделяют наследственные заболевания на 3 группы:
- врожденные патологии глаз, при котором необходимо хирургическое вмешательство;
- небольшие дефекты, которым не нужно специальное лечение;
- аномалии глаз связанные с заболеваниями других органов.
Коломба радужки
Среди заболеваний глаз, передающихся по наследству или же возникающих на начальной стадии развития плода, выделяют:
- микроофтальм (пропорционально уменьшенные глаза);
- дальтонизм (отсутствие возможности различать некоторые или все цвета, либо путать их);
- анофтальм (отсутствие глазных яблок или одного из них);
- альбинизм (отсутствие пигментации в радужке глаза);
- аномалии строения век: птоз (опущение верхнего века), колобома (различные дефекты века), выворот или заворот века;
- аномалии роговицы: помутнение роговицы врожденное; изменение формы, которая покрывает зрачок оболочки - кератоглобус, кератоконус и т.д.;
- врожденная глаукома (повышенное давление внутри глаза). Для него характерна атрофия зрительного нерва, в результате чего полностью исчезает зрение;
- ретролентальная фиброплазия (за хрусталиковое соединительно - тканное повреждение сетчатки и стекловидного тела) - встречается у недоношенных детей и связано с нарушением давления в кювезах;
- врожденная катаракта (невозвратимые изменения в хрусталике глаза). Болезнь характеризуется полным или частичным помутнением хрусталика, через то, что теряет былую прозрачность; человек, может различать лишь часть световых лучей, образы становятся размытыми. Если не лечить заболевание во время, все может закончиться слепотой;
- дакриоцистит (воспалительный процесс вызывающий непроходимость слезных путей);
- внутриглазное кровоизлияние у новорождённый (в результате тяжелых родов);
- поражение сетчатки глаза и зрительного нерва: гипоплазия (недоразвитость), врожденная отслойка сетчатки;
- пороки развития сосудистого тракта глаз (отсутствие зрачка, щелевидный зрачок, множественные зрачки).
Врожденная глаукома
Стоит отметить, что чаще всего проявляют себя катаракта и глаукома.
Такого рода заболевания могут проявлять себя не сразу, а через время (в любом возрасте).
Заболевания, которые проявляются в детском возрасте

Ретинобластома
К группе заболеваний, которые проявляют себя непосредственно после рождения, или же впервые годы жизни относятся:
- нистагм (хаотическое движение глазных яблок);
- ретинобластома (злокачественное образование на сетчатке);
- близорукость.
В более позднем возрасте могут проявить себя:
Причины возникновения врожденных заболеваний глаз
Причины возникновения аномалий глаз разняться, на них большое влияние имеют внутренние факторы и влияние окружающей среды.
Среди основных внутренних причин выделяют:
- нарушение роста нормальных тканей и их замена на патологические виды вовремя внутриутробного развития;
- нарушение нормального развития нормальных тканей как ответ на патогенное действие других;
- тератогенные терминационные периоды (критические периоды внутриутробного развития плода, когда усиливается дифференциация глазных тканей, особенно важным является период с 3 по 7 неделю вынашивания ребенка);
- гормональные нарушения;
- возраст родителей (нарушения встречаются у детей тех родителей, которые решили иметь ребенка после сорока лет, и у тех, кто не достигли 16 - летнего возраста);
- несовместимость резус - факторов плода и матери;
- наличие врожденных аномалий связанных с нарушением обмена веществ;
- хромосомные мутации;
- трудно разрешимые роды или перенесение патологических родов;
- родственные браки и много других факторов.
Основа патологической наследственности - повреждение определенных ядерных наследственных структур половых клеток, которые являются материальными носителями наследственности. Другими словами - это мутация генов, которая провоцирует появление болезней, передающихся по наследству. В некоторых случаях, она может возникнуть спонтанно (по непонятным пока для науки причинам).
Факторы окружающей среды, которые влияют на возникновение внутриутробных аномалий глаз:
- радиация (лучи радия, рентгена могут провоцировать повреждение хромосом, соматических клеток);
- инфекционные заболевания;
- вирусные заболевания (ветрянка, оспа, краснуха, грипп);
- интоксикации различных видов (алкогольные, медикаментозных препаратов).
Лечение врожденных аномалий
С помощью современного оборудования можно вылечить множество заболеваний глаз даже у новорождённый деток. К такому оборудованию относят:
- фундус - камеру (позволяет обследовать глазное дно);
- лазерный сканер;
- электрофизиологический анализатор;
- ультразвуковая игла;
- специальные операционные микроскопы для проведения хирургических вмешательств с ювелирной точностью и другое оборудование.
Некоторые заболевания глаз можно вылечить только хирургическим путем (устраняются анатомические и функциональные недостатки).
В лечении глаукомы очень важно вовремя ее диагностировать и провести офтальмологическую операцию (так появиться больше шансов, что ребенку сохранят зрение).
Полноценное развитие сетчатки, снижение риска развития косоглазия, ослабления зрительного анализатора, амблиопии, а также снижения опасности непроизвольных колебательных движений глаз (нистагмы) при катаракте, специалистами назначается профилактическое и медикаментозное лечение.
Непроходимость слезно - выводящих путей лечиться комплексно (с помощью медикаментов и массажей нижнего века). Эти мероприятия помогают в 99% случаев.
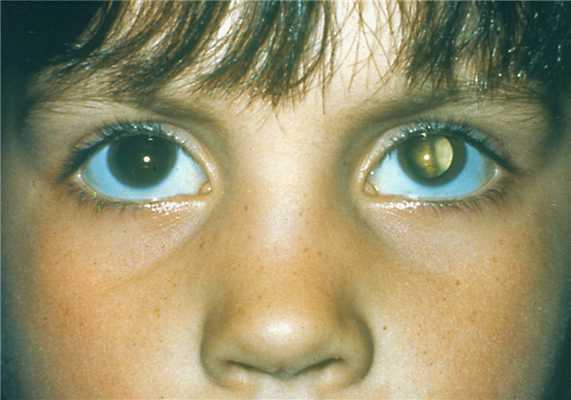
В лечении катаракты важно проводить профилактические мероприятия, которые будут направлены на уменьшение осложнений. Операцию проводят, основываясь на возраст и остроту зрения у ребенка. Если хрусталик сильно помутнен, операцию можно проводить уже в первые пол года жизни. Далее используют специальные корректирующие очки /линзы.
Если птоз выявлен на ранних стадиях, устраняется он оперативно, когда ребенок достигает 2 - 3 летнего возраста. До достижения этого возраста веки поднимают механическим способом (удерживают с помощью лейкопластыря, чтобы нормально развивалось зрение).
Врожденное или возникшее косоглазие, не такое уж невинное заболевание как кажется, так как оно может свидетельствовать о некой возможной патологии зрения. После обследования окулист назначает лечение (медикаменты, физкультура).
Важно в раннем возрасте выявить ангинному (доброкачественное, в основном врожденное образование, состоящее из кровеносных и лимфатических сосудов). Если новообразование не увеличивается в размере, от него избавляются в раннем возрасте - удаляют методом криокоагуляции, или же с помощью косметической хирургической операции.
Профилактика
Чтобы предупредить появление глазных заболеваний (а в некоторых ситуациях спасти жизнь ребенка) можно с помощью использования таких профилактических и лечебных мероприятий для родителей, которые имеют различные проблемы со здоровьем:
- раннее заменное переливание крови (при наличии наследственных эритроблстозов, которые возникли в следствии резус - несовместимости);
- назначение специальной диеты при сахарном диабете и галактоземии;
- использование инсулина при диабете;
- прием эффективных препаратов белка, для излечения гемофилии.
Кроме того, будущим родителям обязательно необходима консультация врача - генетика (если у них имеются заболевания глаз, или первый ребенок имеет какие - либо заболевания глаз). Также можно воспользоваться одним из методов исследования (биохимическим или цитогенетическим) и таким образом предупредить болезни, которые могут передаться генетически.
Своевременная диагностика и врожденных заболеваний, а также их правильное и лечение, является лучшей профилактикой возникновения и развития слепоты у детей и взрослых.
Читайте также:
- Аллергия, астма на лекарства и химические вещества
- Ферменты крови при стрессовой кардиомиопатии (СКМП). Дифференциация с инфарктом миокарда (ОИМ)
- Анатомия: Вегетативная (автономная) нервная система. Функции вегетативной нервной системы.
- Мигрень. Признаки мигрени. Аура при мигрени. Головная боль напряжения.
- Стоимость восстановления утерянного зуба имплантом снижается
