Генетические причины мужского бесплодия. Синдром Клайнфелтера, муковисцидоз
Добавил пользователь Евгений Кузнецов Обновлено: 01.02.2026
Пытаться зачать ребенка иногда гораздо труднее, чем кажется. Хотя человеческий род продолжается, удивительно, сколько должно произойти, чтобы забеременеть. Одним из препятствий на пути к зачатию является бесплодие по мужскому фактору. Если у вашего партнера низкое количество сперматозоидов, нарушена подвижность или что-то не так в его сперме, ваши шансы забеременеть невелики. Проблема не в самой сперме. Некоторые мужчины не могут доставить сперму в матку партнерши, что также крайне затрудняет зачатие. Если вы безрезультатно пытались зачать ребенка в течение 12 месяцев подряд (или шести месяцев для женщин старше 35 лет), пришло время обратиться к специалисту по бесплодию. После некоторых анализов, проведенных как вами, так и вашим партнером, врач сможет понять причину трудностей. Половина пар, обращающихся за лечением бесплодия, считают, что мужской фактор бесплодия имеет определенное отношение к их неспособности зачать ребенка.
Содержание
Это генетика?
Как и в случае с женским бесплодием, причины могут быть самыми разными. В некоторых случаях может быть генетическая связь. Часто, когда специалист по бесплодию видит в сперме мужчины очень низкую концентрацию сперматозоидов или их полное отсутствие, он рекомендует провести генетическое тестирование. Это также касается случаев, когда яички мужчины очень маленькие или неправильной формы. Генетическое тестирование также оправдано в случае нескольких выкидышей. Если ваш врач обнаружит генетическую связь, то следующим шагом обычно является дальнейшее исследование путем генетического консультирования, которое поможет вам определить, будет ли успешным использование спермы вашего партнера. Ваш врач также рассмотрит с вами и вашим партнером некоторые альтернативные варианты.
Генетическое бесплодие по мужскому фактору
Согласно последним исследованиям, около 10%-15% случаев бесплодия по мужскому фактору являются генетическими.
Хотя гормональный дисбаланс, возраст, образ жизни, вес и диета чаще всего связаны с генетикой. Иногда это единственный фактор мужского бесплодия. Вот некоторые из наиболее распространенных генетических причин мужского бесплодия.
- Мутация гена муковисцидоза: Приблизительно один из каждых 32 000 человек кавказской национальности страдает муковисцидозом. Недавно исследователи обнаружили различные формы этого заболевания, которые влияют на фертильность только у мужчин. У мужчин, страдающих муковисцидозом, обычно отсутствует трубка, по которой сперматозоиды попадают из яичек в уретру. Если у партнера-мужчины есть это заболевание, необходимо генетическое консультирование. Вам необходимо определить, являетесь ли вы и ваш партнер носителем генной мутации, вызывающей муковисцидоз, поскольку это будет представлять значительный и серьезный риск для ваших будущих детей. Если МВ присутствует только у мужчины, он обычно производит нормальную сперму. Ваш врач может преодолеть отсутствие семявыносящих протоков, извлекая сперму и используя ее для оплодотворения яйцеклетки с помощью ЭКО.
- Синдром Клайнфельтера: Когда мужчина рождается с лишней Х-хромосомой (половая хромосома XXY), у него может быть синдром Клайнфельтера. Эта распространенная генетическая проблема бесплодия встречается примерно у одного из каждых 500-1000 мужчин. Синдром Клайнфельтера вызывает низкое количество сперматозоидов, отсутствие сперматозоидов в сперме или очень низкий уровень тестостерона. В некоторых случаях у мужчин с синдромом Клайнфельтера в яичках есть здоровые сперматозоиды. В этом случае врач может извлечь сперматозоиды и оплодотворить яйцеклетку с помощью ЭКО.
- Бесплодие по Y-хромосоме: Бывают случаи, когда отсутствует часть Y-хромосомы. Это хромосомы, которые связаны с фертильностью, и если они микроудалены (удалены части), это влияет на способность мужчины вырабатывать здоровые сперматозоиды. В зависимости от типа микроделеций в яичках у мужчины все еще может вырабатываться некоторое количество здоровых сперматозоидов. Мужчины с таким заболеванием передают его своим сыновьям. Это происходит независимо от того, произошло ли зачатие в результате использования вспомогательных репродуктивных технологий или естественным путем.
- Дополнительные генетические проблемы: Диагноз бесплодия ставится как “необъяснимый”. При дальнейшем тестировании врач может обнаружить сбалансированные транслокации. Этот термин относится к перестройке хромосом, которая может быть причиной бесплодия, многочисленных выкидышей или врожденных дефектов у детей. Если ваш врач диагностирует сбалансированную транслокацию, он, скорее всего, порекомендует ЭКО с ПГТ.
У вас есть варианты
Во всех вышеперечисленных случаях, в зависимости от степени генетического мужского фактора бесплодия, донорская сперма является приемлемым вариантом. В случаях, когда генетическое консультирование выявляет высокий риск врожденных пороков развития, донорская сперма часто является лучшим решением для получения здоровой беременности с прекрасным исходом. Если вы задаетесь вопросом, может ли ваше бесплодие по мужскому фактору быть генетическим, обратитесь в План Б. Наша команда найдет ответы и решения для вас и вашего партнера. Не откладывайте свою мечту о создании семьи на потом. Давайте работать вместе.
Азооспермия - симптомы и лечение
Что такое азооспермия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Скатова Бориса Валерьевича, уролога со стажем в 28 лет.
Над статьей доктора Скатова Бориса Валерьевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов
Определение болезни. Причины заболевания
Азооспермия — отсутствие сперматозоидов в эякуляте (семенной жидкости). Является одной из причин бесплодного брака. Распространенность азооспермии среди всех мужчин составляет менее 1%, среди мужчин, состоящих в браке и не имеющих детей — 11-14 % [1] [2] . Азооспермию следует рассматривать, скорее, как патологический симптомокомплекс, а не в качестве самостоятельного заболевания.
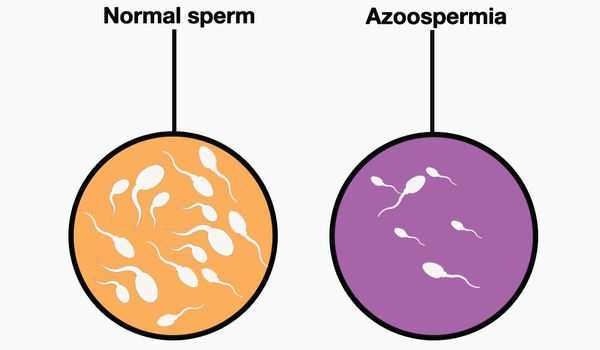
Причины возникновения азооспермии подразделяют на тестикулярные, претестикулярные и посттестикулярные.
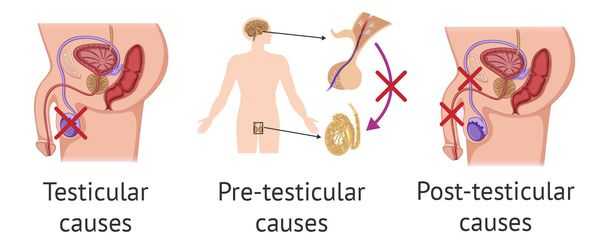
Тестикулярные причины обусловлены:
- генетическими факторами (отсутствием лоскута Y-хромосомы, отвечающего за сперматогенез; синдромом Клайнфельтера — наличие дополнительной женской половой X-хромосомы; муковисцидозом, приводящим к врождённому отсутствию семявыводящих протоков [8] ; синдромом Юнга, характеризующимся систематической закупоркой протоков яичка; синдромом Прадера-Вилли — отсутствием отцовской копии участка хромосомы [9] );
- врождёнными аномалиями (недоразвитием (аплазией) яичек; крипторхизмом — несвоевременным выходом яичек из брюшной полости наружу; варикоцеле);
- осложнениями инфекций (орхитом после перенесённого паротита и другими);
- половыми излишествами (недозреванием половых клеток в придатках яичка);
- сахарным диабетом (нарушением обмена веществ в яичке).
К претестикулярным причинам следует отнести:
- опухоль гипофиза, кровоизлияния в головной мозг;
- дисфункцию гипоталамуса (неправильную выработку гормонов);
- гипогонадотропный гипогонадизм (недостаточность сперматогенеза вследствие отсутствия стимуляции его гонадотропинами);
- токсические воздействия (наркотики, алкоголь, препараты тестостерона, антибиотики, стероиды, противовоспалительные препараты и пестициды);
- воздействие ионизирующей радиации (а также рентгеновского излучения) и лучевой терапии;
- постоянную гипертермию (частое посещение бани или сауны, заболевания, сопровождающиеся высокой температурой);
- тяжёлые физические и психологические нагрузки, стрессы;
- недостаток витаминов и микроэлементов в пище.
Протестикулярные причины заключаются в обструкции (препятствии) и нарушении семенных протоков. Этому способствует:
- проведение вазэктомии, перевязывания семявыводящих протоков и вазографии семенных путей с применением контрастных средств;
- осуществление оперативного вмешательства в область эякуляторных каналов;
- наличие воспалительных заболеваний, опухолей придатков яичка, семенных пузырьков и предстательной железы;
- использование метода грыжесечения (в особенности у детей) с целью пластики грыж полипропиленовых сеток, который вызывает в окружающих тканях фиброз и вовлекает семявыводящие протоки с дальнейшей их полной облитерацией (заращением);
- возникновение ретроградной эякуляции (полный или частичный выброс семенной жидкости в мочевой пузырь) и нарушение эмиссии (сперма не поступает в заднюю часть мочеиспускательного канала);
- онкологические заболевания крови (лейкоз, болезнь Ходжкина) [11] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы азооспермии
Основной симптом — невозможность зачать ребёнка (крайне малое количество сперматозоидов в эякуляте или же их полное отсутствие) при сохранённой сексуальной функции.
Косвенные симптомы:
- обнаружение гена наследственной патологии или её признаков;
- повышение числа антиспермальных тел в эякуляте;

- малое количество семенной жидкости, возникающее во время эякуляции;
- белые непроизвольные выделения из мочеиспускательного канала;
- повышенное оволосение;
- малый размер яичек при их повышенной плотности;
- гипоплазия (уменьшение) предстательной железы;
- сексуальные дисфункции после инфекционного заболевания.
Патогенез азооспермии
Чтобы лучше понять патологические процессы, происходящие со сперматозоидами, рассмотрим нормальную физиологию сперматогенеза.
Сперматозоиды и мужские половые гормоны (андрогены) вырабатываются в основных половых железах мужчины — яичках. Этот процесс называется сперматогенезом. Одни из самых важных клеток яичка — клетки Лейдега (описаны в 1850 году Францем Лейдегом). Они вырабатывают тестостерон — основной мужской половой гормон, а также клетки иммунной системы — макрофаги и лимфоциты. В канальцах яичка осуществляется сперматогенез с активным участием клеток Сертоли. Эти клетки синтезируют множество факторов, участвующих в образовании сперматозоидов: белки, гормоны, биологически активные вещества, именно они определяют объём яичек, качество и количество спермы.
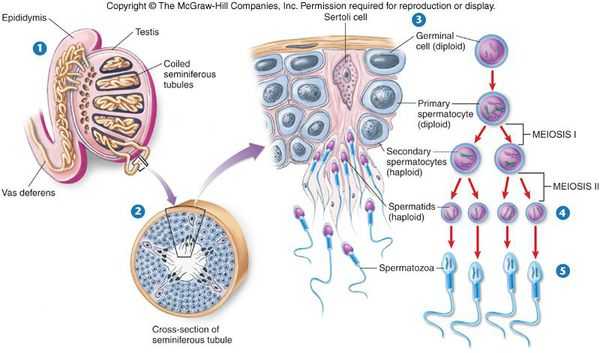
Образование сперматозоидов начинается в канальцах яичка с делением стволовых клеток и заканчивается путём сложных преобразований в зрелые сперматозоиды. Дозревание и концентрация сперматозоидов происходит в небольшом придатке яичка (а именно в его хвосте), где спермии могут сохранять жизнеспособность в течение двух недель. Попадают недозрелые сперматозоиды из более извитых канальцев яичка за счёт смывания их жидким секретом клеток Сертоли в более прямые канальцы, сливающиеся в общий канал придатка яичка. Далее сперма эвакуируется из мужского организма путём эякуляции, при помощи эрекции. В ответ на сексуальные стимулы эректильные парасимпатические нервы выделяют ацетилхолин, который расширяет артерии промежности, увеличивает кровоток в кавернозных и губчатых телах полового члена. Это способствует набуханию пениса — эрекции.
Далее происходит эмиссия — прохождение спермы в мочеиспускательный канал. Подчревные симпатические нервы выделяют адреналин, который вызывает сокращение гладких мышц, окружающих выносящие канальцы и хвост придатка яичка. В момент эякуляции нервы нижнего поясничного и верхнего крестцового центров вызывает сокращение бульбокавернозных мышц, что приводит к резкому выбросу спермы из уретры. Одновременно с этим, импульсы восходящих нервов создают ощущение оргазма.
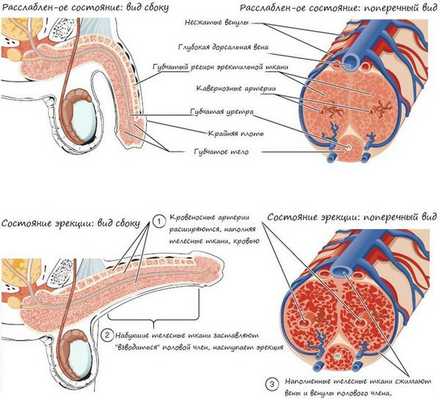
Наконец, детумесценция (прекращение или спад эрекции после эякуляции и оргазма) связана с выделением норадреналина симпатическими нервами, также вырабатывается пролактин. Это приводит к сужению сосудов органа и его последующей вялости. [3]
Патогенез азооспермии разнообразен и зависит от конкретных причин.
При обструктивной азооспермии сперматозоиды вырабатываются в нормальном количестве, но при этом нарушается проходимость протоков. В связи с этим сперматозоиды не могут выйти наружу и оплодотворить яйцеклетку. При непроходимости протока придатка яичка наблюдается нормальный размер яичек и уровень фолликулостимулирующего гормона (ФСГ), а также уплотнение и отёк придатка. [4]
При наследственных аномалиях обращает на себя внимание целостность Y-хромосомы. Этот фактор является необходимым условием нормального строения и функционирования мужской половой системы. Особую роль в сперматогенезе играют три участка длинного плеча этой Y-хромосомы: AZFa, AZFb, AZFc. [5] Иначе они называются “факторами азооспермии”. Потеря одного из них приводит к тяжёлым нарушениям плодовитости (фертильности). Подобное нарушение может возникнуть по причине мутаций зародышевых клеток отцовской линии. При азооспермии эта патология встречается в 5-10% случаев, при олигоспермии — с частотой до 5%. [6] Клинически проявляется в резком нарушении сперматогенеза. При этом эндокринная функция яичек остаётся в норме, а их клеточное строение варьируется от наличия в канальцах зародышевых клеток с нарушением сперматогенеза (очаговый Сертоли), до блокады или ослабления процесса формирования и созревания сперматозоидов. Уровень ФСГ остаётся в норме или немного повышен.
Интересен механизм нарушений при муковисцидозе (кистозном фиброзе). Эта генетическая патология является наиболее распространённым и неизлечимым на данный момент заболеванием белой расы, поражающее одного из 2500 младенцев. Люди с данной болезнью чаще всего умирали, не достигая зрелого возраста, поэтому их фертильность не принималась во внимание. Однако совершенствование диагностики и методов лечения повлияло на увеличение количества больных, способных дожить до 30 лет и более, в связи с чем муковисцидоз приобрёл важное клиническое значение.
Причина муковисцидоза — мутирующий ген CFTR (трансмембранный регулятор муковисцидоза). Нарушение структуры данного белка способствует образованию вязкости секрета бронхов и закупорке (обструкции) дыхательных путей, развитию правожелудочковой недостаточности, нарушению работы поджелудочной железы, непроходиомости кишечника у новорождённых с застоем первородного кала (мекония). Основной признак данного заболевания — повышенная содержание хлорида в поте. Для взятия анализа потоотделение стимулируют местным электрофорезом препарата «пилокарпин». [7]
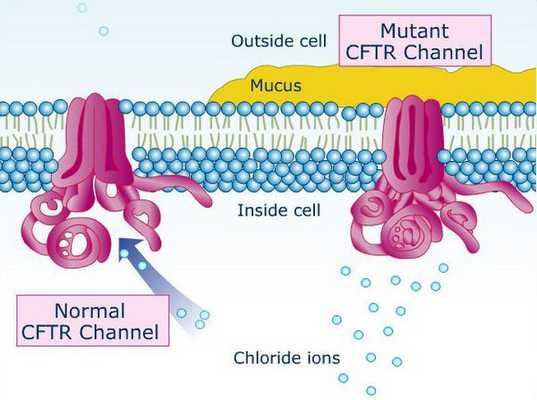
В типичных случаях при муковисцидозе внутримошоночная часть семявыводящего канала либо полностью отсутствует, либо изменена до лентовидной структуры, которая лишена просвета. Тело и хвост придатков яичка недоразвиты, его ткань, в основном, не изменена, но могут быть участки отложения солей кальция в мягких тканях (кальциноз), кистозные и гипоэхогенные (недостаточно плотные) участки (можно обнаружить при УЗИ). Врождённому отсутствию (аплазии) семявыводящего канала и придатка яичка сопутствуют патологические изменения семенных пузырьков: их отсутствие, гипоплазия (недоразвитие), обтурация (закупоривание) и кистозное изменение. В связи с этим уменьшается объём эякулята. Интересно, что фертильность сохраняется у большинства мужчин, а при нарушениях сперматогенеза можно достаточно быстро восстановить фертильность. [8]
Заслуживает внимания в патогенезе азооспермии синдром Прадера-Лабхарта-Вилли. В основе этого синдрома лежит потеря целого кластера на участке 15q11-q13 проксимальной области длинного плеча хромосомы 15. Дети с этим синдромом развиваются медленно. Если в младенчестве они выглядят худыми, то к моменту начала ходьбы они становятся очень толстыми. В зрелом возрасте развивается значительное ожирение при маленьком росте (менее 155 см). Руки и ноги у таких детей маленькие, даже по отношению к небольшому росту, имеется гипопигментация, нарушение умственного развития. У пациентов с синдромом Прадера-Вилли гениталии не развиты, характерен микропенис, двухстороннее неопущение яичек и недоразвитие мошонки. Уровень основных половых гормонов (тестостерона, ФСГ, ЛГ) резко снижен. [9]
Классификация и стадии развития азооспермии
Азооспермия бывает обструктивной, необструктивной (секреторной) и транзиторной (временной).
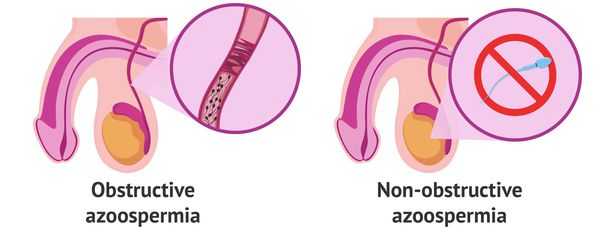
Обструктивная форма азооспермии связан с закупоркой (обструкцией) семявыводящих путей вследствие разных причин.
Необструктивная форма возникает по причине нарушения выработки (секреции) сперматозоидов.
При транзиторной форме заболевания сперматозоиды в эякуляте отсутствуют определённый промежуток времени, однако между подобными эпизодами возможно оплодотворение женщины естественным путём. Транзиторная азооспермия может возникнуть как в связи с обструктивными, так и секреторными причинами. Также временная азооспермия подразумевает, что при исключении токсических или вредных факторов воздействия фертильность мужчины восстанавливается естественным образом. [10]
Осложнения азооспермии
- нарушение репродуктивной функции (бесплодие);
- снижение половой активности;
- семейные проблемы (вплоть до расторжения брака), как следствие вышеизложенных причин;
- психические и неврологические нарушения (бессонница, неустойчивое настроение, неврозы, депрессия, суицидальные попытки).
Диагностика азооспермии
- Развёрнутая спермограмма. В соответствии с рекомендациями Всемирной организации здравоохранения, данный метод диагностики считается достоверным при отсутствии сперматозоидов как минимум в двух пробах, между которыми должно пройти 2-3 недели. Для установления временной азооспермии требуется ещё одна повторная спермограмма с интервалом в 2-3 месяца (столько необходимо времени для образования, созревания и перемещения половых клеток).
- Генетическое исследование крови. Предполагается установление кариотипа, гена белка СFTR, а также анализ на микроделеции (отсутствие) участка AZF Y-хромосомы.
- УЗИ мошонки с описанием размеров, структуры яичек и их придатков.
- ТРУЗИ предстательной железы и семенных пузырьков.
- МСКТ, МРТ тестикул и простаты.
- Исследование в эякуляте маркtрных веществ (цинка, фруктозы, альфа-глюкозидазы).
- Исследование гормонального статуса: тестостерон свободный и связанный, ФСГ, ЛГ, пролактин, ингибин В, ГСПГ — глобулин, связывающий половые гормоны.
- МРТ гипофиза.
- Двухсторонняя биопсия яичка (для оценки сперматогенеза). Более точной результат устанавливается путём проведения открытой диагностической биопсии яичка (TESE). Данный метод диагностике необходимо проводить совместно с забором сперматозоидов через прокол с последующей их криоконсервацией. Это позволит использовать сперматозоиды в дальнейшем при ЭКО и ИКСИ (искусственном оплодотворении).

Если у пациентов с азооспермией или тяжелой олигозооспермией нормальный размер яичек и уровень гормонов, то это может свидетельствовать о наличии обструкции семенного канала. [12]
Лечение азооспермии
Лечение направлено на устранение фактора, приведшего к нарушению репродуктивности (плодовитости) мужчины.
Лечение обструктивной азооспермии
Один из ведущих методов лечения — реконструктивная операция. С её помощью можно восстановить проходимость семявыносящих путей. Для этого применяется пластика уретры, наложение вазо-вазоанастомоза (соустья) или вазо-эпидидимоанастомоза.
Если обструкция семенных путей возникла на уровне придатка яичка, то в таком случае рекомендуется проведение микрохирургической эпидидимовазостомии по типу «конец в конец» или «конец в бок»: соединение семявыносящего протока с протоком придатка яичка происходит ближе (проксимальнее) к уровню обструкции. При этом предпочтительна такая техника операции, как микрохирургическая инвагинация (впячивание) эпидидимовазостомы. [13]
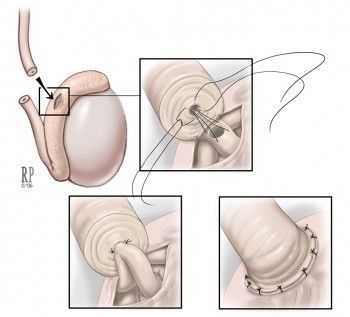
Реконструкция бывает односторонней и двусторонней, причём восстановление проходимости и частота беременностей обычно выше при двусторонней операции. Переход к микрохирургическому этапу вмешательства следует осуществлять в случае подтверждения проходимости семенных канальцев ниже придатка яичка. Анатомическое восстановление проходимости (реканализация) после реконструкции может продлиться от 3 до 18 месяцев.
До микрохирургического вмешательства (а также в случаях невозможности реканализации) необходимо провести извлечение сперматозоидов из придатка яичка (аспирацию) с последующей их криоконсервацией, которая может потребоваться для ИКСИ при неэффективности хирургической реканализации. [14]
Таким образом, реконструкция происходит поэтапно: ревизия мошонки и извлечение сперматозоидов из придатка яичка с последующей криоконсервацией семени, и затем проводится микрохирургическое восстановление семенных путей. [15] Восстановление фертильности после такого метода лечения происходит более чем в 50% случаев.
Лечение секреторной азооспермии
При данной форме азооспермии используется заместительная или стимулирующая гормональная терапия, корректирующая эндокринные расстройства. Этот метод лечения способен привести к восстановлению сперматозоидов в эякуляте. Также гормональная лекарственная терапия может быть очень эффективным способом восстановления фертильности при нарушениях гипоталамо-гипофизарной системы (гипогонадотропном гипогонадизм). В случаях хронических инфекционных процессов проводится антибактериальное и противовоспалительное лечение с учётом возбудителя.
Лечение транзиторной азооспермии
При лечении этой формы заболевания уделяют внимание устранению вредного фактора, а также проводят оперативное или гормональное лечение в зависимости от предпочтительной причины, которая может быть как секреторной, так и обструктивной. Данный случай отличается тем, что тяжёлые нарушения сперматогенеза ещё не наступили, поэтому процесс нарушения фертильности вполне поддаётся быстрому регрессу.
Если же при проведённом хирургическом и консервативном лечении фертильность восстановить не удалось, то следует обратиться к вспомогательным репродуктивным технологиям. ИКСИ является самым эффективным методом искусственного оплодотворения. Для данной процедуры необходимо получить сперматозоиды путём открытой/аспирационной биопсии яичка (TESA/TESE) или придатка яичка (MESA, PESA). [16]
Прогноз. Профилактика
При неустранимых причинах азооспермии (в основном, при генетических нарушениях) успешное лечение мужского бесплодия является трудно выполнимой задачей. В таком случае для оплодотворения супругам стоит воспользоваться донорской спермой. При обструктивной азооспермии шанс зачать ребёнка естественным путём или с использованием метода репродуктивной технологии выше, чем при секреторной форме заболевания. В подавляющем большинстве случаев причинами возникновения азооспермии являются необратимые нарушения работы яичек, приводящие к глубокому нарушению сперматогенеза. [17]
Генетические причины бесплодия (мужского и женского)
Обслуживание на двух языках: русский, английский.
Оставьте свой номер телефона, и мы обязательно перезвоним вам.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначить только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Специалисты Клинического госпиталя на Яузе проводят полный спектр исследований для выявления причин бесплодия у мужчин и женщин и разрабатывают индивидуальные программы лечения для успешного зачатия.
- До 15% пар страдают бесплодием, причем в 50% оно обусловлено мужским фактором
- В 10 — 15%случаев причинами мужского бесплодия являются генетические нарушения (хромосомные перестройки и генные мутации)
- Примерно в 5% случаев причиной женского бесплодия являются хромосомные аберрации (численные и структурные)
Бесплодным считается брак, в котором женщина не может забеременеть на протяжении 12 месяцев при регулярной половой жизни без контрацепции. Бесплодие может быть обусловлено генетическими особенностями одного или обоих супругов.
Точное выявление причин бесплодия позволяет выбрать правильную тактику лечения и значительно ускорить достижение желанного результата — наступления беременности и рождения ребенка.
Не теряйте время на неэффективное лечение! Пройдите точную диагностику.
Анализы, проводимые для выявления генетических причин мужского бесплодия
- кариотипирование;
- экспертная спермограмма;
- анализ мутаций в гене муковисцидоза (CFTR);
- определение делеций локуса AZF хромосомы Y (регионов а, b, c);
- определение индекса фрагментации хроматина (HALO- или TUNEL-тесты);
- FISH-исследование сперматозоидов — выявление численных хромосомных аномалий (анеуплоидий);
- электронно-микроскопическое исследование сперматозоидов (ЭМИС);
- определение числа (CAG)-повторов в гене андрогенового рецептора.
Выявив причины бесплодия и объективно оценив выраженность нарушений, репродуктолог сможет рекомендовать оптимальный для каждой пары метод преодоления бесплодия — заместительная гормональная терапия, искусственная инсеминация, ЭКО с ИКСИ, МЕЗА, ТЕЗА, ПЕЗА, ЭКО с донорской спермой и др. Современные репродуктивные технологии позволяют достичь успеха практически при любой сложности проблемы.
Цены на выявлениие причин бесплодия
- Исследования
- Молекулярно-генетический анализ при неразвивающейся беременности (NGS) 25 000 руб.
- Преимплантационная генетическая диагностика в крио цикле методом NGS (без учета биопсии биологического материала) одного образца, при наличии ДНК в присланном материале 25 000 руб.
- Исследование анеуплоидий в эмбрионах человека 3-го и/или 5-6 дней развития: скрининг 24 хромосом методом сравнительной геномной гибридизации (array-CGH) в криоцикле (от 1 до 7, цена за каждый образец) 28 000 руб.
- Исследование хромосом методом дифференциальной окраски 5 500 руб.
- Обследования
- Эхогистеросальпингоскопия в репродуктологии 8 900 руб.
Внимание! Цены на сайте могут отличаться.
Пожалуйста, уточняйте актуальную стоимость у администраторов по телефону.
Наши специалисты:
Показания к обследованию
Пройдите обследование для исключения генетических причин бесплодия при:
- выраженной олигозооспермии или азооспермии (обструктивной, необструктивной);
- тератозооспермии;
- астенозооспермии:
- азооспермия — отсутствие сперматозоидов в эякуляте (обструктивная — связана с непроходимостью семявыносящих путей, необструктивная — при нарушении образования сперсматозоидов в яичках),
- олигозооспермия — сниженное количество сперматозоидов в эякуляте. О существенном угнетении сперматогенеза говорят при концентрации сперматозоидов менее 5 млн/мл эякулята,
- тератозооспермия — нарушение морфологии сперматозоидов,
- астенозооспермия — нарушение подвижности сперматозоидов.
Генетические факторы бесплодия у мужчин
Генетические причины выраженной олигозооспермии и необструктивной азооспермии:
- хромосомные нарушения— носительство сбалансированной реципрокной или Робертсоновской транслокаций, инверсий и др. структурных изменений кариотипа в большинстве случаев сопровождаются нарушениями сперматогенеза. Аномалии кариотипа встречаются у мужчин с азооспермией и с олигозооспермией.
- аномалии числа половых хромосом — синдром Клайнфельтера (47,ХХУ); некоторые случаи дисомии хромосомы Y (47,XYY). Синдром Клайнфельтера является крайне распространённой патологией: на каждые 500 — 700 новорождённых мальчиков приходится 1 ребёнок с данной патологией. Синдром Клайнфельтера является одной из самых частых причин мужского гипогонадизма (гипергонадотропного гипогонадизма) и бесплодия.
- структурные аномалии половых хромосом.
- делеции локусаAZFхромосомыY. «Фактор азооспермии» — локус АZF включает гены, отвечающие за сперматогенез. Он делится на 3 региона: AZFa, AZFb. AZFc, делеции которых сопровождаются нарушениями сперматогенеза различной степени тяжести. Так, делеции в AZFa обычно сопровождаются синдромом «только клетки Сертоли». В случае делеции локусов AZFb, AZFс возможно обнаружение в тканях яичек сперматозоидов пригодных для процедуры ИКСИ. Делеции в локусе AZF в большинстве случаев возникают denovo в результате мутаций в клетках сперматогенного ряда или на ранних стадиях развития эмбриона. Делеции локуса AZF встречаются у 15% мужчин с выраженной идиопатической олигозооспермией и 20% мужчины с идиопатической необструктивной азооспермией.
- мутации в гене AR — андрогеннового рецептора. Влияние числа (CAG)-повторов на сперматогенез до конца не доказано, однако повреждения гена в области гормонсвязывающего участка (делеции и точковые мутации) достоверно приводят к развитию олигоастенотератозооспермии. Примерно случаев азооспермии или выраженной олигозооспермии связаны с точковыми мутациями в гене рецептора андрогенов.
- мутации в генах, приводящие к развитию гипогонадотропного гипогонадизма (синдром Каллмана и др. состояния).
- мутации в гене муковисцидоза CFTR. Муковисцидоз относится к числу наиболее распространенных моногенных заболеваний в европейской популяции и в среднем встречается с частотой 1 больной ребенок на каждые 2500 новорожденных. Примерно 1 из 25 человек является гетерозиготным носителем мутации в гене CFTR. Мутации в гене CFTR приводят к нарушениям сперматогенеза различной степени тяжести, часто без манифестации других признаков муковисцидоза.
- мутации в гене половой дифференцировки SRY.
Генетические причины обструктивной азооспермии
Мутации в гене муковисцидоза CFTR приводят к врожденному отсутствию семявыносящих протоков (CBAVD, CUAVD) и непроходимости семявыносящих протоков.
Тератозооспермия и астенозооспермия могут быть обусловлены мутациями в отдельных генах или указывать на наличие хромосомных аномалий в кариотипе мужчины, а в сочетании с высокой степенью фрагментации хроматина в сперматозоидах свидетельствуют о нарушении оптимальных условий сперматогенеза и повышенной вероятности наличия численных хромосомных аномалий в сперматозоидах.
Мутации в генах, отвечающих за развитие гонад и их функционирование, в том числе генах, кодирующих гормоны ЛГ, ФСГ и их рецепторы, могут быть причиной бесплодия у мужчин. Однако данные нарушения встречаются настолько редко, что проводить генетические исследования для выявления возможной причины в рамках лечения в клиниках ВРТ не представляется целесообразным. Бесплодие может развиваться как следствие наличия у пациента генерализованного наследственного генетического заболевания (синдром Прадера-Вилли, синдром Нунан, гемохроматоз, анемия Фанкони, бета-талассемия и др.).
К бесплодию у мужчин могут приводить и различные экзогенные факторы облучение, перегрев яичек, курение и чрезмерное потребление алкоголя, перенесенные инфекционные заболевания, производственные яды, лекарства, болезни матери при беременности: сахарный диабет, фенилкетонурия и гипотиреоз, перенесенные инфекционные заболевания.
Анализы, проводимые для выявления генетических причин женского бесплодия
- Кариотпирование
- Преимплантационный генетический скрининг анеуплоидий
- Исследование уровня рецептивности эндометрия
- Исследование мутаций в генах системы гемостаза
- Исследование неравновесной инактивации хромосомы Х
- бесплодии неясного генеза
- неудачных попытках искусственного оплодотворения, в том числе ЭКО
- нарушении имплантации эмбрионов
- невынашивании беременности
- спонтанных абортах и случаях неразвивающейся беременности в анамнезе
Генетические факторы бесплодия у женщин
Хромосомные нарушения:
- нарушения механизмов расхождения хромосом в процессе оогенеза приводят к образованию яйцеклеток с численными хромосомными нарушениями. После 35 лет доля яйцеклеток с хромосомной патологией возрастает и может достигать 80% после 40 лет. Оплодотворение яйцеклетки с хромосомной патологией приводит к формированию анеуплоидного эмбриона. В большинстве случаев (за исключением трисомии хромосом 13, 18, 21 и численных аномалий половых хромосом) такие эмбрионы рано или поздно останавливаются в развитии, что приводит к самопроизвольному аборту или неразвивающейся беременности. Наличие хромосомной патологии у эмбриона также может быть причиной нарушения имплантации в стенку матки.
- хромосомные аберрации— носительство сбалансированной реципрокной или Робертсоновской транслокаций, инверсий и др. структурных изменений кариотипа в большинстве случаев приводят к образованию анеуплоидных яйцеклеток.
- аномалии числа половых хромосом: синдром Шерешевского-Тернера (45,Х); синдром трисомии хромосомы Х (47,ХХХ), синдром Свайера (46,XY).
- структурные аномалии половых хромосом могут быть причиной первичной недостаточности функции яичников.
Молекулярно-генетические нарушения:
- Мутации в генах, отвечающих за гомеостаз — повышенное содержание гомоцистеина, повышенная свертываемость крови и склонность к тромбообразованию — могут быть причиной бесплодия и невынашивания беременности.
- Нарушение рецептивности эндометрия и смещение времени имплантационного окна
- Синдром Мартина-Белл (синдром ломкой fragile X mental retardation syndrome,FRAXA) является наиболее частой причиной умственной отсталости у мальчиков. Развитие синдрома связано с экспансией тринуклеотидных повторов (CGG) в промоторной области гена FMR1 хромосомы Х. У здоровых индивидов число этих повторов колеблется от 6 до 54, а увеличение этого числа свыше 200 повторов приводит к феномену ломкой и клиническому проявлению заболевания. При количестве повторов от 55 до 200 (предмутационное состояние) заболевание в типичной форме не проявляется, но существует высокая вероятность проявления заболевания у потомков. У женщин-носителей предмутационного состояния в случаев развивается синдром раннего истощения яичников.
- Мутации в генах, обуславливающие развитие вторичной недостаточности функции яичников — гипогонадотропного гипогонадизма (нарушения в работе гипоталамо-гипофизарной регулирующей системы). Например, синдром Каллмана и др. состояния.
Также как и в случае мужчин, мутации в генах, отвечающих за функционирование репродуктивной системы, в том числе генах половых гормонов и их рецепторов, могут приводить к бесплодию. Бесплодие может быть следствием наличия генерализованного наследственного генетического заболевания (синдром Прадера-Вилли, адреногенитальный синдром, галактоземия, муковисцидоз, гемохроматоз, бета-талассемия и др.).
Воздействие неблагоприятных факторов окружающей среды, стрессы, перенесенные инфекции, в том числе во время внутриутробного развития, также могут приводить к развитию бесплодия.
Для установления причин бесплодия специалисты Клинического госпиталя на Яузе рекомендуют пройти консультации уролога, акушера-гинеколога, эндокринолога, клинического генетика. Консультация генетика рекомендуется всем парам, обращающимся к помощи ВРТ, и является обязательной при обнаружении той или иной формы генетической патологии у одного из партнеров.
Наши преимущества
- Специалисты.Опытные специалисты высокой квалификации, с учёными степенями помогают докторам решать сложнейшие репродуктивные проблемы пациентов.
- Индивидуальный подход, комплексные решения. Индивидуальные эффективные комплексные программы для решения проблем деторождения семейной пары с использованием всех ресурсов нашего ЦМРТ и многопрофильного госпиталя.
- Генетическая лаборатория. Современная лаборатория молекулярной генетики создана по лучшим мировым стандартам качества — от специального покрытия стен и системы вентиляции, предупреждающей контаминацию (смешение биопрепаратов на молекулярном уровне), до новейшего оборудования и технологий инновационных генетических исследований.
- Международные связи. Генетическая лаборатория нашего госпиталя активно сотрудничает с лабораторией Лондонского университета, генетическими лабораториями BGI Europe и Ingenomix (Испания), международной сетью клиник IVIIVF.
Статья проверена молекулярным биологом, лабораторным генетиком, к.б.н. Кибановым М.В., носит общий информационный характер, не заменяет консультацию специалиста.
Для рекомендаций по диагностике и лечению необходима консультация врача.Мужское бесплодие
Одновременно, снижение или утрата фертильности — способности к зачатию, не имеет характерных признаков (симптомов) в отличие от других нарушений здоровья. По этой причине при отсутствии желанной беременности мужчины не спешат обратиться к специалисту по вопросам бесплодного брака, предполагая наличие проблем у супруги.
Однако на сегодняшний день известно, что не менее 40% всех случаев бесплодия в супружеских парах обусловлены мужским фактором. При этом супруги сталкиваются с проблемой бесплодия при отсутствии проблем с эректильной функцией у мужчины. А наличие детей в предыдущем браке не исключает проблем со способностью к зачатию в будущем.
Что же такое мужской фактор бесплодия? Мужской фактор бесплодия — это снижение количества или отсутствие сперматозоидов в сперме, нарушение их подвижности, строения, оплодотворяющей способности. Важно отметить, что нарушение оплодотворяющей способности сперматозоидов, приводящее к бесплодию, может быть и при нормальных показателях их количества и подвижности. Так, патология акросомы (структурная часть головки сперматозоида), содержащей ферменты, обеспечивающие проникновение сперматозоида в яйцеклетку, приводит к ненаступлению оплодотворения.
Перенесенные инфекции, как причина мужского бесплодия
Одним из факторов, приводящих к снижению фертильности мужчины, является процесс с повреждением семявыносящих путей, органов, участвующих в выработке эякулята: яичек, предстательной железы, семенных пузырьков. Огромный ущерб здоровью наносят инфекции передаваемые половым путем.
Микроорганизмы и продукты их жизнедеятельности повреждают семявыносящие пути непосредственно или в результате вторичного воспаления — физиологического ответа организма на возбудители и токсины, оказывают прямое токсическое действие на сперматозоиды. При отсутствии адекватного лечения процесс хронизируется, вырабатываемые организмом антитела, прикрепляясь к поверхности сперматозоидов, препятствуют прогрессивному их движению к яйцеклетке; повреждают их структуру, препятствуя нормальному взаимодействию с яйцеклеткой. Воспаление придатка яичка и самого яичка влекут за собой повреждение клеток, в которых созревают сперматозоиды, продукцию антиспермальных антител (реакция иммунной системы против собственных клеток — сперматозоидов).
Снижение фертильности в результате воспалительных заболеваний предстательной железы и семенных пузырьков связано также с нарушением образования веществ, участвующих в поддержании жизнедеятельности сперматозоидов в женских половых путях, обеспечении их подвижности и прохождения через естественные барьеры.
Однако не всегда наличие хронического воспалительного заболевания означает снижение фертильности. Для установления этого факта требуется проведение исследований эякулята (спермы), позволяющих выявить снижение количества, нарушение подвижности или строения сперматозоидов.
Одновременно, наличие хронического воспалительного заболевания не всегда является причиной бесплодия и требуется проведение диагностического поиска в отношении других его факторов. Поэтому своевременное обращение к специалисту по бесплодию позволит избежать ухудшения качества половых клеток в ситуациях отсутствия результата от повторно проводимой антимикробной и противовоспалительной терапии.
Генетические причины мужского бесплодия
Нарушения в генетическом материале могут проявляться : от тяжелых заболеваний до бессимптомного носительства. Существуют виды нарушений, влияющих на мужскую фертильность, которые могут послужить фактором патологии беременности в паре супругов или наследственного заболевания у малыша.
Одной из причин мужского бесплодия могут являться микроделеции (AZF). Суть таких нарушений составляет утрата маленьких фрагментов , отвечающих за образование сперматозоидов. Наличие микроделеции у мужчин сочетается с очень низкой концентрацией сперматозоидов (менее 5 млн/мл).
Часто мужчинам с проблемами репродукции назначают исследование кариотипа. Этот анализ выявляет нарушения числа или структуры хромосом. Среди таких нарушений синдром Клайнфельтера, который встречается, главным образом, среди мужчин с отсутствием сперматозоидов. При этом синдроме в кариотипе нарушено число половых хромосом (XXY вместо XY). При кариотипировании могут быть выявлены хромосомные перестройки. У мужчины, являющимся носителем таких перестроек, может не быть существенных нарушений показателей спермы. Однако такое носительство, создавая риск для правильного хромосомного набора эмбриона, может являться причиной прерывания беременности у супруги.
Также необходимо отметить мутации гена муковисцидоза как причину мужского бесплодия. Такое носительство может быть бессимптомным или проявляться в виде нарушения транспорта сперматозоидов из яичек (отсутствие семявыносящих канальцев). В том и в другом случае выявление носительства таких мутаций может предотвратить рождение ребенка с тяжелым наследственным заболеванием — муковисцидозом.
При мужском факторе нарушений репродукции в супружеской паре очень важна консультация врача генетика, который сможет определить необходимый объем обследования, определить тактику преодоления бесплодия с учетом выявленной генетической патологии.
Эндокринные нарушения, приводящие к снижению фертильности у мужчин
Расстройства репродуктивной функции у мужчин могут быть обусловлены эндокринными нарушениями, при которых нарушены продукция гормонов или восприимчивость органов к ним. Органами, обеспечивающими гормональную регуляцию сперматогенеза, являются гипоталамус, гипофиз и яички.
Врожденная или приобретенная в результате травм или заболеваний недостаточность функции гипоталамуса или гипофиза проявляется дефицитом фолликулостимулирующего и лютеинизирующего гормонов и негативно сказывается на процессе образования сперматозоидов. Повышение их секреции связано с нарушением функции яичек. И то и другое приводит к ухудшению показателей спермограммы — олигозооспермии, азооспермии.
Тестостерон — это гормон, который участвует в регуляции сперматогенеза и вырабатывается яичками. Снижение выработки тестостерона яичками может быть связано со следующими состояниями и заболеваниями: варикоцеле, неопущение яичек из брюшной полости в мошонку (крипторхизм), воспалительное заболевание яичек (орхит) вследствие перенесённого эпидемического паротита (свинки) или туберкулеза, хламидийной инфекции, травмы, оперативные вмешательства на органах мошонки, хирургическое лечение паховой грыжи, генетически обусловленные и другие заболевания.
Метаболический синдром, ключевым моментом которого является ожирение, вносит большой негативный вклад в снижение фертильности мужчины. Диагноз «ожирение» выставляют при наличии у мужчины окружности талии более 94 см. Сегодня хорошо известно, что жировая ткань является активным, самостоятельным и самым большим эндокринным органом, который секретирует целый ряд адипокинов — биологически активных белков, оказывающих свое действие как локально, так и системно. Наибольший негативный эффект жировой ткани у мужчин связывают с ее гормоном лептином. Лептин снижает чувствительность андрогенных рецепторов к тестостерону и снижает его уровень за счет усиления перехода тестостерона в эстрадиол в периферических тканях и блокирования синтеза лютеинизирующего гормона в гипофизе.
Наличие сахарного диабета у мужчин так же может приводить и к снижению фертильности. Риск развития мужского бесплодия при диабете зависит от длительности заболевания, выраженности обменных нарушений, адекватности контроля содержания уровня глюкозы и липидов.
К снижению уровня тестостерона приводят и нарушения функции щитовидной железы (гипотиреоз и тиреотоксикоз).
Другие причины
Бесплодие вследствие отсутствия эякулята (аспермии) при сохраненном оргазме может возникать после оперативных вмешательств на спинном мозге, толстом кишечнике, забрюшинном пространстве; при наличии диабетической нейропатии, обструкции семявыносящих путей, врожденных состояниях и нарушениях, после приема антипсихотических, антигипертензивных препаратов, антидепрессантов.
В многочисленных исследованиях доказано отрицательное влияние на сперматогенез повышения температуры мошонки. Учитывая тот факт, что созревание сперматозоидов происходит при температуре порядка 35.0°C, то минимальные колебания вплоть до 0.5°С приводят к ослаблению сперматогенеза. Даже кратковременное воздействие высоких температур, будь то баня, сауна, подогрев сидений в машине, горячий душ приводит к значительному, но временному снижению концентрации сперматозоидов до 6-8 недель. При заболеваниях, сопровождающихся подъемом температуры тела, снижение количества сперматозоидов, а иногда и полное их исчезновение, может наблюдаться до 2,5-3 месяцев. Работа в жарких условиях и воздействие теплового излучения также снижает оплодотворяющую способность сперматозоидов. Малоподвижный образ жизни (работа в сидячем положении) также ассоциируется с повышением температуры мошонки.
Ткань яичка чувствительна к воздействию ионизирующего излучения, приему цитостатиков, наркотических и многих других лекарственных препаратов, воздействию электромагнитного излучения, тяжелых металлов, что также может привести к снижению или утрате фертильности.
Мужской фактор и невынашивание беременности
Многие полагают, что даже если мужской фактор может быть причиной бесплодия в паре, то никак не невынашивания беременности. Может ли мужской фактор повлиять на потерю беременности? На сегодняшний день можно с определенной уверенностью утверждать, что да, это возможно. Во первых, причиной невынашивания беременности могут являться хромосомные нарушения у плода. Не следует забывать, что половину хромосом (генетического материала) зародыш получает от отца. Тем самым и хромосомные нарушения могут иметь отцовское происхождение. Носительство хромосомных нарушений как мужчиной так и женщиной могут явиться причиной хромосомных нарушений у зародыша и если эти нарушения несовместимы с его нормальным развитием, то беременность может замереть, спонтанно прерваться.
Совсем недавно была выявлена еще одна причина нарушений развития эмбриона — это фрагментация ДНК сперматозоида. ДНК сперматозоида достаточно хорошо защищена, однако известно, что под влиянием целого ряда факторов, включающих психологические факторы, стресс, в ДНК сперматозоида при его созревании могут возникать разрывы. Такие повреждения не приводят к нарушению функции сперматозоида и процесс оплодотворения сохраняется. Однако данные повреждения мужского генома (ДНК) могут сказаться негативно при развитии эмбриона и привести к потере беременности.
Как преодолеть мужской фактор бесплодия
В наши дни в большинстве случаев мужской фактор бесплодия это не приговор. С тех пор как в репродукционной медицине появилась поистине революционная технология ИКСИ (инъекция сперматозоида в яйцеклетку) стало возможным лечение бесплодия даже в случаях тяжелого мужского бесплодия. Если в эякуляте присутствуют хотя бы единичные сперматозоиды, их можно использовать для ИКСИ, получать эмбрионы и беременность. В случае азооспермии (отсутствия сперматозоидов) проводится диагностическая биопсия яичек, так как сперматозоиды могут отсутствовать в сперме, но могут присутствовать в яичках, и также могут быть использованы для преодоления бесплодия. ИКСИ рекомендуется и при иммунологическом бесплодии. Необходимо помнить, что ИКСИ не является абсолютной панацеей. В некоторых случаях требуется хирургическое вмешательство, консервативное лечение. Важно отметить, что коррекция гормональных нарушений, гормональная стимуляция сперматогенеза, метаболическая терапия проводится только после определения гормонального статуса мужчины, специалистом, имеющим подготовку по эндокринным аспектам «мужского здоровья».
Криоконсервация сперматозоидов
Криоконсервация (замораживание сперматозоидов) к настоящему времени является достаточно рутинной процедурой, активно используемой в процессе вспомогательных репродуктивных технологий. Целью криоконсервации является длительное хранение мужских половых клеток. Они могут храниться годами и даже десятилетиями.
Образование сперматозоидов в организме мужчины (сперматогенез) — это процесс чрезвычайно чувствительный к факторам внешней среды. Сперматогенез может навсегда прекратиться после воздействия ионизирующих излучений. Известны случаи утраты фертильности спермы у мужчин, прошедших облучение во время службы в армии, имевших воздействие вредных факторов на предприятии. Это может произойти после лечения онкологических заболеваний. Кроме того, нарушение качества спермы может происходить просто с возрастом.
Хотя у нас в стране немногие прибегают к услуге криоконсервации спермы, в некоторых странах это достаточно распространено. Для мужчин из групп риска за рубежом проводятся разъяснения риска того, что они могут полностью лишиться сперматозоидов и никогда не смогут зачать своего ребенка. В этом случае мужчина может решить криоконсервировать и хранить свои сперматозоиды, либо сознательно отказаться от этой процедуры. К сожалению, в нашей стране молодых мужчин практически никогда не предупреждают о такой возможной перспективе, и они непосредственно оказываются перед фактом бесплодия. Однако и у нас любой мужчина, желающий сохранить свои половые клетки, может воспользоваться услугами криобанка.
Читайте также:
- Несеминомная герминативноклеточная опухоль средостения на рентгенограмме, КТ
- Компоненты барьеров легких при хроническом бронхите.
- Инородные тела кишечника. Безоары, желчные камни, аскаридозы кишечника
- Эффекты секретина и его влияние на органы пищеварения
- Дифференциация туберкулеза и рака легкого. Ателектаз туберкулезного легкого
