Гиперкапния - причины, симптомы, диагностика и лечение
Добавил пользователь Дмитрий К. Обновлено: 22.01.2026
Острая дыхательная недостаточность (ОДН) - патологический синдром, характеризующийся резким снижением уровня оксигенации крови. Относится к жизнеугрожающим, критическим состояниям, способным привести к летальному исходу. Ранними признаками острой дыхательной недостаточности являются: тахипноэ, удушье, чувство нехватки воздуха, возбуждение, цианоз. По мере прогрессирования гипоксии развивается нарушение сознания, судороги, гипоксическая кома. Факт наличия и степень тяжести дыхательных расстройств определяется по газовому составу крови. Первая помощь заключается в ликвидации причины ОДН, проведении оксигенотерапии, при необходимости - ИВЛ.
МКБ-10
Общие сведения
Острая дыхательная недостаточность - синдром респираторных расстройств, сопровождающийся артериальной гипоксемией и гиперкапнией. Диагностическими критериями острой дыхательной недостаточности служат показатели парциального давления кислорода в крови (рО2) 50 мм рт. ст. В отличие от хронической дыхательной недостаточности, при ОДН компенсаторные механизмы дыхания даже при максимальном напряжении не могут поддерживать оптимальный для жизнедеятельности газовый состав крови и быстро истощаются, что сопровождается выраженными метаболическими нарушениями жизненно важных органов и расстройствами гемодинамики. Смерть от острой дыхательной недостаточности может наступить в течение нескольких минут или часов, поэтому данное состояние относится к числу ургентных.

Причины ОДН
Этиологические факторы острой дыхательной недостаточности весьма разнообразны, поэтому столкнуться с данным состоянием в своей практической деятельности могут врачи, работающие в отделениях реаниматологии, пульмонологии, травматологии, кардиологии, токсикологии, инфекционных болезней и т. д. В зависимости от ведущих патогенетических механизмов и непосредственных причин выделяют первичную острую дыхательную недостаточность центрогенного, нервно-мышечного, торако-диафрагмального и бронхо-легочного происхождения.
В основе ОДН центрального генеза лежит угнетение деятельности дыхательного центра, которое, в свою очередь, может быть вызвано отравлениями (передозировкой наркотиками, транквилизаторами, барбитуратами, морфином и др. лекарственными веществами), ЧМТ, электротравмой, отеком мозга, инсультом, сдавлением соответствующей области головного мозга опухолью.
Нарушение нервно-мышечной проводимости приводит к параличу дыхательной мускулатуры и может стать причиной острой дыхательной недостаточности при ботулизме, столбняке, полиомиелите, передозировке мышечных релаксантов, миастении. Торако-диафрагмальная и париетальная ОДН связаны с ограничением подвижности грудной клетки, легких, плевры, диафрагмы. Острые дыхательные расстройства могут сопровождать пневмоторакс, гемоторакс, экссудативный плеврит, травмы грудной клетки, перелом ребер, нарушения осанки.
Наиболее обширную патогенетическую группу составляет бронхо-легочная острая дыхательная недостаточность. ОДН по обструктивному типу развивается вследствие нарушения проходимости дыхательных путей на различном уровне. Причиной обструкции могут послужить инородные тела трахеи и бронхов, ларингоспазм, астматический статус, бронхит с гиперсекрецией слизи, странгуляционная асфиксия и др. Рестриктивная ОДН возникает при патологических процессах, сопровождающихся снижением эластичности легочной ткани (крупозной пневмонии, гематомах, ателектазах легкого, утоплении, состояниях после обширных резекций легких и т. д.). Диффузная форма острой дыхательной недостаточности обусловлена значительным утолщением альвеоло-капиллярных мембран и вследствие этого затруднением диффузии кислорода. Такой механизм дыхательной недостаточности более характерен для хронических заболеваний легких (пневмокониозов, пневмосклероза, диффузного фиброзирующего альвеолита и т. д.), однако может развиваться и остро, например, при респираторном дистресс-синдроме или токсических поражениях.
Вторичная острая дыхательная недостаточность возникает в связи с поражениями, впрямую не затрагивающими центральные и периферические органы дыхательного аппарата. Так, острые дыхательные расстройства развиваются при массивных кровотечениях, анемии, гиповолемическом шоке, артериальной гипотонии, ТЭЛА, сердечной недостаточности и других состояниях.
Классификация
Этиологическая классификация подразделяет ОДН на первичную (обусловленную нарушением механизмов газообмена в легких - внешнего дыхания) и вторичную (обусловленную нарушением транспорта кислорода к тканям - тканевого и клеточного дыхания).
Первичная острая дыхательная недостаточность:
- центрогенная
- нервно-мышечная
- плеврогенная или торако-диафрагмальная
- бронхо-легочная (обструктивная, рестриктивная и диффузная)
Вторичная острая дыхательная недостаточность, обусловленная:
- гипоциркуляторными нарушениями
- гиповолемическими расстройствами
- кардиогенными причинами
- тромбоэмболическими осложнениями
- шунтированием (депонированием) крови при различных шоковых состояниях
Подробно эти формы острой дыхательной недостаточности будут рассмотренные в разделе «Причины».
Кроме этого, различают вентиляционную (гиперкапническую) и паренхиматозную (гипоксемическую) острую дыхательную недостаточность. Вентиляционная ДН развивается в результате снижения альвеолярной вентиляции, сопровождается значительным повышением рСО2, артериальной гипоксемией, респираторным ацидозом. Как правило, возникает на фоне центральных, нервно-мышечных и торако-диафрагмальных нарушений. Паренхиматозная ДН характеризуется артериальной гипоксемией; при этом уровень СО2 в крови может быть нормальным или несколько повышенным. Такой вид острой дыхательной недостаточности является следствием бронхо-пульмональной патологии.
В зависимости от парциального напряжения О2 и СО2 в крови выделяют три стадии острых дыхательных расстройств:
- ОДН I стадии - рО2 снижается до 70 мм рт. ст., рСО2 до 35 мм рт. ст.
- ОДН II стадии - рО2 снижается до 60 мм рт. ст., рСО2 увеличивается до 50 мм рт. ст.
- ОДН III стадии - рО2 снижается до 50 мм рт. ст. и ниже, рСО2 увеличивается до 80-90 мм рт. ст. и выше.
Симптомы ОДН
Последовательность, выраженность и скорость развития признаков острой дыхательной недостаточности может различаться в каждом клиническом случае, однако для удобства оценки степени тяжести нарушений принято различать три степени ОДН (в соответствии со стадиями гипоксемии и гиперкапнии).
ОДН I степени (компенсированная стадия) сопровождается ощущением нехватки воздуха, беспокойством пациента, иногда эйфорией. Кожные покровы бледные, слегка влажные; отмечается легкая синюшность пальцев рук, губ, кончика носа. Объективно: тахипноэ (ЧД 25-30 в мин.), тахикардия (ЧСС 100-110 в мин.), умеренное повышение АД.
При ОДН II степени (стадия неполной компенсации) развивается психомоторное возбуждение, больные жалуются на сильное удушье. Возможны спутанность сознания, галлюцинации, бред. Окраска кожных покровов цианотичная (иногда с гиперемией), наблюдается профузное потоотделение. На II стадии острой дыхательной недостаточности продолжают нарастать ЧД (до 30-40 в 1 мин.), пульс (до 120-140 в мин.); артериальная гипертензия.
Диагностика
Зачастую картина острой дыхательной недостаточности разворачивается столь стремительно, что практически не оставляет времени на проведение расширенной диагностики. В этих случаях врач (пульмонолог, реаниматолог, травматолог и т. д.) быстро оценивает клиническую ситуацию для выяснения возможных причин ОДН. При осмотре пациента важно обратить внимание на проходимость дыхательных путей, частоту и характеристику дыхания, задействованность в акте дыхания вспомогательной мускулатуры, окраску кожных покровов, ЧСС. С целью оценки степени гипоксемии и гиперкапнии в диагностический минимум включается определение газового состава и кислотно-основного состояния крови.
Если состояние пациента позволяет (при ОДН I степени) производится исследование ФВД (пикфлоуметрия, спирометрия). Для выяснения причин острой дыхательной недостаточности важное значение могут иметь данные рентгенографии грудной клетки, бронхоскопии, ЭКГ, общего и биохимического анализа крови, токсикологического исследования мочи и крови.
Неотложная помощь при ОДН
Последовательность мероприятий первой помощи определяется причиной острой дыхательной недостаточности, а также ее тяжестью. Общий алгоритм включает обеспечение и поддержание проходимости дыхательных путей, восстановление нарушений легочной вентиляции и перфузии, устранение сопутствующих гемодинамических нарушений.
На первом этапе необходимо осмотреть ротовую полость пациента, извлечь инородные тела (если таковые имеются), произвести аспирацию содержимого из дыхательных путей, устранить западение языка. С целью обеспечения проходимости дыхательных путей может потребоваться наложение трахеостомы, проведение коникотомии или трахеотомии, лечебной бронхоскопии, постурального дренажа. При пневмо- или гемотораксе производится дренирование плевральной полости; при бронхоспазме применяются глюкокортикостероиды и бронходилататоры (системно или ингаляционно). Далее следует незамедлительно обеспечить подачу увлажненного кислорода (с помощью носового катетера, маски, кислородной палатки, гипербарической оксигенации, ИВЛ).
С целью коррекции сопутствующих нарушений, вызванных острой дыхательной недостаточностью, проводится лекарственная терапия: при болевом синдроме назначаются анальгетики; с целью стимуляции дыхания и сердечно-сосудистой деятельности - дыхательные аналептики и сердечные гликозиды; для устранения гиповолемии, интоксикации - инфузионная терапия и т. д.
Прогноз
Последствия остро развившейся дыхательной недостаточности всегда серьезны. На прогноз оказывает влияние этиология патологического состояния, степень респираторных нарушений, скорость оказания первой помощи, возраст, исходный статус. При стремительно развившихся критических нарушениях наступает смерть в результате остановки дыхания или сердечной деятельности. При менее резкой гипоксемии и гиперкапнии, быстром устранении причины острой дыхательной недостаточности, как правило, наблюдается благоприятный исход. Для исключения повторных эпизодов ОДН необходимо интенсивное лечение фоновой патологии, повлекшей за собой жизнеугрожающие нарушения дыхания.
2. Острая дыхательная недостаточность: основные подходы к диагностике и терапии/ Авдеев С.Н.// Практическая пульмонология. - 2005.
3. Интенсивная терапия заболеваний, сопровождающихся отсрой дыхательной недостаточностью/ Прасмыцкий О.Т., Р.Е., Ржеутская. - 2007.
4. Клинические рекомендации по оказанию медицинской помощи пострадавшим с острой дыхательной недостаточностью в чрезвычайных ситуациях/ Саввин Ю.Н., Кудрявцев Б.П.,Шабанов В.Э., Шишкин Е.В. - 2015.
Дыхательная недостаточность ( Легочная недостаточность )
Дыхательная недостаточность — это патологический синдром, сопровождающий ряд заболеваний, в основе которого лежит нарушение газообмена в легких. Основу клинической картины составляют признаки гипоксемии и гиперкапнии (цианоз, тахикардия, нарушения сна и памяти), синдром утомления дыхательной мускулатуры и одышка. ДН диагностируется на основании клинических данных, подтвержденных показателями газового состава крови, ФВД. Лечение включает устранение причины ДН, кислородную поддержку, при необходимости - ИВЛ.
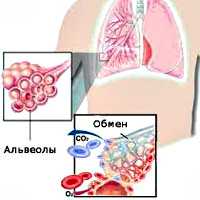
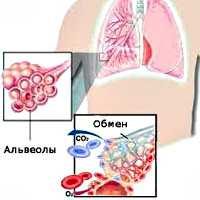
Внешнее дыхание поддерживает непрерывный газообмен в организме: поступление атмосферного кислорода и удаление углекислого газа. Любое нарушение функции внешнего дыхания приводит к нарушению газообмена между альвеолярным воздухом в легких и газовым составом крови. В результате этих нарушений в крови нарастает содержание углекислоты и уменьшается содержание кислорода, что ведет к кислородному голоданию, в первую очередь, жизненноважных органов - сердца и головного мозга.
При дыхательной недостаточности (ДН) не обеспечивается необходимый газовый состав крови, либо он поддерживается за счет перенапряжения компенсаторных возможностей системы внешнего дыхания. Угрожающее для организма состояние развивается при дыхательной недостаточности, характеризующейся снижением парциального давления кислорода в артериальной крови менее 60 мм рт. ст., а также повышением парциального давления углекислоты более 45 мм рт. ст.
Причины
Дыхательная недостаточность может развиваться при различных острых и хронических воспалительных заболеваниях, повреждениях, опухолевых поражениях органов дыхания; при патологии со стороны дыхательной мускулатуры и сердца; при состояниях, приводящих к ограничению подвижности грудной клетки. К нарушению легочной вентиляции и развитию дыхательной недостаточности могут приводить:
- Обструктивные нарушения. Дыхательная недостаточность по обструктивному типу наблюдается при затруднении прохождения воздуха по воздухоносным путям - трахее и бронхам вследствие бронхоспазма, воспаления бронхов (бронхита), попадания инородных тел, стриктуры (сужения) трахеи и бронхов, сдавления бронхов и трахеи опухолью и т. д.
- Рестриктивные нарушения. Дыхательная недостаточность по рестриктивному (ограничительному) типу характеризуется ограничением способности легочной ткани к расширению и спаданию и встречается при экссудативном плеврите, пневмотораксе, пневмосклерозе, спаечном процессе в плевральной полости, ограниченной подвижности реберного каркаса, кифосколиозе и т. д.
- Гемодинамические нарушения. Причиной развития гемодинамической дыхательной недостаточности могут служить циркуляторные расстройства (например, тромбоэмболия), ведущие к невозможности вентиляции блокируемого участка легкого. К развитию дыхательной недостаточности по гемодинамическому типу также приводит право-левое шунтирование крови через открытое овальное окно при пороке сердца. При этом происходит смешение венозной и оксигенированной артериальной крови.
Дыхательная недостаточность классифицируется по ряду признаков:
1. По патогенезу (механизму возникновения):
- паренхиматозная (гипоксемическая, дыхательная или легочная недостаточность I типа). Для дыхательной недостаточности по паренхиматозному типу характерно понижение содержания и парциального давления кислорода в артериальной крови (гипоксемия), трудно корригируемое кислородной терапией. Наиболее частыми причинами данного типа дыхательной недостаточности служат пневмонии, респираторный дистресс-синдром (шоковое легкое), кардиогенный отек легких.
- вентиляционная ("насосная", гиперкапническая или дыхательная недостаточность II типа). Ведущим проявлением дыхательной недостаточности по вентиляционному типу служит повышение содержания и парциального давления углекислоты в артериальной крови (гиперкапния). В крови также присутствует гипоксемия, однако она хорошо поддается кислородотерапии. Развитие вентиляционной дыхательной недостаточности наблюдается при слабости дыхательной мускулатуры, механических дефектах мышечного и реберного каркаса грудной клетки, нарушении регуляторных функций дыхательного центра.
2. По этиологии (причинам):
- обструктивная. При этом типе страдают функциональные возможности аппарата внешнего дыхания: затрудняется полный вдох и особенно выдох, ограничивается частота дыхания.
- рестриктивная (или ограничительная). ДН развивается из-за ограничения максимально возможной глубины вдоха.
- комбинированная (смешанная). ДН по комбинированному (смешанному) типу сочетает признаки обструктивного и рестриктивного типов с преобладанием одного из них и развивается при длительном течении сердечно-легочных заболеваний.
- гемодинамическая. ДН развивается на фоне отсутствия кровотока или неадекватной оксигенации части легкого.
- диффузная. Дыхательная недостаточность по диффузному типу развивается при нарушении проникновения газов через капиллярно-альвеолярную мембрану легких при ее патологическом утолщении.
3. По скорости нарастания признаков:
- Острая дыхательная недостаточность развивается стремительно, за несколько часов или минут, как правило, сопровождается гемодинамическими нарушениями и представляет опасность для жизни пациентов (требуется экстренное проведение реанимационных мероприятий и интенсивной терапии). Развитие острой дыхательной недостаточности может наблюдаться у пациентов, страдающих хронической формой ДН при ее обострении или декомпенсации.
- Хроническая дыхательная недостаточность может нарастатьна протяжении нескольких месяцев и лет, нередко исподволь, с постепенным нарастанием симптомов, также может быть следствием неполного восстановления после острой ДН.
4. По показателям газового состава крови:
- компенсированная (газовый состав крови нормальный);
- декомпенсированная (наличие гипоксемии или гиперкапнии артериальной крови).
5. По степени выраженности симптомов ДН:
- ДН I степени - характеризуется одышкой при умеренных или значительных нагрузках;
- ДН II степени - одышка наблюдается при незначительных нагрузках, отмечается задействованность компенсаторных механизмов в покое;
- ДН III степени - проявляется одышкой и цианозом в покое, гипоксемией.
Симптомы дыхательной недостаточности
Признаки ДН зависят от причин ее возникновения, типа и тяжести. Классическими признаками дыхательной недостаточности служат:
Гипоксемия клинически проявляется цианозом (синюшностью), степень которого выражает тяжесть дыхательной недостаточности и наблюдается при снижении парциального давления кислорода (РаО2) в артериальной крови ниже 60 мм рт. ст. Для гипоксемии характерны также нарушения гемодинамики, выражающиеся в тахикардии и умеренной артериальной гипотонии. При понижении РаО2 в артериальной крови до 55 мм рт. ст. наблюдаются нарушения памяти на происходящие события, а при снижении РаО2 до 30 мм рт. ст. пациент теряет сознание. Хроническая гипоксемия проявляется легочной гипертензией.
Проявлениями гиперкапнии служат тахикардия, нарушения сна (бессонница ночью и сонливость днем), тошнота, головные боли. Быстрое нарастание в артериальной крови парциального давления углекислоты (РаСО2) может привести к состоянию гиперкапнической комы, связанной с усилением мозгового кровотока, повышением внутричерепного давления и развитием отека головного мозга. Синдром слабости и утомления дыхательных мышц характеризуется увеличением частоты дыхания (ЧД) и активным вовлечением в процесс дыхания вспомогательной мускулатуры (мышц верхних дыхательных путей, мышц шеи, брюшных мышц).
- синдром слабости и утомления дыхательной мускулатуры
ЧД более 25 в мин. может служить начальным признаком утомления дыхательной мускулатуры. Урежение ЧД менее 12 в мин. может предвещать остановку дыхания. Крайним вариантом синдрома слабости и утомления дыхательной мускулатуры служит парадоксальное дыхание.
Одышка субъективно ощущается пациентами как нехватка воздуха при чрезмерных дыхательных усилиях. Одышка при дыхательной недостаточности может наблюдаться как при физическом напряжении, так и в спокойном состоянии. В поздних стадиях хронической дыхательной недостаточности с присоединением явлений сердечной недостаточности у пациентов могут появляться отеки.
Осложнения
Дыхательная недостаточность является неотложным, угрожающим для здоровья и жизни состоянием. При неоказании своевременного реанимационного пособия острая дыхательная недостаточность может привести к гибели пациента. Длительное течение и прогрессирование хронической дыхательной недостаточности приводит к развитию правожелудочковой сердечной недостаточности в результате дефицита снабжения сердечной мышцы кислородом и ее постоянных перегрузок. Альвеолярная гипоксия и неадекватная вентиляция легких при дыхательной недостаточности вызывает развитие легочной гипертензии. Гипертрофия правого желудочка и дальнейшее снижение его сократительной функции ведут к развитию легочного сердца, проявляющегося в застое кровообращения в сосудах большого круга.
На начальном диагностическом этапе тщательно собирается анамнез жизни и сопутствующих заболеваний с целью выявления возможных причин развития дыхательной недостаточности. При осмотре пациента обращается внимание на наличие цианоза кожных покровов, подсчитывается частота дыхательных движений, оценивается задействованность в дыхании вспомогательных групп мышц.
В дальнейшем проводятся функциональные пробы для исследования функции внешнего дыхания (спирометрия, пикфлоуметрия), позволяющая провести оценку вентиляционной способности легких. При этом измеряется жизненная емкость легких, минутный объем дыхания, скорость движения воздуха по различным отделам дыхательных путей при форсированном дыхании и т. д.
Обязательным диагностическим тестом при диагностике дыхательной недостаточности является лабораторный анализ газового состава крови, позволяющий определить степень насыщения артериальной крови кислородом и углекислым газом (PаО2 и PаСО2) и кислотно-щелочное состояние (КОС крови). При проведении рентгенографии легких выявляются поражения грудной клетки и паренхимы легких, сосудов, бронхов.
Лечение дыхательной недостаточности
Лечение пациентов с дыхательной недостаточностью предусматривает:
- восстановление и поддержание оптимальной для жизнеобеспечения вентиляции легких и оксигенации крови;
- лечение заболеваний, явившихся первопричиной развития дыхательной недостаточности (пневмонии, экссудативного плеврита, пневмоторакса, хронических воспалительных процессов в бронхах и легочной ткани и т. д.).
При выраженных признаках гипоксии в первую очередь проводится оксигенотерапия (кислородная терапия). Кислородные ингаляции подаются в концентрациях, обеспечивающих поддержание PаО2 = 55— 60 мм рт. ст., при тщательном мониторинге рН и PаСО2 крови, состояния пациента. При самостоятельном дыхании пациента кислород подается масочно или через носовой катетер, при коматозном состоянии проводится интубация и поддерживающая искусственная вентиляция легких.
Наряду с оксигнотерапией проводятся мероприятия, направленные на улучшение дренажной функции бронхов: назначаются антибактериальные препараты, бронхолитики, муколитики, массаж грудной клетки, ультразвуковые ингаляции, лечебная физкультура, проводится активная аспирация секрета бронхов через эндобронхоскоп. При дыхательной недостаточности, осложненной легочным сердцем, назначаются диуретики. Дальнейшее лечение дыхательной недостаточности направлено на устранение вызвавших ее причин.
Прогноз и профилактика
Дыхательная недостаточность является грозным осложнением многих заболеваний и нередко приводит к летальному исходу. При хронических обструктивных заболеваниях легких дыхательная недостаточность развивается у 30% пациентов.Прогностически неблагоприятно проявление дыхательной недостаточности у пациентов с прогрессирующими нейромышечными заболеваниями (БАС, миотония и др.). Без соответствующей терапии летальный исход может наступить в течение одного года.
При всех прочих патологиях, приводящих к развитию дыхательной недостаточности, прогноз разный, однако невозможно отрицать, что ДН является фактором, сокращающим продолжительность жизни пациентов. Предупреждение развития дыхательной недостаточности предусматривает исключение патогенетических и этиологических факторов риска.
1. Интенсивная терапия заболеваний, сопровождающихся острой дыхательной недостаточностью: методические рекомендации/ Прасмыцкий О.Т., Ржеутская Р.Е. - 2001.
3. Дыхательная недостаточность с преимущественным нарушением бронхо-легочных механизмов/ Чеснокова Н.П., Брилль Г.Е., Моррисон В.В., Полутова Н.В.// Научное обозрение. Медицинские науки. - 2017 - №2.
4. Формирование дыхательной недостаточности при хронических обструктивных заболеваниях легких, пути и возможности лечения больных: Автореферат диссертации/ Игнатьев В. А. - 1993.
Гиперкапния
Гиперкапния - это повышение содержания углекислого газа в артериальной крови более 45 мм рт. ст. Состояние чаще всего развивается при снижении вентиляции легких на фоне ХОБЛ и обострения бронхиальной астмы. Причиной синдрома также выступают нервно-мышечные патологии, травмы ребер, критические состояния. Гиперкапния проявляется повышением частоты и нарушением ритма дыхания, дисфункцией миокарда, разнообразной неврологической симптоматикой. Для диагностики используется анализ газов крови, рентгенография ОГК, спирометрия. Лечение включает адекватную респираторную поддержку и комплексную медикаментозную терапию.



Гиперкапния не является самостоятельной нозологической единицей. Она представляет собой клинический синдром в пульмонологии, который отражает неспособность системы органов дыхания поддерживать физиологический уровень углекислого газа в крови. Термин гиперкапния в медицинской литературе отождествляется с вентиляционной («насосной») дыхательной недостаточностью. Истинная частота синдрома не установлена, что обусловлено его высокой распространенностью и частым развитием на фоне других жизнеугрожающих состояний.

Причины гиперкапнии
Появление гиперкапнии связано с резким падением или неадекватным возрастанием альвеолярной вентиляции в тех случаях, когда ресурсов дыхательной системы не хватает для поддержания функции внешнего дыхания. Самыми частыми причинами синдрома выступают эмфизема при тяжелой ХОБЛ и астматический статус, которые сопровождаются резким снижением объема вентиляции в легких. Другие провоцирующие факторы гиперкапнии:
- Длительная интубация. При проведении ИВЛ объем мертвого пространства легких возрастает до 50-70%, в результате чего углекислый газ не может в должной мере выводиться из организма. Риск гиперкапнической дыхательной недостаточности повышается, если интубация проводилась на фоне развития ТЭЛА.
- Нервно-мышечные заболевания. При миастении, полинейропатии, боковом амиотрофическом склерозе поражается дыхательная мускулатура и резко ухудшается легочная вентиляция. Все пациенты с тяжелыми формами таких заболваний страдают от гиперкапнической недостаточности функции дыхания.
- Патологии ЦНС. Причиной гиперкапнии выступают травмы, опухоли и другие патологические процессы, протекающие с поражением дыхательного центра. Без центральной регуляции процессы внешнего дыхания становятся хаотичными и неэффективными.
- Травмы. Изредка гиперкапнический синдром развивается при серьезных повреждениях мышечного и реберного каркаса грудной клетки. Сильные боли и механическое препятствие ограничивают возможности расправления легких, повышают показатели мертвого пространства.
- Критические состояния. Гиперкапния может возникать при относительной гиповентиляции на фоне возрастающей нагрузки на дыхательную систему. Такое состояние наблюдается при сепсисе, разных видах шока, тромбоэмболии.
Патогенез
В норме во вдыхаемом воздухе находится около 0,03% углекислого газа, тогда как в выдыхаемом - до 4%. Такая разница в концентрациях обусловлена процессами тканевого дыхания, в результате которых в венозную кровь попадает большое количество CO2. Еще больше углекислого газа (до 5,5%) находится в альвеолярной среде, которая включает анатомическое мертвое пространство, не участвующее в процессах газообмена.
Удаление двуокиси углерода из организма происходит по градиенту давления: газ диффундирует через альвеолярные стенки, выделяется в окружающую среду на выдохе. Проницаемость легочных мембран для СО2 составляет до 600 мл в минуту при давлении в 1 мм рт. ст., что в 20-25 раз больше, чем показатель диффузионной способности кислорода. Поэтому гиперкапния встречается реже гипоксемии, в основном при тяжелых дыхательных расстройствах.
При нарушении вентиляционной функции легких и развитии гиперкапнии в крови снижается показатель рН, возникает респираторный ацидоз. Патологическое состояние вызывает сужение сосудов легких при одновременном расширении артерий других органов тела, что ухудшает диффузию газов и усугубляет имеющиеся нарушения. При острой гиперкапнии происходит церебральная вазодилатация, увеличивается внутричерепное давление.

Симптомы гиперкапнии
В клинической картине на первый план выходит одышка. Частота дыхания увеличивается боле 30-35 раз в минуту, иногда наблюдается парадоксальное дыхание - втяжение живота и выпячивание грудной клетки на вдохе. Пациенты испытывают постоянную нехватку воздуха, дыхание становится шумным и пыхтящим. При попытках вдохнуть полной грудью необходимо напрягать вспомогательную мускулатуру грудной клетки, живота и шеи.
Вследствие патологических влияний углекислоты возникают признаки нарушения работы сердечно-сосудистой системы. Наблюдается системное расширение сосудов, из-за чего кожа приобретает интенсивную розовую окраску, становится очень теплой на ощупь. При гиперкапнии учащается сердечный ритм и повышается сила сокращений миокарда. Поражение ЦНС представлено нарушениями сна, головными болями, хлопающим тремором.
При быстром нарастании количества СО2 в крови развивается отек головного мозга, который результирует гиперкапнической комой. При этом в нервной ткани активизируется гликолиз и образование лактата, что усиливает явления ацидоза и усугубляет состояние больного. Опасным для жизни признано значение рН крови менее 7,2. При хронической вентиляционной недостаточности нарушается работа дыхательного центра и его адаптация к изменениям показателей кислорода в крови.
Обследованием пациентов с острой формной гиперкапнии занимаются врачи-реаниматологи в рамках экстренного оказания медицинской помощи. Хронические варианты дыхательных нарушений находятся в компетенции пульмонолога. По показаниям к консультации привлекают кардиолога, невролога. Для оценки степени тяжести гиперкапнии и выявлении первопричины ее развития проводится:
- Рентгенография грудной клетки. При острой гиперкапнической недостаточности на фоне ХОБЛ или бронхиальной астмы определяется картина «чистых» легких. Другие причины нарушений состава газов крови могут визуализироваться в виде диффузных двусторонних затемнений, лобарного или сегментарного поражения. На рентгенограммах также можно определить травмы ребер.
- Спирометрия. Исследование функциональной способности легких необходимо пациентам с хронической гиперкапнией для поиска возможных провоцирующих факторов. При эмфиземе наблюдается необратимое снижение ОФВ и ФЖЕЛ, тогда как для бронхиальной астмы типична частично обратимая обструкция.
- ЭКГ. При исследовании определяются признаки перегрузки правых отделов сердца, ишемии миокарда, гипертрофии левого желудочка. У пациентов с длительно существующей пульмонологической патологией диагностируется типичная картина хронического легочного сердца.
- КТ головного мозга. Исследование проводится для исключения неврологических причин гиперкапнии, при подозрении на развитие отека легких на фоне острой быстропрогрессирующей дыхательной недостаточности. Для уточнения диагноза назначается МРТ головного мозга.
- Анализ газового состава крови. По результатам исследование определяется повышение уровня СО2 при одновременном снижении содержания кислорода. Дополнительно исследуется уровень бикарбонатов: возрастание значение более 26 ммоль/л указывает на хроническую гиперкапнию, поскольку для активации компенсаторных механизмов требуется время.

Лечение гиперкапнии
При острой гиперкапнии назначаются неотложные лечебные мероприятия, которые направлены на стабилизацию дыхательной функции. Терапия проводится в ОРИТ и начинается с восстановления адекватной вентиляции: проверки проходимости дыхательных путей, назначения неинвазивной или инвазивной респираторной поддержки с положительным вентиляционным давлением. Фармакотерапия гиперкапнии включает такие группы препаратов:
- Бронходилататоры. Лекарства расширяют просвет бронхов и облегчают вентиляцию легких, уменьшают размеры мертвого пространства, благодаря чему избыток СО2 быстрее выводится из организма.
- Муколитики. Медикаменты усиливают дренажную функцию бронхов, способствуют выведению вязкой мокроты из дыхательных путей, которая может препятствовать нормальному газообмену.
- Диуретики. Препараты используются при осложнении гиперкапнии отеком мозга и перегрузкой кардиоваскулярной системы. Назначаются под постоянным контролем водного баланса, иногда в комбинации с внутривенной инфузионной терапией.
После стабилизации состояния пациентам проводится этиопатогенетическая терапия, направленная на ликвидацию основного заболевания, вызвавшего гиперкапнию. Помимо медикаментов, в комплексном лечении применяются методики постурального дренажа, лечебной физкультуры, физиотерапии. При некоторых нервно-мышечных болезнях длительная ИВЛ является единственно возможным способом поддержания баланса газов крови.
Течение гиперкапнии определяется ее первопричиной, скоростью развития и степенью тяжести симптоматики. Более благоприятный прогноз определяется для пациентов с отсутствием органических поражений легочной паренхимы или дыхательной мускулатуры. Профилактика заключается в предупреждении и раннем выявлении хронических заболеваний легких, индивидуальном подборе параметров при проведении ИВЛ.

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Обеспечивая организм кислородом, дыхательная система одновременно выводит продукт метаболизма - углекислый газ (диоксид углерода, CO2), который кровь приносит из тканей в альвеолы легких, и благодаря альвеолярной вентиляции он удаляется из крови. Так вот, гиперкапния означает аномально повышенный уровень углекислого газа в крови. [1]
Эпидемиология
По данным зарубежной статистики, при ожирении с ИМТ 30-35 синдром гиповентиляции развивается в 10% случаев, в при индексе массы тела 40 и выше - в 30-50%.
Среди пациентов с тяжелой гиперкапнией летальный исход из-за дыхательной недостаточности, в среднем, составляет 65%.
Врачи-пульмонологи называют такие причины повышения содержания диоксида углерода (его парциального давления - РаСО2) в крови, как:
- ;
- обострение астмы и длительное снижение проходимости (обструкция) дыхательных путей, приводящие к астматическому статусу; , которая может быть связана с повреждением альвеол при хроническом облитерирующем бронхиолите, эмфиземе легких, пневмоните, а также силикозе и других пнемокониозах - профзаболеваниях дыхательных путей; ;
- уменьшение дыхательного объема, в том числе, при пневмосклерозе (часто обусловленном хроническим бронхитом); ателектазе легких и хронически протекающей бронхоэктатической болезни; при проблемах с сердцем и некоторых системных заболеваниях; , негативно влияющее на баланс O2 и CO2 в крови из-за поверхностного и прерывистого дыхания; [2]
- снижение тонуса и/или эластичности диафрагмы и межреберных дыхательных мышц при миопатиях дистрофического или неврологического характера, например, миастении, боковом амиотрофическом склерозе, синдроме Гийена-Барре.
Могут быть этиологически связаны гиперкапния и инсульт, черепно-мозговые травмы и новообразования головного мозга - из-за расстройства церебрального кровообращения и повреждения дыхательного центра продолговатого мозга.
Кроме того, отмечается и метаболическая гиперкапния, обусловленная дисбалансом электролитов (нарушением кислотно-основного состояния) при лихорадке, гормональных нарушениях (гиперкортицизме, тиреотоксикозе), нефрологических заболеваниях (почечной недостаточности), метаболическом алкалозе, развитии сепсиса. [3]
Гиперкапния у детей может быть обусловлена:
- ; ;
- аспирацией дыхательных путей новорожденных амниотической жидкостью и меконием; .
У недоношенных младенцев недостаток кислорода в крови - гипоксемия и гиперкапния развиваются при бронхолегочной дисплазии, связанной с длительной искусственной поддержкой дыхательной функции (ИВЛ). [4]
Факторы риска
Помимо частых инфекционных поражений легких - бронхопневмонии и пневмонии, а также всех хронически протекающих бронхолегочных заболеваний, риск гиперкапнии повышается при:
- курении;
- высокой степени ожирения (при избыточном весе с ИМТ более 30-35 процесс дыхания затрудняется); , или вдыхании воздуха, содержащего аномально высокие концентрации СО2;
- гипотермии (переохлаждении);
- раке легких;
- больших дозах алкоголя, передозировке производных опия (угнетающих центральное дыхание);
- деформациях грудной клетки, в частности, при искривлении позвоночника;
- аутоиммунных патологиях с системными фиброзами (ревматоидном артрите, муковисцидозе и др.);
- наличии генетических аномалий - врожденной центральной гиповентиляции или синдрома проклятия Ундины.
В процессе метаболизма клеток в их митохондриях продуцируется углекислый газ, который затем диффундирует в цитоплазму, межклеточное пространство и в капилляры - растворяясь в крови, то есть связываясь с гемоглобином эритроцитов. А удаление CO2 происходит во время дыхания путем газообмена в альвеолах - диффузии газа через альвеолярно-капиллярные мембраны. [5]
В норме (в состоянии покоя) дыхательный объем составляет 500-600 мл; вентиляция легких - 5-8 л/мин, а минутный объем альвеолярной вентиляции - 4200-4500 мл.
Часто ставя знак равенства между гиперкапнией, гипоксией и респираторным ацидозом, физиологи связывают патогенез повышения парциального давления диоксида углерода (РаСО2) в крови с нарушением вентиляции - альвеолярной гиповентиляцией, результатом которой и является гиперкапния.
Кстати, гиперкапния и ацидоз взаимосвязаны, поскольку респираторный ацидоз со снижением рН артериальной крови, является нарушением кислотно-основного состояния при повышении содержания углекислого газа в крови, которое обусловлено гиповентиляцией. Именно респираторным ацидозом объясняются головные боли, дневная сонливость, тремор и судороги, проблемы с памятью. [6]
А вот снижение уровня СО2 в крови - гипокапния и гиперкапния (т. е. его повышение) - состояния диаметрально противоположные. При этом гипокапния возникает при гипервентиляции легких. [7]
Но вернемся к механизму развития гиперкапнии. В процессе легочной вентиляции не весь выдыхаемый воздух (около трети) освобождается от углекислого газа, так как часть его остается в так называемом физиологическом мертвом пространстве дыхательной системы - объеме воздуха в различных ее сегментах, который сразу не подвергается газообмену. [8]
Бронхолегочные заболевания и другие факторы вызывают нарушения легочного капиллярного русла и структуры альвеолярной ткани, уменьшают поверхность диффузии и снижают альвеолярную перфузию, а также увеличивают объем мертвого пространства, где уровень О2 низкий, а содержанием CO2 очень высокое. И при очередном дыхательном цикле (вдохе-выдохе) углекислый газ полностью не выводится, а остается в крови. [9]
Например, при хроническом обструктивном бронхите из-за снижения альвеолярной вентиляции наблюдается гипоксемия и гиперкапния, то есть уровень кислорода в крови снижается, а содержание углекислого газа возрастает. [10]
Хроническая гиперкапния с низким содержанием О2 в крови может быть при отсутствии явных причин, в первую очередь, со стороны органов дыхания. И в таких случаях альвеолярную гиповентиляцию связывают с нарушением (скорее всего, обусловленным генетически) функции центральных хеморецепторов CO2 в продолговатом мозге или хеморецепторов в каротидных телах наружной стенки сонной артерии. [11]
Медленно развивающийся синдром гиперкапнии, точнее, синдром альвеолярной гиповентиляции может быть бессимптомным, а его первые признаки - головные боли, головокружение, ощущение усталости - неспецифичны.
Также симптомы гиперкапнии могут проявляться: сонливостью, гиперемией кожи лица и шеи, тахипноэ (учащенным дыханием), нарушением ЧСС с аритмией, повышением АД, судорожными сокращениями мышц и астериксом (колебательным тремором кистей), обмороками.
Достаточно часто наблюдается диспноэ (одышка), хотя гиперкапния и одышка могут быть связаны опосредованно, поскольку неглубокое, но частое дыхание наблюдается при бронхолегочных заболеваниях (приводящих к ухудшению альвеолярной вентиляции).
Для клинической картины тяжелой гиперкапнии характерны нерегулярное сердцебиение, судороги, спутанность сознания и его потеря, дезориентация, панические атаки. При этом - если мозг и сердце не получают достаточно кислорода - велик риск комы или остановки сердца.
Неотложным состоянием является острая гиперкапния или острая гипоксемическая легочная недостаточность.
А пермиссивная гиперкапния относится к повышенному парциальному давлению СО2. обусловленному гиповентиляцией у пациентов на ИВЛ с повреждением легких при остром респираторном дистресс-синдроме или обострении бронхиальной астмы. [12]
Гиперкинезы
Неосознанно производимые и нецелесообразные с точки зрения физиологии активные движения - гиперкинезы - относятся к патологиям нервной регуляции мышц различной локализации и возникают в результате поражения центральной и соматической нервной системы.
Код по МКБ-10
Причины гиперкинезов
Причины гиперкинезов, как и многих других двигательных аномалий, связаны с частичной дисфункцией церебрального двигательного аппарата, мотонейронов и тормозных нейронов двигательной области коры головного мозга, ствола мозга или спинного мозга, двигательных нервных волокон, нервно-мышечных синапсов и т.д.
Ключом к этиологии гиперкинезов является «неисправность» экстрапирамидной системы ЦНС. Функциональная задача этой чрезвычайно сложной нейромедиаторной системы состоит в регулировании мышечного напряжения и расслабления, контроле положения тела в пространстве и управлении мимикой, а также всеми автоматически возникающими двигательными реакциями организма. Несогласованность работы двигательных центров коры головного мозга, ядер двигательного анализатора (расположенных в подкорке), зубчатых ядер мозжечка и проводящих путей искажает импульсы двигательных нейронов, которые поступают мышцам. Из-за этих нарушений непроизвольная моторика человека приобретает аномальный характер, и тогда диагностируются экстрапирамидные гиперкинезы.
Если органическая или функциональная патология затронула двигательные центры ретикулярной зоны ствола головного мозга, то возникают стволовые дистонические гиперкинезы, а поражение подкорковых двигательных структур дает подкорковые гиперкинезы: хореические, атетоидные, миоклонические.
Важнейшую роль играет биохимический механизм неосознанных движений человека, который базируется на таких основных нейромедиаторах, как дофамин, ацетилхолин и гамма-аминомасляная кислота (ГАМК). Синтезируемый аксонами нервных клеток головного мозга дофамин относится к стимуляторам двигательной активности, а его воздействие уравновешивают нейромедиаторы-антагонисты - ацетилхолин и ГАМК. Если гамма-аминомасляная кислота является основным тормозящим нейромедиатором ЦНС, то ацетилхолин возбуждает нейроны вегетативной нервной системы и обеспечивает передачу нервных импульсов от двигательных нервов к рецепторам постсинаптических мембран периферических нервных окончаний мышц. Кроме того, в трансмиссии двигательных нервных импульсов задействованы и другие «химические посредники»: адреналин, норадреналин, серотонин, глицин, глутаминовая и аспарагиновая кислоты.
Нейрофизиологами установлено, что дисбаланс в выработке организмом данных нейротрансмиттерных веществ и, соответственно, изменение ответной реакции их рецепторов могут быть причиной двигательных расстройств. Также к возникновению экстрапирамидных гиперкинезов непосредственное отношение имеют проблемы с функционированием базальных ганглиев - регулирующих двигательные функции структур подкорки переднего мозга. Поражение данных нейронных узлов и нарушение их связей со спинным мозгом вызывает неуправляемую гиперактивность различных мышечных групп.
Все это может происходить вследствие поражения сосудов мозга (хронической церебральной ишемии); сосудистой компрессии нервов, идущих к мышцам; детского церебрального паралича; заболеваний эндокринной системы (гипертиреоз); аутоиммунных и наследственных патологий (ревматизм, рассеянный склероз, системная красная волчанка). Среди органических причин гиперкинезов также значатся черепно-мозговые травмы, опухоли, нейроинфекции (менингит, энцефалит) или токсические (в первую очередь, медикаментозные) воздействия на структуры головного мозга.
Симптомы гиперкинезов
Тикозный гиперкинез считается наиболее распространенным видом церебральных двигательных нарушений. Он представляет собой машинальные импульсивные движения лицевой и шейной мускулатуры, которые имеют вид частого моргания и зажмуривания глаз, стереотипных гримас, судорожных однообразных наклонов или поворотов головы и т.д. Как отмечают специалисты, данный вид гиперкинеза становится более выраженным, когда человек волнуется или находится в состоянии эмоционального перевозбуждения. Например, тикозный гиперкинез может иметь рефлекторный характер и появляться в качестве ответной реакции человека на слишком громкий звуке или внезапную вспышку света.
Также симптомы гиперкинезов этого вида могут проявляться в виде непроизвольных звуков, возникающих из-за быстрых сократительных движений мышц гортани, глотки или рта. Кстати, большинству пациентов удается на доли секунд сдерживать начало тика, но для этого приходится затрачивать огромные усилия, после чего неизбежен пароксизм (то есть приступ развивается сильнее и длится дольше). Но ни один из видов гиперкинезов, в том числе тики, не дают о себе знать в состоянии сна.
Хореиформные гиперкинезы, которые имеют и такие названия, как хореический гиперкинез, генерализованный гиперкинез или хорея, проявляются в виде аритмичных экспрессивных движений мимической мускулатуры в области бровей, глаз, рта, носа, а также мышц конечностей.
Гемифациальные спазмы или гиперкинезы лица, как правило, наблюдаются на одной стороне лица: судорожные неритмичные сокращения лицевых мышц могут варьироваться от прерывисто частых до практически постоянных. Гиперкинез всего лица называют параспазмом. Когда лицевые гиперкинезы затрагивают мышечное кольцо вокруг глаз, то человек постоянно непроизвольно зажмуривается, и в этом случае диагностируется блефароспазм. Если же сокращаются круговая или радиальные мышцы рта (с вовлечением нижнечелюстной мускулатуры), то такая патология называется орофациальная дистония или оральный гиперкинез, который визуально воспринимается как кривлянье. При нарушениях иннервации подбородочноязычной, шилоязычной и продольных мышц языка появляются гиперкинезы языка, и пациенты с данной проблемой часто помимо воли высовывают язык наружу.
Симптомы гиперкинезов хореического характера часто проявляются в пожилом возрасте при сенильной атрофии участков мозга (из-за нарушений церебрального кровообращения), при инфекциях и травмах мозга, при хореической эпилепсии Бехтерева, при генетически обусловленной болезни Гентингтона. Если довольно частые непроизвольные движения с большой амплитудой размаха появляются в конечностях с одной стороны тела, то неврологи по этим симптомам определяют баллизм, который может говорить даже об опухоли головного мозга.
Такой вид аномальной моторики, как атетоидный гиперкинез, имеет весьма характерные признаки в виде неспешных причудливых изгибаний пальцев, кислей и ступней, но спазмы нередко захватывают лицо, шею и туловище. И такие клинические случаи определяются как хореоатетоидные гиперкинезы или хореоатозы. При данных кинетических нарушениях с течением времени может развиваться значительное ограничение подвижности суставов и мышц (контрактуры).
Дрожательный гиперкинез (тремор) - это очень часто повторяющиеся, достаточно ритмичные, малоамплитудные движения головой (вверх-вниз и влево-вправо), руками (особенно кистями и пальцами), а нередко и всем туловищем. У некоторых дрожание может становиться более интенсивным в спокойном состоянии, у других - при попытках осуществления каких-либо целенаправленных действий. Типичный дрожательный гиперкинез - наиболее показательный признак болезни Паркинсона.
Гиперкинез медленного типа может появляться на фоне низкого мышечного тонуса одних мышц и спастических сокращений других, и это дистонический гиперкинез. Именно такой характер двигательной патологии отмечается у пациентов с гиперкинетическим ДЦП. Также неврологами выделяется скручивающий (торсионный) спазм или деформирующая мышечная дистония, при которой любые действия провоцируют внезапные неконтролируемые неритмичные спиралевидные движения мускулатуры шеи (спастическая кривошея) и туловища, принуждающие человека принимать весьма причудливые статические позы. И чем экстенсивнее процесс, тем выше степень двигательной ограниченности пациента, что через какое-то время приводит к постоянно деформированному пространственному положению тела.
Симптоматика, отличающая миоклонический гиперкинез, проявляется в резких и быстрых дерганьях - синхронных или последовательных ударно-точковых сокращениях одной или нескольких мышц различной локализации (в первую очередь, языка, лицевой части головы и шеи). Затем наступает мышечное расслабление, нередко сопровождаемое тремором. Значительная часть таких двигательных дисфункций вызывается генетическими дегенерациями структур головного мозга и имеет семейный анамнез.
Как отмечают специалисты, проявляющийся подергиваниями отдельных мышц всего тела неврозоподобный гиперкинез в большей степени характерен для детей, и его нужно четко дифференцировать от невроза навязчивых движений. И здесь все решает правильная диагностика.
Читайте также:
