Использование лейцина, фенилаланина для оценки метаболизма белков
Добавил пользователь Morpheus Обновлено: 21.01.2026
Комплексное исследование, направленное на определение содержания аминокислот и их производных в моче в целях диагностики врождённых и приобретенных нарушений аминокислотного обмена.
Состав комплекса: Аланин • Аргинин • Аспарагиновая кислота • Цитруллин • Глутаминовая кислота • Глицин • Метионин • Орнитин • Фенилаланин • Тирозин • Валин • Лейцин • Изолейцин • Серин • Аспарагин • Alpha-аминоадипиновая кислота • Глутамин • Таурин • Гистидин • Треонин • 1-метилгистидин • 3-метилгистидин • Gamma-аминомасляная кислота • Alpha-аминомасляная кислота • Лизин • Цистин • Триптофан • Гомоцистин • Фосфоэтаноламин • Фосфосерин • Этаноламин
Синонимы русские
Аминокислотный профиль, скрининг аминоацидопатий.
Синонимы английские
Amino acid profile, screening of aminoacidopathy.
Метод исследования
Высокоэффективная жидкостная хроматография.
Единицы измерения
Ммоль/моль креат. (миллимоль на моль креатинина).
Какой биоматериал можно использовать для исследования?
Среднюю порцию утренней мочи.
Как правильно подготовиться к исследованию?
- Исключить из рациона алкоголь в течение 24 часов до исследования.
- Исключить прием мочегонных препаратов в течение 48 часов до сбора мочи (по согласованию с врачом).
Общая информация об исследовании
Аминокислоты - это органические соединения, которые являются основными структурными компонентами белков. В свободном или связанном состоянии они участвуют в ферментативных реакциях, гормональных процессах, выполняют роль нейротрансмиттеров, участвуют в метаболизме холестерола, регуляции рН, контроле воспалительных реакций.
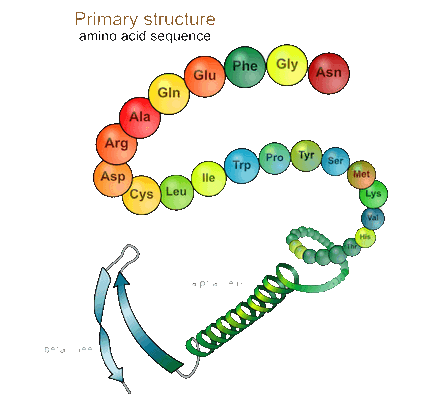
Всего в составе белковых молекул в организме человека было обнаружено 20 аминокислот, из которых часть является незаменимыми, то есть они не синтезируются в организме и должны постоянно присутствовать в употребляемой человеком пище. К незаменимым аминокислотам относятся лизин, гистидин, аргинин, треонин, валин, метионин, триптофан, фенилаланин, лейцин, изолейцин. К заменимым относятся аланин, аргинин, цистин, цистеин, гистидин, глицин, серин, аспарагиновая кислота, тирозин, пролин, оксипролин, глутаминовая кислота. Помимо этого, известен ряд аминокислот, которые являются производными и важными биологическими компонентами других аминокислот.
Анализ аминокислот в моче позволяет оценить их качественный и количественный состав, получить информацию об имеющемся дисбалансе, что может свидетельствовать о пищевых и метаболических нарушениях, лежащих в основе большого числа заболеваний. Следует отметить, что снижение количества той или иной аминокислоты в моче происходит раньше, чем в плазме крови. Учитывая эти обстоятельства и доступность исходного биоматериала, определение аминокислот в моче может быть рекомендовано для оценки ранних изменений аминокислотного состава.
Для определения качественного и количественного состава аминокислот в моче используется метод высокоэффективной жидкостной хроматографии. Он относится к современным хроматографическим методам анализа. Хроматография - это метод разделения и определения веществ, основанный на распределении компонентов между двумя фазами - подвижной и неподвижной. Жидкостная хроматография - метод разделения и анализа сложных смесей веществ, в котором подвижной фазой является жидкость. Он позволяет разделить и выявить количественно более широкий круг веществ с различной молекулярной массой и размерами, в данном случае аминокислот в моче. Исследуются следующие аминокислоты и их производные.
Аланин является одним из источников синтеза глюкозы и регулятором уровня сахара в крови, а также важным энергетическим компонентом для органов центральной нервной системы.
Аргинин участвует в ряде ферментативных реакций и выведении из организма остаточного азота в составе мочевины, креатинина, орнитина, в репаративных процессах.
Аспарагиновая кислота участвует в реакцияхцикла переаминирования и мочевины, синтезе пуриновых и пиримидиновых оснований, регуляции синтеза иммуноглобулинов.
Цитруллин участвует в стимуляции процессов иммунной системы, в процессах детоксикации в печени.
Глутаминовая кислота является нейромедиаторной аминокислотой, стимулирующей передачу возбуждения в синапсах центральной нервной системы. Участвует в обмене белков, углеводов, окислительно-восстановительных процессах, детоксикационных процессах и выведении аммиака из организма. Также принимает участие в синтезе других аминокислот, ацетилхолина, АТФ (аденозинтрифостфата), в переносе ионов калия, входит в состав скелетной мускулатуры.
Глицин является нейромедиаторной аминокислотой, регулирующей процессы торможения и возбуждения в центральной нервной системе. Участвует в выработке порфиринов, пуриновых оснований. Повышает обменные процессы в головном мозге, улучшает умственную работоспособность.
Метионин - это аминокислота, которая необходима для синтеза адреналина, холина. Участвует в обмене жиров, фосфолипидов, витаминов, активирует действие гормонов, ферментов, белков. Является источником серы в выработке серосодержащих аминокислот, в частности цистеина. Метионин также обеспечивает процессы детоксикации, способствует пищеварению, является одним из источников синтеза глюкозы.
Орнитин участвует в синтезе мочевины, снижении концентрации аммиака в плазме крови, регулирует кислотно-щелочной баланс в организме человека. Необходим для синтеза и высвобождения инсулина и соматотропного гормона, для нормального функционирования иммунной системы.
Фенилаланин необходим для синтеза нейромедиаторов: адреналина, норадреналина, допамина. Улучшает работу центральной нервной системы, функционирование щитовидной железы.
Аминокислота тирозин необходима в биосинтезе меланинов, дофамина, адреналина, гормонов щитовидной железы. Улучшает работу надпочечников, щитовидной железы, гипофиза.
Валин является важным источником для функционирования мышечной ткани, участвует в поддержании баланса азота в организме, регулирует восстановительные процессы в поврежденных тканях.
Лейцин является важным компонентом в синтезе холестерина, других стероидов и гормона роста и, следовательно, участвует в процессах регенерации тканей и органов.
Изолейцин участвует в энергетических процессах организма, регулирует уровень глюкозы в крови, необходим для синтеза гемоглобина и также участвует в регенерации кожи, мышечной, хрящевой и костной тканей.
Гидроксипролин является компонентом большинства органов и тканей организма человека, входит в состав коллагена.
Аминокислота серин необходима для синтеза пуриновых и пиримидиновых оснований, а также для ряда других аминокислот (цистеина, метионина, глицина). Участвует в обмене жирных кислот и жиров, в функционировании некоторых ферментов.
Аспарагин является важным регулятором процессов, происходящих в центральной нервной системе (возбуждение-торможение), участвует в метаболизме и синтезе аминокислот в печени.
Альфа-аминоадипиновая кислота является одним из продуктов конечного обмена аминокислот.
Глутамин участвует в синтезе углеводов, других аминокислот, нуклеиновых кислот, ферментов. Обеспечивает поддержание кислотно-щелочного равновесия, необходим для синтеза белков скелетной и гладкомышечной мускулатуры, обладает антиоксидантной активностью.
Таурин способствует увеличению энергетической активности клеток, участвует в процессах заживления и регенерации, нормализует функциональное состояние клеточных мембран.
Треонин необходим в синтезе коллагена и эластина, регулирует обмен веществ за счет участия в функционировании работы печени, белковом и жировом обмене.
1-метилгистидин и 3-метилгистидин являются одними из показателей распада белков мышечной ткани.
Гамма-аминомасляная кислота в основном содержится в центральной нервной системе и головном мозге. Участвует в обменных процессах в данных органах, в процессах нейромедиаторной передачи импульсов, оказывая тормозящее действие на нервную активность, а также играет роль в метаболизме глюкозы.
Альфа-аминомасляная кислота участвует в синтезе некоторых белков и является продуктом биосинтеза офтальмовой кислоты, являющейся структурным компонентом хрусталика глаза.
Пролин входит в состав большинства белков, а также является компонентом инсулина, адренокортикотропного гормона, коллагена. Способствует восстановлению кожи, соединительной ткани.
Лизин входит в состав большинства белков, необходим дляроста, восстановления тканей, синтеза гормонов, ферментов, антител, синтеза коллагена.
Аминокислотный синтез
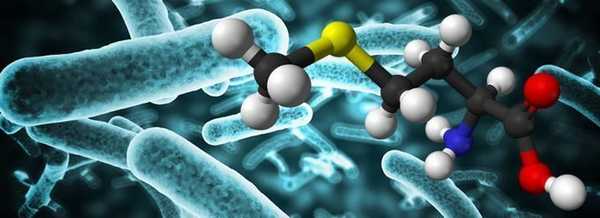
Аминокислоты — органические биологически важные соединения, в молекуле которых одновременно содержатся карбоксильные (-СООН) и аминные группы (-NH2) , и имеющие боковую цепь, специфичную для каждой аминокислоты. Ключевые элементы аминокислот - углерод (C), водород (H), кислород (O) и азот (N). Прочие элементы находятся в боковой цепи определенных аминокислот.
Как известно, пробиотические микроорганизмы (бактерии) синтезируют различные биологически активные вещества: ранее проведенными исследованиями было установлено, что в микробной биомассе пробиотических культур (бифидобактерий и пропионовокислых бактерий), а также в отработанной культуральной жидкости содержатся антимутагенные вещества , ферменты, витамины группы В , короткоцепочечные жирные кислоты и аминокислоты. Отмечено, например, что пропионовокислые бактерии характеризуются очень хорошо развитой биосинтетической способностью и как представители прокариот способны синтезировать все аминокислоты, входящие в состав клеточных белков.
Одной из важнейших функций аминокислот является их участие в синтезе белков, выполняющих каталитические, регуляторные, запасные, структурные, транспортные, защитные и другие функции. Иными словами, пробиотические микроорганизмы играют огромную роль в процессах белкового синтеза и потому являются весьма ценными источиками аминокислот, ферментов и т.п. К слову, природные аминокислоты являются, как правило, оптически активными L - и D формами, которые трудно разделить, вот почему микробный синтез является ныне основным и экономически выгодным в промышленности.
ПОЛУЧЕНИЕ АМИНОКИСЛОТ . Существует четыре промышленных метода получения аминокислот: 1) экстракция из гидролизата белка; 2) химический синтез; 3) биотрансформация соединений-предшественников в ферментере или клеточном реакторе; 4) микробная ферментация.
Успех промышленного получения аминокислот объясняется тем, что химический синтез соединений-предшественников относительно дешев. Кроме того, для производства практически всех протеиногенных аминокислот разработаны методы ферментации, и имеются штаммы, позволяющие получать большие количества продукта. Во многих случаях такой подход экономически оправдан. Широко используются штаммы, усовершенствованные методами генетической инженерии. К настоящему времени закончено секвенирование генома Corynebacterium glutamicum. Полученная генетическая информация поможет ускорить создание новых высокопродуктивных штаммов. Во многих случаях уже клонированы целые опероны, ответственные за биосинтез аминокислот. Изучаются возможности управления обменом веществ клетки методами так называемой метаболической инженерии.
Для более детального рассмотрения темы промышленного интеза аминокислот следует перейти по кнопке-ссылке:
Стоит особенно отметить, что пропионовокислые бактерии могут синтезировать все аминокислоты за счет ассимиляции азота (NH4)2SO4. Б ифидобактерии , также отличаются образованием данных органических соедиинений. В частности, бифидобактерии выделяются синтезом триптофана, который является биологическим прекурсором серотонина (из которого затем может синтезироваться мелатонин) и ниацина (витамина PP или B3) — водорастворимого витамина, участвующего во многих окислительно-восстановительных реакциях, образовании ферментов, обмене липидов и углеводов в живых клетках.
Одним из примеров практического использования способности пробиотических бактерий к аминокислотному (белковому) синтезу , является использование их заквасок в пищевой промышленности, что позволяет получать продукты сбалансированные по аминокислотному составу. Например, при использовании бифидо- и пропионовокислых бактерий в производстве сырокопченых колбас , происходит значительное накопление в продуктах свободных аминокислот, а сумма незаменимых аминокислот становится выше на 29%. Преимущественное накопление глицина, глютаминовой кислоты, валина, фенилаланина, тирозина, лейцина, изолейцина отражает специфическое совместное воздействие на белки и пептиды тканевых эндопептидаз и экзопептидаз, а также биосинтез белков пропионовокислыми бактериями.
Нашли свое применение пробиоти ки и в сельском хозяйстве. Использование бактерий в качестве продуцента белкового корма является более эффективным, так как бактерии образуют до 75% белка по массе, в то время как дрожжи - не более 60%. Например, использование штаммов Propionibacterium freudenreichii subsp. shermanii, для приготовления белкового корма не требует расхода воздуха и энергозатрат на его подачу, так как данные штаммы пропионовокислых бактерий являются анаэробами. Штаммы обладают широким спектром антимикробного действия, что исключает развитие посторонней микрофлоры в процессе биосинтеза и поэтому не требуется наличие специального оборудования для соблюдения условий стерильности. Возможность утилизации разнообразных отходов отраслей промышленности, использующих природное сырье, при наращивании биомассы штаммов ПКБ с целью приготовления белкового корма решает также экологические проблемы предприятий.
АМИНОКИСЛОТЫ, СИНТЕЗИРУЕМЫЕ БИФИДОБАКТЕРИЯМИ И ПРОПИОНОВОКИСЛЫМИ БАКТИЕРИЯМИ
БИФИДОБАКТЕРИИ
также образуют из неорганических азотистых соединений незаменимые аминокислоты, в частности - аланин , валин , аспарагин , синтезируют триптофан .
ПИЩЕВАЯ ЦЕННОСТЬ АМИНОКИСЛОТ
Все эти биосинтезирующие функции бактерий открывают огромные возможности в сфере создания продуктов функционального питания. В современных условиях неблагоприятной экологии и снижения качества питания, с пособность бактерий к синтезу практически важных веществ (аминокислот, различных белковых соединений, витаминов, короткоцепочечных жирных кислот, полисахаридов и т.п.), является одним из перспективных инструментов в решени вопросов профилактики и лечения алиментарных заболеваний.
Известно более 200 природных аминокислот, из них только 20 входят в состав белков. Эти аминокислоты называют протеиногенными — строящими белки. В организме человека наряду с протеиногенными аминокислотами можно найти и другие, которые играют иную роль, например, орнитин, β-аланин, таурин и др. Но в данном разделе мы рассмотрим лишь свойства 20-ти стандартных (протеиногенных заменимых и незаменимых аминокислот), участвующих в биосинтезе белка , а также некоторых других, синтезируемых указанными выше пробиотическими микроорганизмами. Как известно, в виде белков аминокислоты являются вторым (после воды) компонентом мышц, клеток и других тканей человеческого организма. Аминокислоты играют решающую роль в таких процессах, как транспорт нейротрансмиттеров и биосинтезе.
Для тех кто хочет получить общее представление или освежить память об основных понятиях, касающихся аминокислот и синтезе белка из аминокислот, а также о роли аминокислот в питании человека, предлагаем перейти по ссылкам:
КЛАССИФИКАЦИЯ АМИНОКИСЛОТ ПО ЗАМЕНИМЫМ И НЕЗАМЕНИМЫМ
Заменимые аминокислоты - это аминокислоты, поступающие в организм человека с белковой пищей, либо образующиеся в организме из иных аминокислот.
Незаменимые аминокислоты - это аминокислоты, которые не могут быть получены в организме человека с помощью биосинтеза, поэтому должны постоянно поступать в виде пищевых белков. Их отсутствие в организме приводит к явлениям, угрожающим жизни.
Незаменимыми аминокислотами для взрослого здорового человека являются аминокислоты фенилаланин , триптофан , треонин , метионин , лизин , лейцин , изолейцин и валин ; Для детей, дополнительно, гистидин и аргинин .
Классификация аминокислот на заменимые и незаменимые содержит ряд исключений:
- Заменимый гистидин, синтезирующийся в организме человека, должен поступать с белковой пищей, так как его производство недостаточно для нормального поддержания здоровья;
- Заменимый аргинин вследствие ряда особенностей его метаболизма, при некоторых физиологических состояниях организма может быть приравнен к незаменимым;
- Тирозин можно считать заменимой аминокислотой лишь при условии достаточного поступления фенилаланина. У больных фенилкетонурией тирозин становится незаменимой аминокислотой.
Потребность в аминокислотах и белке
Потребность в незаменимых аминокислотах
Существуют стандарты сбалансированности незаменимых аминокислот (НАК), разработанные с учетом возрастных данных. Для взрослого человека (г/сутки): триптофана - 1, лейцина 4—6, изолейцина 3—4, валина 3—4, треонина 2—3, лизина 3—5, метионина 2—4, фенилаланина 2—4, гистидина 1,5—2.
Таблица 1. Международные рекомендации по суточной потребности детей в аминокислотах*
Использование лейцина, фенилаланина для оценки метаболизма белков
Скрининговое обследование для исключения врождённых "ошибок" метаболизма по типу аминоацидопатий (наследственные нарушения обмена аминокислот). Показано взрослым с тяжелым нарушением обмена веществ. Определяемые аминокислоты: аланин (ALA), аргинин (ARG), цитруллин (CIT), пролин (PRO), глицин (GLY), метионин (MET), орнитин (ORN), фенилаланин (PHE), тирозин (TYR), валин (VAL), лейцин (LEU) + изолейцин (ILEU), аспарагиновая кислота (ASP), глутаминовая кислота (GLU).
Наследственные нарушения обмена аминокислот (аминоацидопатии).
Высокоэффективная жидкостная хроматография-масс-спектрометрия (ВЭЖХ-МС).
Мкмоль/л (микромоль на литр).
- Исключить из рациона алкоголь в течение 24 часов до исследования.
- Не принимать пищу в течение 8 часов до исследования, можно пить чистую негазированную воду.
- Полностью исключить (по согласованию с врачом) прием лекарственных препаратов в течение 24 часов перед исследованием.
- Исключить физическое и эмоциональное перенапряжение в течение 30 минут до исследования.
- Не курить в течение 30 минут до исследования.
Актуальность рассмотрения нарушений обмена аминокислот определяется тем, что эта патология отражается в первую очередь на функции нервной системы и является одной из основных причин слабоумия. Знание таких патологий необходимо в практике неонатологов и генетиков для профилактики и коррекции олигофрении.
По возможности синтезироваться аминокислоты в организме делятся заменимые и незаменимые. К незаменимым аминокислотам относятся аргинин, валин, изолейцин, лейцин, метионин, фенилаланин, к заменимым аминокислотам - аланин, глицин, тирозин. При дефекте ферментов на разных этапах трансформации аминокислоты и продукты их превращения могут накапливаться и оказывать отрицательное воздействие на организм.
Различают первичные (врождённые) и вторичные (приобретенные) нарушения метаболизма аминокислот. Врождённые заболевания обусловлены дефицитом ферментов и/или транспортных белков, которые связанны с метаболизмом аминокислот. Приобретенные нарушения аминокислот связаны с заболеваниями печени, ЖКТ, почек, недостаточным или неадекватным питанием, новообразованиями.
В норме наибольшая скорость обмена аминокислот характерна для нервной ткани. Поэтому разнообразные наследственные нарушения обмена являются одной из причин изменения функционирования в первую очередь ЦНС.
К числу наиболее серьезных и достаточно распространенных нарушений обмена относятся аномалии метаболизма фенилаланина и тирозина. Причина фенилкетонурии - врождённый дефицит печеночной фенилаланин-4-гидроксилазы. Это приводит к нарушению концентрации в крови, возникает дефицит тирозиновых и триптофановых производных (меланина, катехоламинов, серотонина). При этом в крови и моче значительно увеличиваются концентрации фенилацетилглутамина, фенилпирувата, фенилацетата. В крови повышается концентрация веществ, которые практически полностью отсутствуют в норме (фенилэтиламин, фенилпируват, фениллактат). Это нейротоксические соединения, они нарушают метаболизм липидов в мозге. В сочетании с дефицитом нейромедиаторов (серотонина) этот механизм считается ответственным за прогрессирующее снижение интеллекта у больных и развитие фенилпировиноградной олигофрении.
Лейциноз ("болезнь кленового сиропа") - заболевание обусловлено дефицитом дегидрогеназы разветвленных кетокислот, которая катализирует реакцию окислительного декарбоксилирования. В результате нарушается окисление оксикислот с разветвленной цепью - ОКРЦ, которые образуются при катаболизме аминокислот с разветвленной цепью (лейцин, изолейцин, валин). У больных моча имеет специфический запах кленового сиропа. При данном заболевании особенно патогенно накопление лейцина. Это истинно кетогенная аминокислота. Кетоновые тела играют большую роль в энергообеспечении мозга, особенно при гипогликемии. Нарушение обмена лейцина приводит к развитию умственной отсталости, судорогам, мышечной ригидности, летаргии, рвоте. Отмечаются гипогликемия и кетоацидоз. Основным методом лечения является специальная диета.
Тирозинозы - болезни нарушения обмена тирозина - имеют несколько генокопий и носят аутосомно-рецессивный и аутосомно-доминантный типы наследования, сцепленные с полом. Заболеваемость - 1/20000 населения. Наиболее распространенной формой заболевания признается альбинизм. Наиболее частый механизм заболевания - дефект медьсодержащего фермента меланобластов тирозиназы, блокирующего превращение тирозина в диоксифенилаланин, из которого образуется эпинефрин и меланин. У альбиносов белые кожа и волосы, розово-красные глаза, фотодерматит. Больные страдают фотобоязнью и плохо видят днем вследствие депигментации сетчатки. Нарушение тирозинового обмена приводит к повреждению печени и развитию цирроза.
Поскольку тирозинозы имеют много генокопий и в патогенезе прослеживаются дефекты разных ферментов метаболизма тирозина, то клинически выделяют и другие формы. Среди них наиболее известны тирозиноз Медеса, гипертирозинемия I и II типов, хоукинсурия. При них тирозинемия с тирозинурией часто сочетаются с печеночной и почечной недостаточностью. Хоукинсурия имеет аутосомно-доминантный тип наследования и характеризуется выраженным слабоумием. Ферментативные дефекты метаболизма тирозина могут сопровождаться нарушением продукции тиреоидных гормонов на основе аминокислоты тирозина. Например, дефект йодтирозиндейодиназы - один из механизмов наследственного гипотиреоза с кретинизмом.
Исследование помогает определить уровень аминокислот в крови, их производных, оценить состояние аминокислотного обмена, диагностировать или подтвердить (при наличии характерных симптомов) нарушения обмена аминокислот. В него входит определение 13 показателей: аланин, аргинин, цитруллин, глицин, метионин, орнитин, фенилаланин, тирозин, лейцин/изолейцин, валин, аспарагиновая кислота, глутаминовая кислота.
Когда назначается исследование?
- Сходные случаи заболевания в семье;
- случаи внезапной смерти в раннем возрасте в семье;
- необычный запах тела и/или мочи ("сладкий", "мышиный", "вареной капусты", "потных ног" и др.);
- неврологические нарушения - нарушения сознания (летаргия, кома), различные типы судорожных приступов, изменение мышечного тонуса (мышечная гипотония или спастический тетрапарез);
- нарушения ритма дыхания (брадипноэ, тахипноэ, апноэ);
- нарушения со стороны других органов и систем (поражение печени, гепатоспленомегалия, кардиомиопатия, ретинопатия);
- изменения лабораторных показателей крови и мочи: нейтропения, анемия, метаболический ацидоз/алкалоз, гипогликемия/гипергликемия, повышение активности печеночных ферментов и уровня креатинфосфокиназы, кетонурии, аммониемии;
- тяжелые нарушения обмена веществ;
- дифференциальная диагностика нарушений азотистого обмена.
Что означают результаты?
Референсные значения *
| Компонент | Референсные значения, мкмоль/л |
| Аланин (ALA) | 72.39 - 528.10 |
| Аргинин (ARG) | 14.30 - 83.27 |
| Валин (VAL) | 56.87 - 236.35 |
| Глицин (GLY) | 55.52 - 368.36 |
| Лейцин (LEU) | 48.97 - 255.92 |
| Метионин (MET) | 5.42 - 29.51 |
| Орнитин (ORN) | 18.51 - 79.68 |
| Пролин (PRO) | 72.13 - 177.07 |
| Тирозин (TYR) | 16.25 - 83.25 |
| Фенилаланин (PHE) | 16.22 - 72.34 |
| Цитруллин (CIT) | 8.16 - 32.91 |
| Аспарагиновая кислота (ASP) | 13.58 - 149.29 |
| Глутаминовая кислота (GLU) | 19.96 - 177.08 |
* - исследование предназначено только для лиц старше 18 лет.
Исследование направлено на оценку количественного содержания в крови аминокислот и ацилкарнитинов, которые являются сложными органическими соединениями, играющими важнейшую роль в обменных процессах организма. Комплексное исследование, включающее в себя 32 показателя, позволяет выявить избыточное или недостаточное количество данных веществ и заподозрить нарушения, происходящие вследствие этого.
* Жирным шрифтом выделены аминокислоты
- L-карнитин, свободный
- Аланин (ALA)
- Аргинин (ARG)
- Ацетилкарнитин (С2)
- Бутирилкарнитин (С4)
- Валин (VAL)
- Гексадеценоилкарнитин (C16:1)
- Гексаноилкарнитин (C6)
- Глицин (GLY)
- Декадиеноноилкарнитин (C10:2)
- Деканоилкарнитин (C10)
- Деценоилкарнитин (C10:1)
- Додеканоилкарнитин (Лауроил, C12)
- Додеценоилкарнитин (C12:1)
- Изовалерилкарнитин (C5)
- Лейцин+Изолейцин (XLE)
- Линолеилкарнитин (C18:2)
- Метионин (MET)
- Миристоилкарнитин (Тетрадеканоил, C14)
- Миристолеилкарнитин (Тетрадеценоил, C14:1)
- Октадеканоилкарнитин (Стеароил, C18)
- Октадеценоилкарнитин (Олеил, C18:1)
- Октаноилкарнитин (C8)
- Октеноилкартинин (C8:1)
- Орнитин (ORN)
- Пальмитоилкарнитин (C16)
- Пролин (PRO)
- Пропионилкарнитин (C3)
- Тетрадекадиеноилкарнитин (C14:2)
- Тирозин (TYR)
- Фенилаланин (PHE)
- Цитруллин (CIT)
Аминокислотный профиль; ацилкарнитиновый профиль.
Amino acid profile; acylcarnitine profile.
Высокоэффективная жидкостная хроматография с тандемной масс-спектрометрией.
- Не принимать пищу в течение 8 часов до исследования, можно пить чистую негазированную воду.
- Исключить из рациона алкоголь в течение 24 часов до исследования.
- Полностью исключить (по согласованию с врачом) прием лекарственных препаратов в течение 24 часов перед исследованием.
- Исключить физическое и эмоциональное перенапряжение в течение 30 минут до исследования.
- Не курить в течение 30 минут до исследования.
- Детям в возрасте до 1 года не принимать пищу в течение 30-40 минут до исследования.
- Детям в возрасте от 1 до 5 лет не принимать пищу в течение 2-3 часов до исследования.
Аминокислоты - это сложные органические вещества, главная функция которых состоит в том, что они являются строительным материалом для синтеза белка в организме. В настоящее время известно несколько сотен химических формул различных аминокислот, но только 20 из них способны участвовать в образовании протеинов. Существует важнейшее деление аминокислот на две группы: заменимые (способные синтезироваться в организме) и незаменимые (могут поступать только в составе пищи). В группу заменимых аминокислот входят аланин, аспарагин, аспаргиновая кислота, глицин, глютамин, глютаминовая кислота, пролин, серин, тирозин, цистеин. К незаменимым аминокислотам у взрослых относятся валин, изолейцин, лейцин, лизин, метионин, треонин, триптофан, фенилаланин, а у детей также аргинин и гистидин.
L-карнитин, или левокарнитин, представляет собой вещество, подобное витаминам группы В, синтезируется в организме и является необходимым для осуществления многих жизненно важных метаболических процессов.
Ацилкарнитины являются органическими веществами, производными карнитина и жирных кислот, являются участниками сложнейших биохимических реакций клеточного метаболизма.
Данный комплекс позволяет оценить количественное содержание наиболее значимых аминокислот и ацилкарнитинов.
Аланин - аминокислота, которая состоит из двух подвидов: альфа (является частью различных белков) и бета (присутствует в составе многих биологически активных веществ, например пантотеновой кислоты). Важнейшим свойством аланина является способность его к превращению в глюкозу в печени (один из путей синтеза глюкозы в организме).
Аргинин - аминокислота, имеющая специфическую функцию в виде участия в синтезе оксида азота NO, который обладает возможностями влияния стенку сосудов. Это позволяет контролировать процессы, в первую очередь, сердечно-сосудистой системы, иммунных и противовоспалительных реакций, дезинтоксикации и регенерации и др.
Валин является основным структурным компонентом белков мышечной и нервной тканей, играя при этом важнейшую роль для скелетной мускулатуры, центральной и вегетативной нервной системы, также принимает участие в работе печени.
Глицин - наиболее известен в составе лекарственного препарата, так как обладает тормозящим действием на нейроны, вызывая успокоительный эффект, а также оказывая нейропротективное, нейрометаболическое, антиоксидантное воздействие в нервной системе.
Лейцин и изолейцин принимают участие во всех видах обменных и энергетических процессов, поддерживают структуру мышц, глюкозу в крови, обеспечивают выносливость и восстановление после физических нагрузок.
Метионин известен как достаточно сильный антиоксидант, является составной некоторых гормонов и других биологически активных веществ. Имеет важное свойство накапливаться в измененных опухолевым процессом тканях, поэтому используется в лучевых методах исследования.
Пролин - аминокислота, необходимая для синтеза коллагена, поэтому она наиболее важна для поддержания тонуса кожи, мышечной ткани, прочности и эластичности хрящевой ткани, а также сосудистой стенки, что способствует профилактике атеросклероза.
Тирозин играет роль в работе мозга (внимание, память, настроение, реакция на стресс и т. д.), щитовидной железы и гипофиза.
Фенилаланин незаменим для работы центральной нервной системы (концентрация внимания, память, ясность мышления, снижение тревожности), также участвует в синтезе гормона мелатонина, регулирующего цикл сна и бодрствования.
Орнитин является промежуточным продуктом в синтезе мочевины, следовательно, участвует в выведении продуктов обмена, также способен превращаться в некоторые другие аминокислоты.
Цитруллин также участвует в цикле мочевины и является субстратом для синтеза аргинина.
L-карнитин поступает из пищи и синтезируется в организме с участием аминокислот метионина и лизина, ряда ферментов, витаминов и микроэлементов. Основная его функция заключается в участии в реакциях энергетического обмена. Также L-карнитин участвует в процессах укрепления костей и мышц, расщепления жировой ткани, снижения глюкозы крови, препятствует накоплению токсинов, что защищает клетки и ткани от их повреждающего воздействия.
В состав комплекса также входит определение содержания достаточно большого количества ацилкарнитинов. Ацилкарнитины представляют собой эфиры карнитина и жирных кислот и подразделяются на короткоцепочечные (С2-С5), среднецепочечные (С6-С12) и длинноцепочечные (С14-С18) в зависимости от длины углеродной цепи присоединенной кислоты. Химические названия этих соединений происходят от латинского обозначения цифр по количеству атомов углерода жирной кислоты, присоединенной к карнитину, например деканоилкарнитин (10 атомов углерода). Ацилкарнитины являются промежуточными веществами в сложных окислительно-восстановительных реакциях, протекающих в митохондриях и приводящих в итоге к синтезу АТФ - основного источника энергии для жизнеобеспечения каждой клетки и всего организма в целом.
Данное комплексное исследование направлено на диагностику различных нарушений метаболизма (обменных процессов) аминокислот или органических жирных кислот (для этого исследуется содержание ацилкарнитинов). Обменные патологии могут быть врожденными (обусловленными генетическими нарушениями) или приобретенными (связаны с нарушением синтеза в организме или усвоения из продуктов питания, разрушением данных соединений в организме или неправильной утилизацией и т. д.). Заболевания, связанные с нарушением обмена аминокислот, объединяются в общее название - аминоацидопатии. Среди врожденных аминоацидопатий наиболее значимыми и часто встречающимися являются фенилкетонурия, алкаптонурия, гомоцистинурия, цитруллинемия, тирозинемия и др. Приобретенные нарушения аминокислотного обмена, как правило, связаны с различными другими заболеваниями, к примеру с сахарным диабетом, онкологическими новообразованиями, хроническими воспалительными или инфекционными процессами ЖКТ, почек, нарушением питания. Ацилкарнитины являются участниками обмена жирных и органических кислот, следовательно, отклонение от нормы их концентрации указывает на нарушения в данных видах обмена, которые имеют свои нозологические формы или синдромы.
Комплексное определение концентрации аминокислот и ацилкарнитинов доступно с помощью использования метода высокоэффективной жидкостной хроматографии с тандемной масс-спектрометрией (ВЭЖХ/МС). В настоящее время данный вид исследования нашел широкое применение для проведения скрининговой диагностики, включающей большое количество показателей, сходных между собой. На первом этапе происходит качественный анализ - разделение изучаемых веществ по их физико-химическим свойствам. Затем, на втором этапе, оцениваются количественные характеристики каждой аминокислоты и ацилкарнитина, результаты которых отражаются в мкмоль/л и сравниваются с диапазоном референсных значений. ВЭЖХ/МС на сегодняшний день является одним из самых точных методов лабораторной диагностики с анализом большого количества показателей одновременно, обладает высокой чувствительностью и специфичностью и выполняется в достаточно короткие сроки, что также имеет значение при некоторых тяжелых формах обменных нарушений.
Кроме патологических процессов и заболеваний, связанных с обменом аминокислот и ацилкарнитинов, следует отметить, что данные вещества широко применяются в спортивном питании. Также в настоящее время популярны системы вегетарианского питания, исключающие поступления в организм белков животного происхождения, а значит, и некоторых незаменимых аминокислот. Комплексное исследование аминокислотного профиля может быть полезно и для данных категорий в целях оценки влияния режима питания на обменные процессы в организме.
Для чего используется исследование?
- Диагностика врожденных (наследственных) и приобретенных заболеваний, связанных с нарушением обмена аминокислот, жирных и органических кислот - при возникновении их клинических симптомов или при отягощенном семейном анамнезе по наличию аминоацидопатий и нарушений метаболизма жирных кислот.
- Дифференциальная диагностика причин патологии азотистого обмена, увеличения в крови содержания аммиака и нарушения его выведения из организма.
- Определение пищевого статуса (особенно у вегетарианцев и при спортивном режиме питания).
- Контроль эффективности терапии при подтвержденном диагнозе обменных нарушений.
- Контроль соблюдения рекомендаций по питанию.
- При подозрении на нарушение метаболизма аминокислот и жирных кислот у детей, проявлениями которых могут быть нарушения работы ЖКТ (рвота, диарея), нарушение психомоторного и психоречевого развития, наличие специфического запаха и окраски пеленок (белья), нарушения кислотно-щелочного равновесия (метаболический ацидоз).
- Скрининг новорождённых, имеющих отягощенный семейный анамнез по обменным нарушениям.
- При нарушении утилизации аммиака и увеличения его концентрации в крови (гипераммониемия).
- Обследование лиц, придерживающихся принципов спортивного питания с употреблением в пищу протеинов или вегетарианства.
- Необходимость контроля соблюдения рекомендаций по питанию или применения лекарственных препаратов.
Референсные значения, мкмоль/л
L-карнитин, свободный: 9.00 - 52.00
Аланин (ALA): 239.00 - 345.00
Аргинин (ARG): 53.00 - 71.00
Ацетилкарнитин (C2): 3.00 - 42.00
Бутирилкарнитин (С4): 0.050 - 1.000
Валин (VAL): 80.00 - 199.00
Гексадеценоилкарнитин (C16:1): 0.070 - 0.510
Гексаноилкарнитин (C6): 0.110 - 0.350
Глицин (GLY): 178.00 - 513.00
Декадиеноноилкарнитин (C10:2): 0.010 - 0.050
Деканоилкарнитин (C10): 0.020 - 0.240
Деценоилкарнитин (C10:1): 0.030 - 1.110
Додеканоилкарнитин (Лауроил, C12): 0.000 - 0.360
Додеценоилкарнитин (C12:1): 0.020 - 0.040
Изовалерилкарнитин (C5): 0.040 - 0.610
Лейцин+Изолейцин (XLE): 70.00 - 145.00
Линолеилкарнитин (C18:2): 0.060 - 1.520
Метионин (MET): 15.00 - 37.00
Миристоилкарнитин (C14): 0.080 - 0.520
Миристолеилкарнитин (C14:1): 0.010 - 0.250
Октадеканоилкарнитин (Стеароил, C18): 0.300 - 2.300
Октадеценоилкарнитин (Олеил, C18:1): 0.700 - 3.100
Октаноилкарнитин (C8): 0.010 - 0.360
Октеноилкартинин (C8:1): 0.010 - 0.330
Орнитин (ORN): 39.00 - 61.00
Пальмитоилкарнитин (C16): 0.250 - 9.700
Пролин (PRO): 110.00 - 417.00
Пропионилкарнитин (C3): 0.210 - 4.700
Тетрадекадиеноилкарнитин (C14:2): 0.000 - 0.110
Тирозин (TYR): 33.00 - 146.00
Фенилаланин (PHE): 45.00 - 93.00
Цитруллин (CIT): 10.00 - 43.00
Референсные значения зависят от особенностей питания, особенностей клинических и лабораторных данных. Интерпретация результатов не может быть проведена только по данному анализу, осуществляется врачом на основании данных всех методов обследования.
Отклонение от нормы концентрации каждой конкретной аминокислоты или ацилкарнитина может подразумевать под собой отдельную патологию, требующую детальной диагностики. Например, при повышении уровня фенилаланина подозревают фенилкетонурию, тирозина - тирозинемию, цитруллина, глутамина - цитруллинемию и т. д. Также это указывает на нарушение в ферментативной системе, участвующей в данных обменных процессах. Аналогично происходит интерпретация концентрации ацилкарнитинов, например, повышение уровня пропионилкарнитина (C3) характерно для пропионовой ацидурии, метилмалоновой ацидурии, недостаточности витамина В12, недостаточности кобаламина C, D или F, что опять же требует комплексного подхода к дифференциальной диагностике.
Алгоритм метаболизма

автор: А. Ю. Барановский, д. м. н., профессор, заведующий кафедрой гастроэнтерологии и диетологии Северо-Западного государственного медицинского университета им. И. И. Мечникова, врач высшей категории
Решение организационных вопросов питания у лиц старших возрастов, разработка и назначение индивидуализированных рационов рационального, профилактического и лечебного питания в существенной степени зависит от правильной оценки врачом нутриционного статуса пожилого человека, особенностей состояния обменных процессов. Именно поэтому профессионально грамотный клиницист, участвующий в решении проблем лечебно-профилактического питания у лиц пожилого и старческого возраста, должен быть достаточно хорошо ориентирован в области основ клинической биохимии и физиологии питания стареющего организма.
Белковый обмен
Белки — сложные азотсодержащие биополимеры, мономерами которых служат аминокислоты (органические соединения, содержащие карбоксильные и аминные группы). Их биологическая роль многообразна. Белки выполняют в организме пластические, каталитические, гормональные, транспортные и другие функции, а также обеспечивают специфичность. Значение белкового компонента питания заключается прежде всего в том, что он служит источником аминокислот.
Аминокислоты делятся на эссенциальные и неэссенциальные в зависимости от того, возможно ли их образование в организме из предшественников. К незаменимым аминокислотам относятся гистидин, лейцин, изолейцин, лизин, метионин, фенилаланин, триптофан и валин, а также цистеин и тирозин, синтезируемые соответственно из метионина и фенилаланина. Девять заменимых аминокислот (аланин, аргинин, аспарагиновая и глутамовая кислоты, глутамин, глицин, пролин и серин) могут отсутствовать в рационе, так как способны образовываться из других веществ. В организме также существуют аминокислоты, которые продуцируются путем модификации боковых цепей вышеперечисленных (например, компонент коллагена — гидроксипролин — и сократительных белков мышц — 3-метилгистидин).
Большинство аминокислот имеют изомеры (D- и L-формы), из которых только L-формы входят в состав белков человеческого организма. D-формы могут участвовать в метаболизме, превращаясь в L-формы, однако утилизируются гораздо менее эффективно.
Взаимоотношение аминокислот
По химическому строению аминокислоты делятся на двухосновные, двухкислотные и нейтральные с алифатическими и ароматическими боковыми цепями, что имеет большое значение для их транспорта, поскольку каждый класс аминокислот обладает специфическими переносчиками. Аминокислоты с аналогичным строением обычно вступают в сложные, часто конкурентные взаимоотношения.
Так, ароматические аминокислоты (фенилаланин, тирозин и триптофан) близкородственны между собой. Хотя фенилаланин является незаменимой, а тирозин — синтезируемой из него заменимой аминокислотой, наличие тирозина в рационе как будто бы «сберегает» фенилаланин. Если фенилаланина недостаточно или его метаболизм нарушен (например, при дефиците витамина С) — тирозин становится незаменимой аминокислотой. Подобные взаимоотношения характерны и для серосодержащих аминокислот: незаменимой — метионина — и образующегося из него цистеина.
Триптофан в ходе превращений, для которых необходим витамин В 6 (пиридоксин), включается в структуру НАД и НАДФ, то есть дублирует роль ниацина. Приблизительно половина обычной потребности в ниацине удовлетворяется за счет триптофана: 1 мг ниацина пищи эквивалентен 60 мг триптофана. Поэтому состояние пеллагры может развиваться не только при недостатке витамина РР в рационе, но и при нехватке триптофана или нарушении его обмена, в том числе вследствие дефицита пиридоксина.
Аминокислоты также делятся на глюкогенные и кетогенные, в зависимости от того, могут ли они при определенных условиях становиться предшественниками глюкозы или кетоновых тел (см. табл. 1).
Таблица 1. Классификация аминокислот
| Виды | Эссенциальные аминокислоты | Неэссенциальные аминокислоты |
| Алифатические | Валин (Г), лейцин (К), изолейцин (Г, К) | Глицин (Г), аланин (Г) |
| Двухосновные | Лизин (К), гистидин (Г, К)* | Аргинин (Г)* |
| Ароматические | Фенилаланин (Г, К), триптофан (Г, К) | Тирозин (Г, К)** |
| Оксиаминокислоты | Треонин (Г, К) | Серин (Г) |
| Серосодержащие | Метионин (Г, К) | Цистеин (Г)** |
| Дикарбоновые и их амиды | Глутамовая кислота (Г), глутамин (Г), аспарагиновая кислота (Г), аспарагин (Г) | |
| Иминокислоты | Пролин (Г) |
Обозначения: Г — глюкогенные, К — кетогенные аминокислоты; * — гистидин незаменим у детей до года; ** — условно-незаменимые аминокислоты (могут синтезироваться из фенилаланина и метионина).
Необходимые азотсодержащие соединения
Поступление азотсодержащих веществ с пищей происходит в основном за счет белка и в менее значимых количествах — свободных аминокислот и других соединений. В животной пище основное количество азота содержится в виде белка. В продуктах растительного происхождения большая часть азота представлена небелковыми соединениями, также в них содержится множество аминокислот, которые не встречаются в организме человека и зачастую не могут метаболизироваться им.
Синтез пуриновых оснований
Человек не нуждается в поступлении с пищей нуклеиновых кислот. Пуриновые и пиримидиновые основания синтезируются в печени из аминокислот, а избыток этих оснований, поступивших с пищей, выводится в виде мочевой кислоты.
В синтезе пиримидиновых колец принимает участие витамин B 12 , для образования пуриновых структур необходима фолиевая кислота. Именно поэтому дефицит этих нутриентов отражается прежде всего на органе с высоким уровнем пролиферации, где идет наиболее интенсивный синтез нуклеиновых кислот, — на кроветворной ткани.
Прием белка
Обычный (но не оптимальный) ежедневный прием белка у среднестатистического человека составляет приблизительно 100 г. К ним присоединяется примерно 70 г белка, секретируемого в полость желудочно-кишечного тракта. Из этого количества абсорбируется около 160 г. Самим организмом в сутки синтезируется в среднем 240-250 г белка. Такая разница между поступлением и эндогенным преобразованием свидетельствует об активности процессов обратного восстановления исходного сложного химического соединения из «осколков», образовавшихся при его метаболизме (ресинтеза белков из аминокислот, а аминокислот из аммиака и «углеродных скелетов» аминокислот).
Азотное равновесие
Для здорового человека характерно состояние азотного равновесия, когда потери белка (с мочой, калом, эпидермисом и т. п.) соответствуют его количеству, поступившему с пищей. При преобладании катаболических процессов возникает отрицательный азотный баланс, который характерен для низкого потребления азотсодержащих веществ (низкобелковых рационов, голодания, нарушения абсорбции белка) и многих патологических процессов, вызывающих интенсификацию распада (опухолей, ожоговой болезни и т. п.). При доминировании синтетических процессов количество вводимого азота преобладает над его выведением, и возникает положительный азотный баланс, характерный для детей, беременных женщин и реконвалесцентов после тяжелых заболеваний.
После прохождения энтерального барьера белки поступают в кровь в виде свободных аминокислот. Следует отметить, что клетки слизистой оболочки желудочно-кишечного тракта могут метаболизировать некоторые аминокислоты (в том числе глутамовую кислоту и аспарагиновую кислоту в аланин). Способность энтероцитов видоизменять эти аминокислоты, возможно, позволяет избежать токсического эффекта при их избыточном введении.
Аминокислоты, как поступившие в кровь при переваривании белка, так и синтезированные в клетках, в крови образуют постоянно обновляющийся свободный пул аминокислот, который составляет около 100 г.
Путь белка
75 % аминокислот, находящихся в системной циркуляции, представлены аминокислотами с ветвящимися цепями (лейцином, изолейцином и валином). Из мышечной ткани в кровоток выделяются аланин, который является основным предшественником синтеза глюкозы, и глутамин. Многие свободные аминокислоты подвергаются трансформации в печени. Часть свободного пула инкорпорируется в белки организма и при их катаболизме вновь поступает в кровоток. Другие непосредственно подвергаются катаболическим реакциям. Некоторые свободные аминокислоты используются для синтеза новых азотсодержащих соединений (пурина, креатинина, адреналина) и в дальнейшем деградируют, не возвращаясь в свободный пул, в специфичные продукты распада.
Роль печени
Постоянство содержания различных аминокислот в крови обеспечивает печень. Она утилизирует примерно ⅓ всех аминокислот, поступающих в организм, что позволяет предотвратить скачки в их концентрации в зависимости от питания.
Первостепенная роль печени в азотном и других видах обмена обеспечивается ее анатомическим расположением — продукты переваривания попадают по воротной вене непосредственно в этот орган. Кроме того, печень непосредственно связана с экскреторной системой — билиарным трактом, что позволяет выводить некоторые соединения в составе желчи. Гепатоциты — единственные клетки, обладающие полным набором ферментов, участвующих в аминокислотном обмене. Здесь выполняются все основные процессы азотного метаболизма: распад аминокислот для выработки энергии и обеспечения глюконеогенеза, образование заменимых аминокислот и нуклеиновых кислот, обезвреживание аммиака и других конечных продуктов. Печень является основным местом деградации большинства незаменимых аминокислот (за исключением аминокислот с ветвящимися цепями).
Инсулиновый ответ
Синтез азотсодержащих соединений (белка и нуклеиновых кислот) в печени весьма чувствителен к поступлению их предшественников из пищи. После каждого приема пищи наступает период повышенного внутрипеченочного синтеза белков, в том числе альбумина. Аналогичное усиление синтетических процессов происходит и в мышцах. Эти реакции связаны прежде всего с действием инсулина, который секретируется в ответ на введение аминокислот и/или глюкозы.
Некоторые аминокислоты (аргинин и аминокислоты с ветвящимися цепями) усиливают продукцию инсулина в большей степени, чем остальные. Другие (аспарагин, глицин, серин, цистеин) стимулируют секрецию глюкагона, который усиливает утилизацию аминокислот печенью и воздействует на ферменты глюконеогенеза и аминокислотного катаболизма. Благодаря этим механизмам происходит снижение уровня аминокислот в крови после поступления их с пищей. Действие инсулина наиболее выражено для аминокислот, содержащихся в кровотоке в свободном виде (аминокислот с ветвящимися цепями), и малозначимо для тех, которые транспортируются в связанном виде (триптофана). Обратное инсулину влияние на белковый метаболизм оказывают глюкокортикостероиды.
Аминокислоты на «экспорт»
Печень обладает повышенной скоростью синтеза и распада белков по сравнению с другими тканями организма (кроме поджелудочной железы). Это позволяет ей синтезировать «на экспорт», а также быстро обеспечивать лабильный резерв аминокислот в период недостаточного питания за счет распада собственных белков.
Особенность внутрипеченочного белкового синтеза заключается в том, что он усиливается под действием гормонов, которые в других тканях производят катаболический эффект. Так, при голодании белки мышц, для обеспечения организма энергией, подвергаются распаду, а в печени одновременно усиливается синтез белков, являющихся ферментами глюконеогенеза и мочевинообразования.
Избыток белка и голодание
Прием пищи, содержащей избыток белка, приводит к интенсификации синтеза в печени и в мышцах, образованию избыточных количеств альбумина и деградации излишка аминокислот до предшественников глюкозы и липидов. Глюкоза и триглицериды утилизируются как горючее или депонируются, а альбумин становится временным хранилищем аминокислот и средством их транспортировки в периферические ткани.
При голодании уровень альбумина прогрессивно снижается, а при последующей нормализации поступления белка медленно восстанавливается. Поэтому хотя альбумин и является показателем белковой недостаточности, он низкочувствителен и не реагирует оперативно на изменения в питании.
7 из 10 эссенциальных аминокислот деградируют в печени — либо образуя мочевину, либо впоследствии используясь в глюконеогенезе. Мочевина преимущественно выделяется с мочой, но часть ее поступает в просвет кишечника, где подвергается уреазному воздействию микрофлоры. Аминокислоты с ветвящимися цепями катаболизируются в основном в почках, мышцах и головном мозге.
Роль мышц
Мышцы синтезируют ежедневно 75 г белка. У среднего человека они содержат 40 % от всего белка организма. Хотя белковый метаболизм происходит здесь несколько медленнее, чем в других тканях, мышечный белок представляет собой самый большой эндогенный аминокислотный резерв, который при голодании может использоваться для глюконеогенеза.
Мышцы являются основной мишенью воздействия инсулина: здесь под его влиянием усиливается поступление аминокислот, увеличивается синтез мышечного белка и снижается распад.
В процессе превращений в мышцах образуются аланин и глутамин, их условно можно считать транспортными формами азота. Аланин непосредственно из мышц попадает в печень, а глутамин вначале поступает в кишечник, где частично превращается в аланин. Поскольку в печени из аланина происходит синтез глюкозы, частично обеспечивающий мышцу энергией, получающийся круго- оборот получил название глюкозо- аланинового цикла.
К азотсодержащим веществам мышц также относятся высокоэнергетичный креатин-фосфат и продукт его деградации креатинин. Экскреция креатинина обычно рассматривается как мера мышечной массы. Однако это соединение может поступать в организм с высокобелковой пищей и влиять на результаты исследования содержания его в моче. Продукт распада миофибриллярных белков — 3-метилгистидин — экскретируется с мочой в течение короткого времени и является достаточно точным показателем скорости распада в мышцах — при мышечном истощении скорость его выхода пропорционально снижается.
Механизм голодания
В отсутствие пищи синтез альбумина и мышечного белка замедляется, но продолжается деградация аминокислот. Поэтому на начальном этапе голодания мышцы теряют аминокислоты, которые идут на энергетические нужды. В дальнейшем организм адаптируется к отсутствию новых поступлений аминокислот (снижается потребность в зависящем от белка глюконеогенезе за счет использования энергетического потенциала кетоновых тел) и потеря белка мускулатуры уменьшается.
Хотите больше информации по вопросам диетологии?
Приобретите информационно-практический журнал «Практическая диетология» в электронном или печатном формате! 6 , который является кофактором ферментов трансаминирования, обеспечивающих синтез заменимых и первый этап катаболизма всех аминокислот. Поэтому повышенный уровень потребления белка требует адекватного повышения количества пиридоксина.
Современные рекомендации по обеспечению пожилых людей и стариков основными питательными веществами, в первую очередь белками, свидетельствуют о целесообразном некотором снижении суточного количества белковых продуктов в пищевом рационе до 0,75-0,8 г/кг веса. Это связано с тем, что интенсивность основных физиологических функций с каждым десятилетием жизни человека после 50 лет снижается почти на 10 % (Rogers J., Jensen G., 2004), потребность белка уменьшается за счет инволюции синтетических и пластических процессов и ферментообразования, продукции гормонов, ряда биологически активных веществ, обеспечения мышечной деятельности и т. д.
Рекомендуемые нормы потребления для белка с учетом приведенных выше показателей составляют 55-62 г/сут (для мужчины весом 77 кг в возрасте 60-70 лет) и 45-52 г/сут (для женщины весом 65 кг в возрасте 60-70 лет) по выводам IV Американского национального исследования по оценке здоровья и питания (2006).
Вместе с тем установлено, что при сохранении физической активности пожилых людей (профессиональной физической нагрузки, занятий физкультурой, работы на дачном участке и т. п.) для поддержания азотного равновесия организма требуется повышение белкового обеспечения пожилого человека в количестве 1-1,25 г/кг в день. Эта же квота пищевого белка полностью обеспечит потребности пожилого человека, находящегося в состоянии стресса, болезни или ранения (Lowenthal D. T., 1990).
Рис. 1. Влияние пищевых веществ на развитие болезней избыточного питания (по А. А. Покровскому)
Дефицит белка = старение
Важно отметить, что организм пожилого человека очень чувствителен как к дефициту экзогенно поступающих белков, так и к их избытку. В условиях белкового дефицита прогрессирующе развиваются процессы дистрофии и атрофии клеточных структур, в первую очередь мышечной ткани, слизистых оболочек (желудочно-кишечного тракта, дыхательной системы и др.), паренхиматозных органов (поджелудочной железы, печени, эндокринных желез и др.), структур иммунной системы. Белковый дефицит питания активизирует процессы старения организма.
Механизмы патологического действия на организм пожилого и старого человека пищевой белковой перегрузки связаны в первую очередь с белковой «агрессией» печени и связанной с этим несостоятельностью ферментных систем, неполной деполимеризацией всех фракций белка, накоплением в крови токсических продуктов незавершенных окислительно-восстановительных реакций и т. д.
Белковая перегрузка
Интоксикационный процесс метаболического генеза при избыточном белковом питании пожилых и старых людей многократно усиливается по причине развития процессов гнилостной кишечной диспепсии в условиях относительной ферментной недостаточности желудка, поджелудочной железы, тонкой кишки и развития синдромов мальдигестии и мальабсорбции, а также кишечного дисбиоза (Барановский А. Ю., Кондрашина Э. А., 2008).
Белковая пищевая перегрузка в рамках интоксикационного синдрома способствует перевозбуждению центральной нервной системы, иногда — состояниям, близким к неврозам. При этом наблюдается повышенный расход витаминов в организме с формированием витаминной недостаточности.
При длительном высокобелковом питании вначале наблюдается компенсаторное усиление, а затем угнетение секреторной функции желудка и поджелудочной железы, повышается риск развития таких заболеваний, как подагра, мочекаменная болезнь.
В следующем выпуске журнала «Практическая диетология» мы продолжим рассказ о геронтологических особенностях основных видов обмена веществ пациентов пожилого и старческого возраста — углеводном и жировом обмене.
Читайте также:
- Нарушения кислотно-основного баланса
- Врожденная эритропоэтическая порфирия (болезнь Гюнтера)
- Тазовая диафрагма женщин. Забрюшинное простанство женщин.
- Физиология сердечно-сосудистой системы и лимфообращения (физиология сердца и системы кровообращения)
- Размеры и линии таза, тазобедренного сустава в норме
