Причины персистирования инфекции в легких.
Добавил пользователь Евгений Кузнецов Обновлено: 31.01.2026
Кашель характерен почти для всех легочных заболеваний. По нашим наблюдениям, около трети пациентов, страдающих заболеваниями респираторной системы и обращающихся за помощью в специализированные амбулаторные клиники, жалуются на хронический персистирующий кашель (ХПК).
Исследования, выполненные в разных странах, свидетельствуют о значительном росте ХПК среди курящих мужчин [1, 2, 4-6]. R. Irwin et al. 1 провели проспективное исследование причин ХПК. В результате были выявлены несколько заболеваний, для которых характерен хронический кашель. Из числа обследованных у 54% выявлен синдром постназального затека (postnasal drip syndrom), y 28% - гастроэзофагеальный рефлюкс, y 7% - хронический бронхит, у 31% - бронхиальная гиперреактивность, у 12% - другие причины кашля, почти у 1% причину установить не удалось. При этом почти у четверти обследованных имелось 2 причины кашля, а у 3% - 3 причины.
Среди некурящих пациентов всех возрастов 93,6% случаев хронического кашля обусловлены тремя заболеваниями [7]:
1) синдром постназального затека;
2) бронхиальная астма;
3) гастроэзофагеальный рефлюкс.
В первую очередь необходимо классифицировать кашель на острый и хронический. Разделение между этими категориями не совсем четкое, однако принято считать, что кашель продолжительностью до 3 нед является острым, а продолжительностью более 3 нед - хроническим.
В клинической практике часто приходится классифицировать кашель в зависимости от причинного фактора. Большое диагностическое значение имеет информация о времени возникновения кашля, его продуктивности, а также сопутствующих симптомах.
В связи с тем что кашель вызывается воздействием различных термических, химических и физических раздражителей, R. Irwin et al. [3] предложили искать причину проявляющегося кашлем заболевания по локализации кашлевых рецепторов.
Выделяют два типа кашлевых рецепторов. Ирритантные рецепторы расположены в дыхательных путях проксимально и возбуждаются под действием экзогенных раздражителей (механических, химических, термических). Волокна расположены дистально и возбуждаются под влиянием эндогенных раздражителей (медиаторов воспаления).
Кроме рецепторов, дуга кашлевого рефлекса включает в себя афферентные и эфферентные нервы, кашлевой центр и дыхательные мышцы [9]. Импульс идет по дуге кашлевого рефлекса через афферентные волокна к центру кашля, расположенному в продолговатом мозге, а затем через эфферентные (моторные) волокна - к мышцам-эффекторам.
Таким образом, кашель - это физиологический защитный механизм, предохраняющий дыхательные пути от воздействия вредных факторов. Локализация кашлевых рецепторов: носовая полость; придаточные пазухи носа; гортань; голосовые связки; глотка; наружный слуховой проход; евстахиева труба; трахея и ее бифуркация; места деления бронхов (бронхиальные шпоры); плевра; перикард; диафрагма; дистальная часть пищевода; желудок.
Диагностика кашля различается в зависимости от его продолжительности.
В диагностике острого кашля основная роль принадлежит сбору анамнеза, осмотру больного и лабораторно-клиническим методам. Диагностика хронического кашля зависит от уже проведенного обследования и выставленного диагноза (например, рак легкого). Если же причина заболевания остается неясной, симптом хронического персистирующего кашля выступает как самостоятельное заболевание [4].
Причинами хронического персистирующего кашля могут быть следующие заболевания.
Это такие заболевания, как синусит, фарингит, ринопатия. Ринопатия (NENAR, non-eosinophil non-allergic rhinopathia) представляет собой заболевание, которое далеко не у всех пациентов вызывает симптом хронического кашля, однако у большинства из них кашель сохраняется до тех пор, пока не будет полностью санирована носоглотка. Для врача общего профиля это особенно важно, так как такие пациенты нуждаются в консультации оториноларинголога. Полипы носовой полости и особенно придаточных пазух также могут быть причиной хронического кашля.
При кашлевом варианте БА наряду с кашлем наблюдаются симптомы гиперчувствительности бронхиального дерева, а одышка и удушье отсутствуют. Этот вариант БА невозможно диагностировать с помощью обычной спирометрии, так как отсутствует бронхообструкция. В диагностике используют бронхопровокационный тест для выявления бронхиальной гиперреактивности.
Пациенты с ХПК обычно предъявляют жалобы на изжогу после приема пищи. Повышенная кислотность в нижнем отделе пищевода - предпосылка для проявления хронического кашля. Для диагностики гастроэзофагеального рефлюкса наиболее целесообразно использовать 24-часовую рH-метрию. Если при рН-метрии подтверждается гастроэзофагеальный рефлюкс как причина хронического кашля, для терапии можно применять прокинетики и блокаторы протонной помпы, например омепразол.
По классификации ВОЗ, хронический бронхит - это заболевание, при котором на протяжении 2 лет не менее 3 мес в году больного беспокоит кашель с мокротой при отсутствии специфических причинных заболеваний, таких как бронхоэктазы, БА или туберкулез.
Бронхоэктатическая болезнь также сопровождается кашлем с выделением мокроты. Диагноз бронхоэктазии можно поставить с помощью компьютерной томографии или бронхографии.
Несмотря на интенсивную диагностику у 2-20% всех обследованных больных причину ХПК выявить не удается. По нашим наблюдениям, в этой категории больных в 2 раза больше женщин, чем мужчин. Возможная причина этому - повышенный кашлевой рефлекс. Кашель же психогенного характера встречается сравнительно редко, в основном у детей.
В редких случаях пролапс задней стенки трахеи и крупных бронхов в результате бронхомаляции даже при обычном дыхании сопровождается кашлем.
Больные с различными неврогенными расстройствами страдают хроническим кашлем, причиной которого является нарушение глотательного рефлекса.
В основе хронического кашля могут лежать заболевания, для которых кашель не столь характерен, например заболевания сердца, артериальная гипертония и т.д. Необходимо учитывать побочное действие ряда лекарств, например ингибиторов ангиотензинпревращающего фермента, бета-блокаторов. Возможно, эти препараты усиливают кашлевой рефлекс в результате повышения чувствительности бронхов.
1. С помощью алгоритма диагностики ХПК можно экономично использовать средства, выделенные на диагностику заболевания.
2. Кашель, сопровождающийся повышением уровня IgE в крови, может быть обусловлен кашлевым вариантом БА или аллергической ринопатией.
3. Больные с ринопатией нуждаются в первую очередь в обследовании оториноларинголога.
4. Серологические исследования на вирусы и бактерии могут выявить причину хронического кашля (например, коклюш).
5. Если причину ХПК не удается установить, необходимо провести бронхоскопию.
6. Эзофагоскопии и рентгенологического исследования пищевода недостаточно для постановки диагноза рефлюкс-эзофагита, необходимо проведение 24-часовой рH-метрии.
7. Диагностику ХПК следует проводить настойчиво, принимая во внимание многообразие возможных причин и не ограничиваясь возможностями данного стационара.
1. Irwin R.S. et al. // Thorax. 1999. V. 46. P. 479.
2. Irwin R.S. et al. // Am. Rev. Respir. Dis. 1990. V. 141. P. 640.
3. Irwin R.S. et al. // Arch. Intern. Med. 1977. V. 137. P. 1186.
4. Kordos P. // Pneumonologie. 1995. V. 49. P. 2.
5. Kordos P., Gebhardt T. // Pneumonologie. 1996. V. 50. P. 427.
6. Kordos P. // Pneumonologie. 2000. V. 53. P. 110.
7. Palombini B.C. et al. // Chest. 1999. V. 116. P. 279.
8. Чучалин А.Г. Хронические обструктивные болезни легких. М., 1998. C. 11.
9. Чучалин А.Г., Абросимов В.Н. Кашель. Рязань, 2000. C. 5-9.
10. Vozehova S. // Cesk Zdrav. 1989. V. 37. P. 437. У некурящих пациентов более 90% случаев хронического кашля обусловлены тремя заболеваниями: синдромом постназального затека; бронхиальной астмой; гастроэзофагеальным рефлюксом.
Хронический персистирующий кашель.
Анатолий Михайлович Резников, профессор, руководитель частной клиники бронхолегочных и аллергических заболеваний, Оберхаузен (Германия).
Ярослав Владимирович Марченков, научный сотрудник НИИ пульмонологии МЗ РФ, Москва
Динамика активности персистирующих инфекций
На основании собственных многолетних данных произведен ретроспективный анализ особенностей динамики активной репликации персистирующих инфекций у детей. В статье описано, как изменяются показатели активной репликации геномов облигатных внутриклеточных пар
Based on our own multi-year data, a retrospective analysis of the dynamics of active replication of persistent infections in children was made. The article describes how the indicators of active replication genomes of obligate intracellular parasites and herpesviruses vary with age and seasonal changes.
Персистирующие инфекции могут являться причиной целого ряда заболеваний. Некоторые из них характеризуются тяжелым клиническим течением, особенно в раннем возрасте. В России, к сожалению, сохраняется высокий уровень детской инфекционной заболеваемости [1]. Известно, что в основном передача инфекции осуществляется в первые годы жизни человека, иногда — внутриутробно. Так, заражение герпес-вирусами человека 1-2, а также 4-6 типов в большинстве случаев реализуется в возрасте до двух лет. Источником инфекции чаще всего является ближайшее окружение ребенка, которое в первые два года его жизни представлено членами семьи и/или обслуживающим персоналом (няни, воспитатели и пр.). За последние пять лет увеличилось число детей в возрасте до одного года, умерших от генерализованных вирусных инфекций [2]. При этом, по данным литературы, у детей маркеры активной персистирующей инфекции выявляют чаще, чем у взрослых [3]. Одним из факторов, обусловливающих высокий уровень репликации инфекционных агентов, является незрелость иммунной системы в раннем возрасте [4]. Несмотря на обилие научных работ, посвященных проблеме персистирующих инфекций, вопрос особенностей динамики их активности остается открытым.
Объект и материалы исследования
Предметом анализа явились данные, полученные при обследовании детей и подростков, находившихся на стационарном лечении в клинике Московского НИИ педиатрии и детской хирургии (в последние годы — Обособленное структурное подразделение Научно-исследовательский клинический институт педиатрии им. акад. Ю. Е. Вельтищева ФГБОУ ВО РНИМУ им. Н. И. Пирогова) Минздрава РФ, и их родителей.
Проанализированы результаты обследования 1079 пациентов, из которых 1064 (98,6%) составили дети и подростки в возрасте от 2 месяцев до 17 лет и 15 (1,4%) взрослых в возрасте от 23 до 52 лет.
У каждого пациента одновременно исследовали от одного до трех образцов различных биологических материалов, всего 2051 образец. Из них осадков мочи — 877 (42,8%); буккальных соскобов — 104 (5,1%); объединенного материала, включающего осадок мочи и буккальный соскоб, — 901 (43,9%); крови — 169 (8,2%) (табл. 1).
Методы исследования
ДНК персистирующих инфекций в исследованных материалах выявляли посредством полимеразной цепной реакции, при постановке которой использовали полные наборы реактивов (kits) для лабораторной диагностики in vitro производства «ВСМ», «Диасан» и «Гентех», г. Москва, Россия. Использовали моноспецифические наборы, укомплектованные нелиофилизированными супермиксами, готовыми к употреблению, замороженными и хранившимися при температуре от -25 до -28 °С. По нашим данным, использование именно таких наборов позволяет достичь наиболее качественных результатов.
Оценивали активность репликации следующих микроорганизмов: Chlamydia trachomatis, Mycoplasma hominis, Ureaplasma urealyticum, цитомегаловирус, вирус Эпштейна-Барр, вирус простого герпеса 1-2 типов.
Среди пациентов девочки и женщины составили 56,7% от числа обследованных, мальчики и мужчины — 43,3%.
Возрастная характеристика пациентов отражена в табл. 2: возраст большинства пациентов составил от двух до 16 лет.
При определении периодов активной репликации персистирующих инфекций в зависимости от возраста фрагмент исследования включал данные, полученные при обследовании 876 пациентов.
Основным критерием отбора явилось одновременное исследование в материале не менее 3 инфекций (герпес-вирусов 4-6 типов и/или облигатных внутриклеточных паразитов). У каждого больного, соответственно, исследовали 3 или 6 инфекций. Такой подход позволил снизить избирательность выборки по той или иной инфекции.
Результаты исследования и их обсуждение
Выявлены следующие закономерности (рис. 1):
Отчетливая закономерность показана для цитомегаловируса: частота выявления ДНК в образцах стабильно снижается до 0 у обследованных взрослых, что можно рассматривать как доказательство зависимости активной репликации цитомегаловируса именно от зрелости иммунной системы (рис. 2).
Аналогичные, хотя и не столь четко выраженные изменения частоты активной репликации в зависимости от возраста можно проследить и для вирусов Эпштейна-Барр и вируса простого герпеса 1-2 типов.
Для ответа на вопрос, существуют ли сезонные изменения активности персистирующих инфекций, мы проанализировали частоту положительных проб в течение двух полных лет; был обследован 871 пациент.
Диаграмма отражает закономерности изменения количества положительных проб Chlamydia trachomatis, Mycoplasma hominis и Ureaplasma urealyticum в течение года (рис. 3).
Вопреки ожиданиям, наибольшая активность Chlamydia trachomatis приходится на период с апреля по июнь. Отмечаются существенные колебания показателя в первом полугодии с максимумом в июне и минимумом в марте и стабильно низкие показатели во втором полугодии.
Частота выявления ДНК Ureaplasma urealyticum крайне нестабильна с декабря по июнь, а в июле резко уменьшается и сохраняется на относительно низком уровне до ноября. В декабре значение показателя возрастает, достигая максимума. Таким образом, общим для исследованных внутриклеточных паразитов является нестабильность и более высокие значения показателя в первом полугодии (для Ureaplasma urealyticum — с декабря по июнь) и, напротив, относительно низкое и стабильное число положительных проб во втором полугодии. Не исключено, что снижение и стабилизация показателя в период с июля по декабрь вызвана улучшением метаболизма, а значит, и адаптивного иммунитета во второй половине лета и осенью.
Для персистирующих герпес-вирусов какой-либо четкой сезонной закономерности не выявлено, однако частота выявления ДНК вируса простого герпеса 1-2 типов стабильно повышается, в мае достигая максимума, а затем снижается к концу года до минимального значения (рис. 4).
Выводы
Проведенное нами исследование позволило сделать следующие выводы:
При исследовании сезонной активности всех облигатных внутриклеточных паразитов выявлена ее существенная вариативность в первом полугодии с максимумом в июне и относительное снижение и стабилизация во втором полугодии.
Литература
- Мазанкова Л. Н., Захарова И. Н. // Рос. вест. перинат. и педиатрии. 2010. № 5. С. 8-11.
- Лобзин Ю. В. Проблемы детских инфекций на современном этапе // Инфекционные болезни. 2009. № 2. С. 7-12.
- Учайкин В. Ф., Нисевич Н. И., Шамшева О. В. Инфекционные болезни и вакцинопрофилактика у детей. М.: ГЭОТАР-медиа. 2006. 688 с.
- Щеплягина Л. А., Круглова И. В. Возрастные особенности иммунитета у детей // РМЖ. № 23, 2009, с. 1564.
Е. И. Шабельникова 1 , кандидат медицинских наук
В. С. Сухоруков, доктор медицинских наук, профессор
Е. А. Ружицкая, кандидат медицинских наук
А. В. Семенов, кандидат медицинских наук
М. В. Кушнарева, доктор медицинских наук, профессор
ФГБОУ ВО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
Проблемы антибактериальной терапии при инфекциях нижних дыхательных путей
Какие назначения необходимы при подозрении на инфекцию нижних дыхательных путей? Какие патогенные факторы играют существенную роль? Как вести больных? Респираторные заболевания являются частой причиной обращения к врачу в Великобритании,
Какие назначения необходимы при подозрении на инфекцию нижних дыхательных путей?
Какие патогенные факторы играют существенную роль?
Как вести больных?
Респираторные заболевания являются частой причиной обращения к врачу в Великобритании, причем в большинстве случаев они относятся к инфекционным [1]. Трем четвертям пациентов, обращающихся с признаками острого заболевания нижних дыхательных путей, врач общей практики назначает антибиотики, хотя лишь в немногих случаях удается выделить возбудителя и антибиотики или вообще не влияют, или мало влияют на естественный ход заболевания [2,3].
Назначая антибиотики, врач руководствуется ожиданиями пациента и старается действовать согласно определенной терапевтической стратегии, хотя зачастую, выписывая рецепт, чувствует, что при этом состоянии антибиотики будут неэффективны [4,5].
Причины, по которым пациент первый раз приходит на прием к своему врачу и затем повторно обращается за консультацией, довольно сложны и часто никак не соотносятся с течением болезни. Как правило, они обусловлены обеспокоенностью своим здоровьем или давлением со стороны друзей, семьи и сотрудников.
При необходимости назначить антибиотик для лечения инфекции нижних дыхательных путей обычно выбирают амоксициллин. Пациенты, повторно обращающиеся к врачу, скорее всего, получат другой антибиотик, например эритромицин или новейшее средство из группы макролидов, хинолонов или пероральный цефалоспорин [3,6].
Проведенные нами недавно исследования показали, что повторное обращение пациентов с инфекциями нижних дыхательных путей, уже получивших назначения на первичном приеме, никак не связано с антибиотикотерапией. Только у 4% таких больных сохранялась бактериальная инфекция и ни у одного из них не было устойчивости к амоксициллину [7]. Повторно приходить на прием побуждают пациентов немедицинские факторы, такие как привычка обращаться к врачу.
Таблица 1. Почему пациенты повторно обращаются к врачу при острой инфекции нижних дыхательных путей
- Пациент неверно представляет себе естественное течение болезни
- Пациент продолжает беспокоиться по поводу симптомов болезни
- Пациенту нравится ходить на прием к врачу
- По настоянию членов семьи, друзей, сотрудников
- У пациента появились соображения, касающиеся важности симптомов
- Инфекция хронизируется или к ней присоединяется другая инфекция
- Проявляется серьезное основное заболевание
При повторном обращении по поводу респираторного заболевания врач общей практики прежде всего должен попытаться установить причину такого обращения (табл. 1). Вполне возможно, что оно вызвано необоснованными ожиданиями пациента, и наилучшим средством здесь было бы объяснение нормальных сроков выздоровления от простуды. Или же есть какое-то основное заболевание, не распознанное на первичной консультации, например астма, недолеченное хроническое обструктивное легочное заболевание, рак или бронхоэктазы.
В том случае если врач считает, что причина в продолжающейся инфекции, необходимо определить возможного возбудителя и выбрать соответствующий антибиотик (табл. 2). Ниже мы обсудим некоторые сложные случаи, которые необходимо иметь в виду [8,9]. Однако нужно помнить, что наиболее распространенными возбудителями остаются Streptоcoccus pneumoniae и респираторные вирусы, а сложные случаи составляют скорее исключение, чем правило в ежедневной общей практике.
Пенициллин-резистентный Streptococcus pneumoniae. Хотя число случаев развития лекарственной устойчивости неуклонно возрастает и представляет серьезную проблему для целого ряда европейских стран, в Англии антибиотикорезистентность пока не считается причиной неудачного лечения инфекций дыхательных путей. Нужно убеждать врачей общей практики проводить пневмококковую вакцинацию населения, входящего в группу риска, а антибиотики назначать строго по показаниям и в адекватной дозе.
Амоксициллин-резистентный Haemophilus influenzae. Haemophilus influenza (Hi) является частой бактериальной причиной обострения хронических обструктивых заболеваний легких (ХОЗЛ), а также вызывает персистирующий бронхит у здоровых взрослых людей. Некоторые антибиотики, такие как эритромицин и цефалоспорины первого поколения, недостаточно эффективны в отношении Hi. Наличие b-лактамазы объясняет отсутствие реакции на амоксициллин. Такие штаммы называются амоксициллин-резистентными Hi (АRHi).
Таблица 2. Возможная причина отсутствия цикла терапии острой инфекции нижних отделов дыхательных путей, назначенной на первом приеме*
Заболеваемость, обусловленная АRHi, растет и составляет сегодня в Великобритании 10-25% общего числа респираторных заболеваний в зависимости от региона. В других странах, таких как Испания, Португалия и некоторые районы Франции, уровень лекарственной устойчивости гораздо выше — это нужно иметь в виду в тех случаях, когда пациент мог заразиться зарубежом.
Об этом возбудителе следует помнить, если у пациента с ХОЗЛ после лечения часто повторяющимися курсами амоксициллина сохраняются симптомы заболевания и гнойная мокрота. В данном случае целесообразным будет недельный курс хинолона или коамоксиклава. От назначения ципрофлоксацина следует воздержаться, если пациент принимает теофиллин.
Moraxella catarrhalis. Некоторым название этого микроорганизма может показаться незнакомым, поскольку раньше его относили к роду Neisseria вида Branhamella.
Это грамотрицательный диплококк, входящий в нормальную микрофлору молодых и пожилых людей. Вслед за Haemophilus influenza и Streptococcus pneumoniae он является третьей по распространенности причиной обострения ХОЗЛ и часто поражает пациентов с тяжелыми хроническими легочными заболеваниями или раком легких.
Обнаружение этого микроорганизма служит показателем тяжести процесса. Сообщалось о недавнем наблюдении 42 случаев пневмонии, вызванной M. catarrhalis, когда около половины пациентов погибло от основного заболевания в течение трех месяцев после обнаружения инфекции.
Важно и то обстоятельство, что практически все штаммы сегодня являются b-лактамазопродуцирующими и соответственно амоксициллинорезистентными. Имеется предположение, что b-лактамаза, продуцируемая M. Catarrhalis, обеспечивает устойчивость к амоксициллину в норме чувствительных респираторных возбудителей, таких как S. pneumoniae и H. influenzae. Проводимая терапия не отличается от той, которая применяется в случаях АРHi (см. выше).
Pseudomonas aeruginosa. Об этом возбудителе нужно помнить в связи с возможностью развития бронхоэктазов и кистозной болезни. Стоит один раз заразиться Pseudomonas aeruginosa, и рецидивы могут следовать один за одним. В настоящее время единственным эффективным пероральным средством является ципрофлоксацин, но к нему быстро развивается устойчивость, и пациентов приходится госпитализировать для проведения внутривенной антибиотикотерапии и физиотерапии.
Другие бактериальные возбудители. Изредка выделяют грамотрицательную кишечную палочку, или Staphylococcus aureus. Эти возбудители чаще связаны с больничными пневмониями, но иногда обнаруживаются у пациентов, недавно выписавшихся из больницы.
Под атипичными обычно подразумеваются инфекции, вызываемые Mycoplasma pneumoniae, Chlamydia psittaci, Chlamydia pneumoniae, Coxiella burnetti и Legionella pneumophila. Лихорадка Q, возбудителем которой служит Coxiella burnetti, встречается редко (как правило, в сельской местности), поэтому не будет упоминаться в дальнейшем. Все атипичные инфекции трудно поддаются распознаванию на ранних стадиях; серологические исследования, проведенные как в острый период, так и в период реконвалесценции, редко дают положительный ответ и не представляют клинической ценности.
Ни один из возбудителей атипичных инфекций не поддается воздействию b-лактамных антибиотиков, что объясняет отсутствие эффекта от назначения амоксициллина.
Mycoplasma pneumoniae. Эпидемия, вызванная этим возбудителем, случается каждые три-четыре года, и в такой период может составлять значительную часть всех респираторных заболеваний.
Обычно она охватывает школьников, студентов и людей среднего возраста; маленькие дети и старики страдают редко.
В отличие от бактериальных инфекций, заболевание начинается постепенно, через 10-14 дней после заражения, проявляясь сухим кашлем или выделением скудной чистой мокроты. Общее недомогание и повышение температуры тела обычно умеренные, при исследовании грудной клетки обнаруживаются незначительные изменения. Иногда такие проявления, как сыпь, буллезный мирингит, а также выявление холодовых агглютининов помогают поставить диагноз.
Микоплазменную инфекцию следует заподозрить, если взрослый человек, до этого не жаловавшийся на здоровье, при отсутствии серьезных патологических симптомов и признаков интоксикации не поддается лечению амоксициллином. В этом случае имеет смысл попробовать назначить антибиотик из группы макролидов; альтернативный подход — тетрациклины. Кашель, как правило, медленно поддается лечению.
Хламидии. Большинствo врачей общей практики время от времени сталкиваются со случаями пситаккоза, вызванного длительным контактом с какой-нибудь любимой домашней птичкой. В последние годы установлено, что наиболее распространенным возбудителем инфекций дыхательных путей является Chlamydia pneumoniae, передающаяся от человека к человеку [10]. Эта инфекция проявляется такими же стертыми симптомами, как и микоплазменная, среди которых выделяются кашель и фарингит. Но, в противоположность микоплазменной инфекции, данное заболевание поражает и пожилых людей, часто вследствие реинфекции.
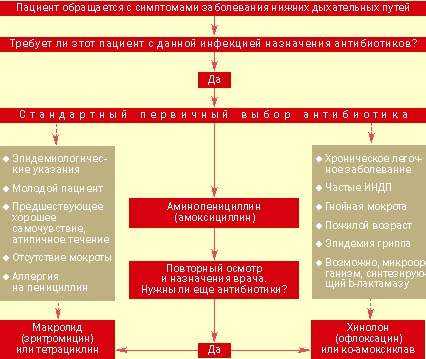 |
| Рисунок 2. Тактика ведения больного с выраженными клиническими показаниями для назначения антибиотиков при остром заболевании нижних дыхательных путей |
В некоторых исследованиях обнаружена связь между Chlamydia pneumoniaе и болезнями коронарных артерий и бронхиальной астмой, возможно обусловленная наличием хламидиального антигена, прикрепляющегося к эндотелию и эпителию. Рекомендуемое лечение — антибиотик из группы макролидов или тетрациклинов.
Legionella pneumophila. Болезнь легионеров все еще находится в центре внимания. Легионелла — редкий возбудитель пневмонии, развивающейся в местах большого скопления людей. Похоже, что легионелла не вызывает такие менее тяжелые заболевания дыхательной системы, как бронхит или инфекции верхних дыхательных путей. Состояние пациентов с болезнью легионеров достаточно тяжелое; обычно им требуется лечение в условиях стационара.
Известна связь этого заболевания с зараженными легионеллами источниками воды, поэтому упоминание пациента о заграничной поездке, пребывании в отеле или больнице, ванне джакузи помогает врачу общей практики правильно поставить диагноз. Нередко встречаются такие осложнения, как дыхательная недостаточность и энцефалит, поэтому все больные, даже в сомнительных случаях, должны быть направлены на госпитальное обследование.
- Практические советы по ведению больных с инфекциями дыхательных путей
Назначение антибиотиков. Подход к ведению больных с острыми инфекциями нижних дыхательных путей представлен на рис. 2. Ключевым моментом является принятие решения о назначении или неназначении антибиотиков. Большинство врачей общей практики считают необходимым применение антибиотиков при серьезных системных нарушениях, постоянном выделении гнойной мокроты, появлении местных признаков поражения легких и отягощенности предшествующими заболеваниями. Если уже решено использовать этот вид лечения, выбор нужного препарата не представляет особого труда.
| Рисунок 3. Пациентам, входящим в группу риска, необходимо провести пневмококковую вакцинацию |
В большинстве случаев назначается амоксициллин. Согласно последним рекомендациям, доза амоксициллина принята равной 500 мг (а не 250 мг, как было раньше), чтобы снизить частоту развития резистентности пневмококков. Однако эта проблема лучше разрешается путем уменьшения общего количества назначений антибиотиков при инфекциях нижних дыхательных путей.
Врач общей практики не должен рекомендовать больному прием антибиотиков просто потому, что это самый легкий способ, или в случае, когда нет четких клинических показаний для их назначения. Проблемы резистентности возбудителей инфекций дыхательных путей решаются при назначении антибиотиков, обусловленном строгими показаниями. Снабжение пациентов простыми информационными листками значительно снижает необходимость повторных консультаций.
Литература
1. Office of Population Censuses and Surveys. Morbidity statistics from general practice: foutrh national study 1992. London: HMSO, 1995 (Series MB5;3).
2. Orr P. H., Scherer K., Macdonald A., Moffatt M. E. Randomosed placebo controlled trials of antibiotics for acute bronchitis: a critical review of the literature. J Fam Pract 1993; 36:507-512.
3. Macfarlane J. T., Holmes W. F., Macfarlane R. M., Lewis S. Contemporary use of antibiotics in 1089 adults presenting with acute lower respiratory tract illness in general practice in the UK: implications for developing managment guidelines. Respiratory Medicine, 1997; 91:427-434.
4. Holmes W. F., Macfarlane J. T., Macfarlane R. M., Lewis S. The influence of antibiotics and other factors on reconsultation for acute lower respiratory tract illness in primary care. Br J Gen Pract (in press).
5. Macfarlane J. T., Holmes W. F., Macfarlane R. M. Acutr lower respiratory tract illness in general practice; a study of the view on 787 patients and their influence on antibiotic prescribing. BMJ, 1997; 315:1211-1214.
6. Macfarlane J. T, Colville A., Guion A., Macfarlane R. M., Rose D. H. Prospective study of aetiology and outcome of adult lower respiratory tract infection in the community. Lancet, 1993; 341:511-514.
7. Macfarlane J., Prewett J., Rose D., Gard P., Guion A., Cunnigham R., Myint S. A prospective, case control study of the aetiology of community acquired lower respiratory tract infections in adult who felt to improve with initial antibiotics. BMJ, 1997; 315:1206-1210.
8. Venkatesan P., Innes J. A. Antibiotic resistance in common acute respiratory pathogenes. Thorax, 1995; 50:481-483.
9. Anon. Lower respiratory tract infections. MeReC Bulletin 1994; 5:5-8.
10. Torres A., ElEbiary M. Relevance of Chlamydia pneumoniae in community acquired respiratory infections. Eur Respir J, 1993; 6:7-8.
11. Macfarlane J. T., Holmes W. F., Macfarlane R. Reducing reconsultations for acute lower respiratory tract illness with an information leaflet. Br J Gen Pract, 1997; 47:710-722.
Интерстициальные болезни легких
Интерстициальные болезни легких - группа заболеваний, протекающих с развитием диффузного воспаления стромы легких, главным образом бронхиол и альвеол. Отражением подобных изменений являются лихорадка, общее недомогание, потеря массы тела, непродуктивный кашель, сухие инспираторные хрипы, легочная недостаточность (одышка, тахипноэ), правожелудочковая сердечная недостаточность. Диагноз интерстициальных болезней подтверждается данными рентгенографии и КТ легких, исследования ФВД, биопсии легкого. В качестве лечения назначается стероидная терапия (или цитостатики), бронходилататоры, оксигенотерапия.
МКБ-10
Общие сведения
Интерстициальные болезни легких (ИБЛ) - различные поражения легких, патоморфологической основой которых являются хроническая диффузная воспалительная инфильтрация альвеол, мелких бронхов, легочных капилляров с исходом в фиброз. В число ИБЛ входят 130 заболеваний ясной и неясной этиологии. У пациентов, госпитализируемых в отделения пульмонологии, те или иные интерстициальные болезни легких диагностируются в 10-15% случаев. Преобладающим контингентом больных являются мужчины в возрасте 40-70 лет, в большинстве случаев курящие. Одни заболевания этой группы имеют обратимый характер течения и относительно благоприятный прогноз, другие рано приводят к инвалидизации и даже летальным исходам.
Классификация интерстициальных болезней легких
В настоящее время за основу принята классификация ИБЛ, выработанная в 2002 г. Американским торакальным обществом (ATS) и Европейским респираторным обществом (ERS). Согласно данной классификации выделяют интерстициальные болезни легких:
1. С установленной этиологией:
- лекарственные, лучевые, токсические ИБЛ
- пневмомикозы, ассоциированные с ВИЧ-инфекций
- ИБЛ на фоне коллагенозов (склеродермии, дерматомиозита, ревматоидного артрита, СКВ) и пневмокониозов (асбестоза, силикоза, бериллиоза)
- ИБЛ на фоне инфекций (атипичной пневмонии, диссеминированного туберкулеза легких, пневмоцистной пневмонии и пр.)
- ИБЛ на фоне экзогенного аллергического альвеолита
2. Идиопатические интерстициальные пневмонии:
- неспецифическая, десвамативная, острая, лимфоидная, криптогенная организующаяся;
- идиопатический легочный фиброз
3. Гранулематозные:
- ИБЛ на фоне саркоидоза, гранулематоза Вегенера, гемосидероза легких, экзогенного аллергического альвеолита
4. Ассоциированные с другими заболеваниями:
- патологией печени (хроническим гепатитом, первичным билиарным циррозом печени), кишечника (НЯК, болезнь Крона), ХПН
- наследственными заболеваниями (нейрофиброматозом)
- злокачественными опухолями
- ассоциированные с гистиоцитозом Х, лимфангиолейомиоматозом, легочным протеинозом, первичным амилоидозом легких.
Патоморфологическая классификация интерстициальных болезней легких различает следующие виды интерстициального фиброза: простой, десквамативный, лимфоцитарный, гигантоклеточный, а также облитерирующий бронхиолит с пневмонией.
Причины интерстициальных болезней легких
На сегодняшний день этиологические механизмы большинства ИБЛ остаются невыясненными. Достоверно можно говорить лишь о причинах интерстициальных болезней легких с известной этиологией. В их числе - ингалирование неорганических веществ, органической пыли, паров ртути; прием токсичных лекарственных средств (циклофосфамида, пеницилламина, блеомицина и др.), лучевая терапия.
В основе развития ИБЛ могут лежать рецидивирующие бактериальные, грибковые и вирусные пневмонии, туберкулез органов дыхания, респираторный дистресс-синдром, бронхоальвеолярный рак. Кроме этого, интерстициальные болезни легких могут сопутствовать коллагенозам, болезням крови (гемолитической анемии, тромбоцитопенической пурпуре, хроническому лимфолейкозу), наследственным заболеваниям и др. Самым значимым фактором риска ИБЛ является курение.
В патогенезе интерстициальных болезней легких выделяют острую, хроническую и терминальную стадии. В острую стадию поражение затрагивает легочные капилляры и альвеолярный эпителий, развивается внутриальвеолярный отек. В этот период может иметь место полная обратимость изменений или их прогрессирование. При переходе ИБЛ в хроническое течение отмечаются обширные повреждения легких (распространённый фиброз). В терминальную стадию происходит полное замещение альвеол и капиллярной сети фиброзной тканью с формированием расширенных полостей (легкое в виде «пчелиных сот»).
Симптомы интерстициальных болезней легких
Несмотря на многообразие этиологических форм ИБЛ, их клиническое течение во многом похоже и характеризуется общими и респираторными симптомами. Часто заболевание начинается исподволь, а проявления носят нечеткий, неспецифический характер.
Общая симптоматика может включать лихорадку, недомогание и быструю утомляемость, потерю массы тела. Определяющую роль в клинической картине интерстициальных болезней легких играют признаки дыхательной недостаточности. Наиболее ранним и постоянным симптомом служит одышка: вначале она возникает или усиливается только при нагрузке, затем становится постоянной и прогрессирующей. Одышка обычно носит инспираторный характер и сопровождается свистящими хрипами, что может быть ошибочно принято за бронхиальную астму.
Характерным симптомом ИБЛ является непродуктивный кашель - сухой или со скудной слизистой мокротой. К более поздним признакам ИБЛ относятся цианоз и формирование «пальцев Гиппократа». С большой частотой встречаются деформации грудной клетки. При тяжелых формах развивается легочно-сердечная недостаточность.
У детей интерстициальные болезни легких протекают с постоянным кашлем, стридором, часто сопровождаются формированием бронхоэктазов. Лица старше 70 лет болеют крайне редко, однако в старшем возрасте ИБЛ часто сопровождаются аритмиями, инфарктом миокарда, ОНМК.
Диагностика интерстициальных болезней легких
При осмотре больного пульмонологом обращает внимание тахипноэ, несоответствие выраженности одышки физикальным изменениям в легких. Во время аускультации на вдохе прослушиваются крепитирующие хрипы различной локализации. В крови - умеренный лейкоцитоз и повышение СОЭ; по данным ИФА - отрицательные серологические тесты на наличие Ат к микоплазме, легионеллам, риккетсиям. Проводится анализ газового состава крови и КЩС (артериальная гипоксемия на ранних этапах сменяется гиперкапнией в терминальной стадии).
Большую информационную ценность в диагностики интерстициальных болезней легких представляют рентгенологические методы (рентгенография и КТ легких). На ранних стадиях на рентгено- и томограммах можно увидеть деформацию и усиление легочного рисунка, мелкоочаговые тени, снижение прозрачности легочных полей ( феномен «матового стекла»); в дальнейшем развивается рентгенологическая картина интерстициального фиброза и картина «сотового легкого».
По данным спирометрии чаще обнаруживается рестриктивный тип нарушений легочной вентиляции, снижение легочных объемов. При развитии легочной гипертензии на ЭКГ обнаруживается гипертрофия миокарда правых отделов сердца. Диагностическая бронхоскопия позволяет провести бронхоальвеолярный лаваж; при ИБЛ в промывных вод бронхов преобладают нейтрофилы. Кроме этого, в ходе эндоскопического исследования может быть выполнена трансбронхиальная биопсия легких. Также в отдельных случаях прибегают к открытой или трансторакальной биопсии легочной ткани.
Лечение и прогноз интерстициальных болезней легких
Первым шагом в лечении ИБЛ должен стать отказ от курения, взаимодействия с вредными производственными факторами, токсическими лекарственными препаратами. Вся последующая терапия проводится параллельно с лечением основного заболевания.
В большинстве случаев препаратами первой линии при интерстициальных болезнях легких являются кортикостероиды (преднизолон), которые в течение 1-3 мес. назначаются в высоких дозировках с последующим переходом на поддерживающую дозу. При отсутствии положительной динамики в течение года назначаются цитостатики (циклофосфамид, азатиоприн, хлорамбуцил). Из других фармпрепаратов используются бронходилататоры (внутрь и в виде ингаляций), однако они эффективны только на стадии обратимой бронхиальной обструкции. При артериальной гипоксемии (РаО2
Исходами ИБЛ могут быть улучшение, стабилизация состояния, прогрессирование легочного фиброза, летальный исход, реже - спонтанный регресс изменений (например, при неспецифической интерстициальной пневмонии). Средняя продолжительность жизни пациентов колеблется от 1 года при болезни Хаммана-Рича до 10 и более лет при респираторном бронхиолите. Профилактика интерстициальных болезней легких возможна только в случае известной этиологии.
1. Интерстициальные заболевания легких: точка зрения практического врача/ Петров Д.В., Овсянников Н.В., Капралов Э.А., Капустьян О.В.// Практическая пульмонология. - 2014 - №1.
2. Интерстициальные заболевания легких: вопросы терминологии, классификации и эпидемиологии/ Гаврисюк В.К.
3. Патоморфология интерстициальных болезней легких: Учебно-методическое пособие/ Костылева О.А., Тусупбекова М.М., Ким Н.Б., Косицын Д.Л. - 2012.
Хронические неспецифические заболевания легких ( ХНЗЛ )
Хронические неспецифические заболевания легких - это различные в этиологическом и патоморфологическом отношении болезни дыхательной системы, протекающие с постоянным продуктивным кашлем и диспноэ вследствие преимущественного поражения бронхов или паренхимы. Включают в себя такие нозологически самостоятельные формы, как хронический бронхит, БЭБ, бронхиальную астму, эмфизему легких, пневмосклероз, хроническую пневмонию. ХНЗЛ диагностируются по результатам спирографии, рентгеновского и эндоскопического обследования. Методы лечения ХНЗЛ могут включать фармакотерапию, бронхоскопическую санацию, физиотерапию, ЛФК; при стойких морфологических изменениях - хирургическое лечение.
Группа хронических неспецифических заболеваний легких (ХНЗЛ) объединяет болезни органов дыхания, имеющие различные причины и механизмы развития, но сходные клинические проявления и морфофункциональные нарушения. Показатели заболеваемости ХНЗЛ в регионах России варьируют от 12 до 29 случаев на 1000 населения.
Показатель ХНЗЛ увеличивается с возрастом и достигает своего пика в возрастной группе 40-60 лет. Среди пациентов большинство составляют мужчины. В структуре ХНЗЛ преобладает хронический бронхит (около 60%), бронхиальная астма (~35%), бронхоэктазы (около 4%), на остальные болезни приходится менее 1%.
Причины ХНЗЛ
Основными факторами, определяющими частоту заболеваемости населения хроническими неспецифическими заболеваниями легких, являются высокий уровень загрязненности воздушной среды, профессионально-производственные вредности, острые инфекционные заболевания дыхательных путей, негативные привычки. Более высокие эпидемиологические показатели по ХНЗЛ отмечаются в индустриальных городах, где в атмосферном воздухе регистрируется содержание поллютантов (оксидов азота, диоксида серы, диоксида углерода, пыли, взвешенных частиц и др.), превышающее ПДК в 3-5 раз.
Основной профессиональный контингент среди пациентов с ХНЗЛ составляют лица, подвергающиеся сквознякам, воздействию загазованности, запыленности, раздражающих запахов на рабочем месте. Многочисленные исследования подтверждают связь между частотой развития ХНЗЛ и длительным курением (свыше 10 лет). Преморбидными состояниями для клинически выраженных форм ХНЗЛ выступают частые и затяжные ОРВИ, повторные острые бронхиты и пневмонии, хронические заболевания верхних дыхательных путей, аллергические заболевания, иммунные нарушения.
Патогенез
В основе морфогенеза различных хронических неспецифических заболеваний легких лежит один из трех механизмов: бронхитогенный, пневмониогенный и пневмонитогенный. Бронхитогенный путь развития ХНЗЛ связан с нарушением бронхиальной проходимости и дренажной функции бронхов. По такому механизму развиваются заболевания с обструктивным компонентом: хронический бронхит, БЭБ, бронхиальная астма и эмфизема легких. Пневмониогенный механизм лежит в основе формирования хронической пневмонии и хронического абсцесса легкого, которые являются осложнениями бронхопневмонии или крупозной пневмонии. При этих заболеваниях выражен рестриктивный компонент. Пневмонитогенный путь определяет развитие интерстициальных заболеваний легких.
Исходом любого из названных морфогенетических механизмов ХНЗЛ служит развитие пневмосклероза (пневмофиброза, пневмоцирроза), легочной гипертензии, легочного сердца и сердечно-легочной недостаточности. Хронические неспецифические заболевания легких рассматриваются как фактор риска развития туберкулеза легких, рака легкого.
Классификация
Впервые это понятие "ХНЗЛ" было введено в обращение на международном симпозиуме пульмонологов, состоявшемся в 1959 г. в Лондоне. Тогда в группу ХНЗЛ были включены три нозологии:
Спустя три года на научной конференции в Москве этот список бы дополнен еще тремя заболеваниями:
Специфические поражения легких (туберкулез), профессиональные болезни (пневмокониозы) и бронхопульмональный рак в эту группу включены не были.
В современной пульмонологии вопросы классификации хронических неспецифических заболеваний легких остаются дискуссионными. Так, ряд авторов дополнительно относят к ХНЗЛ интерстициальные болезни легких. Другие возражают, что самостоятельными нозологиями из ХНЗЛ являются лишь хр. бронхит, эмфизема и бронхиальная астма; остальные же (пневмосклероз, хр. пневмония, бронхоэктазы) носят синдромальный характер и должны рассматриваться как осложнения основных, самостоятельных форм. Существование хронической пневмонии также признается не всеми исследователями.
Основные формы ХНЗЛ
Хронический бронхит
Как и другие хронические неспецифические заболевания легких, часто является следствием затяжного течения острого бронхита вирусной этиологии (развившегося на фоне гриппа, кори, аденовирусной или РС-инфекции) или бактериального генеза (вызванного длительной персистенцией в бронхах гемофильной палочки, пневмококка и др.). Может развиваться в результате продолжительного воздействия на воздухоносные пути химических и физических факторов (курения, запыленности воздуха, загрязнения промышленными отходами).
По распространенности может быть локальным или диффузным; по типу воспаления - катаральным или слизисто-гнойным; по наличию/отсутствию бронхиальной обструкции - обструктивным и необструктивным; по характеру морфологических изменений в бронхах - атрофическим, полипозным, деформирующим. Клиническими критериями хронического бронхита служат 2-3 обострения воспалительного процесса в год на протяжении 2-х лет с ежегодной продолжительностью не менее 3-х месяцев. Больных беспокоит постоянный кашель с мокротой. Во время обострений кашель усиливается, мокрота становится гнойной, присоединяется субфебрильная температура, потливость. Исходами и осложнениями хронического бронхита могут становиться хроническая пневмония, ателектаз легкого, эмфизема, пневмофиброз.
Бронхиальная астма
Является второй по частоте формой хронических неспецифических заболеваний легких. Характеризуется гиперреактивностью бронхиального дерева, приводящей к гиперсекреции бронхиальной слизи, отеку и пароксизмальному спазму воздухоносных путей. К основным клиническим типам относятся неатопическая, атопическая, смешанная, аспирин-индуцированная, профессиональная БА.
Клинически БА любого генеза проявляется повторяющимися приступами экспираторной одышки. В их развитии выделяют 3 периода: предвестников, удушья и обратного развития. Предвестниками, сигнализирующими о приближающемся приступе БА, могут служить покашливание, слизистые выделения из носа, явления конъюнктивита, двигательное беспокойство. Во время приступа удушья появляется свистящее дыхание, резкая одышка с удлиненным выдохом, диффузный цианоз, непродуктивный кашель. Больные принимают вынужденное вертикальное положение с приподнятым плечевым поясом. При тяжелом приступе смерть больного может наступить от дыхательной недостаточности. В период обратного развития приступа при кашле начинает отделяться мокрота, уменьшается количество хрипов, дыхание становится свободным, исчезает одышка.
Между приступами состояние больных БА вполне удовлетворительное. При длительном анамнезе хронического неспецифического заболевания легких развивается обструктивная эмфизема, легочное сердце, легочно-сердечная недостаточность.
Хроническая обструктивная эмфизема легких
Представляет собой хроническое неспецифическое заболевание легких, морфологической основой которого выступает стойкое расширение просвета респираторных бронхиол и альвеол в результате хронической обструкции воздухоносных путей на фоне хронического бронхита и облитерирующего бронхиолита. Легкие приобретают повышенную воздушность, становятся перераздутыми, увеличенными в размерах.
Клинические проявления эмфиземы обусловлены резким сокращением площади газообмена и нарушением легочной вентиляции. Симптоматика нарастает постепенно, по мере распространения патологических изменений на большую площадь легочной ткани. Беспокоит прогрессирующая одышка, кашель со скудной слизистой мокротой, похудание. Обращает внимание бочкообразное расширение грудной клетки, синюшность кожи, утолщение ногтевых фаланг пальцев рук по типу барабанных палочек. При эмфиземе часты инфекционные осложнения, легочные кровотечения, пневмоторакс. Причиной смерти становится тяжелая дыхательная недостаточность.
Бронхоэктатическая болезнь
Морфологическим субстратом настоящей формы хронических неспецифических заболеваний легких служат мешковидные, цилиндрические или веретенообразные расширения бронхов. Бронхоэктазы могут носить локальный или диффузный характер, врожденное или приобретенное происхождение. Врожденные бронхоэктазы обусловлены нарушениями развития бронхиального дерева в пренатальном и постнатальном периодах (в результате внутриутробных инфекций, при синдроме Зиверта-Картагенера, муковисцидозе и др.). Приобретенные бронхоэктазы могут формироваться на фоне рецидивирующих бронхопневмоний, хр.бронхита, длительного нахождения инородного тела в бронхах.
Основные респираторные симптомы включают постоянный кашель, выделение желто-зеленой мокроты с запахом, иногда кровохарканье. Обострения протекают по типу обострений хронического гнойного бронхита. Внелегочный симптомокомплекс при бронхоэктатической болезни представлен деформацией пальцев в виде барабанных палочек и ногтей в форме часовых стекол, «теплым» цианозом. Осложнениями хронического неспецифического заболевания легких может стать легочное кровотечение, абсцесс легкого, сердечно-легочная недостаточность, амилоидоз, гнойный менингит, сепсис. Каждое из этих состояний представляет потенциальную опасность для жизни пациента с ХНЗЛ.
Хроническая пневмония
Патоморфологические изменения при хронической пневмонии сочетают воспалительный компонент, карнификацию, хр.бронхит, бронхоэктазы, хронические абсцессы, пневмофиброз, поэтому в настоящее время данное хроническое неспецифическое заболевание легких как самостоятельная нозология признается не всеми авторами. Каждое обострение хр.пневмонии приводит к появлению новых очагов воспаления в легочной ткани и увеличению площади склеротических изменений.
К постоянным симптомам, сопровождающим течение хронической пневмонии, следует отнести кашель с отделением мокроты (слизисто-гнойной в фазе ремиссии и гнойной в фазе обострения) и стойкие хрипы в легких. В остром периоде повышается температура тела, возникают боли в груди в проекции инфильтрата, дыхательная недостаточность. Заболевание может осложняться легочно-сердечной недостаточностью, абсцедированием, эмпиемой плевры, гангреной легких и др.
Пневмосклероз
Хроническое неспецифическое заболевание легких, протекающее с замещением функционирующей паренхимы соединительной тканью, носит название пневмосклероза. Является следствием воспалительно-дистрофических процессов, приводит к сморщиванию, безвоздушности и уплотнению легочной ткани. Часто развивается в исходе хр.бронхита, БЭБ, хр.пневмонии, ХОБЛ, пневмоконикозов, плевритов, фиброзирующего альвеолита, туберкулеза и мн. др. По распространенности изменений различают локальный (очаговый) и диффузный пневмосклероз. По степени выраженности разрастания соединительной ткани выделяют три стадии патологического процесса - пневмофиброз, пневмосклероз, пневмоцирроз.
Проявляется как признаками причинно значимого заболевания, так и признаками дыхательной недостаточности (одышкой, кашлем, синюшным оттенком кожи, «пальцами Гиппократа»). В стадии цирроза легкого резко выражена деформация грудной клетки, отмечается атрофия грудных мышц. Больной ослаблен, быстро устает, теряет в массе. Течение основного заболевания ведет к прогрессированию пневмосклероза, а пневмосклероз утяжеляет основную патологию.
Диагностика
Диагноз различных форм хронических неспецифических заболеваний легких устанавливается пульмонологом с учетом особенностей клинического течения патологии и результатов инструментальной и лабораторной диагностики.
- Лучевая диагностика. Для подтверждения характера морфологических изменений проводится обзорная рентгенография легких, которая при необходимости дополняется линейной томографией или КТ грудной клетки.
- Визуализация бронхов. С целью выявления структурных изменений в бронхиальном дереве выполняется бронхоскопия (при необходимости с забором мокроты или биопсией), бронхография.
- Анализы. При помощи анализа мокроты и смыва с бронхов (микроскопического и микробиологического) можно уточнить активность воспалительного процесса в бронхах и причину его возникновения.
- Спирометрия. Оценить функциональные резервы легких при хронических неспецифических заболеваниях помогает исследование ФВД.
- Кардиодиагностика. Выявить признаки гипертрофии правого желудочка сердца возможно путем электрокардиографии и ЭхоКГ.
Лечение ХНЗЛ
Лечение хронических неспецифических заболеваний легких зависит от этиологических факторов, патогенетических механизмов, степени морфофункциональных изменений, остроты процесса. Однако можно выделить некоторые общие подходы к лечению различных самостоятельных форм ХНЗЛ.
Консервативная терапия
С целью купирования инфекционно-воспалительных процессов в бронхах и легких подбираются противомикробные препараты с учетом чувствительности микрофлоры. Назначаются бронхолитические, отхаркивающие и секретолитические средства. С целью санации бронхиального дерева осуществляется бронхоальвеолярный лаваж. В этом периоде широко используются постуральный дренаж, вибромассаж, СВЧ и УФО на грудную клетку. Во время приступов затруднения дыхания рекомендуются бронходилататоры, оксигенотерапия.
Вне обострения показано диспансерное наблюдение пульмонолога, лечение в санатории, ЛФК, спелеотерапия, аэрофитотерапия, прием растительных адаптогенов и иммуномодуляторов. С десенсибилизирующей и противовоспалительной целью могут назначаться глюкокортикостеродиды. Для адекватного контроля над течением БА подбирается базисная терапия.
Хирургическое лечение
Вопрос о хирургической тактике при хронических неспецифических заболеваниях легких ставится в случае развития стойких локальных морфологических изменений легких или бронхов. Чаще всего прибегают к резекции пораженного участка легкого либо пневмонэктомии. При двухстороннем диффузном пневмосклерозе может быть показана трансплантация легких.
Читайте также:
