Примеры побочных эффектов лучевой терапии с аппликатором меланомы хориоидеи
Добавил пользователь Евгений Кузнецов Обновлено: 22.01.2026
Меланома хориоидеи — это пигментная опухоль злокачественного характера собственной сосудистой оболочки глаза (хориоидеи). Данная опухоль является одной из самых частых внутриглазных новообразований. Меланома хориоидеи является основной причиной смертности и инвалидизации онкобольных с поражением органа зрения. Заболевание может протекать практически бессимптомно, но при этом имеет высокую склонность к метастазированию, поэтому проблема ее выявления на начальных стадиях является крайне актуальной.
Этиологические факторы
Большинство случаев меланомы хориоидеи являются спорадическими, то есть обусловлены теми или иными мутациями клетки-предшественницы меланоцитарного звена, которая может дать начало патологическому опухолевому клону. Кроме того, есть предположение о наследственной причине данного заболевания. Воздействие такого типичного провоцирующего фактора для меланомы кожи, как повышенная инсоляция, для этой опухоли также не исключается.
В группе риска находятся пожилые люди (средний возраст манифестации опухоли — 60 лет). Немного чаще болеют мужчины. Склонны к появлению меланомы хориоидеи обладатели светлой кожи и волос, невусов и веснушек.
Клиническая картина
Жалобы пациентов зависят от размера и локализации меланомы хориоидеи, а также от наличия сопутствующих осложнений, к которым относятся: отслойка сетчатки вторичного характера, появление дегенеративных процессов в сетчатке, помутнение хрусталика.
На первичном приеме у офтальмолога обычно определяется снижение остроты зрения, появление перед глазом слепых участков (скотом), гемианопсий (выпадения половин поля зрения). В случае позднего обращения, больные жалуются на боль в глазу (вторичная глаукома), расширение сети сосудов. Также на склере может определяться пигментное пятно (экстраокулярный рост новообразования).
Стадии развития меланомы хориоидеи
Согласно международной классификации различают 4 стадии развития данной опухоли. Критерии распространенности опухолевого процесса:
- Т1 — размер меланомы 10 мм и менее, толщина — 2,5 мм и менее.
- Т2 — размер новообразования 10-16 мм, наибольшая толщина составляет 2,5-10 мм.
- Т3 — размером 16 мм и/или толщина более 10 мм без распространения за пределы глазного яблока.
- Т4 — наибольший размер опухоли 16 мм и/или толщина более 10 мм с распространением за пределы глазного яблока.
Также выделены 4 клинические стадии меланомы хориоидеи. Для каждой из них характерны определенные симптомы заболевания:
- Для первой, так называемой стадии «спокойного глаза», свойственно отсутствие ярких клинических проявлений и жалоб. Возможно наличие помутнения сетчатки, также могут определяться дефекты поля зрения.
- Вторая стадия характеризуется появлением боли в глазах, воспаления, покраснения глазного яблока, отека век.
- На третьей стадии меланома хориоидеи выходит за границы глазного яблока, формируется экзофтальм, склера теряет целостность.
- Четвертая стадия сопровождается генерализацией процесса. Общее состояние пациента ухудшается. Больные жалуются на сильную боль, снижается масса тела, нарастает интоксикация. Появляются метастазы меланомы внутренних органов: печени, легких, костей. Поражение того или иного органа провоцирует появление соответствующих симптомов. Может выявляться дальнейшее снижение остроты зрения, чувство пелены или тумана перед глазами. Данные проявления вызываются кровотечениями в стекловидное тело, помутнением хрусталика.
Симптомы второй и третьей стадии меланомы хориоидеи ярко выражены при расположении опухоли в центральной или парацентральной части глазного дна. Для периферической локализации новообразования характерно длительное отсутствие субъективных ощущений. В этом случае меланома выявляется либо случайно, либо на стадии распада опухоли и ее вторичных проявлений.
Виды меланомы глаза
Разработана классификация меланомы хориоидеи по морфологическому признаку. В зависимости от клеточной структуры, выделяют следующие типы данной опухоли:
- Веретеноклеточный.
- Эпителиоидный.
- Смешанный (микстмеланома).
- Фасцикулярный.
- Некротический.
Данная классификация имеет определенные недостатки, так как некротическая меланома хориоидеи определяется клинически, а вот определить ее клеточную принадлежность из-за обширного некроза невозможно. Веретенообразный и фасцикулярный тип имеют сходный прогноз. В связи с этим, в настоящее время морфологически принято выделять только 2 типа: веретеноклеточный и эпителиоидный. Смешанная форма занимает промежуточное положение. Ее прогноз зависит от преобладания тех или иных клеток. Наименее благоприятной прогностически считается эпителиоидноклеточная меланома хориоидеи.
Диагностика
Учитывая клинические особенности меланомы хориоидеи, ее диагностика, особенно на начальных этапах, представляет определенные трудности. Помимо анализа жалоб больного и клинико-анамнестических данных, учитываются результаты следующих инструментальных исследований:
- Биомикроскопии.
- Офтальмоскопии.
- Ультразвукового исследования глаза.
- Диафаноскопии и др.
Меланома хориоидеи является новообразованием с высоким риском появления метастазов. Поэтому при обследовании пациента необходимо использовать также методы диагностики метастатических очагов: УЗИ органов брюшной полости и лимфатических узлов, рентгенографию легких, КТ, МРТ.

Способы лечения меланомы хориоидеи
Выделяют органосохраняющие методы лечения данной опухоли и хирургический метод без сохранения глаза. В случаях, когда не удается сохранить глаз, производят энуклеацию — изолированное удаление глазного яблока или экзентерацию — иссечение вместе с глазным яблоком всего содержимого орбитальной полости.
Показания к энуклеации:
- Опухоль значительного размера.
- Распространение меланомы на диск зрительного нерва.
- Полное отсутствие зрительной функции.
- Экстрабульбарный рост опухоли.
- Вторичная глаукома.
После удаления глазного яблока, проводится имплантация внутреннего протеза и последующее наружное протезирование. Эти меры позволяют не только достичь хорошего косметического результата, но и препятствуют деформации лица.
К органосохраняющим методам лечения меланомы хориоидеи относятся:
Лучевая терапия. В зависимости от способа подведения излучения, лучевую терапию при данном заболевании проводят контактным или дистанционным способом. Контактное облучение, или брахитерапия, представляет собой имплантацию радиоактивных элементов вблизи очага меланомы.
Показания к проведению брахитерапии:
- Отсутствие признаков распада.
- Диаметр новообразования до 15 мм.
- Отстояние от диска зрительного нерва не менее 2 диаметров самого диска.
Брахитерапия является самым эффективным методом органосохраняющего лечения при меланоме хориоидеи. Его применение способно снизить вероятность образования метастазов опухоли.

В составе системного лечения, актуально проведение иммунной терапии. Также при оказании помощи больным с меланомой хориоидеи в поздних стадиях учитываются особенности ее метастазирования. Для данной опухоли характерно изолированное поражение печени метастазами. В таких случаях с успехом применяется химиоэмболизация данного органа.
Такой распространенный метод лечения меланомы кожи, как таргетная терапия, при меланоме хориоидеи не применяется, так как при данном виде опухоли отсутствуют специфичные BRAF-мутации.
Профилактика и диспансерное наблюдение
Рекомендовано пожизненное наблюдение за больными, которые получали лечение меланомы хориоидеи. После проведения лучевой терапии и удаления новообразования, офтальмолог должен осматривать пациентов каждые полгода в течение 2 лет, а далее — 1 раз в год. С целью раннего выявления метастазов назначают УЗИ органов брюшной полости и рентгенографию легких 1-2 раза в год.
Прогноз для жизни при меланоме хориоидеи
Продолжительность жизни при данном виде рака зависит от локализации и размера опухоли, возраста пациента, морфологии новообразования, проведенного лечения и других особенностей. Пятилетняя выживаемость на начальных стадиях меланомы хориодиеи после применения органосохраняющих радикальных методов составляет 93%, десятилетняя — 89%. На поздних стадиях, при выявлении метастазов печени медиана выживаемости составляет лишь 4-6 месяцев. Для пациентов с метастатическим поражением других органов годичная выживаемость составляет 76%.
Лечение меланомы: какое место в нем занимают методы лучевой терапии
Когда речь идет о лечении меланомы, большинство представляет кожные новообразования - темного цвета, неправильной формы. Но, во-первых, злокачественная опухоль при меланоме может быть беспигментной, а во-вторых, меланома локализуется не только на коже. Насколько сложной задачей является лечение меланомы, и какое место в нем занимают методы лучевого лечения (радиохирургия и лучевая терапия) - рассказывает сайт МИБС.

Что такое меланома?
Меланома (иногда встречается название “меланобластома”) - злокачественная опухоль из меланоцитов, клеток, вырабатывающих естественный пигмент меланин, поглощающий УФ-лучи для защиты кожи от ионизирующего воздействия солнечного света. Преимущественно, локализуется в коже, однако меланома может возникнуть в любом органе, в состав тканей которого входят меланоциты (слизистые оболочки и ткани глазного яблока).
Факторы, повышающие риск развития меланомы, хорошо изучены:
- загар;
повышение пигментации кожи, вызванное воздействием ультрафиолетового излучения (как солнечного, так и искусственного - в соляриях), - важнейший фактор риска меланомы; его вес в развитии меланомы настолько высок, что солярии запрещены в некоторых странах, а во многих под запретом находится их использование несовершеннолетними - наследственность;
те, у кого в семейной истории есть случаи меланомы, должны максимально внимательно отнестись к пунктам этого списка - фенотип;
чем светлее волосы и кожа у человека, тем выше вероятность меланомы - солнечные ожоги;
особенно перенесенные в детском и подростковом возрасте могут сыграть роковую роль - именно в этих местах чаще всего возникают злокачественные опухоли кожи - перенесенная меланома;
те, кто прошел через лечение меланомы, должны быть намного внимательнее - иммунитета от этого заболевания нет; наоборот, рецидивы меланомы - частое явление - образования на коже;
невусы (родинки или родимые пятна), особенно в количестве более 50 - серьезный повод регулярно проходить обследование у дерматолога и защищать кожу от избытка ультрафиолета; доброкачественное новообразование меланоформный невус (он же: диспластический меланоцитарный невус, синдром атипического невуса) - дает аналогичный повод; - пигментная ксеродерма;
наследственное заболевание, проявляющееся в повышенной чувствительности кожного покрова к ультрафиолету, также требует более внимательного отношению к любым изменениям на коже
Меланома и ее статистика
Но значительный объем данных о природе меланомы обусловлен не простотой визуальной диагностики (которая, как будет показано в следующем разделе, проста не во всех аспектах), а той агрессивностью, которая делает меланому одним из самых смертельных онкологических заболеваний в мире, и самым смертельным видом рака кожи. Согласно последним статистическим исследованиям, меланома кожи (составляет основную часть всех меланом) встречается в семь раз реже, чем другие виды рака кожи, но количество ежегодных смертей от меланомы выше в 2,5 раза.
Заболеваемость меланомой в семь раз меньше, чем другими видами рака кожи, а смертность - в 2,5 раза выше
Высокие статистические показатели объясняют важность, которое имеет лечение меланомы для человечества. В целом же, меланома занимает 19-е место среди других онкологических заболеваний в мире, немного уступая раку яичников, злокачественным опухолям мозга и нервной системы.
Диагностика меланомы
Лечение меланомы, как и любой опухоли, проходит успешнее, если новообразование выявлено на ранней стадии. В теории, ранняя диагностика меланомы кожи - простая задача. Визуальное изменение существующих невусов (частичная потеря пигментации, “рваные” края, асимметрия, выпадение волос и др.) привлекают внимание человека либо его близких. Пациент обращается к врачу-дерматологу или дерматологу-онкологу, где проходит визуальное неинвазивное обследование - дерматоскопию, которая позволяет буквально “заглянуть” в глубокие слои кожи для оценки распространенности опухоли (зачастую, меланома растет вглубь кожи, что означает более неблагоприятный прогноз, чем рост в горизонтальной плоскости). Стандарт современной диагностики меланомы - применение цифрового дерматоскопа, позволяющего получить снимки интересующего участка кожи в электронном виде для последующего наблюдения в динамике, или для получения срочной консультации либо “второго мнения”.
Однако на практике отсутствие должной онконастороженности приводит к игнорированию ранних симптомов меланомы кожи. А коварство заболевания состоит в том, что меланома может начать метастазировать даже при небольшом размере новообразования. Это приводит к тому, что пациент обращается на поздней стадии, когда требуется не только лечение первичной меланомы, но и ее метастазов.
Особенного подхода требует диагностика увеальной (внутриглазной меланомы). Сосудистая оболочка (хориоидея) и сетчатка глаза также содержат меланоциты, вырабатывающие меланин для защиты этих структур от ультрафиолетового излучения, попадающего внутрь глазного яблока. Опухолевое поражение этих структур, независимо от его природы, обычно имеет специфические симптомы (зоны “выпадения” изображения, вспышки, “молнии” и т.д.), которые должны насторожить и привести к квалифицированному офтальмологу, не только способного идентифицировать меланому, но и обладающего необходимым оборудованием для первичной диагностики новообразования, которое позволит начать лечение без промедления.
Наиболее сложная задача - диагностика меланомы слизистых оболочек. Иногда новообразования видны невооруженным глазом (например, меланома слизистой рта, меланома вульвы). Но меланома в скрытых местах (например, слизистой кишечника) может быть выявлена уже после того, как пациент обратится к врачу по поводу метастазов меланомы и будет начат поиск первичной опухоли. К счастью, меланома слизистых оболочек встречается крайне редко. По современным данным ее доля - не более 5% всех случаев меланомы.
Для окончательного подтверждения диагноза “меланома кожи” должна быть проведена биопсия образца ткани опухоли. Чрезвычайная опасно проводить частичный забора препарата, например, методом соскоба, при котором повышается вероятность распространения опухолевых клеток, - на морфологическое исследование следует направлять препарат тканей, иссеченных с определенным запасом по контуру. Лечение меланомы слизистых оболочек и внутриглазной меланомы следует начинать после всестороннего инструментального обследования, чаще всего УЗИ, КТ и МРТ с контрастом.
Диагностика метастазов меланомы
При подтверждении первичного диагноза, перед тем, как начать лечение первичного очага меланомы, необходимо провести диагностику для выявления возможных метастазов опухоли. Именно вторичная меланома намного чаще становится причиной смерти, чем первичное новообразование. Лимфогенные метастазы меланомы появляются в регионарных лимфатических узлах, а распространяемые с кровотоком гематогенные метастазы меланомы чаще всего отмечаются в печени, легких, костях, и головном мозге. Наиболее опасными являются метастазы в головной мозг.
Диагностика метастазов меланомы может включать:
- биопсию сторожевого лимфоузла;
- УЗИ периферических лимфоузлов, органов брюшной полости, малого таза и забрюшинного пространства;
- компьютерную томографию (КТ) органов грудной полости;
- магнитно-резонансную томографию (МРТ) или КТ органов брюшной полости с контрастированием (при локализации первичной меланомы кожи на нижней половине туловища или на нижних конечностях проводится КТ/МРТ органов малого таза с контрастированием);
- КТ/МРТ головного мозга с контрастом;
- уровень лактатдегидрогеназы (ЛДГ) в крови;
- при подтверждении начала метастазирования может быть проведено ПЭТ или ПЭТ-КТ всего тела.
Целесообразность каждого из видов диагностики определяет лечащий врач исходя из обоснованности подозрений наличия и степени метастатического поражения. Полученные результаты являются важной информацией для правильного подбора тактики лечения меланомы.
Лечение меланомы
Тактика лечения разрабатывается исходя из локализации меланомы и распространенности опухолевого процесса.
Лечение меланомы на ранних стадиях
При отсутствии распространения в другие части организма (I-II стадии), меланома кожи подлежит хирургическому иссечению с обязательным морфологическим исследованием удаленного фрагмента тканей. Также может быть проведено удаление сторожевого лимфоузла для морфологической диагностики на предмет распространения меланомы через лимфатическую систему. Без подтверждения распространенности процесса методы лекарственной терапии применяются редко.
Лучевое лечение меланомы
Лечение меланомы кожи и меланомы слизистых оболочек методами лучевой терапии (в т.ч. радиохирургии и протонной терапии) не демонстрирует должного эффекта, поэтому не получило распространения в клинической практике, уступив хирургии. Однако при меланоме глаза (увеальная меланома) которая представлена меланомой сосудистой оболочки (меланома хориоидеи) и меланомой радужной оболочки, высокоточное подведение высоких доз ионизирующего излучения (радиохирургия и протонная терапия) показывает высокие результаты, сравнимые, по эффективности, с удалением (энуклеацией) глазного яблока.
Протонная терапия является более сложным и более дорогим методом, к тому же лечение меланомы глаза протонами требует длительного курса лечения. Поэтому наиболее широко в мировой практике распространена радиохирургия, при которой высокая разовая доза ионизирующего излучения приводит к остановке биологических процессов в клетках опухоли.
Радиохирургия на Гамма-ноже, выполняемая в Онкологической клинике МИБС, позволяет получить органосохраняющее лечение меланомы глаза с соблюдением высоких международных стандартов. При этом стоимость лечения на Гамма-ноже, как правило, не превышает стоимости операции по удалению глазного яблока или пораженных его участков, при этом качество жизни пациента после радиохирургического лечения опухоли глаза - несоразмеримо выше, т.к. сохраняется не только орган (глазное яблоко), но и, в подавляющем большинстве случаев, его функция (зрение).
Лечение метастазов меланомы
Метастатическая меланома требует комплексного подхода к лечению. В зависимости от особенностей конкретного случая, врачи (именно так - в Онкологической клинике МИБС лечение опухолей проводится с привлечением междисциплинарного консилиума врачей различных специальностей) определят тактику лечения из сочетания таких методов, как иммунотерапия, таргетная терапия, химиотерапия, в т.ч. изолированная перфузия конечности (“прокачивание” высокой дозы химиопрепарата через временно “отключенные” от кровеносной системы сосуды руки или ноги при специфически локализованных вторичных меланомах кожи и мягких тканей), хирургия, лучевая терапия, радиохирургия.
Лучевое лечение метастазов меланомы
Принято считать, что лучевые методы в лечении меланомы и ее метастазов не применяются. Действительно, до того, как современные методики высокоточного воздействия высокими дозами ионизирующего излучения стали доступны в России, пациентам выполнялась паллиативная лучевая терапия при множественном поражении головного мозга, поражении костей, мягких тканей и лимфоузлов, а также лучевая терапия на ложе удаленных единичных метастазов.
При этом богатый клинический опыт ведущих мировых онкоцентров, оснащенных радиохирургическими системами Гамма-нож, в число которых входит и Онкологическая клиника МИБС, доказывает эффективность радиохирургии при олигометастатическом поражении головного мозга. Гамма-нож быстро (обычно, за один сеанс) и эффективно разрушает метастазы меланомы, защищая от повреждения здоровые ткани головного мозга. Радиохирургия также может применяться в качестве паллиативного лечения, разрушая наиболее опасные метастазы в головном мозге, в том числе и у пациентов в относительно тяжелом общем состоянии: радиохирургическое вмешательство неинвазивно, бескровно, безболезненно, не требует анестезии. Такой подход способен продлить жизнь пациента, сохраняя ее качество и давая больше шансов на успех системного лечения метастатической меланомы лекарственными препаратами (иммунотерапия, таргетная терапия, химиотерапия). Аналогичным образом радиохирургия на Кибер-ноже, также доступная в Онкологической клинике МИБС, может применяться для “точечного” лечения наиболее опасных метастазов меланомы, локализованных в других частях тела (чаще - в легких и печени).
Предстоит лечение меланомы? Обратитесь в МИБС сейчас, чтобы узнать о всех возможностях, которые предлагает современная медицина в Вашем случае!

Иванов Павел Игоревич
Заведующий отделением нейрорадиологии.
Нейрохирург высшей категории, кандидат медицинских наук.
Действительный член Всемирного Общества пользователей Гамма-Ножа (LGKS).
Действительный член Европейского Общества функциональной и стереотаксической нейрохирургии (ESSFN).
Действительный член Образовательного комитета Международного Общества Стереотаксической Радиохирургии (ISRS) .
Доцент кафедры нейрохирургии Военно-Медицинской Академии им. С.М. Кирова.
Примеры побочных эффектов лучевой терапии с аппликатором меланомы хориоидеи
ФГБУ "НИИ глазных болезней" РАМН, Москва
Кафедра офтальмологии ГБОУ ДПО "Российская медицинская академия последипломного образования"
Выживаемость больных меланомой хориоидеи больших размеров
Журнал: Вестник офтальмологии. 2014;130(4): 39‑44
Стоюхина А.С., Чесалин И.П. Выживаемость больных меланомой хориоидеи больших размеров. Вестник офтальмологии. 2014;130(4):39‑44.
Stoiukhina AS, Chesalin IP. Survival rates for large choroidal melanomas. Vestnik Oftalmologii. 2014;130(4):39‑44. (In Russ.).
В современной онкологии одним из важных критериев оценки эффективности лечения принято считать 5- и 10-летнюю выживаемость больных после проведенного лечения.
Общая 5-летняя выживаемость больных меланомой хориоидеи (МХ) после лечения, по данным литературы, составляет 72% [1]. Следует подчеркнуть, что авторы не приводят сведений о зависимости выживаемости от метода лечения и исходных размеров опухоли. В то же время имеются данные о 79-95% 5-летней [2, 3] и 85% 10-летней [4] выживаемости больных МХ после брахитерапии (БТ).
Что касается энуклеации как метода лечения глаз с МХ, то имеются сведения, указывающие на зависимость смертности в течение 5 лет после энуклеации от исходных размеров опухоли. Так, при малых меланомах она составляет 16%, при опухолях средних размеров - 32%, а при больших МХ достигает 53% [5]. Спустя 15 лет после публикации указанных сведений появились исследования J. Gambrelle и соавт. [6], доказывающие низкую 5-летнюю специфическую выживаемость после первичной энуклеации (всего 31,45%). Все перечисленные данные касаются европейской популяции больных, в которой, как известно, преобладает смешанно-клеточный гистотип меланомы, который следует расценивать как один из неблагоприятных прогностических факторов 8.
В немногочисленной отечественной литературе приведены сравнительные показатели продолжительности жизни больных МХ после локального разрушения опухоли и энуклеации при больших МХ [10, 11]. Но в данных работах отсутствует сравнительная характеристика результативности как органосохранного, так и ликвидационного (энуклеация) лечения с учетом исходных размеров опухоли.
Как известно, при анализе выживаемости больных МХ имеют значение не только клиническая стадия и размеры опухоли, но и ее гистологический, генетический типы и уточненная причина смерти [13].
По данным COMS, 2-, 5- и 10-летний уровень метастазирования МХ составляет 10, 25 и 34% соответственно и только у 0,24% больных метастазы выявляют в момент постановки диагноза [14]. Но каждый 1 мм увеличения толщины меланомы повышает риск метастазирования в течение 10 лет на 5% [15]. Таким образом, исходные размеры опухоли являются определяющими для оценки витального прогноза.
С учетом изложенного возрастает значение метрической классификации меланом хориоидеи.

В настоящее время существуют две наиболее часто используемые метрические классификации МХ. Речь идет о классификациях J. Shields [16] и COMS (Collaborative Ocular Melanoma Study) [17]. Параметры МХ, согласно приведенным классификациям, представлены в табл. 1.
Как следует из табл. 1, в классификации COMS значительно увеличена толщина меланом в группе средних и больших опухолей. Это, естественно, привело к расширению показаний для их органосохранного лечения. Локальное разрушение опухоли (БТ, транспупиллярная термотерапия - ТТТ) начали проводить при проминенции ее более 6 мм [18, 19].
Обоснованием такого подхода к лечению МХ явились сведения о том, что общая и специфическая смертность, а также продолжительность жизни без метастазов достоверно не различаются после энуклеации и органосохранного лечения больших МХ [11, 20, 21].
В связи с изложенным была сформулирована цель настоящего исследования: проанализировать 5-летнюю специфическую выживаемость пациентов с большими МХ (по классификации J. Shields) с учетом проведенного лечения.
Материал и методы
Методом сплошной выборки исследована медицинская документация 103 больных, получивших лечение по поводу больших МХ в различных специализированных офтальмологических центрах Москвы в течение 2002-2007 гг. и находящихся на диспансерном наблюдении в городском офтальмоонкологическом центре при Московской офтальмологической больнице. В исследование включены пациенты с исходной проминенцией опухоли от 5,0 до 10,2 мм, так как при наличии б́ольшей проминенции опухоли органосохранное лечение не проводили. Исходный диаметр основания опухоли варьировал от 7,3 до 20 мм. До начала лечения, по данным проведенного общего обследования, метастазы у всех пациентов отсутствовали.
Органосохранное лечение получили 60 человек. БТ была выполнена 46 пациентам (в 37 случаях однократно), БТ в сочетании с ТТТ - 14 больным (в одном случае с последующей эндорезекцией опухоли). В этой группе у 16 больных была выполнена вторичная энуклеация.
Первичная энуклеация по поводу большой МХ проведена 63 больным.
Протоколы патогистологического исследования, подтверждающие диагноз МХ, изучены во всех 79 случаях.
Статистическая обработка результатов выполнена в программах Microsoft Excel и Statistica 6.0. Для оценки выживаемости использовали метод Каплана-Мейера и двувыборочный анализ по Гехану-Вилкоксону, в котором группирующей переменной являлся тип лечения.
Результаты и обсуждение
В зависимости от проведенного лечения пациенты разделены на две группы. 1-ю группу составили лица, получившие органосохранное лечение (в том числе и те, которым была выполнена вторичная энуклеация), во 2-й группе единственным методом лечения была первичная энуклеация. Характеристика обеих групп представлена в табл. 2.
Как следует из табл. 2, представленные группы по показателям практически не различались и все МХ по проминенции выходили за пределы 6 мм, иными словами, были отнесены к большим опухолям.
В 1-й группе от гематогенного метастазирования умерли 16 (26,67%) больных в среднем через 4,06±1,03 года после начала лечения. Обращает на себя внимание тот факт, что средний исходный диаметр опухоли у этих больных составил 15,37±1,24 мм, что достоверно отличалось (р=0,002) от исходного диаметра у пациентов без метастазов (13,12±0,78 мм). Достоверных различий в исходной проминенции МХ получено не было (6,68±0,64 и 7,06±0,44 мм соответственно). Таким образом, нельзя исключить из факторов риска метастазирования и диаметр опухоли.
У 16 больных этой группы была выполнена вторичная энуклеация в среднем через 2,95±1,44 года после начала лечения. До лечения у этих больных средняя максимальная проминенция опухоли составляла 7,33±1,82 мм, а средний максимальный диаметр - 13,82±1,52 мм. Таким образом, указанные параметры меланомы у этих больных существенно не отличались от исходных размеров опухоли у пациентов, получивших только органосохранное лечение.
Как показывают наши наблюдения, вторичную энуклеацию после органосохранного лечения больших МХ пришлось выполнить у 26,67% больных, основной причиной для энуклеации явился продолженный рост опухоли.
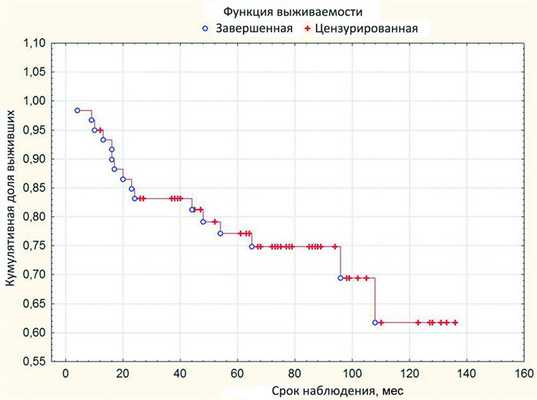
При анализе по Каплану-Мейеру 5-летняя выживаемость без энуклеации составляет 0,7708, стандартная ошибка 0,0563, а 9-летняя - достигает 0,6175 при стандартной ошибке 0,0988 (рис. 1). Рисунок 1. Рис. 1. Выживаемость без энуклеации после проведения органосохранного лечения.
И тем не менее, в наших наблюдениях в среднем через 35 мес энуклеация оказалась необходимой практически у каждого 4-го больного. Полученные данные совпадают с данными литературы о высоком риске энуклеации после проведении БТ с рутением-106 в течение 5 лет наблюдения [2].
Во 2-й группе от гематогенного метастазирования умерли 10 (15,83%) пациентов в среднем через 5,2±1,54 года после энуклеации. Несмотря на то что исходные размеры опухолей у этих больных несколько превышали таковые у больных без метастазов, статистической значимости различий не получено.
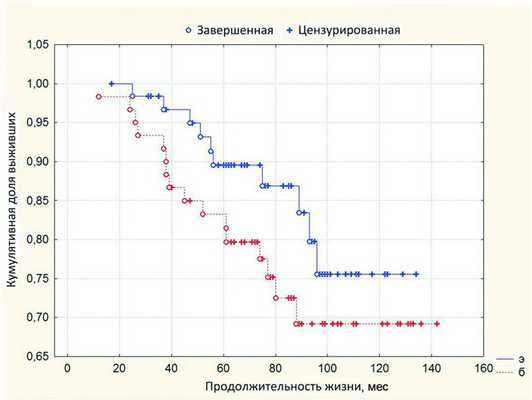
Таким образом, в группе больных, перенесших первичную энуклеацию, витальный прогноз оказался несколько лучше, чем после органосохранного лечения. Тем не менее при проведении двухвыборочного анализа по Геноху-Вилкоксону статистически значимой разницы в выживаемости (р=0,11) у пациентов этих двух групп не получено (рис. 2). Рисунок 2. Рис. 2. Выживаемость после органосохранного лечения (б) и первичной энуклеации (э). Разница продолжительности жизни также оказалась статистически недостоверной (р=0,17).
Как видно из табл. 3 , имеются различия в результатах, полученных в ходе исследований [11, 20], которые можно объяснить разным подходом к формированию групп исследования. К примеру, в работе Т.В. Шириной [20] сравниваются группы больных, получивших только органосохранное лечение, с группой больных, которым была проведена и первичная, и вторичная энуклеация. С нашей точки зрения, это не совсем корректно, так как проведение предшествующего органосохранного лечения также может оказывать влияние на витальный прогноз (техника проведения операции, гистотип опухоли). Кроме того, при исследовании общей выживаемости не учтен возраст больных в анализируемых группах. А между тем хорошо известно, что старший возраст больных - один из факторов риска метастазирования меланомы. В работе А.А. Ярового и соавт. [11] сравниваются показатели метастазирования после органосохранного лечения и первичной энуклеации больших меланом. Случаи вторичной энуклеации не включены в исследование. Хотя доказано, что продолжительность жизни больных с момента выявления метастазов может достигать 62 мес и зависит от общеонкологического лечения [12].
Заключение
Как показали наши исследования, при условии однотипности исходных биометрических показателей опухоли после первичной энуклеации витальный прогноз несколько лучше, чем после органосохранного лечения, даже с учетом старшего возраста больных этой группы.
Следует отметить, что после органосохранного лечения за более короткий промежуток времени (в 1,3 раза) от гематогенного метастазирования умерли в 1,6 раза больше больных, чем после первичной энуклеации, хотя при анализе по Гехану-Вилкоксону подтверждения статистической значимости этих различий не получено.
Таким образом, в каждом конкретном случае большой МХ следует подходить индивидуально и решать вопрос о методе лечения с учетом возраста больных, размеров опухоли и психологического настроя пациентов. Следует учитывать, что даже при отсутствии достоверной разницы выживаемости у пациентов со средними МХ, получивших БТ и перенесших энуклеацию, имеются различия в качестве жизни: у пациентов, перенесших энуклеацию, достоверно ниже частота тревожных состояний, связанных с риском рецидива опухоли [22].
Органосохраняющее лечение увеальной меланомы и других внутриглазных опухолей у взрослых
Безоперационное лечение внутриглазных опухолей является важной частью клинической практики Онкологической клиники МИБС. Да, опухоли глаза, значительная доля которых приходиться на увеальную меланому, - немногочисленны. Но современные методы лечения позволяют, при своевременном обращении, сохранить не только глазное яблоко, но и остроту зрения. Поэтому вопрос информирования о возможностях органосохраняющего лечения - важен для общества. Подробнее - в материале МИБС…

Когда речь идет о лечении внутриглазных опухолей, целесообразно рассматривать его на примере увеальной меланомы, как наиболее часто диагностируемой первичной опухоли органов зрения.
Что такое увеальная меланома?
Увеальная меланома - злокачественное новообразование из клеток меланоцитов, растущее внутри глазного яблока, в одном из его слоев. Женщины более подвержены этому заболеванию, наиболее часто диагноз устанавливается у пациентов старше 50 лет.
От локализации опухоли в глазном яблоке зависит ее название:
- меланома хориоидеи (меланома сосудистой оболочки глаза) - наиболее распространенная внутриглазная опухоль взрослых; составляет до 85% увеальных меланом;
- меланома цилиарного тела - опухоль, расположившаяся в тканях “соединительного звена” между радужкой и сосудистой оболочкой, диагностируется в 10% всех случаев увеальных меланом;
- меланома радужной оболочки - наиболее редкая меланома радужки составляет около 5% всех увеальных меланом.
В связи с тем, что подавляющее большинство увеальных меланом приходится на меланому хориоидеи, целесообразно считать тождественными эти два понятия для упрощения понимания подходов к диагностике и лечению. Также справедливо рассматривать указанные подходы и для лечения других внутриглазных опухолей.
Увеальная меланома: лечение
Вся тяжесть выявления увеальной меланомы ложится на плечи офтальмолога, который по ряду симптомов может не только заподозрить наличие опухоли, но и указать на ее тип, проведя комплексную диагностику. Ключевое значение имеет опыт врачей, выполняющих визуальную (офтальмолог) и инструментальную (радиолог) диагностику, в первую очередь, МРТ - в России регистрируется всего около 1000 случаев опухолей глаза в год и возможность получить консультацию коллег, встречавшихся в своей практике с данным заболеванием, гарантирует более высокое качество медицинской помощи. Для того, чтобы повысить точность диагностики в любом регионе России, МИБС предлагает услугу “второе мнение”, заключающееся в дистанционном направлении имеющихся снимков МРТ, КТ, ПЭТ-КТ на рассмотрение специалистам МИБС с получением письменного заключения.
После того, как диагноз “увеальная меланома” будет подтвержден, пациенту совместно с врачом-офтальмологом предстоит ответить на крайне важный вопрос - какой метод лечения выбрать?
Энуклеация (полное удаление) глазного яблока до конца 70-х годов прошлого века являлась единственным действенным способом, которым проводили лечение меланомы хориоидеи. К сожалению, несмотря на развитие альтернативных методов, и сегодня лечение “меланомы глаза” в пределах офтальмологической клиники, в которую обратится пациент за установлением диагноза, во многих случаях будет означать удаление глазного яблока и сопутствующие ему физическую инвалидность и психологическую травму, значительно снижающие качество жизни. К тому же стоимость пластической реконструкции и индивидуального глазного протезирования после энуклеации, зачастую, превышает стоимость высокотехнологичного лечения, демонстрирующего сравнимую эффективность.
Современная офтальмология использует ряд методов, позволяющих избежать удаления глазного яблока: частичная резекция пораженных тканей органа (например, хирургическое лечение меланомы радужной оболочки глаза является наиболее оптимальным ввиду удобного доступа и возможности ранней визуальной диагностики), разрушение опухоли лазером (лазерная фотокоагуляция), термотерапия, криотерапия и лучевое лечение.
Наиболее сложным, с точки зрения принятия оптимального решения, является выбор в пользу лучевого лечения увеальной меланомы, которое при условии соблюдения современных протоколов, показывает эффективность на уровне хирургии. Если применение брахитерапии (контактного подведения радиоактивных элементов к опухоли) может быть предметом дискуссии об эффективности такого лечения, в особенности, при достижении опухолью значительного размера, то более современная радиохирургия на Гамма-ноже, а тем более, лечение увеальной меланомы протонами, демонстрируют показатели эффективности и безопасности, не уступающие даже хирургическому лечению.
Но, по объективным причинам - необходимо дорогостоящее оборудование, а также точное соблюдение протоколов радиохирургии и протонной терапии, - современное лучевое лечение увеальной меланомы не может быть выполнено в офтальмологической клинике. И выбор в пользу “лучей” будет означать не только передачу пациента в профильную клинику, но и оплату пациентом услуг в другом лечебном учреждении. К сожалению, очень часто финансовый интерес офтальмолога становится причиной неполного информирования о возможностях высокотехнологичного лечения внутриглазных опухолей в России.
Радиохирургия сохраняет не только глазное яблоко, но и зрение
Современные методы лучевого лечения опухолей (в т.ч. опухолей глаза) реализуются на сложном оборудовании в специализированных центрах, примерами которых является Онкологическая клиника МИБС и Центр протонной терапии МИБС. Многочисленные исследования подтвердили эффективность высокоточного облучения высокими дозами радиации в лечении меланомы хориоидеи, а опыт и технологии, находящиеся на вооружении специалистов МИБС, позволяют пациенту, независимо от типа и стадии опухоли, получить помощь согласно лучшим международным протоколам.
Чаще всего при увеальной меланоме проводится радиохирургия - управляемая подача тонких пучков элементарных частиц фотонов, из множества пересечений которых формируется зона однородно высокой, смертельной для злокачественных клеток, дозы, соответствующая форме опухоли. В таком случае остальные структуры глаза и находящиеся на пути каждого отдельного пучка излучения здоровые ткани (в т.ч. головного мозга) получают значительно меньшие дозы, размер которых задается исходя из подтвержденных значений толерантных доз (не вызывающих необратимых биологически нарушений).
В зависимости от расположения, формы и размера новообразования, радиохирургия увеальной меланомы может быть выполнена Гамма-ножом или Кибер-ножом. МИБС имеет в своем распоряжении обе этих системы, и выбор наиболее оптимальной технологии производится лечащим врачом после предварительной оценки клинического случая.
Протонная терапия в лечении увеальной меланомы не демонстрирует такого выдающегося преимущества, как при лечении других опухолей - особенность расположения глазного яблока позволяет безопасно подвести высокие дозы радиации и с помощью радиохирургии на Гамма-ноже. При этом стоимость лечения Гамма-ножом несравнимо ниже при одинаковом уровне достигаемой эффективности.
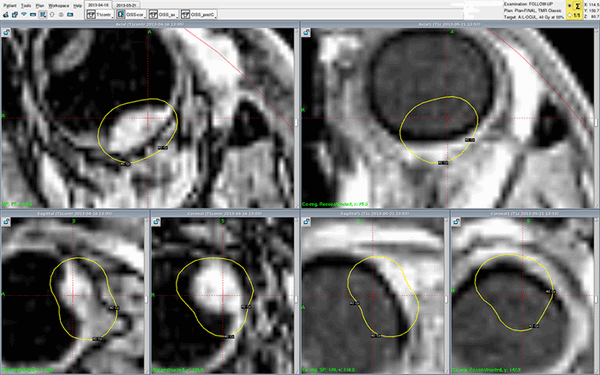
Реальный клинический случай - лечение меланомы хориоидеи Гамма-ножом Gamma-Knife Perfexion в Онкологической клинике МИБС. Снимки МРТ с контрастом (слева - до, справа - после лечения). Меланома хориоидеи на правом снимке, сделанном во время контрольного обследования всего через один месяц (!), не визуализируется - желтые контуры изначального расположения опухоли нанесены для сравнения. Опухоль исчезла. Без операции, с сохранением глазного яблока.
Благодаря органосохранности, оптимальной стоимости и высокой эффективности, количество пациентов МИБС, получивших современное безоперационное лечение увеальной меланомы на Гамма-ноже, составляет уже более трех десятков. Учитывая общую статистику заболеваемости, можно утверждать, что наши врачи и медицинские физики имеют одну из самых высоких компетенций по лечению увеальных меланом не только в России, но и в мире.
Безоперационное вторичных внутриглазных опухолей
Еще одной статистически значимой группой опухолей органов зрения являются метастазы первичных опухолей, расположенных в других частях тела. Метастазы в глазное яблоко чаще всего вовлекают хориоидею, и чаще всего это - метастазы рака легкого. В таком случае радиохирургия также может применяться для разрушения вторичных раков. Но такое решение должно учитывать возможность лечения первичной опухоли и комплексной терапии всех метастазов.
Имеет ли смысл протонная терапия в лечении увеальной меланомы и других внутриглазных опухолей?
В случае с лечением внутриглазных опухолей основное преимущество протонов - минимальное облучение здоровых тканей, - нивелируется тем, что аналогичного уровня безопасности можно достичь и при радиохирургии. И более высокая стоимость лечения протонами делает ее применение при увеальной меланоме нецелесообразным.
Эффективное лечение первичного очага, как профилактика метастазов меланомы хориоидеи
Независимо от того, какой метод был выбран, откладывать лечение увеальной меланомы не стоит - примерно половина пациентов с этим диагнозом погибают от метастазов. Это связано как с активным метастазированием через кровеносные сосуды, так и с низким вниманием к возможным органам-мишеням. Увеальная меланома чаще всего метастазирует в печень (более, чем в 90% случаев метастатического поражения) и легкие (24%). Реже поражаются головной мозг, кожа, кости, лимфоузлы, второй глаз и его орбита.
При своевременном выявлении крупных одиночных метастазов меланомы хориоидеи их лечение также может быть проведено методами радиохирургии и протонной терапии в стенах МИБС.
Если у Вас есть подтвержденный диагноз “увеальная меланома”, или имеются подозрения и Вы уже прошли первичную инструментальную диагностику по месту жительства, обратитесь в любой из Диагностических центров МИБС за “вторым мнением”. Если диагноз подтвердится, наши специалисты смогут дать заключение о возможности и целесообразности применения радиохирургии или протонной терапии, которые доступны пациентам в Онкологической Клинике МИБС и Центре протонной терапии МИБС.
Не дайте болезни шансов - обратитесь сейчас!
Лечение меланомы сетчатки глаза на Гамма-ноже
Меланома сетчатки глаза - агрессивная злокачественная опухоль, растущая из меланоцитов (клеток пигментированной части эпителия сетчатки). Этот вид внутриглазных опухолей встречается гораздо реже, чем увеальная меланома, растущая из клеток частей лежащей под сетчаткой сосудистой оболочки (меланома радужки, цилиарного тела, хориоидеи). Однако лечение увеальной меланомы и меланомы сетчатки не имеют весомых отличий в тактике и методах.
Вырабатываемый меланоцитами меланин защищает сетчатку от повреждений, вызываемых излучением части ультрафиолетового спектра (видимой и длинноволновой), которые не задерживаются роговицей. Однако при воздействии высоких доз ультрафиолета, особенно при наличии генетической склонности, начинается бесконтрольный рост меланоцитов, из которых и формируется опухоль.
Симптомы меланомы сетчатки глаза
Ранние стадии заболевания, как правило, протекают бессимптомно. В это время заболевание может быть выявлено случайно, например, при проведении офтальмоскопии по несвязанным причинам. По мере роста опухоли ухудшается зрение, появляется боль в пораженном глазном яблоке и симптомы, обусловленные повреждением сетчатки: “мертвые зоны”, “плавающие” световые пятна, искры, вспышки и др. При дальнейшем разрастании новообразования происходит деформация глазного яблока, повреждения его структур: дефекты и темные пятна на радужной оболочке, склере, покраснение склеры в зоне контакта с опухолью. В запущенных случаях наступает потеря зрения.
Первичное обращение к офтальмологу и проведенный визуальный осмотр (офтальмоскопия) является базовым методом диагностики. Если опухоль находится в недоступной для визуального выявления части глазного яблока, то обнаружить ее поможет ультразвуковое исследование (УЗИ) глаза и магнитно-резонансная томография. Эти же методы, а также ангиография сосудов глаза являются базой для постановки диагноза.
Для окончательного подтверждения диагноза может быть проведена аспирационная биопсия новообразования.
Метастазы меланомы сетчатки глаза
Важной частью лечения меланомы сетчатки глаза является стадирование - определение распространенности опухолевого процесса, в т.ч. наличия метастазов. Чаще всего этот вид опухолей метастазирует в легкие и печень, реже наблюдаются метастазы в головной мозг. Поэтому пациентам с таким диагнозом выполняется развернутый клинический анализ крови, печеночные пробы, УЗИ органов брюшной полости, рентгенография или компьютерная томография легких, МРТ головного мозга с контрастом.
Лечение меланомы сетчатки глаза
В зависимости от клинического случая может быть избрана органосохранная или ликвидационная тактика. Долгое время лечение меланомы сетчатки, как и других видов злокачественных внутриглазных опухолей (напр., меланомы хориоидеи), означало практически неизбежную энуклеацию (удаление) глазного яблока. С развитием технологий лучевого воздействия, в первую очередь, радиохирургии, врачи получили возможность проводить бесконтактное разрушение опухолей. Для пациента это означает возможность сохранить не только глаз, как косметический орган, но и зрение.
Выполненная по современным стандартам радиохирургия на Гамма-ноже по эффективности сравнима с удалением глазного яблока. Это касается как остановки опухолевого процесса, так и риска метастазирования.
Иногда эффект может дать брахитерапия (контактная лучевая терапия радиоактивными элементами). Применение иммунотерапии и таргетного лечения, в отличие от меланомы кожи, не дает преимуществ перед лучевыми методами.
Органосохраняющее лечение меланомы сетчатки: радиохирургия на Гамма-ноже
Безоперационное разрушение биологических тканей высокими дозами ионизирующего излучения - радиохирургия, - не уступает в эффективности радикальной хирургии, демонстрируя высокие показатели безрецидивности и отсутствия метастазирования. Безопасность современной радиохирургии обеспечивается точным подведением радиации в заданный объем, пространственная форма которого отвечает объему опухолевого поражения. Радиохирургия, как правило, проводится за один сеанс.
Лечение внутриглазной меланомы может быть проведено Гамма-ножом или Кибер-ножом: обе системы обеспечивают высокую точность и безопасность лечения. Однако Гамма-нож, ввиду особенностей конструкции, - дешевле в эксплуатации, что позволяет предложить меньшую стоимость лечения.
Богатый опыт отделения радиохирургии Онкологической клиники МИБС позволяет провести безоперационное лечение в подавляющем большинстве случаев меланомы глаза. Получить предварительное заключение о возможности лечения можно дистанционно, без визита в Клинику.
Лечение метастазов меланомы сетчатки глаза
В случае метастатического процесса лечение метастазов внутриглазной меланомы (в т.ч. меланомы сетчатки) также может быть выполнено в отделении Радиохирургии МИБС. При метастазах в головной мозг пациенту показано лечение Гамма-ножом, при наличии метастазов в печень или легкие эффективной будет радиохирургия на Кибер-ноже либо на высокоточном линейном ускорителе TrueBeam STx.
Стоимость лечения меланомы сетчатки глаза в МИБС
Сравнительная стоимость органосохраняющего лечения меланомы сетчатки Гамма-ножом, как правило, ниже, чем общая стоимость хирургического лечения. При сравнении необходимо учитывать не только стоимость операции по энуклеации глазного яблока, но и стоимость косметической коррекции. При этом радиохирургия обеспечивает несравнимо более высокое качество жизни.
Общая стоимость радиохирургического лечения зависит от особенностей клинического случая (объем, форма, распространенность опухоли, состояние пациента и т.д.) и рассчитывается индивидуально.
Звоните сейчас, чтобы получить больше информации о возможностях Онкологической клиники МИБС.
Читайте также:
- Техника заднего доступа по Kocher-Langenbeck к тазобедренному суставу
- Аденомы слюнных желез. Характеристика аденом слюнных желез.
- Диафрагма таза женщин. Строение диафрагмы таза у женщин.
- Чем опасен дисбактериоз у ребенка? Симптомы и лечение дисбактериоза у детей
- Введение в лучевую диагностику лимфатических узлов шеи: лучевая анатомия, методы исследования
