Синдром Фиссенжер-Рандю (Fiessinger-Rendu) - синонимы, авторы, клиника
Добавил пользователь Евгений Кузнецов Обновлено: 21.01.2026
11‑летний мальчик из Хорватии страдал бронхиальной астмой с шести лет. За полгода до госпитализации течение болезни значительно ухудшилось — приступы астмы стали плохо купироваться ранее назначенными препаратами. Затем пациент стал жаловаться на плохой аппетит и частые головные боли, начали нарастать одышка и цианоз. В связи с этим мальчика положили в терапевтическое отделение больницы.
Маленький пациент жаловался на одышку при нагрузке и несколько обострений астмы, одно из которых завершилось госпитализацией в предыдущем месяце. При обострениях ребенку назначали системные кортикостероиды с постепенным снижением дозировки, впрочем, без уменьшения хронической гипоксии и других симптомов. На момент поступления пациент получал:
- ингаляции адреномиметика и глюкокортикостероида (флутиказон и салметерол 250 мкг / 50 мкг два раза в день);
- бронхолитик монтелукаст — 5 мг один раз в день;
- ингаляции адреномиметика сальбутамола по мере необходимости (на момент поступления — четыре раза в день).
С детства мальчик страдал атопическим дерматитом, в грудном возрасте была аллергия на коровье молоко, с трех лет беспокоили носовые кровотечения. В шесть лет ребенку диагностировали бронхиальную астму из‑за повторяющихся эпизодов хрипов и положительного бронхопровокационного теста с физической нагрузкой. Кожная аллергопроба показала чувствительность к домашнему пылевому клещу и травяной пыльце. После того как пациенту поставили диагноз «астма», его регулярно наблюдал детский пульмонолог. Последние два года заболевание протекало бессимптомно — без профилактики и назначения сильнодействующих препаратов.
Когда мальчика привезли в больницу, его общее состояние характеризовалось как «средней степени тяжести»: одышка, кожа и видимые слизистые оболочки — бледные, до синюшности, гипоксия в состоянии покоя (уровень кислорода в крови (SaO2) 92 % при норме ≥ 95 %). Кроме того, над левым легким выслушивались прерывистые шумы, справа везикулярное дыхание было ослаблено. При осмотре врачи обнаружили две телеангиэктазии на левой щеке и дискретные телеангиэктазии на спине. При ультразвуковом исследовании сердца патологии не выявлено, легочной гипертензии нет.
Телеангиэктазии представляют собой расширение мелких сосудов кожи невоспалительной природы, проявляющиеся сосудистыми звёздочками или сеточками.
Спирометрия (специальное исследование функции дыхательной системы) показала жизненную ёмкость лёгких (ЖЕЛ) 2,65 л (79 % от нормального показателя), объем форсированного выдоха в 1 секунду (ОФВ1) 2,61 л (97 % нормы), соотношение ОФВ1/ЖЕЛ = 95 % (норма). После ингаляции бронхолитика ОФВ1 и ЖЕЛ увеличились на 5 %. Однако при бронхиальной астме прирост в таком случае составляет более 12 %.
Нехарактерные для астмы показатели спирометрии заставили врачей усилить диагностический поиск. Мальчику назначили бронхоскопию. Она показала сдавление левого бронха в язычковом сегменте легкого, а на рентгенограмме в области этого бронха была видна однородная масса мягких тканей размером 20 × 30 мм (рис. 1). Нельзя было исключить опухолевый рост. К счастью, при компьютерной томографии (КТ) выявлена не опухоль, 35‑миллиметровая артериовенозная мальформация (АВМ) в области сдавленного бронха и небольшая АВМ в верхушке правого легкого (рис. 2). АВМ слева имела одну питающую артерию и большую аневризму. Правая АВМ получала питание из двух артерий (рис. 3, 4).
Артериовенозная мальформация (АВМ) — патологическая связь между венами и артериями, обычно врожденная. Мальформации могут появиться в любом органе, однако наиболее опасны в цереброспинальной зоне.
Рисунок 1. Рентген грудной клетки показал однородную массу мягких тканей 20 × 30 мм в язычковом сегменте левого легкого, рядом с тенью сердца Рисунок 2. Трехмерная компьютерная томографическая ангиография показала 35‑мм сосудистую мальформацию в передней части левой верхней доли с одной питающей артерией (ответвление легочной артерии) и одной отводящей веной Рисунок 3.
A. Артериовенозная мальформация и аневризма сегментарной ветви легочной артерии.
B. Состояние после эмболизации сегментарной левой ветви легочной артерии с окклюзией артериовенозной аномалии. Рисунок 4.
A. Артериовенозная мальформация верхушки правого легкого с двумя питающими артериями.
B. Состояние после эмболии одной из артерий АВМ. C. Состояние после эмболии второй артерии АВМ.
Во время госпитализации мальчику провели генетический анализ, в результате обнаружилась мутация в гене трансмембранного белка эндоглина, что типично для синдрома Рандю — Ослера.
Болезнь Рандю́ — О́слера (Рандю — Ослера — Ве́бера) , синдром Ослера, семейная геморрагическая телеангиэктазия, — наследственное заболевание, в основе которого лежит неполноценность сосудистого эндотелия, в результате чего на разных участках кожи и слизистых оболочках губ, рта, во внутренних органах образуются множественные ангиомы и телеангиэктазии (виды аномалий сосудов), которые могут кровоточить. Названа болезнь по именам врачей, описавших ее в конце XIX — начале XX века. Передается заболевание Рандю—Ослера по аутосомно-доминантному типу; встречается у одного из 5000 человек.
Для лечения этого случая болезни Рандю—Ослера врачи приняли решение эмболизировать (избирательно закупорить, — прим. ред.) мальформации в легких с помощью спиралей из нержавеющей стали (рис. 5). Спирали вводили с помощью катетера через бедренную артерию. Диаметр спиралей был равен или на 10 % превышал диаметр артерий, питающих мальформации (рис. 3, 4). После операции ток крови через АВМ прекратился (рис. 6). Пульсоксиметрия показала увеличение кислородной сатурации периферической крови с 92 % до 97 % непосредственно на воздухе.
Исчезла болезненная бледность, мальчик стал лучше переносить нагрузки. Симптомы удушья и дыхательной недостаточности не проявлялись в течение всего периода наблюдения (шесть месяцев после процедуры). Кроме того, врачи с помощью МРТ головного мозга и шейного отдела позвоночника убедились в отсутствии угрожающих жизни пациента церебро-спинальных АВМ. Углубленный сбор анамнеза выявил положительную семейную историю болезни Рандю — Ослера: у двоюродного брата отца пациента была диагностирована АВМ в головном мозге.
Рисунок 5. Рентгенография грудной клетки со стальными спиралями после эмболизации легочных артериовенозных мальформаций в правом и левом легком Рисунок 6. Ангиограмма после эмболизации лёгочной артерии обеих артериовенозных мальформаций
Как не спутать астму с другой патологией
Этот случай интересен тем, что пациенту первоначально неправильно диагностировали бронхиальную астму и пять лет лечили от заболевания, которого не было. Диагноз не вызывал сомнений, поскольку у мальчика имели место аллергическая предрасположенность, частая одышка, низкая переносимость физических нагрузок и несколько типичных астматических приступов. При КТ-ангиографии выявлено две АВМ — по одной в правом и левом легком. Клинический диагноз — болезнь Рандю — Ослера — врачи поставили на основании трех критериев Кюрасао (носовое кровотечение, слизистые телеангиэктазии и легочные АВМ), а затем подтвердили генетически.
Астма — распространенное заболевание, однако многие болезни имеют схожие симптомы. Это следует учитывать особенно в тех случаях, когда симптомы астмы плохо поддаются терапии [4]. Согласно решению конгресса Американского торакального общества, для определения рефрактерной или тяжелой астмы используются большие и малые критерии. Большие критерии:
- а) непрерывное или почти непрерывное (> 50 % года) лечение пероральными кортикостероидами;
- b) необходимость лечения высокодозными ингаляционными кортикостероидами.
- а) одно или несколько обострений астмы в год;
- b) ежедневное использование β2‑агониста короткого действия из‑за симптомов астмы;
- c) обструкция дыхательных путей (ОФВ1 Источники
Современные аспекты терапии наследственной геморрагической телеангиоэктазии (болезни Рандю-Ослера).
Несмотря на определенные успехи в познании наследственной геморрагической телеангиэктазии (болезни Рандю-Ослера), особенно в области генетики, исследований висцеральных сосудистых мальформаций, вопросы лечения этого страдания остаются нерешенными. В настоящей работе приводится обзор работ, посвященных терапии болезни Рандю-Ослера, с учетом исследований последний лет; и представлены перспективные направления в решении этой проблемы.
Ливандовский Ю. А., Земсков Е. В. Современные данные о лечении наследственной геморрагической телеангиэктазии. Врач скорой помощи №12 // 2010.
Болезнь Рандю-Ослера (наследственная геморрагическая телеангиэктазия, НГТ) известна более века. Она проявляется сосудистыми изменениями типа телеангиэктазий слизистых оболочек и кожных покровов, а также висцеральными мальформациями печени, лёгких, головного мозга и других органов. Вторым важным клиническим признаком болезни служат геморрагии из телеангиэктазий носа, желудочно-кишечного тракта и т. д.. Третьим - наследственная природа болезни, которая сопряжена с аутосомно-доминантным типом наследования. Если в семье болен один из родителей, то теоретически у каждого ребёнка имеется 50% вероятность быть больным.
В последние десятилетия достигнуты несомненные успехи в молекулярной генетике, которые позволили выделить 4 типа болезни Рандю-Ослера. Многочисленные научные исследования подтвердили генетическую неоднородность заболевания. 2 Показано,что мутации эндоглин-корригирующего гена, расположенного на 9 хромосоме, (9q 34.1) связаны с НГТ I типа . 4 Второй вариант (НГТ II) вызван мутацией гена ALK 1(activin-receptor like kinase 1), который располагается на хромосоме 12, вблизи от центромеры (12q11-q19).7 При этих типах НГТ мутация приводит к болезни путём гаплотической недостаточности. Доказано и существование третьего варианта (НГТ III) [11], связанного с геном, расположенным на хромосоме 5. Четвёртый вариант (НГТ IV) c проявлениями ювенильного полипоза, объясняют мутацией в гене SMAD4. 14
В диагностике НГТ играют роль прежде всего, клинические признаки, а генетические исследования дополняют наши познания об этом заболевании. В последнее время появились данные, говорящие о том, что для выявления НГТ у потенциальных больных могут быть использованы и биологические показатели. Так уменьшение уровня ангиопоэтина 2 и растворимого эндоглина в крови свидетельствует в пользу данной патологии. [15]
Общие подходы лечения данного заболевания представлены в таблице 1.
Основные направления в терапии болезни Рандю-Ослера Таблица 1 .
Направления терапии
1. эстроген-прогестероновые препараты
2. даназол
3. октреотид
4. термическая лазерная коагуляция кровоточащих телеангиэктазий
5. лазерная фотокоагуляция при эндоскопии
1. транскатетерная эмболизация сосудов
2. трансплантация печени
1. транскатетерная эмболизация сосудов
2. резекция доли лёгкого
1. пероральная и парентеральная железотерапия
2. трансфузии эритроцитарной массы
Рецидивирующие носовые кровотечения обычно являются доминирующим признаком в клинической картине заболевания. Они значительно снижают качество жизни пациентов и служат причиной поиска эффективных подходов профилактики и лечения. Острые обильные носовые кровотечения могут привести к смерти. [16]
Широко применяются традиционные методы воздействия (местные гемостатические средства, тампонада носа гемостатической губкой и др. ). При значительных кровотечениях назначают этамзилат (дицинон) внутрь или внутривенно. Для борьбы с кровотечениями широко используют антифибринолитические препараты (местно, внутрь и парентерально) [17], учитывая, в частности, и факт повышения фибринолитической активности в местах телеангиэктазий.[18]
C целью остановки носового кровотечения могут быть использованы локальные лазерные воздействия. 20
Чрескожная эмболизационная терапия остаётся методом выбора при тяжёлых массивных кровотечениях и даёт значительное улучшение качества жизни пациента как в отношении тяжести, частоты, так и продолжительности носовых кровотечений на протяжении первого месяца и года после эмболизации. Но данный метод хорош, когда выполняется опытными руками, так как сама манипуляция может стать причиной многих серьёзных осложнений. 22 Ещё один способ лечения жизнеугрожающих носовых кровотечений у больных НГТ такой, как дермопластика слизистой перегородки носа, так же является эффективным методом остановки кровотечений, который с одной стороны улучшает качество жизни пациента в отношении рецидивирования носовых кровотечений [25], а с другой -может приводить к различным осложнениям (появление запаха из носа, образование корок, снижение обоняния, утяжеление синусовой инфекции), ухудшающим самочувствие пациента.[26]
Было опубликовано много работ, посвящённых гормональной терапии НГТ эстрогенами 27, но результаты оказались неоднозначными.
Видимо, в настоящее время нецелесообразно проводить локальные термо и химио каутеризации, которые способны вызвать повреждение носовых структур.
Показано, что у больных НГТ имеется высокий уровень фактора роста эндотелия сосудов (VEGF), который может быть напрямую связан с развитием телеангиэктазий. В связи с этим, появились экспериментальные исследования применения ингибитора эндотелиального фактора роста бевацузимаба (авастатина) в виде назального спрея с целью урежения частоты носовых кровотечений. [31] В литературе есть данные о совместном использовании интраназального подслизистого введения бевацизумаба и лазерного прижигания. Результаты этого комбинированного метода лечения выявили преимущества перед назначением одного бевацузимаба. Отмечено значительнoе уменьшение степени и частоты носовых кровопотерь и снижение потребности в гемотрансфузиях, повышение работоспособности пациентов с НГТ. [32]
Прошло около девяти лет с того момента, когда впервые были описаны гемостатические эффекты тамоксифена, назначенного в качестве химиотерапии больной с раком молочной железы I стадии и НГТ.[33] И сравнительно недавно было проведено первое клиническое исследование, посвящённое влиянию антиэстрогенновой терапии тамоксифеном на выраженность носовых кровотечений при НГТ. Так у 25 пациентов, рандомизированных на две группы, был продемонстрирован положительный эффект тамоксифена в дозе 20 мг/сут в отношении частоты и тяжести носовых кровотечений. [34]
В эксперименте на культуре эндотелиальных клеток было показано повышение экспрессии белков генами ENG и ALK-1 под воздействием ралоксифена, являющегося селективным стимулятором эстрогеновых рецепторов. В связи с этим возникло предложение использовать данный препарат для лечения, к примеру, носовых кровотечений у женщин, страдающих остеопорозом, в постменопаузе.[35]
Интересные результаты были получены голландскими учёными, проводившими исследования влияния N-ацетилхолина (АЦХ) на выраженность эпистаксиса и качество жизни больных НГТ . Оказывается, АЦХ, обладая антиоксидантными свойствами, способен снижать частоту, тяжесть и продолжительность носовых кровотечений. При этом максимальный положительный эффект АЦХ наблюдался у лиц мужского пола и у носителей мутации в гене ENG, в то время как у представительниц прекрасного пола и у носителей дефекта в гене ALK-1 значительного улучшения состояния выявлено не было. [36]
В этом году группой французских учёных была впервые установлена возможность применения для лечения сосудистых дисплазий при НГТ печально известного седативного средства талидомида. В опытах на мышах, гетерозиготных по мутантному гену ENG, было показано, что лечение талидомидом способно стимулировать выработку тромбоцитарного фактора роста-В (PDGF-B) эндотелиоцитами и активировать созревание сосудистой стенки за счёт размножения интрамуральных клеток (перицитов). Прижизненное исследование назального эпителия у небольшой группы пациентов с НГТ также выявило эффективность талидомида в отношении носовых кровотечений, частота и выраженность которых значительно снизилась на фоне стабилизации сосудистой стенки и повышения уровня гемоглобина. Таким образом, как заявляют авторы работы, талидомид может стать новой стратегией лечения НГТ.[37]
При введении больных с НГТ не стоит, видимо, забывать и старых методов лечения, в частности, гипероксибаротерапию, при осуществлении которой отмечено уменьшение объёма и частоты носовых кровотечений или их прекращение более чем у половины больных. [38]
С целью профилактики носовых кровотечений следует исключить приём алкогольных напитков, включая пиво, острых блюд, уксуса, пряностей, которые, как показывают клинические наблюдения, могут провоцировать геморрагии. Не рекомендуется назначать лекарственные препараты, нарушающие функциональные свойства тромбоцитов (нестероидные противовоспалительные средства и др.), а также антикоагулянты, фибринолитики, способные ухудшить течение геморрагического диатеза.
Наружные кожные кровоточащие телеангиэктазии, которые представляют косметическую проблему, требуют локальной лазеротерапии или применения криовоздействия. [39]
При выраженных желудочно-кишечных кровотечениях с гемостатической целью применяют комбинацию низких доз эстрогена и прогестерона [40,41], механизм воздействия которых мало изучен, однако, у больных наблюдается меньшая потребность в гемотрансфузиях.
Эффект применения эндоскопической локальной лазеротерапии при желудочно-кишечных геморрагиях не оправдал оптимистических ожиданий. [42]
Поражения печени при разбираемом заболевании могут иметь многие причины, важнейшими из которых являются сосудистые мальформации, телеангиэктазии, аневризмы, артериовенозные шунты.
Шунт из печёночной артерии в воротную вену вызывает портальную гипертензию, способствующую развитию желудочно-кишечных кровотечений, асцита. Вследствие сосудистых аномалий печени, хронической ишемии ткани этого органа возможна картина "псевдоцирроза".
Спиральная компьютерная томография выявляет у ¾ больных те или иные васкулярные аномалии в печени, у половины больных - артериопортальные шунты.
Для больных НГТ с тяжёлым поражением печени единственным эффективным методом лечения на сегодняшний день является ортотопическая трансплантация печени (ОТП). 56. Показаниями к трансплантации печени у больных с данной патологией могут служить следующие обстоятельства: сердечная недостаточность в связи с сосудистыми изменениями печени, билиарный некроз, ведущий к печёночной недостаточности, выраженная портальная гипертензия и т. д.
Трансплантация печени устраняет возможность развития гепатобилиарного сепсиса и предупреждает развитие сердечно-лёгочной недостаточности, значительно улучшая качество жизни пациентов.
Согласно результатам наблюдения за пациентами, перенёсшими ОТП, долгосрочная выживаемость составляет 75% (9 пациентов из 12 оперированных), при этом у выживших после трансплантации печени наблюдалось повышение качества жизни как за счёт урежения частоты носовых кровотечений, так и вследствие расширения режима физических нагрузок.[58].
Если у больных отсутствуют признаки портальной гипертензии, печёночной недостаточности, нет грубых сосудистых изменений, то специальной активной терапии им не требуется.
Сосудистые мальформации головного мозга выявляются, прежде всего, с помощью магнитно-резонансного исследования у 5-10% пациентов с НГТ. Они способны вызывать различные клинические симптомы (головную боль, эпилептические приступы, картину ишемических атак, редко - кровоизлияния).
При церебральных мальформациях могут потребоваться нейрохирургические подходы или стереотаксическая артериовенозная эмболотерапия. [60]
Вопрос о хирургическом вмешательстве при бессимптомных церебральных мальформациях, обнаруженных при магнитно-резонансном исследовании, остаётся дискутабельным.
В заключение, следует отметить, что данное заболевание, протекающее с ангиоматозным типом кровоточивости, обычно не является прямым противопоказанием для проведения экстренных и плановых оперативных вмешательств (аппендэктомии, холецистэктомии и др.)
Таким образом, приведённые в настоящей работе данные о современной тактике терапии различных проявлений наследственной геморрагической телеангиэктазии позволяют надеяться на то, что в ближайшем будущем появятся новые подходы в решении сложных вопросов этого сосудистого страдания.
Резюме
В статье представлен обзор современных взглядов на лечение относительно редкого сосудистого заболевания — наследственной геморрагической телеангиэктазии. Подчёркиваются успехи в понимании генетических основ данного страдания.
Список используемой литературы:
Синдром Фиссенжер-Рандю (Fiessinger-Rendu) - синонимы, авторы, клиника
Саратовский государственный медицинский университет
Наследственный геморрагический ангиоматоз (болезнь Ослера-Рандю)
Описаны этиология, патогенез, клинические и патоморфологические критерии диагностики наследственного геморрагического ангиоматоза, принципы терапии данного заболевания. Приведены случаи собственных наблюдений.
Целью данной работы является ознакомление врачей с этиологией, патогенезом, клиническими и патоморфологическими критериями диагностики, а также принципами терапии наследственного геморрагического ангиоматоза (НГА).
Определение, история. НГА — редкое семейное заболевание кожи и слизистых оболочек, проявляющееся образованием множественных ангиоподобных пятен, узелков и телеангиэктазий вследствие геморрагической вазопатии с дефектом мезенхимы [1—3].
Встречается с частотой 1—2: 100 000, наследуется по аутосомно-доминантному типу с различной пенетрантностью гена, расположенного в локусе 9q33—34 [1, 4]. В 1896 г. H. Rendu впервые описал сочетание множественных телеангиэктазий с носовыми кровотечениями у членов одной семьи. В 1901 г. W. Osler выделил наследственные геморрагические телеангиэктазии в самостоятельный синдром [1]. Впоследствии такое сочетание получило название «наследственная геморрагическая телеангиэктазия Ослера—Рандю» [1—2, 5].
Патогенез. По данным современных авторов, в результате мутации гена, кодирующего белок эндотелиальных клеток эндоглин, связывается трансформирующий фактор роста β. Это ведет к утрачиванию опорных структур сосудов (перициты, гладкие мышечные клетки, эластические волокна), дефекту их мышечного и эластического слоев, разрушению контактов между эндотелиальными клетками, длительной дилатации и ломкости капилляров [3—4].
Патоморфология. Изменения выявляются в верхней части дермы (или слизистой оболочки) в виде множественных мешковидных расширений капиллярных сосудов; их стенки состоят из одного эндотелия и окружены рыхлой соединительной тканью [1—2].
Клиническая картина. Заболевание нередко начинается в 10-летнем возрасте, проявляясь частыми носовыми кровотечениями и телеангиэктазиями на коже и слизистых оболочках. Симптоматика усиливается к 20—40 годам. Болеют как мужчины, так и женщины. Изменения на коже и слизистых оболочках представлены сосудистыми пятнами типа телеангиэктазий величиной от булавочной головки до 0,5—3 см в диаметре, бледнеющими при надавливании, или пурпурными милиарными ангиоматозными узелками. Провокационные пробы «жгута» и «щипка» отрицательные. Локализация: лицо (щеки, лоб, подбородок), ушные раковины, реже — грудь, сгибательные поверхности конечностей, почти всегда — слизистые оболочки носа, рта, губ и языка. Сосудистые узелки могут выявляться также и во внутренних органах (легкие, желудочно-кишечный тракт, печень, мочевой пузырь), мягкой мозговой оболочке, сетчатке глаз.
Сосудистые узелки и телеангиэктазии склонны к периодическим, часто внезапным кровотечениям, особенно в пубертатном периоде, во время беременности, инфекционных заболеваний, а также при проведении врачебных манипуляций, чистке зубов. В результате частых и повторных кровотечений возможно развитие анемий.
При лабораторном обследовании не обнаруживается изменений показателей свертываемости крови, тромбоцитов, ретракции сгустка, времени кровотечения [1—4].
Течение. Патологические изменения с увеличением возраста усиливаются и без лечения существуют на протяжении всей жизни.
Прогноз сомнительный из-за возможности возникновения обширных кровотечений.
Диагностика. Диагноз основывается на анамнезе, клинической и гистологической картине заболевания.
Дифференциальный диагноз проводится с телеангиэктазиями при циррозе печени, гемофилией, тромбоцитопенической пурпурой, диффузной ангиокератомой туловища Фабри.
Лечение. Исключение физических нагрузок и травм. Остановка и профилактика кровотечений (препараты кальция, аминокапроновая кислота, викасол и др.). Устранение постгеморрагической анемии (препараты железа, витамин В12, фолиевая кислота, гемотрансфузии). При упорных кровотечениях назначают эстрогены. Сосудоукрепляющие средства (витамины C, P). Удаление отдельных элементов с помощью электрокоагуляции, криотерапии, лазеродеструкции [1—4].
Приводим собственные клинические наблюдения.
Больная С., 35 лет, заболела в 12-летнем возрасте, когда стали беспокоить частые кровотечения из носа, а к 20 годам на коже и слизистых оболочках появились множественные расширенные сосуды и мелкие красного цвета узелки. К врачам не обращалась. Лечение не получала. Сходные симптомы отмечает у близких родственников по материнской линии. В настоящее время имеет беременность сроком 36 нед, во время которой отметила усиление проявлений заболевания. Направлена на консультацию в клинику кожных и венерических болезней СГМУ.
В анамнезе: ОРВИ, грипп, ангина.
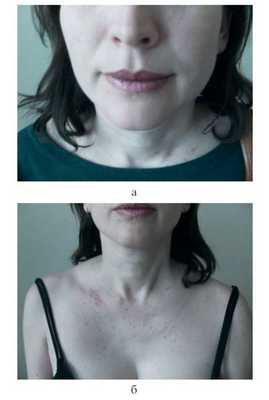
Объективно: на коже лица и верхней части груди отмечаются множественные расширения капилляров величиной от булавочной головки до горошины, располагающиеся в виде телеангиэктатических сплетений, паукообразные сосудистые невусы, бледнеющие при надавливании. На ушных раковинах, пальцах кистей, слизистой оболочке губ и языка имеются пурпурные милиарные узелки, слегка возвышающиеся над уровнем нормальной кожи и слизистых оболочек. Субъективных ощущений нет. Пробы «жгута» и «щипка» отрицательные (рис. 1). Рисунок 1. Больная С., 35 лет. Болезнь Ослера—Рандю. а — звездчатые сосудистые невусы, милиарные пурпурозные узелки на лице; б — расширенные капилляры и милиарные пурпурозные узелки на груди. Общее состояние пациентки удовлетворительное. Общие анализы крови и мочи без патологии. Показатели свертываемости крови, количества тромбоцитов, ретракции сгустка, времени кровотечения без отклонений от нормы.
Назначена терапия: аскорутин по 1 таблетке 3 раза в сутки в течение 1 мес, наблюдение дерматолога по месту жительства.
Больная А., 12 лет, заболела в 10-летнем возрасте, когда периодически стала отмечать обильные носовые кровотечения без видимой причины. Спустя 2 года на лице, груди, руках и ногах возникли множественные пятнистые и узелковые высыпания синюшно-красного цвета, не сопровождающиеся субъективными ощущениями. К врачу не обращалась. Не лечилась. Направлена педиатром на консультацию в клинику кожных болезней СГМУ для установления диагноза.
В анамнезе: ветряная оспа, ОРВИ, ангина, грипп. Семейного характера заболевания выяснить не удалось.
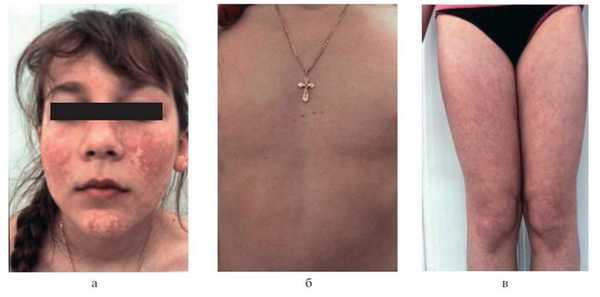
Объективно: на коже лица (щеки, лоб, подбородок, спинка носа) имеются множественные ангиоматозные красно-фиолетовые пятна диаметром от 5 мм до 1 см, склонные к группировке и слиянию, бледнеющие при надавливании, телеангиэктазии. На туловище (грудь, живот), верхних и нижних конечностях — диссеминированные мелкие сосудистые пятна и пурпурные узелки величиной от булавочной головки до горошины, синюшно-красного цвета, слегка возвышающиеся над уровнем нормальной кожи. При осмотре слизистой оболочки носа определяются телеангиэктазии и точечные ангиоподобные узелки. Провокационные пробы «жгута» и «щипка» отрицательные (рис. 2). Рисунок 2. Больная А., 12 лет. Болезнь Ослера—Рандю. а — множественные ангиоматозные красно-фиолетовые пятна, склонные к группировке и слиянию на лице; б — ангиоподобные узелки и сосудистые пятна на груди; в — множественные пурпурозные узелки и сосудистые пятна на бедрах. Субъективных ощущений нет. Общее состояние пациентки удовлетворительное. Общий анализ крови и мочи без патологии. Показатели свертываемости крови, количества тромбоцитов, ретракции сгустка, время кровотечения без отклонений от нормы.
Больная Ш., 15 лет, заболела за 1 нед до обращения к врачу дерматовенерологу, когда без видимой причины на слизистой оболочке рта и по всему кожному покрову возникли множественные кровоизлияния и мелкие красного цвета узелки без субъективных ощущений.
В анамнезе: простудные заболевания, обильные носовые и менструальные кровотечения. О наличии подобной патологии среди близких родственников сведений не имеет.
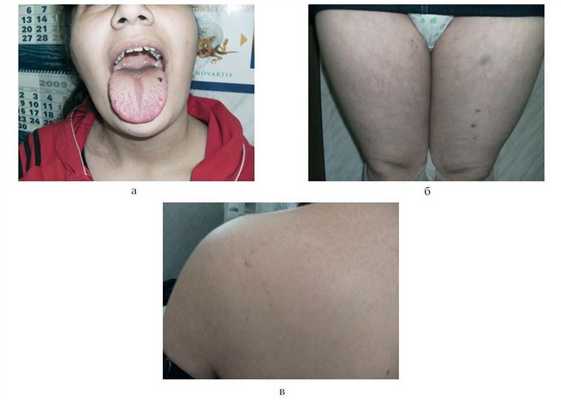
Объективно: на туловище, верхних и нижних конечностях — диссеминированные мелкие пурпурного цвета узелки, кровоизлияния, сосудистые пятна. На слизистой оболочке твердого неба и на языке имеются геморрагические эффлоресценции. Пробы «жгута» и «щипка» отрицательные (рис. 3). Рисунок 3. Больная Ш., 15 лет. Болезнь Ослера—Рандю. а — геморрагические эффлоресценции на слизистой оболочке твердого неба и языке; б — мелкоузелковые и геморрагические высыпания на бедрах; в — сосудистые пятна и пурпурозные узелки в области спины. Общее состояние не нарушено. Общий анализ крови и мочи без патологии. Показатели свертывания крови, количества тромбоцитов, ретракции сгустка, времени кровотечения в пределах нормы.
Рекомендовано наблюдение дерматолога и лечение по месту жительства.
Таким образом, приведенные наблюдения иллюстрируют трудности диагностики НГА ввиду редкости данной патологии. Однако тщательно собранный анамнез, характерная клиническая картина в сочетании с кровотечениями и нередко выявленный семейный характер заболевания дают возможность своевременно распознать данную патологию.
Болезнь Рандю-Ослера. Причины, симптомы и лечение
К перечисленным в заголовке синонимическим диагнозам можно добавить еще несколько названий, часто употребляемых для обозначения данного заболевания, например, синдром Ослера, болезнь Рандю-Ослера-Вебера, геморрагическая телеангиэктазия и т.п.). Все они указывают на наиболее распространенный вид наследственной патологии сосудов: суть ее заключается в мелкоочаговом аномальном растяжении и истончении капиллярных стенок, что приводит к образованию множественных телеангиэктазий (сосудистых «звездочек», точек, «сеточек» и т.д.) с тенденцией к кровоточивости.
Эпидемиологическая картина характеризуется крайней неравномерностью и территориальной зависимостью. Так, болезнь Рандю-Ослера обнаруживается у каждого двухсотого из жителей Нидерландских Антильских островов, тогда как в других регионах земного шара частота встречаемости может не превышать 1:100 000.
2. Причины
На сегодняшний день в отношении патогенеза остаются вопросы. Согласно наиболее аргументированной и общепринятой точке зрения, характерная клиническая картина возникает вследствие аномального, неправильного строения тканей, из которых на этапе внутриутробного развития формируются стенки микрососудов: в них практически нет эластичных мышечных волокон, а оболочкой эндотелиальной стенки служит соединительная ткань. При таком составе сосудистая стенка отличается хрупкостью, уязвимостью и неустойчивостью к растяжениям, она легко образует аневризмы и разрывы, - что и приводит к кровотечениям.
3. Симптомы и диагностика
Несмотря на то, что заболевание обусловлено генетически, проявляться оно начинает, как правило, лишь после 6-8 лет жизни. Первые видимые телеангиэктатические очаги обычно локализуются на губах, деснах, крыльях носа, щеках, мочках ушей. С годами телеангиэктазий становится больше, они появляются на новых участках и, кроме того, меняется их морфология: от маленьких красных точек к «паутинкам» и заметно выступающим ярко-красным узелкам. С возрастом усугубляется также геморрагическая тенденция.
Типичным и одним из первых симптомов болезни Рандю-Ослера являются носовые кровотечения. Их интенсивность в различных случаях варьирует: от сравнительно коротких и скудных до упорных и очень продолжительных. В истории медицины зафиксированы случаи смерти от кровопотери при геморрагической телеангиэктазии.
По мере прогрессирования сосудисто-стеночной несостоятельности телеангиэктатические очаги могут образовываться не только на слизистых и коже, но и на внутренних органах (головной мозг, ЖКТ, легкие, почки и т.д.). Соответственно, даже мелкие аневризмы или кровотечения в этом случае становятся очень опасными: высок риск развития тяжелой анемии и фатальной сердечнососудистой недостаточности.
Диагностика базируется на изучении анамнеза болезни (одним из ключевых признаков являются частые упорные кровотечения) и семейного анамнеза (наследственный фактор), а также на выявлении характерных телеангиэктазий. Как правило, на коже или слизистых оболочках они визуализируются уже при осмотре и не оставляют сомнений, однако вероятность латентных внутренних кровотечений создает показания к назначению эндоскопических исследований. Обязательно назначаются также общеклинический анализ крови и коагулограмма.
4. Лечение
Первоочередными задачами являются предотвращение опасных геморрагий и купирование анемии, - в ряде случаев с этой целью назначают переливания крови. Длительное время терапевтическим стандартом при болезни Рандю-Ослера считалась тампонада носа, однако в настоящее время все больше специалистов отказываются от этого метода, находя в нем массу недостатков при малой эффективности. Сегодня в числе лечебных средств применяется орошение раствором аминокапроновой кислоты, различные методики коагуляции (крио-, электро-, лазерная) и искусственной эмболизации наиболее проблемных артерий. Наличие крупных аневризм зачастую вынуждает прибегать к хирургическому их устранению.
Пациентам с наследственной геморрагической телеангиэктазией приходится соблюдать особую диету и соблюдать все меры предосторожности, чтобы избегать травмирования кровоточивых и потенциально опасных очагов.
Наиболее востребованные операции- коронарное шунтирование, в том числе, мини-инвазивное коронарное шунтирование
- ангиопластика
- стентирование
- замена сердечного клапана
- имплантация кардиостимуляторов (ЭКС)
- пересадка сердечных клапанов
- коррекция врожденных пороков сердца
- удаление аневризмы
Если вы обнаружили у себя подобные симптомы, возможно, это сигнал заболевания, поэтому рекомендуем проконсультироваться с нашим специалистом.
Диагностика- ЭКГ (электрокардиограмма)
- ЭхоКГ (эхокардиография)
- Нагрузочный тест (велоэргометрия, тредмил)
- Коронарография
- Липидный профиль
- Консультация врача сердечно-сосудистого хирурга, кмн - от 5000 р.
- Биохимический анализ крови (стандартная, 10 показателей) - 2470 р.
- Биохимический анализ крови (расширенаяая, 14 показателей) - 3565 р.
- Общий анализ крови - 675 р.
- ЭКГ (электрокардиография) - 1500 р.
- ЭхоКГ (эхокардиография, УЗИ сердца) - 4500 р.
- Нагрузочный тест (велоэргометрия) - 5000 р.
- Холтеровское (суточное) мониторирование ЭКГ . - 4000 р.
- СМАД (суточное мониторирование АД) - 4000 р.
- Липидный профиль - 1060 р.
Мы стараемся оперативно обновлять данные по ценам, но, во избежание недоразумений, просьба уточнять цены в клинике.
Данный прайс-лист не является офертой. Медицинские услуги предоставляются на основании договора.
Болезнь Рандю-Ослера-Вебера
Болезнь Рандю-Ослера-Вебера - одна из наиболее часто встречающихся наследственных геморрагических телеангиэктазий, причиной которой выступает несостоятельность сосудистой стенки некоторых капилляров. Симптомами заболевания служат частые носовые кровотечения, телеангиэктазии на коже и слизистых оболочках, при тяжелых формах могут возникать желудочные и легочные геморрагии и хроническая железодефицитная анемия. Диагностика осуществляется с помощью осмотра больного, эндоскопических исследований, иногда - изучения наследственного анамнеза. Специфического лечения болезни Рандю-Ослера-Вебера на сегодняшний день не существует, используют различные гемостатические мероприятия и поддерживающую терапию.
Общие сведения
Болезнь Рандю-Ослера-Вебера (наследственная геморрагическая телеангиэктазия) - наследственная вазопатия, характеризующаяся неполноценностью эндотелия, что приводит к развитию телеангиэктазий и трудно останавливаемых кровотечений. Заболевание было описано на рубеже XIX-XX веков исследователями Анри Рандю, Уильямом Ослером и Фредериком Парксом Вебером. Дальнейшие исследования врачей-генетиков доказали наследственную природу заболевания, оно передается по аутосомно-доминантному типу. Пенетрантность патологического гена на сегодняшний день неизвестна (как неизвестен, собственно, и сам ген), болезнь Рандю-Ослера-Вебера с равной долей вероятности поражает как мужчин, так и женщин, однако степень выраженности симптомов отличается у разных больных. Встречаемость патологии довольно высока и оценивается на уровне 1:5000. Помимо наследственных форм болезни описаны случаи спорадического развития симптомов.
Причины болезни Рандю-Ослера-Вебера
Этиология и патогенез болезни Рандю-Ослера-Вебера в настоящее время остаются предметом для научных дискуссий. Последние данные генетики указывают, что у больных нарушена структура трансмембранного белка эндотелиоцитов - эндоглина или киназы-1. Однако это не объясняет сосудистую дисплазию, признаками которой является отсутствие у некоторых сосудов мышечной и эластической оболочек. Это приводит к тому, что сосудистая стенка представлена лишь одним эндотелием и окружающей его рыхлой соединительной тканью. Так как сердечно-сосудистая система является производным мезенхимы, это дает повод некоторым исследователям считать болезнь Рандю-Ослера-Вебера вариантом эмбриональной мезенхимальной дисплазии. Лишенные мышечной и эластической оболочек сосуды формируют микроаневризмы, которые, легко повреждаясь, приводят к геморрагиям.
Упорность кровотечений при болезни Рандю-Ослера-Вебера объясняется еще и тем, что немаловажную роль в процессе гемостаза играет спазм кровеносных сосудов около места повреждения. При отсутствии мышечной оболочки рефлекторный спазм становится невозможным, тем самым сильно затрудняется формирование тромба и остановка кровотечения. Предположительно, дефекты некоторых рецепторов эндотелия также затрудняют процесс свертывания крови при болезни Рандю-Ослера-Вебера. Подтверждением того факта, что геморрагии при данной патологии не связаны напрямую с системой гемостаза, служит нормальный уровень всех факторов свертывания у больных. Лишь при тяжелых случаях заболевания могут наблюдаться тромбоцитопения и дефицит других факторов, однако они имеют вторичный характер и обусловлены коагулопатией потребления.
Симптомы болезни Рандю-Ослера-Вебера
Первые проявления болезни Рандю-Ослера-Вебера становятся заметны в возрасте 5-10 лет, они представлены формирующимися телеангиэктазиями на коже носа, лица, ушных раковин, губ, а также слизистых оболочках полости рта. Выделяют три типа сосудистых нарушений, которые отражают основные этапы их развития - ранний, промежуточный и узловатый. Ранние телеангиэктазии имеют вид слабых красноватых точек и пятнышек. Промежуточный тип сосудистых нарушений характеризуется образованием на коже заметных сеточек, «паучков» и звездочек. Узловатые телеангиэктазии представляют собой узелки размером 5-8 миллиметров, несколько выступающие над поверхностью кожи или слизистых оболочек. Скорость трансформации сосудистых нарушений, а также их количество и возраст появления отражает тяжесть конкретного случая болезни Рандю-Ослера-Вебера.
Помимо телеангиэктазий у больных со временем развиваются геморрагические нарушения, обычно первыми возникают упорные и беспричинные носовые кровотечения. Выявить их источник даже при эндоскопической риноскопии очень сложно, применение гемостатических губок и турунд нередко не способствуют остановке кровотечения и даже провоцируют его еще сильнее. Известны случаи летального исхода по причине носового кровотечения при болезни Рандю-Ослера-Вебера. Как правило, при такой клинической картине больного направляют на обследование к гематологу, однако признаков коагулопатии при этом не выявляется. Если геморрагии имеют длительный или профузный характер, то к симптомам кровотечения присоединяются также головокружения, обмороки, бледность и другие анемические проявления.
В более тяжелых случаях болезни Рандю-Ослера-Вебера у больных могут возникать признаки желудочного (мелена, рвота кофейной гущей, слабость) и легочного кровотечений. Иногда больные жалуются на одышку, слабость, цианоз - это является признаком право-левого шунтирования крови в легких из-за артериовенозных фистул. Телеангиэктазии возникают не только на поверхности кожи, встречаются также церебральные и спинальные формы сосудистых нарушений. Это приводит к эпилептическим припадкам, субарахноидальным кровоизлияниям, параплегиям, а также развитию абсцессов головного мозга. Некоторые семейные формы болезни Рандю-Ослера-Вебера проявляются преимущественно церебральными симптомами и нарушениями при умеренной выраженности кожных телеангиэктазий и носовых кровотечений.
Диагностика болезни Рандю-Ослера-Вебера
Диагностика болезни Рандю-Ослера-Вебера производится на основании жалоб больного, физикального осмотра, эндоскопических исследований желудочно-кишечной и дыхательной систем. Если имеются признаки или подозрения на развитие церебральных нарушений, то производят магнитно-резонансную томографию головы. Пациенты жалуются на частые и упорные носовые кровотечения, кровоточивость десен, нарушения аппетита, кровохарканье. При осмотре выявляются различные типы телеангиэктазий на коже лица, туловища, шеи, слизистых оболочках рта и носовой полости. Эндоскопические исследования (ларингоскопия, бронхоскопия, ЭГДС) также выявляют сосудистые нарушения в гортани и трахее, желудочно-кишечном тракте, некоторые из них кровоточат.
Общий и биохимический анализы крови, часто назначаемые пациенту, могут не выявлять никаких нарушений, в том числе и патологий системы гемостаза. Лишь при выраженных кровотечениях сначала проявляются признаки хронической железодефицитной анемии - уменьшение уровня гемоглобина, количества эритроцитов, снижение цветового показателя. Однако в случае развития артериовенозных шунтов в легких может наблюдаться обратная картина полицитемии. В случае дальнейшего нарастания частоты и объемов кровотечений к анемическим симптомам присоединяются и признаки нарушения системы гемостаза - уменьшение уровня тромбоцитов и других факторов свертываемости. Это связано с развитием коагулопатии потребления, свидетельствующей о тяжелой форме болезни Рандю-Ослера-Вебера.
В случае составления наследственного анамнеза и выявления у родственников признаков болезни Рандю-Ослера-Вебера необходимо производить профилактические медицинские обследования с детства. Особенно это необходимо при наличии в симптомокомплексе церебральных нарушений - в таком случае, начиная с подросткового возраста, нужно производить профилактическую магнитно-резонансную томографию. На МРТ и КТ головного мозга могут выявляться субарахноидальные кровотечения и признаки абсцесса мозга. Своевременное выполнение профилактических обследований может выявить подобные изменения на раннем этапе, что позволит их успешно устранить без тяжелых последствий для пациента.
Лечение и прогноз болезни Рандю-Ослера-Вебера
Специфического лечения болезни Рандю-Ослера-Вебера не существует, в основном прибегают к поддерживающим мерам. Носовые кровотечения лучше всего останавливать путем лазерной абляции, однако и она не защитит от их рецидива. Кратковременный эффект остановки геморрагии может дать орошение полости носа охлажденным раствором аминокапроновой кислоты, поэтому специалисты рекомендуют больным постоянно иметь его дома. В случае развития легочных и желудочно-кишечных кровотечений их можно остановить эндоскопическими техниками, а при их обильности прибегают к помощи хирургов. Хирургическое вмешательство также показано при таких осложнениях болезни Рандю-Ослера-Вебера, как право-левое шунтирование и субарахноидальное кровоизлияние. Кроме того, назначается поддерживающее лечение витаминами и препаратами железа при анемии. В тяжелых случаях прибегают к переливанию крови или эритроцитарной массы.
Прогноз болезни Рандю-Ослера-Вебера во многих случаях неопределенный, так как все зависит от степени выраженности сосудистых нарушений. Прояснить картину в этом отношении может помочь наследственный анамнез - как правило, симптоматика патологии у родственников довольно сходная. Резко ухудшает прогноз превалирование церебральных проявлений заболевания, которые часто приводят к эпилепсии, инсультам, абсцессам мозга. При развитии даже незначительного носового кровотечения больные должны в срочном порядке обращаться в медицинские учреждения, поскольку остановить его в домашних условиях нередко не представляется возможным.
Читайте также:
