Состояние воспалительной реакции кишечника у недоношенных новорожденных детей
Добавил пользователь Алексей Ф. Обновлено: 28.01.2026
Некротический энтероколит новорожденных (НЭК) - это неспецифическое заболевание воспалительного характера, которое вызывается инфекционными агентами на фоне повреждения слизистой оболочки кишечника или ее функциональной незрелости. Симптомы включают соматические реакции и абдоминальные проявления. При длительном течении наблюдаются признаки перфорации кишечника и клиника перитонита. Диагностика НЭК сводится к физикальному обследованию, оценке симптомов по шкале Walsh и Kliegman и рентгенографии. Лечение зависит от стадии заболевания, может быть как консервативным, так и хирургическим.

Общие сведения
Некротический энтероколит новорожденных или «болезнь выживших недоношенных» - это гетерогенная патология, которая характеризуется развитием язв и некрозов стенки кишечника с дальнейшей перфорацией. Более 90% больных детей - недоношенные, с массой тела до 1500г. Общая заболеваемость составляет 0,5-3 на 1000 новорожденных. Прогноз, как правило, неясен, т. к. для НЭК характерно резкое ухудшение состояния на фоне мнимого благополучия. Часто требуется хирургическое вмешательство. Летальность в зависимости от формы колеблется от 25 до 55%. Даже после успешного проведения операции показатель смертности составляет свыше 60%. При условии выживания ребенка наблюдается тяжелый период реабилитации, остается высокий риск послеоперационных осложнений.
Причины НЭК новорожденных
Некротический энтероколит новорожденных - полиэтиологическое заболевание. Основными патогенетическими факторами являются гипоксия и ишемия в перинатальном периоде, нерациональное питание новорожденного и заселение кишечника аномальными микроорганизмами. К способствующим факторам относятся преждевременные роды, эклампсия, травмы ЦНС при родах, иммунодефицитные состояния у ребенка, аномалии развития кишечника, отягощенный семейный анамнез.
Ишемия кишечника может быть обусловлена внутриутробной асфиксией плода, при которой наблюдается централизация кровообращения, постановкой катетера в пупочную артерию, влекущей за собой спазм артерий и их тромбоэмболию, явлением «сгущения крови» и артериальной гипотензией, при которых нарушается ток крови и поступление питательных веществ. К алиментарным причинам развития некротического энтероколита новорожденных относят питание ребенка искусственными смесями и их резкую смену, использование гипертонических растворов, повреждающих слизистую оболочку кишечника, врожденную непереносимость молока, непосредственную инвазию патогенных агентов через ЖКТ. Наиболее часто причиной НЭК становятся Kl. pneumonia, E. coli, клостридии, стафилококки, стрептококки и грибы рода Candida.
Классификация НЭК новорожденных
По скорости развития выделяют следующие формы некротического энтероколита новорожденных:
В зависимости от массивности поражения различают следующие варианты НЭК:
- Локальный. Патологические изменения наблюдаются на ограниченном отрезке кишечника.
- Полисегментарный. Характерно поражение сразу нескольких участков.
- Паннекроз или тотальный. В патологический процесс втягивается весь кишечник.
Симптомы и осложнения НЭК новорожденных
Некротический энтероколит новорожденных может возникать в первые 24 часа после родов (ранняя форма) или после 1 месяца жизни (поздняя форма), средний возраст детей на момент появления симптомов - 1-2 недели. Все проявления данной патологии можно разделить на 3 группы: соматические, абдоминальные, генерализованные. Первыми, как правило, появляются абдоминальные симптомы, которые почти сразу дополняются соматическими. Генерализованные проявления НЭК отмечаются при прогрессировании заболевания и возникновении перфорации кишечника, что, в зависимости от формы, может происходить через 1-3 дня.
В группу соматических симптомов входят патологические реакции организма на развитие НЭК: приступы апноэ, респираторный дистресс, олигурия, ухудшение микроциркуляции (позитивный симптом «белого пятна»). К абдоминальным признакам НЭК относятся симптомы раздражения брюшной полости и дисфункция ЖКТ: потеря аппетита, метеоризм, рвота желчью и кровью, отсутствие перистальтических шумов, мелена, асцит, покраснение кожи, отечность подкожной жировой клетчатки и резкое напряжение мышц передней брюшной стенки. Нарушения в организме ребенка, возникшие в результате прогрессирования некротического энтероколита новорожденных, объединяют в группу генерализованных проявлений. Сюда входят гипертермия, переходящая в гипотермию, артериальная гипотония, бледность и диффузный цианоз, выраженная вялость и сонливость, ДВС-синдром, дыхательная и сердечно-сосудистая недостаточность.
Большинство осложнений некротического энтероколита новорожденных, как правило, развиваются после проведенного хирургического лечения. Наиболее часто после оперативного вмешательства возникает кишечный свищ, синдром «укороченной кишки», хроническая диарея, демпинг-синдром, обезвоживание, синдром мальабсорбции, стриктура толстого кишечника, абсцесс, задержка физического развития. Также при НЭК могут встречаться патологические состояния, вызванные полным парентеральным питанием: дефицит витамина D (рахит), поражение печени (гепатит) и костей (деминерализация).
Диагностика НЭК новорожденных
Диагностика некротического энтероколита новорожденных включает в себя сбор анамнеза, клиническое, лабораторное и инструментальное обследование. Анамнестические данные могут помочь педиатру и детскому хирургу установить возможную этиологию, проследить за динамикой заболевания. При объективном осмотре выявляются присутствующие на данный момент клинические симптомы - абдоминальные, соматические и генерализованные проявления. Специфических лабораторных тестов для подтверждения НЭК не существует. Информативными являются следующие данные, полученные при проведении лабораторных исследований: лейкоцитоз со сдвигом формулы влево, лейкопения и тромбоцитопения в ОАК, ацидоз и гипоксемия при определении газового состава крови, гиперкалиемия и гипонатриемия в электролитном спектре, диспротеинемия и выявления С-реактивного протеина в белковом спектре, обнаружение крови в кале при пробе Грегерсена. С целью выявления инфекционного возбудителя проводится бактериальный посев, ИФА и ПЦР.
Ведущую роль в диагностике некротического энтероколита новорожденных играют инструментальные методы: рентгенография, УЗИ, КТ и МРТ. Они дают возможность визуализировать отек стенок кишечного тракта, плюс-ткань, наличие воздуха в брюшной полости, в просвете портальной или печеночной вен, а также отсутствие перистальтики на серии последовательных снимков. В педиатрии для подтверждения диагноза «некротический энтероколит новорожденных» и определения стадии заболевания применяется шкала Walsh и Kliegman. При использовании данной шкалы учитываются присутствующие у ребенка соматические симптомы, проявления со стороны желудочно-кишечного тракта и рентгенологические признаки. В зависимости от количества и выраженности проявлений выделяют подозреваемый НЭК (1а и 2а ст.), явный НЭК (2а и 2б ст.), прогрессирующий НЭК (3а и 3б ст.). Это имеет существенное значение при выборе тактики лечения.
Дифференциальная диагностика некротического энтероколита новорожденных проводится с такими патологиями как неонатальный сепсис, пневмония, пневмоперитонеум, кишечная непроходимость различного генеза, аппендицит новорожденного, бактериальный перитонит и спонтанная перфорация кишечника.
Лечение НЭК новорожденных
Тактика лечения некротического энтероколита новорожденных зависит от тяжести состояния ребенка и стадии заболевания. Детям с 1а, 1б и 2а стадиями показана консервативная терапия. С момента постановки диагноза отменяется энтеральное питание и проводится постановка назо- или орогастрального зонда с целью декомпрессии. Ребенок переводится на полное парентеральное питание (TPN) в соответствии с клиническими протоколами. Параллельно назначаются антибактериальные препараты из групп пенициллинов (ампициллин) и аминогликозидов II поколения (гентамицин) в комбинации с медикаментами, действующими на анаэробную микрофлору (метронидазол). При неэффективности выбранной антибиотикотерапии применяют цефалоспорины III-IV поколения (цефтриаксон) в сочетании с аминогликозидами III поколения (амикацин). Таким детям рекомендованы пробиотики и эубиотики для нормализации кишечной микрофлоры. Также проводят СВЧ-терапию, вводят иммуномодуляторы и гамма-глобулины.
Детям с 2б, 3а и 3б стадиями показано хирургическое вмешательство. Объем операции зависит от распространенности поражения кишечника. Как правило, проводится экономная резекция пораженного участка с формированием энтеростомы или колостомы. При локальных формах НЭК возможно наложение анастомоза по типу «конец в конец». После операции назначается инфузионная терапия и медикаментозное лечение, аналогичное более ранним стадиям.
Прогноз и профилактика НЭК новорожденных
Исход НЭК зависит от тяжести общего состояния ребенка и стадии заболевания. Так как данные показатели почти всегда отличаются нестабильностью, прогноз считается сомнительным даже на фоне полноценного лечения. Профилактика некротического энтероколита новорожденных включает в себя антенатальную охрану здоровья плода, рациональное ведение беременности, грудное вскармливание в физиологических объемах. Согласно некоторым исследованиям, риск развития заболевания снижается при использовании эубиотиков, пробиотиков и IgA у детей из группы риска. При высоком риске преждевременных родов применяют глюкокортикостероиды с целью профилактики РДС.
Недоношенные дети
Недоношенные дети - это дети, родившиеся ранее срока родов, функционально незрелые, с массой ниже 2500 г и длиной тела менее 45 см. Клинические признаки недоношенности включают непропорциональное телосложение, открытые швы черепа и малый родничок, невыраженность подкожно-жирового слоя, гиперемию кожных покровов, недоразвитие половых органов, слабость или отсутствие рефлексов, слабый крик, интенсивную и длительную желтуху и др. Выхаживание недоношенных детей подразумевает организацию специального ухода - температурного режима, влажности, уровня оксигенации, вскармливания, при необходимости - проведение интенсивной терапии.
Недоношенными считаются дети, рожденные в период с 28 по 37 неделю беременности, имеющие массу тела 1000-2500 г и длину тела 35-45 см. Наиболее устойчивым критерием считается срок гестации; антропометрические показатели, в силу их значительной вариабельности, относятся к условным критериям недоношенности. Ежегодно в результате самопроизвольных преждевременных родов или искусственно индуцированного прерывания беременности на поздних сроках недоношенными появляются на свет 5-10% детей от общего числа новорожденных.
По определению ВОЗ (1974 г.), плод считается жизнеспособным при гестационном сроке более 22 недель, массе тела от 500 г, длине тела от 25 см. В отечественной неонатологии и педиатрии рождение плода ранее 28 недели гестации, имеющего массу тела менее 1000 г и длину менее 35 см расценивается как поздний выкидыш. Однако, если такой ребенок родился живым и прожил после рождения не менее 7 суток, он регистрируется как недоношенный. Уровень неонатальной смертности среди недоношенных детей намного выше такового среди доношенных младенцев, и в значительной мере зависит от качества оказания медицинской помощи в первые минуты и дни жизни ребенка.
Причины недоношенности
Все причины, приводящие к рождению недоношенных детей можно объединить в несколько групп. К первой группе относятся социально-биологические факторы, включающие слишком юный или пожилой возраст родителей (моложе 18 и старше 40 лет), вредные привычки беременной, недостаточное питание и неудовлетворительные бытовые условия, профессиональные вредности, неблагоприятный психоэмоциональный фон и др. Риск преждевременного родоразрешения и рождения недоношенных детей выше у женщин, не планировавших беременность и пренебрегающих медицинским сопровождением беременности.
Вторую группу причин составляет отягощенный акушерско-гинекологической анамнез и патологическое течение настоящей беременности у будущей мамы. Здесь наибольшее значение имеют аборты в анамнезе, многоплодие, гестозы, гемолитическая болезнь плода, преждевременная отслойка плаценты. Причиной рождения недоношенных детей могут служить непродолжительные (менее 2-х лет) интервалы между родами. Нередко недоношенные дети рождаются у женщин, прибегающих к экстракорпоральному оплодотворению, однако это связано не с самим фактом использования ВРТ, а скорее - с «женским» фактором, препятствующим оплодотворению естественным путем. Неблагоприятно на вынашивании беременности сказываются гинекологические заболевания и пороки развития гениталий: цервицит, эндометрит, оофорит, фиброма, эндометриоз, двурогая седловидная матка, гипоплазия матки и др.
К третьей группе причин, нарушающих нормальное созревание плода и обуславливающих повышенную вероятность рождения недоношенных детей, относятся различные экстрагенитальные заболевания матери: сахарный диабет, гипертоническая болезнь, пороки сердца, пиелонефрит, ревматизм и др. Часто преждевременные роды провоцируются острыми инфекционными заболеваниями, перенесенными женщиной на поздних сроках гестации.
Наконец, рождение недоношенных детей может быть связано с патологией и аномальным развитием самого плода: хромосомными и генетическими болезнями, внутриутробными инфекциями, тяжелыми пороками развития.
Классификация недоношенности
С учетом обозначенных критериев (срока гестации, массы и длины тела) выделяют 4 степени недоношенности:
I степень недоношенности - родоразрешение происходит на сроке 36-37 недель гестации; масса тела ребенка при рождении составляет 2500-2001 г, длина - 45-41 см.
II степень недоношенности - родоразрешение происходит на сроке 32-35 недель гестации; масса тела ребенка при рождении составляет 2001-2500 г, длина - 40-36 см.
III степень недоношенности - родоразрешение происходит на сроке 31-28 недель гестации; масса тела ребенка при рождении составляет 1500-1001 г, длина - 35-30 см.
IV степень недоношенности - родоразрешение происходит ранее 28 недель гестации; масса тела ребенка при рождении составляет менее 1000 г, длина - менее 30 см. В отношении таких детей используется термин «недоношенные с экстремально низкой массой тела».
Внешние признаки недоношенности
Для недоношенных детей характерен ряд клинических признаков, выраженность которых коррелирует со степенью недоношенности.
У глубоко недоношенных детей все роднички и швы черепа открыты, черепные кости податливые, мозговой череп преобладает над лицевым. Характерно недоразвитие ушных раковин, слабое развитие ногтей (ногтевые пластинки не доходят до кончиков пальцев), слабая пигментация сосков и околососковых кружков. Половые органы у недоношенных детей недоразвиты: у девочек отмечается зияние половой щели, у мальчиков - неопущение яичек в мошонку (крипторхизм).
Недоношенные дети, рожденные на сроке 33-34 недели гестации и позже, характеризуются большей зрелостью. Их внешний облик отличается розовым цветом кожных покровов, отсутствием пушка на лице и туловище, более пропорциональным телосложением (меньшей головой, более высоким расположением пупка и пр.). У недоношенных детей I-II степени сформированы изгибы ушных раковин, выражена пигментация сосков и околососковых кружков. У девочек большие половые губы практически полностью прикрывают половую щель; у мальчиков яички расположены у входа в мошонку.
Анатомо-физиологические особенности недоношенных детей
Недоношенность определяется не столько антропометрическими показателями, сколько морфофункциональной незрелостью жизненно важных органов и систем организма.
Характерными особенностями органов дыхания у недоношенных детей являются узость верхних дыхательных путей, высокое стояние диафрагмы, податливость грудной клетки, перпендикулярное расположение ребер относительно грудины. Данные морфологические особенности недоношенных детей обусловливают поверхностное, частое, ослабленное дыхание (40-70 в мин.), склонность к апноэ длительностью 5-10 секунд (апноэ недоношенных). Вследствие недоразвития эластической ткани легких, незрелости альвеол, сниженного содержания сурфактанта у недоношенных детей легко возникает синдром дыхательных расстройств (застойные пневмонии, респираторный дистресс-синдром).
Незрелость сердечно-сосудистой системы характеризуется лабильностью пульса, тахикардией 120-180 в мин., приглушенностью сердечных тонов, артериальной гипотонией (55-65/20-30 мм рт. ст.). При наличии врожденных пороков сердца (открытого Боталлова протока, открытого овального окна) могут выслушиваться шумы. Вследствие повышенной ломкости и проницаемости сосудистых стенок легко возникают кровоизлияния (подкожные, во внутренние органы, в мозг).
Морфологическими признаками незрелости ЦНС у недоношенных детей служат слабая дифференцировка серого и белого вещества, сглаженность борозд мозга, неполная миелинизация нервных волокон, обедненная васкуляризация подкорковых зон. Мышечный тонус у недоношенных детей слабый, физиологические рефлексы и двигательная активность снижены, реакция на раздражители замедлена, терморегуляция нарушена, имеется склонность как к гипо-, так и гипертермии. В первые 2-3 недели у недоношенного ребенка могут возникать преходящий нистагм и косоглазие, тремор, вздрагивания, клонус стоп.
У недоношенных детей отмечается функциональная незрелость всех отделов желудочно-кишечного тракта и низкая ферментовыделительная активность. В связи с этим недоношенные дети предрасположены к срыгиваниям, развитию метеоризма, дисбактериоза. Желтуха у недоношенных детей выражена интенсивнее и сохраняется дольше, чем у доношенных новорожденных. Вследствие незрелости ферментных систем печени, повышенной проницаемости гематоэнцефалического барьера и бурного распада эритроцитов у недоношенных детей может легко развиваться билирубиновая энцефалопатия.
Функциональная незрелость почек у недоношенных детей приводит к изменению электролитного баланса (гипокальциемии, гипомагниемии, гипернатриемии, гиперкалиемии), декомпенсированному метаболическому ацидозу, склонности к возникновению отеков и быстрому обезвоживанию при неадекватном уходе.
Деятельность эндокринной системы характеризуется задержкой становления циркадного ритма выделения гормонов, быстрым истощением желез. У недоношенных детей отмечается низкий синтез катехоламинов, часто развивается транзиторный гипотиреоз, в первые дни жизни редко проявляется половой криз (физиологический мастит, физиологический вульвовагинит у девочек).
У недоношенных детей более быстрыми темпами, чем у доношенных, развивается ранняя анемия, имеется повышенный риск развития септицемии (сепсиса) и септикопиемии (гнойного менингита, остеомиелита, язвенно-некротического энтероколита).
В течение первого года жизни нарастание массы и длины тела у недоношенных детей происходит очень интенсивно. Однако по антропометрическим показателям недоношенные дети догоняют рожденных в срок сверстников только к 2-3 годам (иногда к 5-6 годам). Отставание в психомоторном и речевом развитии у недоношенных детей зависит от степени недоношенности и сопутствующей патологии. При благоприятном сценарии развития недоношенного ребенка выравнивание происходит на 2-ом году жизни.
Дальнейшее физическое и психомоторное развитие недоношенных детей может идти наравне со сверстниками или запаздывать.
Среди недоношенных детей чаще, чем среди доношенных сверстников встречаются неврологические нарушения: астено-вегетативный синдром, гидроцефалия, судорожный синдром, вегето-сосудистая дистония, детский церебральный паралич, гиперактивность, функциональная дислалия либо дизартрия. Почти у трети недоношенных детей обнаруживается патология органа зрения - близорукость и астигматизм различной степени выраженности, глаукома, косоглазие, отслойка сетчатки, атрофия зрительного нерва. Недоношенные дети склонны к частым повторным ОРВИ, отитам, на фоне чего может развиваться тугоухость.
Женщины, родившиеся недоношенными, во взрослой жизни часто страдают нарушениями менструального цикла, признаками полового инфантилизма; у них может отмечаться угроза самопроизвольного прерывания беременности и преждевременных родов.
Особенности ухода за недоношенными детьми
Дети, рожденные недоношенными, нуждаются в организации особого ухода. Их поэтапное выхаживание осуществляется специалистами неонатологами и педиатрами сначала в родильном доме, затем в детской больнице и поликлинике. Основными составляющими ухода за недоношенными детьми являются: обеспечение оптимального температурно-влажностного режима, рациональной кислородотерапии и дозированного вскармливания. У недоношенных детей осуществляется постоянный контроль электролитного состава и КОС крови, мониторирование газового состава крови, пульса и АД.
Глубоко недоношенные дети сразу после рождения помещаются в кувезы, где с учетом состояния ребенка поддерживается постоянная температура (32-35°С), влажность (в первые дни около 90%, затем 60-50%), уровень оксигенации (около 30%). Недоношенные дети I-II степени обычно размещаются в кроватках с обогревом или в обычных кроватках в специальных боксах, где поддерживается температура воздуха 24-25°С.
Недоношенные дети, способные самостоятельно поддерживать нормальную температуру тела, достигшие массы тела 2000 г, имеющие хорошую эпителизацию пупочной ранки, могут быть выписаны домой. Второй этап выхаживания в специализированных отделениях детских стационаров показан недоношенным, не достигшим в первые 2 недели массы тела 2000 г, и детям с перинатальной патологией.
Кормление недоношенных детей следует начинать уже в первые часы жизни. Дети с отсутствующим сосательным и глотательным рефлексами получают питание через желудочный зонд; если сосательный рефлекс выражен достаточно, но масса тела менее 1800 г - ребенка вскармливают через соску; дети с массой тела свыше 1800 г могут быть приложены к груди. Кратность кормлений недоношенных детей I-II степени 7-8 раз в сутки; III и IV степени - 10 раз в сутки. Расчет питания производится по специальным формулам.
Недоношенные дети с физиологической желтухой, должны получать фототерапию (общее УФО). В рамках реабилитации недоношенных детей на втором этапе полезно общение ребенка с матерью, контакт «кожа к коже».
Диспансеризация недоношенных детей
После выписки дети, рожденные недоношенными, нуждаются в постоянном наблюдении педиатра в течение первого года жизни. Осмотры и антропометрия проводятся еженедельно в первый месяц, 1 раз в две недели - в первом полугодии, 1 раз в месяц - во втором полугодии. На первом месяце жизни недоношенные дети должны быть осмотрены детским хирургом, детским неврологом, детским травматологом-ортопедом, детским кардиологом, детским офтальмологом. В возрасте 1 года детям необходима консультация логопеда и детского психиатра.
С 2-недельного возраста недоношенные дети нуждаются в профилактике железодефицитной анемии и рахита. Профилактические прививки недоношенным детям выполняются по индивидуальному графику. На первом году жизни рекомендуются повторные курсы детского массажа, гимнастики, индивидуальных оздоровительных и закаливающих процедур.
Сепсис новорожденных
Сепсис новорожденных - генерализованная гнойно-септическая инфекция, характеризующаяся наличием первичного очага и циркуляцией инфекции в крови. Сепсис новорожденных проявляется признаками инфекционного токсикоза (температурной реакцией, вялостью, диспепсией, землистой окраской кожных покровов) и образованием гнойных метастатических очагов в различных органах (мозговых оболочках, легких, костях, печени и пр.). Диагноз сепсиса у новорожденных устанавливается на основании клинических критериев и выделения возбудителя при бактериологическом посеве крови. Лечение сепсиса новорожденных включает системную антибиотикотерапию, санацию первичного и метастатических гнойных очагов, посиндромную терапию.
Сепсис новорожденных - общий инфекционный процесс, обусловленный попаданием условно-патогенной и гноеродной микрофлоры из локальных очагов в кровяное русло и сопровождающийся тяжелыми системными проявлениями. По данным зарубежной педиатрии, частота сепсиса новорожденных составляет 0,1-0,8%; среди недоношенных и детей с перинатальной патологией, находящихся в ОРИТ, - 14%. Неонатальная смертность, обусловленная сепсисом новорожденных, высока и стабильна - около 30-40%. Развитию сепсиса способствуют недостаточная сформированность барьерных механизмов и иммунитета у новорожденных, пограничные состояния периода новорожденности, патологическое протекание перинатального периода, сложность ранней диагностики септических состояний.
Причины
В настоящее время доминирующее место (около 50%) среди возбудителей сепсиса новорожденных принадлежит грамположительной флоре (главным образом, стафилококкам, гемолитическому стрептококку группы А). Чуть реже (до 40% случаев) выявляется грамотрицательная микрофлора (кишечная палочка, синегнойная палочка, клебсиелла и др.); в 10% этиологическими агентами выступает смешанная флора (часто ассоциация стафилококка с грибами Candida).
Со стороны матери факторами, способствующими бактериальной контаминации новорожденного, выступают бактериальный вагиноз, кольпиты, эндометрит. Большое значение имеет степень и характер иммуносупрессии у новорожденного, которые могут быть связаны с неполноценным питанием или приемом лекарств беременной, наследственным иммунодефицитом или ВИЧ-инфекцией. В отдельных случаях причиной вспышек сепсиса новорожденных становится несоблюдение санитарного режима в родильных или детских отделениях.
Классификация
По времени развития выделяют внутриутробный и постнатальный (ранний неонатальный и поздний неонатальный) сепсис новорожденных. Внутриутробный сепсис предполагает антенатальное или интранатальное инфицирование плода; при этом первичный гнойно-септический очаг располагается вне организма ребенка (чаще всего в его роли выступает плацентит, хорионит, хориоамнионит и т. д.). В случае постнатального сепсиса первичный гнойно-воспалительный очаг всегда располагается в организме самого новорожденного.
Ранний неонатальный сепсис новорожденных развивается в первые 4-ро суток жизни ребенка. Клинические течение заболевания обычно молниеносное, с быстрым развитием полиорганнной недостаточности, летальным исходом в 5-20% случаев. Поздний неонатальный сепсис новорожденных манифестирует на 5-й день и позднее. Характеризуется медленно прогрессирующим течением, возникновением вторичных септических очагов, 5-10%-ной летальностью.
Течение сепсиса новорожденных может быть молниеносным (3-7 дней), острым (до 4-8 недель), подострым (до 1,5-3 месяцев), затяжным (более 3 месяцев). С учетом локализации первичного септического очага и входных ворот различают: пупочный, кожный, легочный, ринофарингеальный, отогенный, риноконъюнктивальный, кишечный, урогенный, катетеризационный и др. виды сепсиса новорожденных. Сепсис новорожденных может протекать в форме септицемии или септикопиемии.
Симптомы сепсиса новорожденных
Септицемия или сепсис новорожденных без метастазов обычно развивается на фоне предшествующего мокнущего пупка, конъюнктивита, гнойничковой сыпи, опрелостей, стоматита. Предвестниками сепсиса новорожденных могут выступать вялость или беспокойство, снижение аппетита, обильные частые срыгивания, плохая прибавка в весе. В период разгара развивается температурная реакция (гипер- или гипотермия), отечный синдром или эксикоз, гипотрофия. Характерным признаком сепсиса новорожденных является грязновато-серый (землистый) оттенок кожных покровов, желтушность, мраморность кожи, сыпь.
Вследствие токсического поражения различных органов возникают гепатоспленомегалия, пневмопатия (тахипноэ, цианоз), кардиопатия (тахикардия или брадикардия, артериальная гипотензия), диспепсия, мочевой синдром (олигурия, анурия, ОПН), геморрагический синдром, надпочечниковая недостаточность. Чаще всего септицемия осложняется присоединением пневмонии, которая выступает как самостоятельное интеркуррентное заболевание.
Септикопиемия или сепсис новорожденных с гнойными метастазами характеризуется возникновением на фоне интоксикации вторичных очагов отсева в мозговых оболочках, легких, костях, печени, других органах. Чаще всего септикопиемия протекает с развитием гнойного менингита, абсцедирующей пневмонии, остеомиелита; реже - с формированием абсцесса печени, гнойного артрита, панофтальмита, медиастинита, флегмоны желудка или кишечника. В восстановительном периоде происходит санация пиемических очагов, стихание токсикоза, постепенное восстановление нарушенных функций.
Молниеносная форма сепсиса новорожденных протекает с развитием септического шока: стремительным ухудшением состояния ребенка, снижением температуры тела, брадикардией, кровоточивостью, отеком легких, острой почечной недостаточностью. Летальный исход при молниеносном течении сепсиса новорожденных наступает в течение 3-5 суток.
Диагностика сепсиса новорожденных
Диагноз сепсиса новорожденного может быть заподозрен неонатологом или педиатром на основании лихорадки свыше 3 дней или прогрессирующей гипотермии; гиперлейкоцитоза, сменяющегося лейкопенией; повышением содержания в крови маркеров инфекционного процесса (СРБ, интерлейкина-8, прокальцитонина).
Факт бактериемии при сепсисе новорожденных подтверждается путем посева крови на стерильность. Важное значение имеет выявление первичного гнойного очага и метастатических очагов, микробиологического исследование отделяемого из них (бактериологическое исследование мазка с конъюнктивы, мочи на микрофлору, соскоба/отделяемого с кожи на микрофлору, мазка из глотки, кала на дисбактериоз и т. п.).
Дифференциальная диагностика сепсиса новорожденных осуществляется с локализованными гнойно-воспалительными заболеваниями (пневмонией, медиастинитом, перитонитом, менингитом, энтероколитом), генерализованными вирусными инфекциями (цитомегалией, герпесом, энтеровирусной инфекцией) и микозами (кандидозом, аспергиллезом) и др. Для этого используются дополнительные лабораторные методы - ПЦР, ИФА, микроскопия.
Лечение сепсиса новорожденных
Терапия при сепсисе новорожденных проводится одновременно в нескольких направлениях и включает санацию септического и пиемических очагов, подавление циркуляции возбудителя в крови, коррекцию нарушенных функций.
Основу этиологического лечения сепсиса новорожденных составляет антибиотикотерапия: эмпирическая комбинированная до уточнения характера микрофлоры) и целенаправленная после получения антибиотикограммы. Противомикробные препараты вводятся внутривенно, в максимальных возрастных дозировках в течение 10-15 суток с последующей сменой. Чаще всего в клинической практике для лечения сепсиса новорожденных в различных сочетаниях используются цефалоспорины, аминогликозиды, аминопенициллины, карбапенемы и др.
С целью местного лечения гнойных очагов производится вскрытие фурункулов и абсцессов, перевязки с антибактериальными и ферментными препаратами; назначается УВЧ, СВЧ, электрофорез.
Патогенетическая терапия сепсиса новорожденных включает иммунокоррекцию (плазмаферез, гемосорбцию, введение иммуноглобулинов), проведение дезинтоксикационной терапии (внутривенной инфузии глюкозо-солевых растворов и свежезамороженной плазмы), адекватную кислородотерапию и т. д. При сепсисе новорожденных обязательно проводится мониторинг состояния жизненно-важных функций: АД, ЧСС, ЭКГ, КОС и газового состава крови, биохимических показателей (сахара крови, креатинина, электролитов), гематокрита.
В остром периоде сепсиса целесообразно пребывание новорожденных в кувезе, кормление материнским молоком, тщательный уход. В восстановительном периоде к лечению подключается гимнастика, массаж, лечебные ванны.
Прогноз и профилактика сепсиса новорожденных
Прогноз сепсиса новорожденных серьезный: летальность составляет от 30-40% до 60% среди глубоко недоношенных детей. У выздоровевших детей в отделенном периоде могут отмечаться частые ОРВИ, пиелонефрит, анемия, перинатальная энцефалопатия.
Профилактика сепсиса новорожденных включает выявление и санацию инфекций мочеполовой сферы у беременной, соблюдение противоэпидемических мероприятий медперсоналом родильных домов и отделений новорожденных, тщательный гигиенических уход за новорожденным, естественное вскармливание. Вопрос о сроках вакцинации новорожденных с сепсисом против туберкулеза и против гепатита В , проводимой в первые дни жизни, решается в индивидуальном порядке.
Воспаление кишечника у детей: когда нужна запись к педиатру?
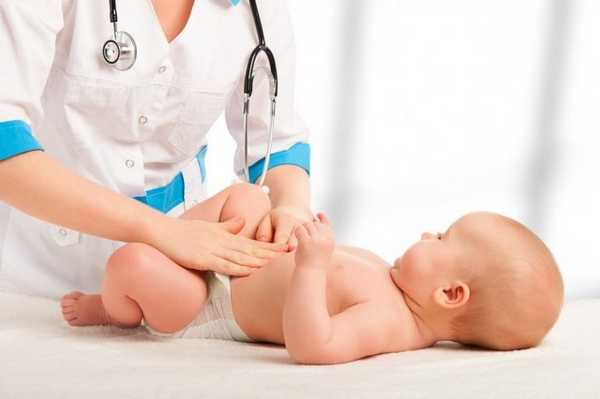
В раннем детстве, когда ребёнок только появился на свет, у него могут развиваться различные патологии, опасные для здоровья. Но особенно опасно развитие острого воспаления кишечника (некротизирующего энтероколита), особенно у недоношенных малышей. Обычно проблема возникает с увеличением объёма питания, на фоне дефицита кислорода в стенках кишки активизируется инфекция, которая может привести к перфорации кишечника. поэтому важно знать тревожные признаки, при которых нужна немедленная запись к педиатру или вызов скорой помощи, а также профилактика, в том числе и за счет грудного вскармливания и режимных мероприятий.
Тревожные признаки: запись к педиатру
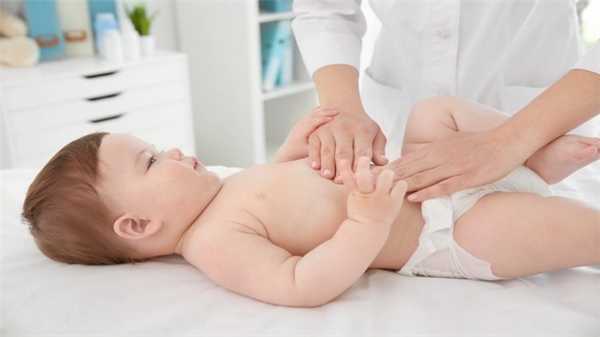
Любые признаки беспокойства и нарушения стула должны стать поводом для записи к педиатру. Важно обращать внимание на беспокойство ребёнка, вздутие живота и задержку стула по мере увеличения объёма питания. Немедленная запись к педиатру нужна при обнаружении в стуле прожилок крови на фоне вздутия, колик и прижимания ножек к животу. Малыш может постоянно плакать, много срыгивать. Если же открывается рвота, особенно с примесями желчи и слизи, нужна не запись к педиатру и ожидание приема, а вызов по телефону скорой помощи и немедленная госпитализация в стационар.
Диагностика воспаления кишечника в клинике
Опасно любое воспаление кишечной стенки, но особенно серьезна ситуация у недоношенных и ослабленных малышей, перенесших гипоксию, у них может выявляться НЭК (это некротизирующий энтероколит). Определить его может рентгенография или УЗИ брюшной полости, где определяется вздутие кишечных петель и расширение вен печени. В кишечнике, так же как и брюшной полости, будет содержаться большое количество газовых пузырьков, выделяемых бактериями внутри кишечника при развитии воспаления.
Диагностику НЭК можно разделить на три этапа в зависимости от степени активности воспаления и определяемых симптомов:
- Стадия 1 — подозрение на НЭК. У ребёнка будут проявляться неспецифические или общие симптомы, которые могут указывать на некротический энтероколит. Симптомы включают вялость, суетливость и лихорадку. Рентген на этой стадии показывает вздутие живота или расширение желудка, но воспаление рентгенография не определяет.
- Стадия 2 — подтверждение НЭК. Рентген показывает четкие признаки поражения с наличием крупных газовых пузырей в кишечнике. Звуки кишечника будут отсутствовать из-за пареза кишки.
- Стадия 3 — осложнения НЭК. Кишечник поврежден до такой степени, что в стенке кишечника имеются отверстия, развивается перитонит (воспаление брюшины). У ребёнка также наблюдается сильное апноэ во сне, низкое кровяное давление и токсикоз.
Как лечится некротический энтероколит: подавление инфекции
Младенцы с НЭК должны быть госпитализированы. Врач примет во внимание возраст ребёнка, состояние здоровья, стадию НЭК и толерантность к различным лекарствам до начала лечения. Лечение включает в себя следующие этапы и методы:
- Прекращение кормлений, чтобы желудок был пуст, ребёнок получает необходимые жидкости и питательные вещества внутривенно.
- Назогастральный зонд, вставленный из носа в желудок, позволяет отсасывать газ, образующийся в брюшной полости. Это снимает отек, вздутие живота и помогает ребёнку бороться с инфекцией.
- Курс антибиотика, часто назначаемый внутривенно необходим для того, чтобы была подавлена инфекция, провоцирующая воспаление кишки.
- В крайних случаях ребёнка помещают на ИВЛ, чтобы легкие и кровь получали достаточное количество кислорода.
Операция необходима только в тяжелых случаях НЭК. Детский хирург удаляет участок кишечника, где инфекция образовала дефекты стенки, сшивает остальную часть желудочно-кишечного тракта. Хирурги стремятся удалить как можно меньше толстой кишки и сохранить как можно больше ее ткани. Если кишечник кажется здоровым и может пережить инфекцию, тогда хирурги удаляют только газ и откачивают жидкость из желудочно-кишечного тракта. Менее 25% детей нуждается в хирургическом вмешательстве, а остальные лечатся за счет терапии и антибиотиков. Продолжительность лечения и скорость выздоровления варьирует у каждого пациента, и может потребоваться от нескольких недель до нескольких месяцев, чтобы желудочно-кишечный тракт ребёнка восстановился.
За ребёнком, возможно, придется наблюдать в течение всего периода детства, нужна запись к педиатру, чтобы предотвратить возникновение других инфекций и осложнений, связанных с НЭК. Врач может предоставить конкретные рекомендации по питанию и уходу за ребёнком. Своевременное лечение, наряду с последующим уходом, помогает предотвратить любые осложнения НЭК.
Осложнения НЭК: перитонит, нарушение усвоения питания
Без лечения НЭК может привести к следующим проблемам:
- Распространение инфекции. При отсутствии лечения в течение длительного времени бактерии из кишечника могут распространяться в другие части тела через кровоток. Широко распространенная инфекция органов и связанное с ней подавление иммунного ответа может вызвать смертельное заболевание, называемое сепсисом.
- Метаболические проблемы и нарушение усвоения питания. Так как кишечник не функционирует правильно, организм не может правильно усваивать питание. Это может привести к таким состояниям, как гипогликемия (низкий уровень сахара в крови), дефицит белка. НЭК может также привести к повышенной кислотности крови (ацидоз), что может повредить почки.
- Респираторные и сердечно-сосудистые проблемы. У ребёнка также высок риск развития проблем с сердцем и легкими из-за гипотонии и дыхательной недостаточности, когда организм не получает достаточного количества кислорода из легких.
Грудное вскармливание против НЭК
Нет единой профилактики некротического энтероколита, так как его причина неизвестна. Но определено достаточно четко, что грудное вскармливание снижает риск НЭК у недоношенных детей. Эксперты по педиатрии отмечают, что дети, находящиеся на исключительно грудном вскармливании, не подвержены такому риску НЭК, как искусственники. Недоношенным детям, которым дают пищу через трубку (энтеральное питание), следует давать сцеженное молоко, чтобы минимизировать риск НЭК. Грудное вскармливание также полезно для детей с низким весом при рождении. Исследование показало, что кормление детей с низкой массой тела при рождении питанием, состоящим по меньшей мере из 50% грудного молока, в первые 14 дней после рождения снижает риск развития НЭК в шесть раз.

Склонен ли ваш ребёнок к аллергическим заболеваниям и что является аллергеном? Пройдите тест и узнайте чего стоит ребёнку избегать и какие меры предпринять.
Некротизирующий энтероколит у ребенка: в чем причины воспаления?

Некротический энтероколит или НЭК является опасным для жизни состоянием, которое поражает недоношенных малышей или новорожденных. Болезнь может начинаться, как любая другая желудочно-кишечная инфекция, но острое воспаление, которое сопровождается нарушение притока крови к кишечной стенке, может в конечном итоге разрушить привести к образованию очагов некроза. Каковы причины некротического энтероколита у ребёнка, почему развивается воспаление, и чем оно опасно?
Некротический энтероколит у малыша: что это?

Некротический энтероколит — это острое воспаление желудочно-кишечного тракта, локализованное на участке тонкой или толстой кишки. При нем ткани страдает от гипоксии (дефицит притока крови), из-за чего возникает повреждение и гибель клеток. Сильное воспаление кишечника приводит к тому, что малыш не может полноценно усваивать пищу. Название формируется из трех терминов:
- «Некротический» — означает поврежденный, мертвый;
- «Энтеро» — поражение тонкой кишки;
- «Колит» — означает воспаление толстой кишки, которая является терминальной частью кишечника.
НЭК встречается у одного из каждых 2000-4000 новорожденных. Патология наиболее распространена среди недоношенных малышей с весом при рождении менее 2 кг. Малыш с массой тела менее 1,5 кг рискует еще больше в силу незрелости. Почти у 10% детей весом менее 1.5 кг со временем развивается некротический энтероколит. В 80% случаев страдают недоношенные малыши. НЭК редко встречается у малышей, рожденных с нормальной массой тела, и у детей более старшего возраста.
Каковы причины воспаления?
Точная причина некротического энтероколита у детей неизвестна. Эксперты, однако, подозревают, что снижение кровоснабжения кишечника создает условия для размножения бактерий, содержащихся в проглоченной пище, что приводит к воспалению. Дети, страдающие гипоксией (низкий уровень кислорода в крови) в силу каких-либо патологических состояний, также находятся в опасности. Кишечник не стерилен, в нем всегда присутствуют бактерии, и на фоне подавления местной иммунной защиты в силу нарушений кровообращения, они инициируют воспаление.
Острое активное воспаление при НЭК увеличивает риск перфорации стенки кишечника. Бактерии выходят через отверстия и проникают в другие органы брюшной полости, распространяя инфекцию и формируя острый перитонит. Энтероколит могут провоцировать несколько видов бактерий, но наиболее часто провокаторами являются E.coli, клостридии, клебсиелла и стафилококк.
Факторы риска развития НЭК: роль инфекции
Некоторые условия или ситуации могут сделать ребёнка более восприимчивым к развитию НЭК:
- Преждевременные роды. У недоношенных детей только частично развился и созрел желудочно-кишечный тракт, физиологически снижен иммунитет, что увеличивает шансы на развитие инфекции.
- Врожденные пороки развития. Наличие врожденных пороков, таких как проблемы с сердцем, дыхательная недостаточность, а также гипогликемия, могут повышать риск развития НЭК. Эти условия обычно вызывают снижение уровня кислорода в крови, что нарушает питание кишечной стенки.
- Инфекция в раннем детстве. Развивающиеся инфекции, особенно поражения желудочно-кишечного тракта, в раннем детстве могут увеличить шансы развития у ребёнка некротического энтероколита. Развитие сепсиса (серьезная генерализованная инфекция) также увеличивает риск.
- Материнские инфекции. Если мать перенесла инфекции во время беременности, то ребёнок рискует получить НЭК после рождения. Примером является амнионит, воспаление амниотического мешка, которое также может распространиться на плод.
Гипоксия: снижение кислорода в крови при НЭК
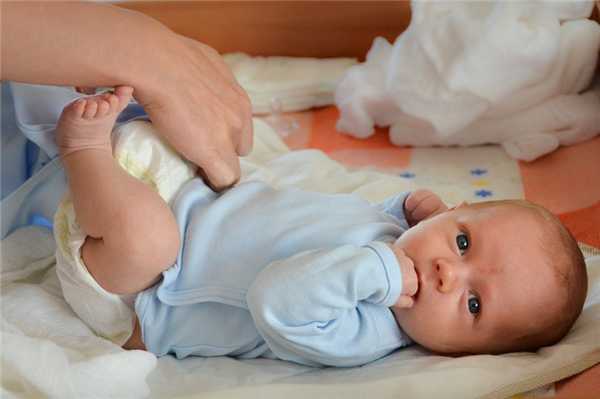
Особую роль в развитии НЭК играет кровь, а точнее низкий уровень кислорода в ней из-за врожденных проблем или патологий после рождения. Обычно гипоксию провоцируют проблемы во время родов: ребёнок, который не получает достаточного количества кислорода при рождении, может иметь низкий уровень кислорода в крови на протяжении нескольких часов или суток, что подвергает их риску возникновения НЭК. Длительные роды, узлы пуповины и асфиксия при родах, состояния, при которых ребёнок не получает достаточного количества кислорода во время родов силу того, что кровь поступает в очень ограниченном количестве, также провоцирует НЭК. Своевременное лечение НЭК жизненно важно для безопасности ребёнка. Если воспаление приводит к перфорации кишечника, это угрожает гибелью малыша.
Симптомы некротического энтероколита у ребёнка
Чем младше ребёнок, тем сложнее в ранней стадии определить НЭК. Для него типично вздутие живота и отек кишечной стенки. У ребёнка также будет боль в животе, он будет болезненным при прикосновении. Формируется задержка пищи в желудке и кишечнике, что означает, что питание не перерабатывается и не выходит в виде стула. Если у ребёнка отходит стул, то он будет содержать жидкую кровь или сгустки крови. Типична повторная рвота, содержимое будет зеленоватым или желтым из-за наличия желчи.
Кроме того, определяется учащенное и нерегулярное дыхание, может также возникать пауза в дыхании, которая называется апноэ. Формируется выраженная лихорадка с эпизодами повышения и снижения, вялость, суетливость и колики, ребёнок постоянно плачет или стонет.
Читайте также:
- Вызванная биоэлектрическая активность. Пневмоэнцефалографическое исследование при эпилепсии
- КТ, МРТ при инородном теле глазницы
- Одонтогенные опухоли и опухолеподобные образования. Фиброма полости рта.
- Ростовые факторы бактерий. Ауксотрофы. Прототрофы. Классификация факторов стимулирующих рост бактерий. Пусковые факторы роста бактерии.
- Ангиография в диагностике ранений шеи, груди, живота
