Дыхательная рентгенокимография. Анализ дыхательной рентгенокимографии
Добавил пользователь Евгений Кузнецов Обновлено: 28.01.2026
Заболевания органов дыхания на протяжении ряда лет являются наиболее актуальной проблемой современного здравоохранения. Во всем мире наблюдается рост острых и хронических респираторных заболеваний (ХРЗ). Особую значимость приобретает рост заболеваемости хронической обструктивной болезнью легких (ХОБЛ) и бронхиальной астмой (БА). Немаловажное значение при диагностике ХРЗ имеют лабораторные методы исследования. Особый вес они приобретают при дифференциальной диагностике патологий, т. к. большинство пульмонологических заболеваний имеют схожие респираторные проявления. В статье представлены основные лабораторные методы исследования, применяемые при диагностике и дифференциальной диагностике ХРЗ. Приводятся показатели референсных значений при различных бронхолегочных заболеваниях. Уделяется внимание интерпретации и обоснованию исследования общего анализа крови, острофазовых белков, изменения уровня IgE, эозинофильного катионного белка. Обосновывается включение в план обследования натрийуретического пептида (NT-proBNP) при дифференциальной диагностике одышки, сочетанной с хронической сердечной недостаточностью. Основные положения лабораторной диагностики приведены в соответствии с современными отечественными и международными клиническими рекомендациями по ведению пациентов с ХОБЛ, БА, внебольничной пневмонией.
Ключевые слова: хроническая обструктивная болезнь легких, ХОБЛ, бронхиальная астма, лабораторная диагностика, хронические респираторные заболевания.
Для цитирования: Игнатова Г.Л., Антонов В.Н. Возможности лабораторных методов исследования в дифференциальной диагностике заболеваний дыхательных путей. РМЖ. Медицинское обозрение. 2019;3(9(I)):14-17.
G.L. Ignatova, V.N. Antonov
South Ural State Medical University, Chelyabinsk
For several years, respiratory system diseases are the most urgent problem of modern health care. Acute and chronic respiratory diseases (CRD) are increasing worldwide. Of particular importance is the increase in the incidence of chronic obstructive pulmonary disease (COPD) and bronchial asthma in patients. By no means unimportant are the laboratory test methods in the CRD diagnosis. This has a special weight in the differential diagnosis of pathologies since most pulmonological diseases have similar respiratory manifestations. The article provides an overview of the main laboratory test methods used in the diagnosis and differential diagnosis of CRD. Also, it shows the reference value indices for various broncho-pulmonary diseases. The data on the interpretation and justification of complete blood count, acute phase proteins, changes in the IgE level, and eosinophilic cationic protein are presented. The article gives t he justification for the natriuretic peptide (NT-proBNP) inclusion in the differential diagnosis of dyspnea in a comprehensive course with chronic heart failure. The main provisions of laboratory diagnostics are given in accordance with modern domestic and international clinical guidelines for patient management with chronic obstructive pulmonary disease, bronchial asthma, and community-acquired pneumonia.
Keywords: chronic obstructive pulmonary disease (COPD), bronchial asthma, laboratory diagnosis, chronic respiratory diseases.
For citation: Ignatova G.L., Antonov V.N. Laboratory test method possibilities in the differential diagnosis of respiratory tract diseases. RMJ. Medical Review. 2019;9(I):14-17.
В статье представлены основные лабораторные методы исследования, применяемые при диагностике и дифференциальной диагностике хронических респираторных заболеваний
Заболевания органов дыхания являются наиболее актуальной проблемой современного здравоохранения [1, 2]. Во всем мире наблюдается рост острых и хронических респираторных заболеваний (ХРЗ). Всемирная организация здравоохранения (ВОЗ) уделяет данной проблеме немалое внимание. Под эгидой ВОЗ в 2006 г. был создан Всемирный альянс по борьбе с хроническими респираторными заболеваниями (GARD С Global Alliance against Chronic Respiratory Diseases). Деятельность данной организации является частью глобальной работы по профилактике хронических заболеваний и борьбе с ними. По мнению ВОЗ, необходимо предпринять усилия по улучшению диагностики и медицинского обслуживания населения. Во многих странах недостатки диагностики большинства ХРЗ влекут недостаточность лечения данных заболеваний, а в некоторых случаях имеется дефицит основных лекарственных средств. К числу наиболее распространенных ХРЗ эксперты ВОЗ относят бронхиальную астму (БА), хроническую обструктивную болезнь легких (ХОБЛ), аллергические проявления респираторных заболеваний, профессиональные заболевания легких и легочную гипертензию (ЛГ). Основными факторами риска развития данных заболеваний являются курение табака, загрязнение воздуха вне и внутри помещений, различные аллергены, профессиональные факторы риска [1].
В клинической практике врачи первичного звена и пульмонологи сталкиваются как с изолированными формами данных заболеваний, так и с их сочетанным течением.
БА и ХОБЛ: для каждого заболевания характерны различные фенотипы, но у 10Р20% больных присутствуют признаки как ХОБЛ, так и БА [3]. В 2014 г. впервые выделен фенотип перекреста БА и ХОБЛ (ACOS: asthma-COPD overlap syndromе С синдром перекрывания астмы и ХОБЛ). Выявление данного синдрома позволяет прежде всего пульмонологу назначать рациональную терапию, в частности ингаляционные глюкокортикостероиды (ИГКС).
БА и аллергические заболевания: до 80% пациентов с симптомами БА имеют признаки тех или иных аллергических заболеваний [4]. В то же время наличие атопии не всегда говорит о присутствии у больного БА.
Профессиональные заболевания: в классификации основных профессиональных заболеваний особой строкой прописаны БА и ХОБЛ, развивающиеся вследствие воздействия промышленных аллергенов и ирритантов, вызывающих хронический воспалительный процесс [5].
ЛГ и ее прямое следствие С хроническое легочное сердце являются наиболее частыми осложнениями
ХРЗ [6].
Немаловажное значение при диагностике ХРЗ имеют лабораторные методы исследования. Особый вес они приобретают при дифференциальной диагностике, т. к. большинство пульмонологических заболеваний имеют схожие респираторные проявления.
Анализ крови
Общий анализ крови
Общий анализ крови (ОАК) относится к обязательным лабораторным методам исследования, рекомендованным международными и отечественными клиническими рекомендациями по соответствующим нозологиям, а также входит в алгоритмы оказания медицинской помощи согласно медико-экономическим стандартам [7, 8].
ОАК включает в себя определение концентрации гемоглобина, количества эритроцитов, лейкоцитов и тромбоцитов, величины гематокрита и эритроцитарных индексов, скорости оседания эритроцитов (СОЭ), подсчет лейкоцитарной формулы. Последнее особенно важно в свете новых рекомендаций GOLD (Global Initiative for Chronic Obstructive Lung Disease С Глобальная инициатива по ХОБЛ) и GINA (Global Initiative for Asthma С Глобальная инициатива по бронхиальной астме) при учете эозинофильного воспаления у пациентов с БА и ХОБЛ. Референсные значения нормы составляют от 50 до 250 клеток в 1 мкл. Критическим уровнем является 450 клеток в 1 мкл, что указывает на патологический процесс, связанный с возможным влиянием эозинофилов на воспалительный процесс. При этом, как подчеркивают некоторые авторы, гиперэозинофилия может не коррелировать с тканевой эозинофилией и содержанием эозинофилов в бронхоальвеолярном лаваже [9]. Кроме того, уровень эозинофилов в периферической крови является важным показателем при решении вопроса о применении ИГКС у пациентов с ХОБЛ, а также при эскалации или деэскалации терапии.
Острофазовые белки
Острофазовые белки (ОБ) С это белки коагуляции, транспортные белки, которые также являются медиаторами иммунной системы. ОБ непосредственно участвуют в процессах элиминации повреждающих факторов, способствуют локализации очага повреждения и восстановлению нарушенной структуры клеток и органов, а также их функций. Фибриноген в большей степени имеет отношение к сосудистым реакциям при воспалении, в то же время другие маркеры, будучи многофункциональными, участвуют в реализации многочисленных иммунных процессов [10].
С-реактивный белок (СРБ) С стимулятор иммунных реакций, в т. ч. фагоцитоза, принимает участие в Т- и В-иммунных ответах, активирует классическую систему комплемента. Синтез СРБ происходит преимущественно в гепатоцитах, инициируется антигенами, иммунными комплексами, бактериями, грибами, при травме. Как правило, СРБ в сыворотке здорового человека отсутствует, за исключением некоторых физиологических процессов [10]. Тест на СРБ имеет прямую корреляцию с СОЭ. Оба показателя резко возрастают в начале заболевания, но СРБ реагирует раньше, чем изменяется СОЭ. В лабораторной диагностике этот тест применяется для наблюдения за течением заболевания и контроля эффективности проводимой терапии. Кроме того, концентрация СРБ в крови ассоциирована с активностью заболевания и стадией процесса.
Уровень фибриногена имеет тенденцию к увеличению при различных воспалительных реакциях, это чувствительный маркер воспаления и некроза тканей, основной белок плазмы, напрямую влияющий на скорость оседания эритроцитов. С ростом концентрации фибриногена СОЭ также увеличивается. Рост концентрации фибриногена в плазме, в т. ч. при нормальных значениях, коррелирует с увеличением риска осложнений сердечно-сосудистых заболеваний.
Прокальцитонин (ПКТ) является более специфичным маркером бактериальной инфекции, чем СРБ. Является предшественником гормона кальцитонина и вырабатывается несколькими типами клеток в различных органах под влиянием провоспалительных агентов, в первую очередь бактерий. Уровень ПКТ выше 2 нг/мл с высокой вероятностью свидетельствует об инфекционной природе воспаления [11]. Контроль динамики уровня ПКТ может служить дополнительным высокоинформативным методом оценки эффективности проводимой терапии при инфекционном процессе.
Натрийуретические пептиды
У 60% пациентов старше 65 лет наблюдается сочетанное течение ХРЗ, чаще всего с сердечно-сосудистыми заболеваниями. На этом этапе чрезвычайно важна дифференциальная диагностика одышки, как наиболее частого симптома при коморбидных заболеваниях. Определенную помощь в этом вопросе оказывает определение натрийуретических пептидов С BNP и NT-proBNP.
Для исключения хронической сердечной недостаточности принято использовать порог менее 125 пг/мл для возраста до 75 лет; порог менее 450 пг/мл для возраста старше 75 лет; для исключения острой сердечной недостаточности С менее 300 пг/мл [12].
Иммуноглобулин Е
IgE был выделен в 1960-х гг. из сывороток больных атопией и множественной миеломой. При контакте IgE, адсорбированного на клетках, с аллергеном образуются комплексы « IgE-специфический антиген», что сопровождается проникновением ионов кальция внутрь клетки-мишени, активацией в ней различных биохимических процессов и повышением концентрации гистамина и других биологически активных веществ (БАВ) из тучных клеток, базофилов и эозинофилов, на мембране которых как раз и фиксированы IgE. Поступление вышеперечисленных БАВ в межклеточное пространство сопровождается местной воспалительной реакцией, которую в клинике мы видим в виде ринита, бронхита, БА, анафилактического шока [13].
Как указывает ряд авторов, при анализе уровня IgE необходимо учитывать некоторые особенности и диагностические ограничения.
При определении специфического IgE не следует преувеличивать его диагностическую роль и диагноз аллергии выставлять лишь на основании этого показателя.
Обнаружение аллерген-специфического IgE не является 100% патогномоничным.
В то же время отсутствие специфического IgE или его низкая концентрация в сыворотке периферической крови не исключает возможности участия IgE-зависимого механизма.
Антитела других классов иммуноглобулинов, имеющие высокую специфичность для данного аллергена, особенно класса IgG, могут в некоторых случаях стать причиной ложноотрицательных результатов.
Высокие концентрации общего IgE, к примеру у отдельных больных атопическим дерматитом, могут давать ложноположительные результаты.
Сходные результаты для различных аллергенов не означают их одинакового клинического значения, т. к. способность к связыванию с IgE у разных аллергенов может различаться [13].
Для определения сенсибилизации к респираторным аллергенам и оценки вероятности аллергического характера патологии при неясной симптоматике у пациентов с заболеваниями верхних дыхательных путей применяется тест Phadiatop ImmunoCAP. Он направлен на выявление IgE к смеси наиболее распространенных ингаляционных аллергенов (пыльцы деревьев, трав, аллергенов шерсти домашних животных, клещей домашней пыли, плесени). Это исследование предназначено для первичного скрининга с учетом возможной одновременной сенсибилизации к разным аллергенам или перекрестной сенсибилизации с охватом аллергенов, которые обычно являются основой развития атопии.
Эозинофильный катионный белок
Эозинофильный катионный белок (eosinophilic cationic protein С ECP) представляет собой один из компонентов специфических секреторных гранул эозинофилов человека. Основные свойства ЕСР обусловлены высоким содержанием аргинина. ECP связан с механизмами антигельминтной, антибактериальной, противоопухолевой, а также определенной противовирусной активности эозинофилов. Выраженное эозинофильное воспаление, которое наблюдается при аллергической реакции, может приводить к повреждению собственных тканей, одним их механизмов которого является токсическое действие ECP. Уровень ECP в большинстве случаев коррелирует с тяжестью клинических симптомов БА, отражая выраженность эозинофильного компонента воспаления, и может служить маркером определения тяжести БА с определенными ограничениями. У пациентов с атопией наблюдаются более высокие концентрации ECP, даже когда число эозинофилов в периферической крови имеет нормальные значения. В условиях широкого применения иммунобиологических препаратов для таргетной терапии важно, что уровень ECP превышает норму как при IgE-опосредованной, так и при не-IgE-опосредованной атопии.
Определение a1-антитрипсина
В Федеральных клинических рекомендациях по ведению пациентов с ХОБЛ подчеркивается, что пациентам с ХОБЛ моложе 45 лет, пациентам с быстрым прогрессированием ХОБЛ или при наличии эмфиземы преимущественно в базальных отделах легких рекомендуется определять уровень α1-антитрипсина в крови [8].
Связь дефицита α1-антитрипсина с повышенным риском развития эмфиземы легких была впервые показана в работах Laurell и Eriksson, которые в 1963 г. описали отсутствие α1-фракции у больных с панацинарной эмфиземой [14]. В дальнейшем была описана связь врожденного дефицита данного белка с заболеваниями печени. При воспалительном процессе в легочной ткани α1-антитрипсин подавляет функцию эластазы, выделяющейся из нейтрофилов, предотвращая деградацию белка соединительной ткани (эластина) в стенках альвеол и развитие эмфиземы легких. Он модулирует локальный иммунный ответ, обладает антиоксидантным и антимикробным действием, ингибирует протеолитические ферменты апоптоза. Концентрация α1-антитрипсина значительно повышается при остром воспалении различной этиологии, инфекционных, ревматических заболеваниях, злокачественных процессах, при заместительной терапии эстрогенами, приеме пероральных контрацептивов, повышении уровня эстрогенов при беременности, воспалительных процессах в гепатоцитах. Дефицит α1-антитрипсина коррелирует с высоким риском развития патологии легких [8].
Цитология мокроты. Клеточный состав индуцированной мокроты может характеризовать тип воспаления, который определяют по содержанию в мокроте эффекторных воспалительных клеток С эозинофилов, нейтрофилов, лимфоцитов, макрофагов. В настоящее время принято различать 4 клеточных фенотипа: 1) эозинофильный, если количество эозинофилов более 2%; 2) нейтрофильный при числе нейтрофилов 61% и выше; 3) смешанный; 4) неэозинофильный (менее 2% клеток) и ненейтрофильный (менее 61% клеток) [8, 15].
Определение данных фенотипов имеет чрезвычайно важное значение в выборе терапии, в частности при назначении ИГКС или антибактериальных препаратов.
Бактериологический анализ мокроты имеет диагностическое значение только при инфекционном обострении заболеваний, а также при определении чувствительности к антибиотикам [8].
Заключение
Основу диагностики и дифференциальной диагностики основных респираторных заболеваний конечно же составляют клинические методы исследования. Тщательный сбор анамнеза, учет различных нюансов эпидемиологии, особенностей индивидуума обеспечивают до 90% точности диагноза. В этой связи нельзя не вспомнить блестящие клинические описания болезней классиков русской терапевтической школы, когда диагноз напрямую был связан с опытом и наблюдательностью врача. Применение современных методов диагностики существенно облегчает постановку диагноза, но и может увести от правильной трактовки клинической ситуации. В этой связи становится актуальным тщательный анализ всех полученных клинических, лабораторных, инструментальных методов диагностики. Только сопоставив и тщательно взвесив все данные, думающий врач может прийти к единственно правильному решению.
Большинство лабораторных показателей не имеют 100% патогномоничного значения. Риск врачебной ошибки при этом повышается. Задача клинициста и врача лабораторной диагностики С свести этот риск к минимуму. Поэтому правильная интерпретация лабораторных показателей с учетом всех возможных нюансов играет важную роль в клинической медицине.
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Дыхательная рентгенокимография. Анализ дыхательной рентгенокимографии
Значение оценки показателй КЩР. Рентгено-функциональные методы изучения внешнего дыхания
Исследование показателей кислотно-щелочного равновесия во время операции позволяет вносить коррективы в ведение наркоза и искусственной вентиляции, определять адекватность дыхания и кровообращения в каждый отдельный момент операции (Р. А. Мейтина с соавт., 1962).
Определение величин кислотно-щелочного баланса параллельно с исследованием газового состава крови дает возможность получить наиболее подробную характеристику эффективности газообмена в раннем послеоперационном периоде (В. Д. Герасимова, Л. Е. Сеферовский и Э. П. Сваджян, 1965).
Проведенные в клинике общей хирургии I ММИ им. И. М. Сеченова исследования показателей кислотно-щелочного равновесия (О. А. Долина и С. Г. Птушкина, 1966) позволили применить в клинической практике патогенетически обоснованную терапию нарушений процессов газообмена в организме.

Рентгено-функциональные методы изучения внешнего дыхания
Рентгенологический метод традиционно применяется для оценки функции внешнего дыхания. В пульмонологической клинике перед рентгено-функциональными методами ставятся две задачи: 1) наряду с рентгено-морфологическими признаками помочь рентгенологу в постановке рентгенологического диагноза; 2) предоставить дополнительную информацию о легочных объемах, вентиляции и кровотоке, получение которой методами функциональной диагностики невозможно или слишком обременительно. Естественно, что в данной главе рассматривается только вторая сторона рентгено-функциональных методов.
Не вызывает сомнения зависимость функциональных потерь от величины и распространенности морфологических изменений, выявляемых при рентгенологическом исследовании. Однако опыт показывает, что в ряде случаев наблюдается несоответствие клинико-рентгенологической картины и фактических функциональных изменений в пораженном легком, выявленных при раздельной спирографии. Этому вопросу посвящена специальная работа Vaccarezza, Lanari, Soubrie (1947).
Основываясь на сравнительном изучении данных рентгенологического и бронхоспирометрического исследований у более 400 больных с хирургическими заболеваниями легких, мы можем подтвердить мнение Vaccarezza с соавт. и Gaensler (1952), что при воспалительных заболеваниях легких (специфических и неспецифических), при поражениях паренхимы легкого выраженные морфологические изменения не сопровождаются ожидаемыми большими функциональными потерями в пораженном легком.
Наоборот, при небольших плевральных наложениях может наблюдаться резкое снижение вентиляции и особенно газообмена на стороне поражения. Наши исследования показали также, что при раке легкого может иметь место практически полное отсутствие газообмена, то есть функциональное выключение легкого, тогда как опухоль занимает лишь небольшой участок легочной паренхимы (А. В. Григорян, Б. П. Федоров и С. В. Лохвицкий, 1966). Аналогичные данные получены при электрокимография у больных раком легкого (В. Я. Фридкин, В. Э. Гельштейн и В. Н. Орлов, 1959; С. Я. Марморштейн, 1962; Lissneiv 1962).
Для изучения легочной вентиляции предложен ряд специальных рентгенологических методов, к которым относятся рентгенокимография, полиграфия (диплография), рентгенопневмография, денсография и др.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Дыхательная рентгенокимография — один из старейших рентгено-функциональных методов, предложенный еще в 1911 году польским врачом Sabat. Рентгенокимография обеспечивает объективную регистрацию состояния движения органа во времени и дает возможность сравнивать участие далеко расположенных его отделов или различных органов (К. В. Помельцов, 1965).
Принцип рентгенокимографии заключается в том, что контуры движущихся органов на снимке имеют форму зубчатой кривой, причем высота зубца отражает величину, а ширина у основания — время смещения. Технически это осуществляется путем прохождения рентгеновых лучей через узкую щель (0,5 мм) в свинцовой пластинке или решетку, в которой щели расположены на расстоянии 12 мм друг от друга (многощелевой кимограф). Во время производства снимка решетка или кассета с пленкой приводится в движение, причем больной продолжает дышать.
В настоящее время наиболее распространена многощелевая непрерывная рентгенокимография, при которой движется решетка, а кассета с пленкой остается неподвижной. При дыхательной рентгенокимографии щели решетки обычно располагают вертикально, так как в этом направлении происходит основной компонент движения диафрагмы и ребер. Исследование производят в двух проекциях — передней (прямой) и боковой, причем переднюю рентгенокимограмму обычно производят при спокойном дыхании, а боковую — при глубоком (Л. Д. Линденбратен, 1960).
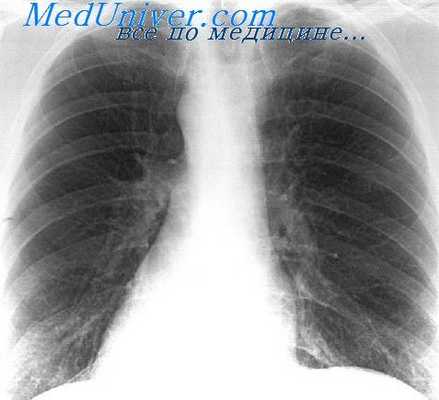
Анализ дыхательной рентгенокимограммы заключается в изучении формы дыхательных зубцов и сравнении зубцов диафрагмы и ребер. Каждый дыхательный зубец состоит из двух колен: крутого и более короткого колена вдоха и пологого удлиненного колена выдоха. Удлинение колена выдоха служит признаком обструктивной дыхательной недостаточности.
Сравнительное изучение зубцов различных участков диафрагмы и ребер может указать на неравномерность вентиляции различных отделов легкого, но чаще всего деформация зубцов отмечается при плевро-диафрагмальных и плевро-костальных сращениях.
Я. Л. Шик (1936) предложил измерять диафрагмально-реберный коэффициент, который позволяет объективно анализировать и характеризовать типы дыхания. Диафрагмально-реберный коэффициент (сокращенное обозначение — ДРК) представляет отношение амплитуды зубцов диафрагмы к амплитуде зубцов заднего отдела V ребра. Грудному типу дыхания соответствует ДРК не более 3, брюшному — 6 и выше. ДРК от 3 до 6 относится к смешанному типу дыхания.
Е. Л. Кевеш и В. И. Бураковский (1955) провели сравнительное изучение рентгенокимографии у легочных больных. Они считают, что дыхательная рентгенокимография представляет ценный метод, дающий возможность получить сравнительное представление о вентиляционной способности одного легкого по отношению к другому. Однако возможности его ограничены, так как не позволяют установить поглощение кислорода, определяющее эффективность дыхания. Поэтому, по мнению Е. Л. Кевеша и В. И. Бураковского, рентгенокимография, спирография и бронхоспирометрия должны дополнять друг друга и служить для комплексного углубленного изучения дыхательной функции легких в клинике грудной хирургии.
Оценка внешнего дыхания
Спирометрия и оценка альвеолярного воздуха
Обследование пациента при легочной патологии
Операбельность пациентов с легочной патологией
Бронхи легких. Обезболивание при бронхоскопии
Анестезия при бронхологических исследованиях
Оснащение и техника бронхоскопии
Манипуляции при бронхоскопии. Бронхография
Показания, техника бронхографии
Бронхография. Бронхоспирометрия
Техника бронхоспирометрии
Комплексное бронхологическое исследование и его осложнения
Осложнения бронхологических исследований
Исследование сосудов легких и камер сердца
Ангиопульмонография. Азигография
Легкие при ревматизме
Диагностические вмешательства при патологии легких и средостения
Обследования в пульмонологии
Обследование пациента
Перкуссия и осмотр пациента
Внешний осмотр пациента
Объективный осмотр пациента
Оценка мышц и суставов пациента
РЕНТГЕНОКИМОГРАФИЯ
РЕНТГЕНОКИМОГРАФИЯ [рентгено- (по имени В. Рентгена) + кимография] — метод регистрации движений органа путем его рентгенографии. Для этого производят рентгенографию на одну пленку в разные фазы движения органа, что достигается применением свинцовой пластины с одной или несколькими щелями, помещаемой между источником излучения и пленкой. Во время съемки пластина или кассета с рентгеновской пленкой должны перемещаться относительно друг друга.
С помощью Р. исследуют гл. обр. дыхательные движения диафрагмы и ребер, пульсацию сердца и магистральных сосудов грудной полости.
При Р. контуры движущегося органа приобретают на рентгенограмме (рентгенокимограмме) зубчатую форму, причем величина и форма зубцов отражают характер движений. Обязательным условием Р. является достаточная контрастность исследуемого органа по отношению к соседним тканям (напр., сердца на фоне легочной ткани).
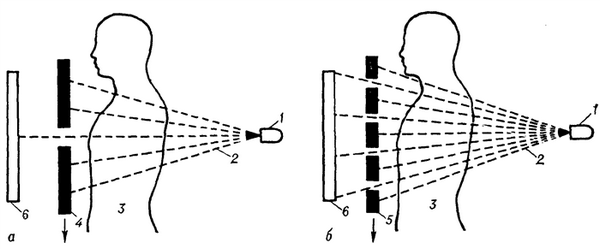
Рис. 1. Принципиальная схема рентгенокимографии: а — однощелевая рентгенокимография; б — многощелевая рентгенокимографии; 1 — источник рентгеновского излучения; 2 — пучок рентгеновского излучения; 3 — тело пациента; 4 — однощелевая свинцовая пластина; 5 — многощелевая свинцовая пластина (кимографическая решетка); 6 — кассета с рентгеновской пленкой; стрелкой указано направление движения свинцовой пластины (при горизонтальном расположении щелей).
Различают одно- и многощелевую Р. (рис. 1). При однощелевой Р. между рентгеновской пленкой и пациентом устанавливают свинцовую пластину с одной узкой щелью, а кассета с пленкой во время съемки приводится в движение по горизонтали или вертикали. При многощелевой Р. используют пластину с большим числом узких щелей. Во время исследования (съемки) приводится в движение либо пластина (непрерывная Р.), либо кассета с рентгеновской пленкой (ступенчатая Р.).
Метод однощелевой Р. впервые был предложен в 1911 г. варшавским врачом Сабатом (В. Sabat), а еще через год Гетт и Розенталь (Th. Gott, S. Rosenthal) применили его в клинике. В 1928 г. Штумпф (P. Stumpf) предложил метод и аппарат для многощелевой Р. В СССР конструкция многощелевого рентгенокимографа впервые была разработана в 1933 г. В. Г. Гинзбургом. Большой вклад в развитие Р. в СССР внесли М. А. Иваницкая, К. Б. Тихонов, В. В. Зодиев и др.
Хотя однощелевая Р., при к-рой возможно изучение лишь отдельных точек движущегося контура, не нашла широкого применения, она обладает по сравнению с многощелевой Р. весьма существенным преимуществом: благодаря удлинению пути движения пленки за то же время съемки кимографические зубцы растянуты и в них можно выделить значительно больше деталей. Поэтому однощелевая Р. может применяться для уточнения данных, полученных при многощелевой Р.
Противопоказанием к Р. является крайне тяжелое состояние больного. Нецелесообразна Р. и в том случае, если есть возможность проведения электрокимографии (см.), более полно характеризующей функции сердца, крупных сосудов и легких.
Р. осуществляется с помощью рентгеновского аппарата (см.), снабженного специальным механическим устройством — рентгенокимографом. В простейшем однощелевом рентгенокимографе свинцовая пластина с горизонтальной щелью шириной 1 мм фиксируется между телом пациента и рентгеновской пленкой, перемещающейся по вертикали на 12 мм за 2,4 сек. В многощелевом рентгенокимографе набор свинцовых пластин (кимографическая решетка) образует систему щелей шириной 0,5 мм с расстоянием между ними 12 или 36 мм. Кимографическая решетка также расположена между телом пациента и пленкой. Устройство позволяет перемещать с помощью электромеханического привода либо кимографическую решетку относительно неподвижной пленки, либо пленку форматом 30 X 40 см относительно неподвижной решетки на 36 мм за время от 2 до 6 сек. Направление движения устанавливается поворотом кимографической решетки относительно штатива на угол до ±90° с фиксацией через каждые 15°.
Упрощенным вариантом многощелевого рентгенокимографа является кимокассета, представляющая собой рентгенографическую кассету для пленки форматом 24 X 30 см, совмещенную в одном корпусе с кимографической решеткой. Кимографиче-ская решетка со щелями шириной 0,5 мм и расстоянием между ними 12 мм перемещается на 11,5 мм за 2 или 3 сек. Кимокассета снабжена электросекундомером, пультом управления, электрическим блоком.
Существует разновидность многощелевого рентгенокимографа — так наз. защищенный, или дистанционный, рентгенокимограф, в к-ром кимографическая решетка расположена между телом пациента и источником рентгеновского излучения, что снижает дозу облучения пациента примерно в 15—20 раз.

Рис. 2. Рентгенокимограмма диафрагмы и ребер в норме: контуры диафрагмы и ребер имеют зубчатую форму, амплитуда зубцов отражает дыхательные движения (зубцы на контуре сердца не имеют диагностического значения).
Рентгенокимографию диафрагмы и ребер выполняют с помощью кимографической решетки, расстояние между щелями к-рой 36 мм. Движения решетки горизонтальные, а щели ее располагаются вертикально. Время движения решетки — 6 сек., что позволяет при обычном дыхании зарегистрировать на пленке 1,5—2 полных дыхательных цикла (рис. 2). Для изучения тонуса и двигательной способности диафрагмы при Р. применяют функциональные пробы: Мюллера (попытка вдоха при закрытой голосовой щели) и нюхательную (быстрый и глубокий вдох через нос). По отношению амплитуды нисходящей (правой) части зубца к амплитуде его восходящей (левой) части определяют инспираторно-экспираторный коэффициент. Уменьшение этого коэффициента указывает на патол. удлинение выдоха, что является ранним признаком эмфиземы легких. Определяют также частоту, глубину и ритм дыхательных движений, их синхронность с обеих сторон. По амплитуде движений диафрагмы и ребер вычисляют показатели вентиляционной способности легких. Опускание диафрагмы на 1 см соответствует увеличению объема воздуха в правом легком на 110 мл, (в левом — на 90 мл). Подъем задней части V ребра на 1 см соответствует увеличению объема воздуха в правом легком на 800 мл (в левом— на 700 мл).
Рентгенокимография сердца и магистральных сосудов грудной полости. До разработки и внедрения в практику электрокимографии Р. была основным методом рентгенол. регистрации движения сердца, аорты и легочного ствола. Она применяется для оценки сократительной способности миокарда, выявления участков инфаркта, рубцовых полей и аневризматических выпячиваний в стенке сердца, для диагностики аритмий, определения волны регургитации при пороках сердца и др. Для выполнения Р. применяют решетку, в к-рой расстояние между горизонтально расположенными щелями составляет 12 мм. Съемку производят на глубине вдоха. Выдержку выбирают с таким расчетом, чтобы в одной полосе рентгенокимограммы было получено 3 зубца.
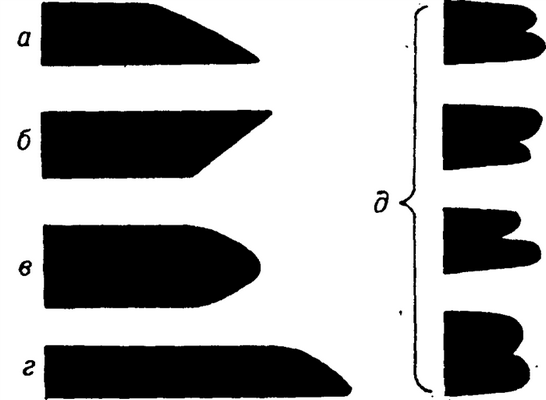
Рис. 3. Типичная форма рентгенокимо-графических зубцов сердца и магистральных сосудов: а — желудочковый зубец; б — зубец магистрального сосуда; в — желудочковый зубец при брадикардии; г — желудочковый зубец при тахикардии; д — варианты предсердных зубцов.
Рентгенокимографические зубцы желудочков, предсердий и магистральных сосудов имеют различную форму (рис. 3). Желудочковые зубцы в норме остроконечные с прямым нижним (систолическим) и пологим верхним (диастолическим) контуром; зубцы аорты и легочного ствола остроконечные и по форме являются зеркальным отображением желудочковых зубцов. Предсердные зубцы имеют расщепленную вершину. Форма зубцов связана также с частотой сокращений: для брадикардии типичен зубец с симметричными сторонами и закругленной вершиной, для тахикардии — острый, копьевидный.

Рис. 4. Рентгенокимограмма сердца и магистральных сосудов в норме: амплитуда зубцов на контурах сердца и магистральных сосудов отражает их пульсацию.

Рис. 5. Рентгенокимограмма сердца при экссудативном перикардите: отсутствие зубцов на контурах сердца свидетельствует об отсутствии их пульсации вследствие накопления жидкости в полости перикарда.
По рентгенокимограмме определяют протяженность контура каждого отдела сердца или магистрального сосуда, частоту сокращений, их ритм, амплитуду, продолжительность систолы и диастолы, соотношение частоты, ритма и глубины пульсации разных отделов сердца и магистральных сосудов (рис. 4, 5).
Библиография: Зодиев В. В. и Разумов Н. П. Многощелевая рентгенокимо-графия сердца и больших сосудов и ее клиническое значение, М., 1953; Линденбратен Л. Д. и Наумов Л. Б. Методы рентгенологического исследования органов и систем человека, Ташкент, 1976; М а к т а з И. П. и д р. Рентгенокимографические приборы, М., 1980; Соболев В. И. Основы рент-генокимографии легочного дыхания, Л., 1948; Тихонов К. Б. Техника рентгенологического исследования. Л., 1978.
Читайте также:
