Острые миелоидные лейкозы - клиника, диагностика
Добавил пользователь Евгений Кузнецов Обновлено: 29.01.2026
Острая миелоидная лейкемия у взрослых - клиника, лечение
В большинстве случаев анамнез и выявляемые при осмотре симптомы сходны с таковыми при ОЛЛ. Боли в костях и выявляемые при рентгенологическом обследовании инфильтраты в них при ОМЛ менее распространены. Заболевания ЦНС встречаются очень редко. Увеличение лимфатических узлов также менее распространено, чем при ОЛЛ.
При миеломоноцитарной (М4) и моноцитарной (М5) лейкемии являются обычными инфильтраты в деснах, приводящие к «гипертрофии» десен. Кожные инфильтраты также нередки при этих формах лейкемии и связаны с высоким тотальным уровнем WBC и высоким уровнем лизозимов сыворотки крови и мочи, которые выделяются опухолью.
Наиболее распространенные диагностические признаки: бледность кожных покровов, гепатоспленомегалия, пурпура и боли в костях. Часто повышен уровень WBC, как правило, хорошо выявляются миелобласты. Для подтверждения диагноза проводят исследование костного мозга с использованием специального соответствующего окрашивания.

Морфологическая классификация острых лейкемий. Доля подтипов острых лейкемий миелоидного и моноцитарного происхождения (%).
Лечение острой миелобластной лейкемии
Индукция ремиссии: целью индукции является восстановление костного мозга и клиническая ремиссия. Чтобы этого добиться, необходима интенсивная терапия крови, тромбоцитов и применение антибиотиков в период гипоплазии, неизбежно сопровождающее химиотерапию.
Используется комбинация высоких доз цитозинарабинозида и даунорбицина. Идарубицин и митоксантрон не представляются более эффективными, чем даунорбицин. Добавление таких трех лекарств, как этопозид, флюдарабин или тиогуанин, не дает улучшения результатов. Количество бластов в крови и костном мозге обычно быстро снижается при супрессии нормального гематопоэза.
В настоящее время, когда возможно применить врачебные навыки, смертность на этой стадии составляет 10%. В период гипоплазии дальнейшая цитотоксическая терапия часто необходима, если все еще есть проявления болезни со стороны костного мозга, которые приводят к интенсификации гипоплазии и повышают риск.
Поэтому индукция ремиссии является процедурой, требующей очень хороших навыков, которую лучше проводят в учреждениях, имеющих подготовленный медицинский персонал и сиделок. Очень важен внимательный контроль жидкости и электролитного баланса, быстрое оперативное выявление и лечение инфекций. Профилактическое лечение ЦНС обычно не проводят.
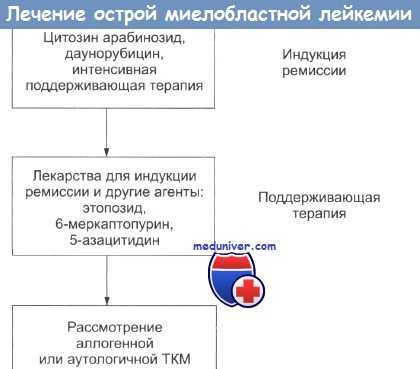
Поддерживающая терапия острой миелобластной лейкемии
Поддержание продукции элементов крови очень важно в фазе интенсивной индукции ремиссии. Трансфузия тромбоцитов оказывается наиболее действенной в предотвращении гибели от геморрагии. Показания к трансфузии тромбоцитов обсуждаются в отдельной статье на сайте (рекомендуем пользоваться формой поиска на главной странице сайта).
Переливание крови весьма важно при анемии, но его нужно избегать в ситуациях, когда WBC очень высок (выше 100 х х 109/л), поскольку могут возникнуть лейкостазы в сосудах головного мозга. Для снижения WBC перед трансфузией могут быть использованы химиотерапия и, если необходимо, лейкаферез. Применение гемопоэтических ростовых факторов описано в отдельной статье на сайте (рекомендуем пользоваться формой поиска на главной странице сайта).
Во время интенсивной терапии хорошо помогает использование подкожно вводимых внутривенных подключичных катеторов (катетер Хикмана).
Для предотвращения инфекции пациентов инструктируют, как правильно мыться, особенно аккуратно в области промежности. При выявлении сепсиса зубов и полости рта нужно немедленно приступать к лечению. Пища должна быть термически обработана и чистая — свежие салаты лучше исключить. Очень важно регулярное обследование полости рта, кожи и промежности, должны проводиться регулярные посевы для выявления патогенов, таких как Klebsiella или Pseudomonas. В некоторых случаях дается котримоксазол с профилактической целью для предотвращения развития оппортунистических инфекций, таких как Pneumocystis carinii.
У многих пациентов развивается жар, лихорадка на некоторых стадиях в период нейтропении. Лечение инфекции у больных с нейтропенией обсуждается в отдельной статье на сайте (рекомендуем пользоваться формой поиска на главной странице сайта). Часто невозможно поставить бактериологический диагноз. Наиболее фатальными инфекциями являются те, которые вызваны представителями группы граммотрицательных микроорганизмов. Инфекции, появляющиеся вокруг линии Хикмана, вызывают микроорганизмы, частично присутствующие на коже в норме, такие как Staphyloccocus epidermidis и S. aureus. Для лечения этих явлений часто используют антибиотики ванкомицин и тейкопланин.
Оппортунистические инфекции являются причиной значительных затруднений в диагностике у пациентов с высокой температурой и легочными инфильтратами. Инфекции, вызванные микроскопическими грибами, Pneumocystis carinii, и менее распространенные цитомегаловирусные и другие вирусные инфекции должны быть также приняты во внимание.

После того как взяты посевы крови при приступе жара, проводится внутривенная терапия широким спектром антибиотиков. Такие режимы обычно включают аминогликозид и цефалоспорин, часто добавляют метронидазол, особенно если наблюдают ухудшение клинических проявлений через 24 ч. При выявлении легочных инфильтратов могут применяться высокие дозы котримоксазола для борьбы с Pneumocystis, амфотерицин В для подавления грибной инфекции и ацикловир для подавления герпеса.
Результаты лечения и новые подходы: Полная ремиссия наблюдается у 65% пациентов моложе 60 лет и у 50% — старше этого возраста. Поэтому развитие новых подходов к индукции ремиссии в группах с плохим прогнозом является важной областью в дальнейших исследованиях. Новые подходы включают в себя использование анти-CD33 моноклональных антител (гемтузумаб).
Более интенсивные поддерживающие режимы также изучаются и могут пролонгировать длительность ремиссии. У пожилых пациентов токсичность повышена и интенсификация режимов проблематична. Худший исход наблюдается у тех больных старше 60 лет, у которых высокий уровень WBC и плохие характеристики статуса, а также у пациентов, у которых ОМЛ развилась после миелодиспластического синдрома (9:11).
Цитогенетические изменения прогностически важны: t(q;11), 5q, inv3 — неблагоприятны, и t(8;21) — имеет благоприятный прогноз. В общем, выживаемость в течение 10-летнего периода без проявления болезни составляет около 30%.
Несмотря на то что результаты стандартной интенсивной химиотерапии при ОМЛ улучшаются, долгосрочный прогноз до сих пор остается плохим для большинства пациентов. Подходы с использованием ТКМ (особенно аллогенной) не годятся для большинства пациентов, так как ОМЛ — болезнь людей пожилого возраста. Аллогенная ТКМ обычно применяется при первом полном ответе и, по сравнению со стандартным лечением, похоже, снижает лейкемические рецидивы на 20%. Некоторые из этих положительных результатов проявляются из-за лейкемического эффекта отторжения.
Современные исследования показывают преимущество аллогенной трансплантации с долгосрочным эффектом без проявлений болезни у примерно 50% пациентов. Этому необходимо противопоставить острую смертность, особенно от аллогенной ТКМ. Показано, что аутологичная ТКМ снижает риск рецидивов. Эта процедура более широко применима, чем аллогенная ТКМ, поскольку подходящий донор не нужен. При аллогенной ТКМ обычно используются высокие дозы циклофосфамида и ТО. При аутологичной ТКМ режимы могут базироваться лишь на одной химиотерапии. Гемопоэтические ростовые факторы делают возможным повышение интенсивности лечения, не вызывая стимуляции лейкемической пролиферации.
Для пожилых пациентов в большинстве случаев есть дополнительные проблемы, связанные с сопутствующими заболеваниями, не позволяющие применить интенсивный метод. Несмотря на это, во многих исследованиях исключают пациентов старше 60 лет без достаточных оснований, и требуется более усовершенствованный метод. Возможно, аллогенная или аутологичная трансплантация более низкой интенсивности даст лучший результат.
Лечение рецидивов острой миелобластной лейкемии
Хотя индукция второй ремиссии возможна у пациентов, которые дали рецидив после прерывания лечения, такая ремиссия обычно непродолжительна. Для пациентов моложе 60 лет вторая ремиссия иногда может быть достигнута использованием высоких доз цитозинарабинозида. Для молодых людей и тех, у кого обнадеживающий прогноз, есть шанс лечения с использованием аллогенной или аутологичной ТКМ, обычно с предшествующей реиндукционной химиотерапией.
Исследования, сравнивающие аллогенную и аутологичную трансплантацию, не могут быть рандомизированы, за исключением тех двух случаев, когда донор пригоден или не пригоден к рассмотрению как суррогатная «генетическая» случайная выборка. Поэтому и технические, и клинические трудности не вносят ясности, какой метод предлагает лучший результат. Рецидивы со стороны центральной нервной системы лечат по сходной схеме как при ОЛЛ.
Лечение острой промиелоцитарной лейкемии (M3)
Острая промиелоцитарная лейкемия (ОПЛ) составляет 10% от общего количества случаев заболевания ОМЛ. Индукция ремиссии осложняется десеменированной внутрисосудистой коагуляцией в тех случаях, когда применяется цитохимическая химиотерапия. Представляется, что это происходит из-за высвобождения прокоагулянтов (цистеиновая протеиназа).
Клетки дифференцируются in vitro в ответ на полностью транс-ретиноивую кислоту (ATRA, третинон). Когда применяют ATRA для лечения пациента с ОПЛ, костный мозг медленно (в течение 2 месяцев) возвращается в норму (кроме типичного t(15;17) кариотипа) и десеменированной внутрисосудистой коагуляции не происходит. Побочные эффекты: сухая кожа, головные боли и потенциально опасный гиперлейкоцитоз (который может вызвать отек легких). Через 6 месяцев у пациентов бывают рецидивы.
Новые исследования предполагают, что химиотерапия как дополнение к лечению ATRA может дать хорошие результаты. Точка разрыва при транслокации хромосом t(15;17) расположена около гена, кодирующего а-рецептор ретиноевой кислоты на 17 хромосоме, и использование ATRA только улучшает ситуацию в тех случаях, когда у пациента имеется такая транслокация.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Острый миелоидный лейкоз
Острый миелоидный лейкоз – злокачественное заболевание системы крови, сопровождающееся неконтролируемым размножением измененных лейкоцитов, снижением количества эритроцитов, тромбоцитов и нормальных лейкоцитов. Проявляется повышенной склонностью к развитию инфекций, лихорадкой, быстрой утомляемостью, потерей веса, анемией, кровоточивостью, образованием петехий и гематом, болями в костях и суставах. Иногда выявляются изменения кожи и припухлость десен. Диагноз устанавливается на основании клинических симптомов и данных лабораторных исследований. Лечение – химиотерапия, трансплантация костного мозга.
МКБ-10
Общие сведения
Острый миелоидный лейкоз (ОМЛ) – злокачественное поражение миелоидного ростка крови. Неконтролируемая пролиферация лейкозных клеток в костном мозге влечет за собой подавление остальных ростков крови. В результате количество нормальных клеток в периферической крови уменьшается, возникают анемия и тромбоцитопения. Острый миелоидный лейкоз является самым распространенным острым лейкозом у взрослых. Вероятность развития болезни резко увеличивается после 50 лет. Средний возраст пациентов составляет 63 года. Мужчины и женщины молодого и среднего возраста страдают одинаково часто. В старшей возрастной группе наблюдается преобладание лиц мужского пола. Прогноз зависит от вида острого миелоидного лейкоза, пятилетняя выживаемость колеблется от 15 до 70%. Лечение осуществляют специалисты в области онкологии и гематологии.
Причины острого миелоидного лейкоза
Непосредственной причиной развития ОМЛ являются различные хромосомные нарушения. В числе факторов риска, способствующих развитию таких нарушений, указывают неблагоприятную наследственность, ионизирующее излучение, контакт с некоторыми токсическими веществами, прием ряда лекарственных препаратов, курение и болезни крови. Вероятность возникновения острого миелоидного лейкоза увеличивается при синдроме Блума (низкий рост, высокий голос, характерные черты лица и разнообразные кожные проявления, в том числе гипо- или гиперпигментация, кожная сыпь, ихтиоз, гипертрихоз) и анемии Фанкони (низкий рост, дефекты пигментации, неврологические расстройства, аномалии скелета, сердца, почек и половых органов).
Острый миелоидный лейкоз достаточно часто развивается у больных с синдромом Дауна. Прослеживается также наследственная предрасположенность при отсутствии генетических заболеваний. При ОМЛ у близких родственников вероятность возникновения болезни повышается в 5 раз по сравнению со средними показателями по популяции. Самый высокий уровень корреляции выявляется у однояйцевых близнецов. Если острый миелоидный лейкоз диагностируется у одного близнеца, риск у второго составляет 25%. Одним из важнейших факторов, провоцирующих ОМЛ, являются заболевания крови. Хронический миелоидный лейкоз в 80% случаев трансформируется в острую форму болезни. Кроме того, ОМЛ нередко становится исходом миелодиспластического синдрома.
Ионизирующее излучение вызывает острые миелоидные лейкозы при превышении дозы 1 Гр. Заболеваемость увеличивается пропорционально дозе облучения. На практике имеет значение пребывание в зонах атомных взрывов и аварий на атомных электростанциях, работа с источниками излучения без соответствующих защитных средств и радиотерапия, применяемая при лечении некоторых онкологических заболеваний. Причиной развития острого миелоидного лейкоза при контакте с токсическими веществами является аплазия костного мозга в результате мутаций и поражения стволовых клеток. Доказано негативное влияние толуола и бензола. Обычно ОМЛ и другие острые лейкозы диагностируются спустя 1-5 лет после контакта с мутагеном.
В числе лекарственных средств, способных провоцировать острые миелоидные лейкозы, специалисты называют некоторые препараты для химиотерапии, в том числе ингибиторы ДНК-топоизомеразы II (тенипозид, этопозид, доксорубицин и другие антрациклины) и алкилирующие средства (тиофосфамид, эмбихин, циклофосфамид, хлорамбуцил, кармустин, бусульфан). ОМЛ также может возникать после приема хлорамфеникола, фенилбутазона и препаратов мышьяка. Доля лекарственных острых миелоидных лейкозов составляет 10-20% от общего количества случаев заболевания. Курение не только повышает вероятность развития ОМЛ, но и ухудшает прогноз. Средняя пятилетняя выживаемость и продолжительность полных ремиссий у курильщиков ниже, чем у некурящих.
Классификация острого миелоидного лейкоза
Классификация острого миелоидного лейкоза по версии ВОЗ очень сложна и включает в себя несколько десятков разновидностей заболевания, разделенных на следующие группы:
- ОМЛ с типичными генетическими изменениями.
- ОМЛ с изменениями, обусловленными дисплазией.
- Вторичные острые миелоидные лейкозы, возникшие в результате лечения других заболеваний.
- Болезни с пролиферацией миелоидного ростка при синдроме Дауна.
- Миелоидная саркома.
- Бластная плазмацитоидная дендритноклеточная опухоль.
- Другие виды острого миелоидного лейкоза.
Тактика лечения, прогноз и продолжительность ремиссий при разных видах ОМЛ могут существенно различаться.
Симптомы острого миелоидного лейкоза
Клиническая картина включает в себя токсический, геморрагический, анемический синдромы и синдром инфекционных осложнений. На ранних стадиях проявления острого миелоидного лейкоза неспецифичны. Отмечается повышение температуры без признаков катарального воспаления, слабость, утомляемость, потеря веса и аппетита. При анемии присоединяются головокружения, обморочные состояния и бледность кожных покровов. При тромбоцитопении наблюдаются повышенная кровоточивость и петехиальные кровоизлияния. Возможно образование гематом при незначительных ушибах. При лейкопении возникают инфекционные осложнения: частые нагноения ран и царапин, упорные повторные воспаления носоглотки и т. д.
В отличие от острого лимфобластного лейкоза при остром миелоидном лейкозе отсутствуют выраженные изменения со стороны периферических лимфатических узлов. Лимфоузлы небольшие, подвижные, безболезненные. Иногда выявляется увеличение лимфатических узлов в шейно-надключичной области. Печень и селезенка в пределах нормы или незначительно увеличены. Характерны признаки поражения костно-суставного аппарата. Многие больные острым миелоидным лейкозом предъявляют жалобы на боли различной степени интенсивности в области позвоночника и нижних конечностей. Возможны ограничения движений и изменения походки.
В числе экстрамедуллярных проявлений острого миелоидного лейкоза – гингивит и экзофтальм. В отдельных случаях наблюдаются припухлость десен и увеличение небных миндалин в результате инфильтрации лейкозными клетками. При миелоидной саркоме (составляет около 10% от общего количества случаев острого миелоидного лейкоза) на коже пациентов появляются зеленоватые, реже – розовые, серые, белые или коричневые опухолевидные образования (хлоромы, кожные лейкемиды). Иногда при поражениях кожи обнаруживается паранеопластический синдром (синдром Свита), который проявляется воспалением кожных покровов вокруг лейкемидов.
В развитии острого миелоидного лейкоза выделяют пять периодов: начальный или доклинический, разгара, ремиссии, рецидива и терминальный. В начальном периоде острый миелоидный лейкоз протекает бессимптомно или проявляется неспецифической симптоматикой. В периоде разгара токсический синдром становится более выраженным, выявляются анемический, геморрагический и инфекционный синдромы. В период ремиссии проявления острого миелоидного лейкоза исчезают. Рецидивы протекают аналогично периоду разгара. Терминальный период сопровождается прогрессирующим ухудшением состояния больного и завершается летальным исходом.
Диагностика и лечение острого миелоидного лейкоза
Решающую роль в процессе диагностики играют лабораторные анализы. Используют анализ периферической крови, миелограмму, микроскопические и цитогенетические исследования. Для получения образца тканей выполняют аспирационную биопсию костного мозга (стернальную пункцию). В анализе периферической крови больного острым миелоидным лейкозом обнаруживается снижение количества эритроцитов и тромбоцитов. Количество лейкоцитов может быть как повышенным, так и (реже) пониженным. В мазках могут выявляться бласты. Основанием для постановки диагноза «острый миелоидный лейкоз» становится обнаружение более 20% бластных клеток в крови либо в костном мозге.
Основой лечения острого миелоидного лейкоза является химиотерапия. Выделяют два этапа лечения: индукцию и консолидацию (постремиссионную терапию). На этапе индукции выполняют лечебные мероприятия, направленные на уменьшение количества лейкозных клеток и достижение состояния ремиссии. На этапе консолидации устраняют остаточные явления болезни и предотвращают рецидивы. Лечебную тактику определяют в зависимости от вида острого миелоидного лейкоза, общего состояния больного и некоторых других факторов.
Наиболее популярная схема индукционного лечения – «7+3», предусматривающая непрерывное внутривенное введение цитарабина в течение 7 дней в сочетании с одновременным быстрым периодическим введением антрациклинового антибиотика в течение первых 3 дней. Наряду с этой схемой в процессе лечения острого миелоидного лейкоза могут применяться другие лечебные программы. При наличии тяжелых соматических заболеваний и высоком риске развития инфекционных осложнений в результате подавления миелоидного ростка (обычно – у больных старческого возраста) используют менее интенсивную паллиативную терапию.
Программы индукции позволяет добиться ремиссии у 50-70% пациентов с острым миелоидным лейкозом. Однако без дальнейшей консолидации у большинства больных наступает рецидив, поэтому второй этап лечения рассматривается, как обязательная часть терапии. План консолидационного лечения острого миелоидного лейкоза составляется индивидуально и включает в себя 3-5 курсов химиотерапии. При высоком риске рецидивирования и уже развившихся рецидивах показана трансплантация костного мозга. Другие методы лечения рецидивных ОМЛ пока находятся в стадии клинических испытаний.
Прогноз острого миелоидного лейкоза
Прогноз определятся разновидностью острого миелоидного лейкоза, возрастом больного, наличием или отсутствием миелодиспластического синдрома в анамнезе. Средняя пятилетняя выживаемость при разных формах ОМЛ колеблется от 15 до 70%, вероятность развития рецидивов – от 33 до 78%. У пожилых людей прогноз хуже, чем у молодых, что объясняется наличием сопутствующих соматических заболеваний, являющихся противопоказанием для проведения интенсивной химиотерапии. При миелодиспластическом синдроме прогноз хуже, чем при первичном остром миелоидном лейкозе и ОМЛ, возникшем на фоне фармакотерапии по поводу других онкологических заболеваний.
Хронический миелолейкоз
Хронический миелолейкоз – это злокачественное миелопролиферативное заболевание, характеризующееся преимущественным поражением гранулоцитарного ростка. Может долгое время протекать бессимптомно. Проявляется склонностью к субфебрилитету, ощущением полноты в животе, частыми инфекциями и увеличением селезенки. Наблюдаются анемия и изменение уровня тромбоцитов, сопровождающиеся слабостью, бледностью и повышенной кровоточивостью. На заключительной стадии развиваются лихорадка, лимфоаденопатия и кожная сыпь. Диагноз устанавливается с учетом анамнеза, клинической картины и данных лабораторных исследований. Лечение – химиотерапия, радиотерапия, пересадка костного мозга.
Хронический миелолейкоз – онкологическое заболевание, возникающее в результате хромосомной мутации с поражением полипотентных стволовых клеток и последующей неконтролируемой пролиферацией зрелых гранулоцитов. Составляет 15% от общего количества гемобластозов у взрослых и 9% от общего числа лейкозов во всех возрастных группах. Обычно развивается после 30 лет, пик заболеваемости хроническим миелолейкозом приходится на возраст 45-55 лет. Дети до 10 лет страдают исключительно редко.
Хронический миелолейкоз одинаково распространен у женщин и у мужчин. Из-за бессимптомного или малосимптомного течения может становиться случайной находкой при исследовании анализа крови, взятого в связи с другим заболеванием или во время профилактического осмотра. У части больных хронический миелолейкоз выявляется на заключительных стадиях, что ограничивает возможности терапии и ухудшает показатели выживаемости. Лечение проводят специалисты в области онкологии и гематологии.
Причины
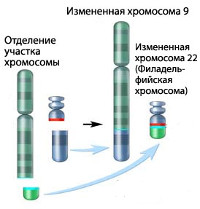
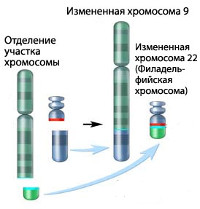
Хронический миелолейкоз считается первым заболеванием, при котором достоверно установлена связь между развитием патологии и определенным генетическим нарушением. В 95% случаев подтвержденной причиной хронического миелолейкоза является хромосомная транслокация, известная как «филадельфийская хромосома». Суть транслокации заключается во взаимной замене участков 9 и 22 хромосом. В результате такой замены формируется устойчивая открытая рамка считывания. Образование рамки вызывает ускорение деления клеток и подавляет механизм восстановления ДНК, что увеличивает вероятность возникновения других генетических аномалий.
В числе возможных факторов, способствующих появлению филадельфийской хромосомы у больных хроническим миелолейкозом, называют ионизирующее облучение и контакт с некоторыми химическими соединениями.
Патогенез
Итогом мутации становится усиленная пролиферация полипотентных стволовых клеток. При хроническом миелолейкозе пролиферируют преимущественно зрелые гранулоциты, но аномальный клон включает в себя и другие клетки крови: эритроциты, моноциты, мегакариоциты, реже – В- и Т-лифоциты. Обычные гемопоэтические клетки при этом не исчезают и после подавления аномального клона могут служить основой для нормальной пролиферации кровяных клеток. Для хронического миелолейкоза характерно стадийное течение.
- При первой, хронической (неактивной) фазе отмечается постепенное усугубление патологических изменений при сохранении удовлетворительного общего состояния.
- Во второй фазе хронического миелолейкоза – фазе акселерации изменения становятся явными, развиваются прогрессирующие анемия и тромбоцитопения.
- Заключительной стадией хронического миелолейкоза является бластный криз, сопровождающийся быстрой экстрамедуллярной пролиферацией бластных клеток.
Источником бластов становятся лимфатические узлы, кости, кожа, ЦНС и т. д. В фазе бластного криза состояние больного хроническим миелолейкозом резко ухудшается, развиваются тяжелые осложнения, завершающиеся гибелью больного. У некоторых пациентов фаза акселерации отсутствует, хроническая фаза сразу сменяется бластным кризом.
Симптомы хронического миелолейкоза
Клиническая картина определяется стадией заболевания. Хроническая фаза в среднем продолжается 2-3 года, в некоторых случаях – до 10 лет. Для этой фазы хронического миелолейкоза характерно бессимптомное течение или постепенное появление «легких» симптомов: слабости, некоторого недомогания, снижения трудоспособности и чувства переполнения живота. При объективном осмотре больного хроническим миелолейкозом может обнаруживаться увеличение селезенки. По анализам крови выявляется повышение количества гранулоцитов до 50-200 тыс./мкл при бессимптомном течении заболевания и до 200-1000 тыс./мкл при «легких» признаках.
На начальных стадиях хронического миелолейкоза возможно некоторое снижение уровня гемоглобина. В последующем развивается нормохромная нормоцитарная анемия. При исследовании мазка крови пациентов с хроническим миелолейкозом отмечается преобладание молодых форм гранулоцитов: миелоцитов, промиелоцитов, миелобластов. Наблюдаются отклонения от нормального уровня зернистости в ту или иную сторону (обильная или очень скудная). Цитоплазма клеток незрелая, базофильная. Определяется анизоцитоз. При отсутствии лечения хроническая фаза переходит в фазу акселерации.
О начале фазы акселерации может свидетельствовать как изменение лабораторных показателей, так и ухудшение состояния пациентов. Возможно нарастание слабости, увеличение печени и прогрессирующее увеличение селезенки. У больных хроническим миелолейкозом выявляются клинические признаки анемии и тромбоцитопении или тробоцитоза: бледность, быстрая утомляемость, головокружения, петехии, кровоизлияния, повышенная кровоточивость. Несмотря на проводимое лечение, в крови пациентов с хроническим миелолейкозом постепенно увеличивается количество лейкоцитов. При этом отмечается возрастание уровня метамиелоцитов и миелоцитов, возможно появление единичных бластных клеток.
Бластный криз сопровождается резким ухудшением состояния больного хроническим миелолейкозом. Возникают новые хромосомные аномалии, моноклоновое новообразование трансформируется в поликлоновое. Отмечается нарастание клеточного атипизма при угнетении нормальных ростков кроветворения. Наблюдаются ярко выраженные анемия и тромбоцитопения. Суммарное количество бластов и промиелоцитов в периферической крови составляет более 30%, в костном мозге – более 50%. Пациенты с хроническим миелолейкозом теряют вес и аппетит. Возникают экстрамедуллярные очаги незрелых клеток (хлоромы). Развиваются кровотечения и тяжелые инфекционные осложнения.
Диагностика
Диагноз устанавливается на основании клинической картины и результатов лабораторных исследований. Первое подозрение на хронический миелолейкоз часто возникает при повышении уровня гранулоцитов в общем анализе крови, назначенном в порядке профилактического осмотра или обследования в связи с другим заболеванием. Для уточнения диагноза могут использоваться данные гистологического исследования материала, полученного при стернальной пункции костного мозга, однако окончательный диагноз «хронический миелолейкоз» выставляется при выявлении филадельфийской хромосомы при помощи ПЦР, флюоресцентной гибридизации или цитогенетического исследования.
Вопрос о возможности постановки диагноза хронический миелолейкоз при отсутствии филадельфийской хромосомы остается дискутабельным. Многие исследователи считают, что подобные случаи могут объясняться комплексными хромосомными нарушениями, из-за которых выявление данной транслокации становится затруднительным. В ряде случаев филадельфийскую хромосому можно обнаружить при использовании ПЦР с обратной транскрипцией. При отрицательных результатах исследования и нетипичном течении заболевания обычно говорят не о хроническом миелолейкозе, а о недифференцированном миелопролиферативном/миелодиспластическом расстройстве.
Лечение хронического миелолейкоза
Тактику лечения определяют в зависимости от фазы заболевания и выраженности клинических проявлений. В хронической фазе при бессимптомном течении и слабо выраженных лабораторных изменениях ограничиваются общеукрепляющими мероприятиями. Больным хроническим миелолейкозом рекомендуют соблюдать режим труда и отдыха, принимать пищу, богатую витаминами и т. д. Лечение может включать:
- Монохимиотерапию. При повышении уровня лейкоцитов используют бусульфан. После нормализации лабораторных показателей и уменьшения селезенки пациентам с хроническим миелолейкозом назначают поддерживающую терапию или курсовое лечение бусульфаном. При бластных кризах осуществляют лечение гидроксикарбамидом.
- Радиотерапию. Облучение обычно используют при лейкоцитозе в сочетании со спленомегалией. При снижении уровня лейкоцитов делают паузу продолжительностью не менее месяца, а затем переходят на поддерживающую терапию бусульфаном. Радиотерапию также назначают при хлоромах.
- Полихимиотерапию. В прогрессирующей фазе хронического миелолейкоза возможно использование одного химиопрепарата или полихимиотерапии. Применяют митобронитол, гексафосфамид или хлорэтиламиноурацил. Как и в хронической фазе, проводят интенсивную терапию до стабилизации лабораторных показателей, в последующем переходят на поддерживающие дозы. Курсы полиохимиотерапии при хроническом миелолейкозе повторяют 3-4 раза в год.
- Гемокоррекцию. При неэффективности терапии используют лейкоцитаферез. При выраженной тромбоцитопении, анемии выполняют переливания тромбоконцентрата и эритроцитарной массы.
- ТКМ.Пересадку костного мозга проводят в первой фазе хронического миелолейкоза. Продолжительной ремиссии удается достичь у 70% пациентов.
- Удаление селезенки. При наличии показаний осуществляют спленэктомию. Экстренная спленэктомия показана при разрыве или угрозе разрыва селезенки, плановая – при гемолитических кризах, «блуждающей» селезенке, рецидивирующих периспленитах и резко выраженной спленомегалии, сопровождающейся нарушением функций органов брюшной полости.
Прогноз
Прогноз при хроническом миелолейкозе зависит от множества факторов, определяющим из которых является момент начала лечения (в хронической фазе, фазе активации или в период бластного криза). В качестве неблагоприятных прогностических признаков хронического миелолейкоза рассматривают значительное увеличение печени и селезенки (печень выступает из-под края реберной дуги на 6 и более см, селезенка – на 15 и более см), лейкоцитоз свыше 100x10 9 /л, тромбоцитопению менее 150x10 9 /л, тромбоцитоз более 500х10 9 /л, повышение уровня бластных клеток в периферической крови до 1% и более, повышение суммарного уровня промиелоцитов и бластных клеток в периферической крови до 30% и более.
Вероятность неблагоприятного исхода при хроническом миелолейкозе возрастает по мере увеличения количества признаков. Причиной гибели становятся инфекционные осложнения или тяжелые геморрагии. Средняя продолжительность жизни пациентов с хроническим миелолейкозом составляет 2,5 года, однако при своевременном начале терапии и благоприятном течении заболевания этот показатель может увеличиваться до нескольких десятков лет.
Острый лейкоз
Острый лейкоз – опухолевое поражение кроветворной системы, морфологической основой которого выступают незрелые (бластные) клетки, вытесняющие нормальные гемопоэтические ростки. Клиническая симптоматика острого лейкоза представлена прогрессирующей слабостью, немотивированным подъемом температуры, артралгиями и оссалгиями, кровотечениями различных локализаций, лимфаденопатией, гепатоспленомегалией, гингивитами, стоматитами, ангинами. Для подтверждения диагноза необходимо исследование гемограммы, пунктата костного мозга, биоптата подвздошной кости и лимфоузлов. Основу лечения острых лейкозов составляют химиотерапевтические курсы и сопроводительная терапия.
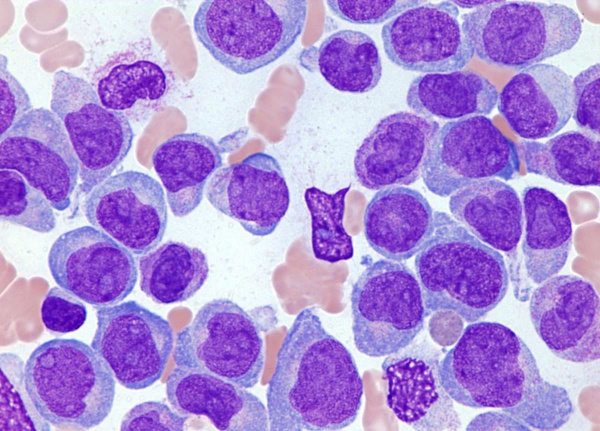
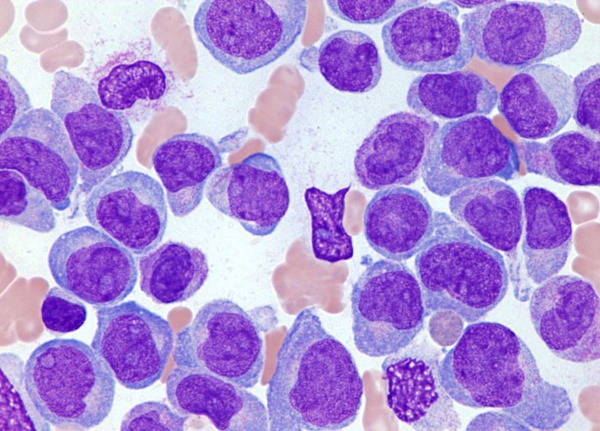
Острый лейкоз - форма лейкемии, при которой нормальное костномозговое кроветворение вытесняется мало дифференцированными клетками-предшественниками лейкоцитов с их последующим накоплением в периферической крови, инфильтрацией тканей и органов. Термины «острый лейкоз» и «хронический лейкоз» отражают не только длительность течения заболевания, но также морфологическую и цитохимическую характеристику опухолевых клеток. Острый лейкоз является наиболее частой формой гемобластозов: он развивается у 3-5 из 100 тыс. человек; соотношение взрослых и детей – 3:1. При этом у лиц старше 40 лет статистически чаще диагностируется острый миелоидный лейкоз, а у детей – острый лимфобластный лейкоз.
Причины острого лейкоза
Первопричиной острого лейкоза является мутация гемопоэтической клетки, дающей начало опухолевому клону. Мутация кроветворной клетки приводит к нарушению ее дифференцировки на ранней стадии незрелых (бластных) форм с дальнейшей пролиферацией последних. Образующиеся опухолевые клетки замещают нормальные ростки гемопоэза в костном мозге, а в дальнейшем выходят в кровь и разносятся в различные ткани и органы, вызывая их лейкемическую инфильтрацию. Все бластные клетки несут в себе одинаковые морфологические и цитохимические признаки, что свидетельствует в пользу их клонального происхождения от одной клетки-родоначальницы.
Причины, запускающие мутационный процесс, не известны. В гематологии принято говорить о факторах риска, повышающих вероятность развития острого лейкоза. В первую очередь, это генетическая предрасположенность: наличие в семье больных с острым лейкозом практически утраивает риск заболевания у близких родственников. Риск возникновения острого лейкоза повышается при некоторых хромосомных аномалиях и генетических патологиях - болезни Дауна, синдроме Клайнфельтера, Вискотта-Олдрича и Луи-Барра, анемии Фанкони и др.
Вероятно, что активация генетической предрасположенности происходит под действием различных экзогенных факторов. В числе последних могут выступать ионизирующая радиация, химические канцерогены (бензол, мышьяк, толуол и др.), цитостатические препараты, используемые в онкологии. Нередко острый лейкоз становится следствием противоопухолевой терапии других гемобластозов – лимфогранулематоза, неходжкинских лимфом, миеломной болезни. Подмечена связь острых лейкозов с предшествующими вирусными инфекциями, угнетающими иммунную систему; сопутствующими гематологическими заболеваниями (некоторыми формами анемий, миелодисплазиями, пароксизмальной ночной гемоглобинурией и др.).
Классификация острого лейкоза
В онкогематологии общепринята международная FAB-классификация острых лейкозов, дифференцирующая различные формы заболевания в зависимости от морфологии опухолевых клеток на лимфобластные (вызываемые низкодифференцированными предшественниками лимфоцитов) и нелимфобластные (объединяющие остальные формы).
1. Острые лимфобластные лейкозы взрослых и детей:
- пре-В-форма
- В-форма
- пре-Т-форма
- Т-форма
- ни Т ни В-форма
2. Острые нелимфобластные (миелоидные) лейкозы:
- о. миелобластный (вызван неконтрорлируемой пролиферацией предшественников гранулоцитов)
- о. моно- и о. миеломонобластный (характеризуются усиленным размножением монобластов)
- о. мегакариобластный (связан с преобладанием недифференцированных мегакариоцитов – предшественников тромбоцитов)
- о. эритробластный (обусловлен пролиферацией эритробластов)
3. Острый недифференцированный лейкоз.
Течение острых лейкозов проходит ряд стадий:
- I (начальную) - преобладают общие неспецифические симптомы.
- II (развернутую) - характеризуется четко выраженными клиническими и гематологическими симптомами гемобластоза. Включает: дебют или первую «атаку», неполную или полную ремиссию, рецидив или выздоровление
- III (терминальную) – характеризуется глубоким угнетением нормального гемопоэза.

Симптомы острого лейкоза
Манифестация острого лейкоза может быть внезапной или стертой. Типично начало, характеризующееся высокой лихорадкой, интоксикацией, потливостью, резким упадком сил, анорексией. Во время первой «атаки» больные отмечают упорные боли в мышцах и костях, артралгии. Иногда начальная стадия острого лейкоза маскируется под ОРВИ или ангину; первыми признаками лейкемии могут быть язвенный стоматит или гиперпластический гингивит. Довольно часто заболевание обнаруживается случайно при профилактическом исследовании гемограммы или ретроспективно, когда острый лейкоз переходит в следующую стадию.
В развернутом периоде острого лейкоза развиваются анемический, геморрагический, интоксикационный и гиперпластический синдромы.
Анемические проявления обусловлены нарушением синтеза эритроцитов, с одной стороны, и повышенной кровоточивостью – с другой. Они включают бледность кожных покровов и слизистых, постоянную усталость, головокружение, сердцебиение, повышенное выпадение волос и ломкость ногтей и др. Усиливается выраженность опухолевой интоксикации. В условиях абсолютной лейкопении и упадка иммунитета легко присоединяются различные инфекции: пневмонии, кандидоз, пиелонефрит и т. д.
В основе геморрагического синдрома лежит выраженная тромбоцитопения. Диапазон геморрагических проявлений колеблется от мелких единичных петехий и синяков до гематурии, десневых, носовых, маточных, желудочно-кишечных кровотечений и пр. По мере прогрессирования острого лейкоза кровотечения могут становиться все массивнее вследствие развития ДВС-синдрома.
Гиперпластический синдром связан с лейкемической инфильтрацией как костного мозга, так и других органов. У больных острым лейкозом наблюдается увеличение лимфоузлов (периферических, медиастинальных, внутрибрюшных), гипертрофия миндалин, гепатоспленомегалия. Могут возникать лейкозные инфильтраты кожи (лейкемиды), оболочек мозга (нейролейкоз), поражение легких, миокарда, почек, яичников, яичек и др. органов.
Полная клинико-гематологическая ремиссия характеризуется отсутствием внекостномозговых лейкемических очагов и содержанием бластов в миелограмме менее 5% (неполная ремиссия – менее 20%). Отсутствие клинико-гематологических проявлений в течение 5 лет расценивается как выздоровление. В случае увеличения бластных клеток в костном мозге более 20%, их появления в периферической крови, а также выявления внекостномозговых метастатических очагов диагностируется рецидив острого лейкоза.
Терминальная стадия острого лейкоза констатируется при неэффективности химиотерапевтического лечения и невозможности достижения клинико-гематологической ремиссии. Признаками данной стадии служат прогрессирование опухолевого роста, развитие несовместимых с жизнью нарушений функции внутренних органов. К описанным клиническим проявлениям присоединяются гемолитическая анемия, повторные пневмонии, пиодермии, абсцессы и флегмоны мягких тканей, сепсис, прогрессирующая интоксикация. Причиной смерти больных становятся некупируемые кровотечения, кровоизлияния в мозг, инфекционно-септические осложнения.
Диагностика острого лейкоза
Во главе диагностики острых лейкозов стоит оценка морфологии клеток периферической крови и костного мозга. Для гемограммы при лейкемии характерна анемия, тромбоцитопения, высокая СОЭ, лейкоцитоз (реже лейкопения), присутствие бластных клеток. Показателен феномен «лейкемического зияния» - промежуточные стадии между бластами и зрелыми клетками отсутствуют.
С целью подтверждения и идентификации разновидности острого лейкоза выполняется стернальная пункция с морфологическим, цитохимическим и иммунофенотипическим исследованием костного мозга. При исследовании миелограммы обращает внимание увеличение процента бластных клеток (от 5% и выше), лимфоцитоз, угнетение красного ростка кроветворения (кроме случаев о. эритромиелоза) и абсолютное снижение или отсутствие мегакариоцитов (кроме случаев о. мегакариобластного лейкоза). Цитохимические маркерные реакции и иммунофенотипирование бластных клеток позволяют точно установить форму острого лейкоза. При неоднозначности трактовки анализа костного мозга прибегают к проведению трепанобиопсии.
С целью исключения лейкемической инфильтрации внутренних органов производится спинномозговая пункция с исследованием ликвора, рентгенография черепа и органов грудной клетки, УЗИ лимфатических узлов, печени и селезенки. Кроме гематолога, больные острым лейкозом должны быть осмотрены неврологом, офтальмологом, отоларингологом, стоматологом. Для оценки тяжести системных нарушений может потребоваться исследование коагулограммы, биохимического анализа крови, проведение электрокардиографии, ЭхоКГ и др.
Дифференциально-диагностические мероприятия направлены на исключение ВИЧ-инфекции, инфекционного мононуклеоза, цитомегаловирусной инфекции, коллагенозов, тромбоцитопенической пурпуры, агранулоцитоза; панцитопении при апластической анемии, В12 и фолиеводефицитной анемии; лейкемоидных реакций при коклюше, туберкулезе, сепсисе и др. заболеваниях.

Лечение острого лейкоза
Пациентов с острым лейкозом лечат в стационарах онкогематологического профиля. В палатах организуется усиленный санитарно-дезинфекционный режим. Больные с острым лейкозом нуждаются в проведении гигиенической обработки полости рта, профилактики пролежней, туалета половых органов после физиологических отправлений; организации высококалорийного и витаминизированного питания.
Непосредственно лечение острых лейкозов проводится последовательно; основные этапы терапии включают достижение (индукцию) ремиссии, ее закрепление (консолидацию) и поддержание, профилактику осложнений. Для этого разработаны и используются стандартизированные схемы полихимиотерапии, которые подбираются гематологом с учетом морфологической и цитохимической формы острого лейкоза.
При благоприятной ситуации ремиссия обычно достигается в течение 4-6 недель усиленной терапии. Затем, в рамках консолидации ремиссии проводится еще 2-3 курса полихимиотерапии. Поддерживающая противорецидивная терапия осуществляется еще в течение не менее 3-х лет. Наряду с химиотерапией при остром лейкозе необходимо проведение сопроводительного лечения, направленного на предупреждение агранулоцитоза, тромбоцитопении, ДВС-синдрома, инфекционных осложнений, нейролейкемии (антибиотикотерапия, переливание эритроцитарной, тромбоцитарной массы и свежезамороженной плазмы, эндолюмбальное введение цитостатиков). При лейкемической инфильтрации глотки, средостения, яичек и др. органов проводится рентгенотерапия очагов поражения.
В случае успешного лечения достигается уничтожение клона лейкозных клеток, нормализация кроветворения, что способствует индукции длительного безрецидивного периода и выздоровления. Для предупреждения рецидивов острого лейкоза может быть проведена трансплантация костного мозга после предварительного кондиционирования путем химиотерапии и тотального облучения.
По имеющимся статистическим сведениям, использование современных цитостатических средств приводит к переходу острого лейкоза в фазу ремиссии у 60-80% больных; из них у 20-30% удается добиться полного выздоровления. В целом прогноз при острых лимфобластных лейкозах более благоприятен, чем при миелобластных.
Острые миелоидные лейкозы - клиника, диагностика
Характеристика острого миелобластного лейкоза М0, M1, М2 - критерии диагностики
Острый миелобластный лейкоз (М0, M1, М2). Термин «острый миелобластный лейкоз» объединяет три подтипа заболевания, которые отличаются друг от друга по степени дифференцированности, зрелости лейкемических клеток — миелобластов. В классификации FAB эти варианты обозначены цифрами: М0 — недифференцированный ОМЛ, M1 — острый миелоидный лейкоз без созревания, М2 — острый миелоидный лейкоз с созреванием.
Острый миелобластный лейкоз с минимальной дифференцировкой (М0) составляет приблизительно 5 % от всех острых нелимфобластных лейкозов. Как указывалось, данный диагноз может быть установлен только при выполнении иммунофенотипирования, поскольку при цитохимическом анализе клетки не могут быть отнесены к какому-либо подтипу. Принципиальным является обнаружение с помощью моноклональных антител при проточной цитофлюорометрии фермента миелопероксидазы.
Клетки при М0 экспрессируют также следующие миелоидные антигены: CD13, CD33, CD34. Для этой формы лейкоза не найдены характерные, ассоциированные только с этим подтипом острого миелоидного лейкоза хромосомные аберрации. Прогноз при стандартном лечении неблагоприятный.
Острый миелобластный лейкоз без признаков созревания клеток (Ml) составляет 15 % от всех ОМЛ. При этой форме ОМЛ определяется минимальная степень миелоидной дифференцировки, т. е. в пунктате костного мозга определяется менее 3 % промиелоцитов, отсутствуют палочки Ауэра. Цитохимически миелопероксидаза определяется в небольшом проценте бластных клеток. Типичными иммунофенотипическими маркерами являются CD13, 14, 15, 33, 34, HLA-DR.
Несколько чаще, чем при других морфологических формах ОМЛ, встречается инверсия хромосомы 3 — inv(3), что ассоциируется с тромбоцитозом в дебюте болезни; в 3 % случаях при M1 обнаруживается t(9;22).
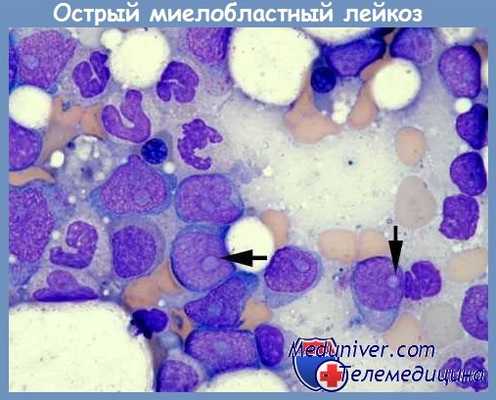
Острый миелобластный лейкоз с признаками созревания (М2) составляет около 25 % от всех острых миелоидных лейкозов. Характерные иммунофенотипические маркеры — CD13, 15, 33, 34, HLA-DR. В 1/3 всех случаев М2 определяется t(8;21). Эта транслокация встречается, хотя и очень редко, и при миеломонобластных острых лейкозах. Для миелобластных лейкозов вообще нехарактерны увеличение в размерах органов, экстрамедуллярные поражения.
При остром миелоидном лейкозе с t(8;21) у 25 % больных обнаруживается спленомегалия, у 20 % — хлоромы, описаны эозинофилия, морфологические признаки аномального созревания нейтрофилов (гипогранулярность, псевдопельгеровская аномалия). Известны случаи обнаружения незначительного числа бластных клеток в пунктате костного мозга (менее 20 %) в момент диагностики острого миелоидного лейкоза с t(8;21). При малом количестве бластных клеток больным с t(8;21) все равно ставят диагноз острого лейкоза, а не МДС.
Как отмечалось, эта группа острого миелоидного лейкоза в настоящее время рассматривается как отдельный лейкемический клинико-патологический синдром, в современной классификации выделяется в рамках отдельной категории — острый миелоидный лейкоз с определенными хромосомными аберрациями. В результате указанной транслокации в область гена, кодирующего ЕТО-протеин и находящегося на длинном плече хромосомы 8, переносится ген AML1, расположенный на длинном плече хромосомы 21 и кодирующий транскрипционный регуляторный фактор CBFа.
Итогом транслокации является химерный ген AML1-ETO и соответственно белок CBFa-ETO. В норме белок CBFa напрямую связывается с молекулой ДНК, к нему присоединяется белок CBFp, увеличивая аффинность CBFa к ДНК. В результате образования этого белкового комплекса происходит активация транскрипции генов белков, ответственных за миелоидную дифференцировку (IL-3, GM-CSF, миелопероксидаза). Химерный белок не утрачивает способности связываться с ДНК, однако в результате его действия происходит ингибирование транскрипции и соответственно нарушаются механизмы дифференцировки миелоидных клеток.
Для острого миелобластного лейкоза с t(8;21) характерен хороший ответ на химиотерапию и хорошие долгосрочные результаты. Клетки данного варианта острого миелоидного лейкоза очень чувствительны к воздействиям цитозин-арабинозида, особенно в высоких дозировках. В связи с этим при использовании в программах лечения данного варианта острого миелоидного лейкоза трех и более курсов этого препарата в дозе 3 г/м2 в течение 3 дней вероятность безрецидивной выживаемости больных возрастает до 70 %.
При этой форме острого миелобластного лейкоза описан уникальный феномен персистенции в период полной клинико-гематологической ремиссии минимальной остаточной популяции лейкемических клеток. Это определяется с помощью ПЦР, которая позволяет обнаруживать 1 клетку, несущую указанную транслокацию, среди 104-5 нормальных. У больных, завершивших лечение и находящихся в полной ремиссии длительное время (до 8 лет), методом ПЦР обнаруживается продукт химерного гена CBFa-ETO вследствие t(8;21).
Этот факт заставляет предположить, что указанная транслокация, хотя и является маркером заболевания, не представляет собой финального этапа лейкемогенеза, и требуются дополнительные воздействия для превращения указанного клона в истинно лейкемический.
Среди острых миелобластных лейкозов с дифференцировкой (М2) выделяют еще один подтип с характерной цитогенетической аномалией и клиниколабораторными признаками — острый миелобластный лейкоз с базофилией и t(6;9). Прогноз при данной форме лейкоза крайне неблагоприятный. Базофилия изредка встречается при вариантах М4.
Читайте также:
- ВПЧ-обусловленный плоскоклеточный рак ротоглотки - лучевая диагностика
- Мониторинг концентрации лекарства в плазме. Коррекция дозы лекарств - полипрагмазия
- Лучевая диагностика несеминомной герминативноклеточной опухоли средостения на рентгене, КТ
- КТ, цистография при травме мочевого пузыря
- Симптомы и признаки рака (злокачественных новообразований)
